尿嘧啶化的吲哚七甲川菁染料及制备方法和应用与流程
本发明涉及医药领域,特别涉及一种尿嘧啶化的吲哚七甲川花菁染料及其制备方法,该吲哚七甲川花菁染料可用于细胞线粒体Hg2+的检测。
背景技术:
汞是一种对人体具有很强毒性的环境污染物。其中二价汞离子(Hg2+)是其毒性的主要形式,它可以在某些水生生物中累积,随着其它的食肉动物的食用而进入食物链。Hg2+一旦被人体摄入,迅速地被分布到各个组织和器官,其中细胞中的线粒体是Hg2+的主要积累部位。Hg2+降低了线粒体膜电位,与多种蛋白发生结合,导致细胞死亡。近年来,国内外发展了各种高灵敏度、高选择性的Hg2+检测方法,如紫外吸收光度法、红外分析法、电化学法等。但是据我们所知,在这些检测方法中,基于细胞器定位的Hg2+荧光探针仅有两篇。
吲哚七甲川菁染料是一种传统的有机染料,其特点是其最大吸收和发射波长在近红外区(700-900nm),可用于荧光标记和金属离子检测,包括Hg2+。然而据文献调研,该类染料用于细胞线粒体Hg2+的检测还未见报道。
技术实现要素:
本发明的目的是提供一种尿嘧啶化的吲哚七甲川菁染料及制备方法和应用。所述吲哚七甲川菁染料可用于制备检测细胞中线粒体中Hg2+浓度的试剂盒中的荧光探针,该探针具有线粒体靶向、近红外光吸收、荧光显影与特异性接合Hg2+的特点。
实现本发明的技术方案:
一种尿嘧啶化的吲哚七甲川菁染料,有以下结构:
其中,R为H或F,当R为H时,所示结构为IR-DT;当R为F时,所示结构为IR-DFT。。
尿嘧啶化的吲哚七甲川菁染料制备方法,有以下步骤:
(1)N,N-二甲基甲酰胺(DMF)为反应试剂和溶剂,环己酮与三氯氧磷(POCl3)发生Vilsmeimer-Haack甲酰化反应,反应6小时后,反应液经异丙醚沉淀,抽滤,滤饼经有机溶剂A重结晶后得化合物3;
(2)六甲基二硅胺(HMDS)为反应溶剂,在126℃下,尿嘧啶或氟尿嘧啶与三甲基氯硅烷(TMSCl)反应5h,得到羰基被硅基保护的中间体,直接减压浓缩除去六甲基二硅胺;接着,硅基保护的尿嘧啶或氟尿嘧啶中间体与1,3-二溴丙烷发生单取代反应,反应液经过水洗、氯仿萃取、无水硫酸镁干燥、抽滤、浓缩,柱分离纯化得末端溴代的化合物(1a,1b);
(3)乙腈为溶剂,将步骤(2)所得末端溴代化合物(1a,1b)与2,3,3-三甲基3H吲哚发生卤代烃反应,制得含N-嘧啶基团侧链的2,3,3-三甲基3H吲哚季铵盐(2a,2b),经有机溶剂B沉淀、抽滤、干燥后直接进行步骤(4);
(4)无水乙醇为有机溶剂,在无水醋酸钠催化下,双醛氯代环己烯中间体3与含有N-嘧啶基团侧链的2,3,3-三甲基3H吲哚季铵盐(2a,2b)缩合反应,经硅胶柱层析、有机溶剂C重结晶得纯品(IR-DT,IR-DFT)。
步骤(1)中所述其中环己酮:POCl3:DMF的摩尔比是1:4:5。
步骤(2)中所述单取代反应条件:105℃加热,反应时间为2h。
步骤(3)中所述卤代烃反应条件:在氩气保护下,81℃加热回流,反应23h。
步骤(1)所述有机溶剂A为甲醇、乙醇、丙酮、乙酸乙酯的任意一种或几种组合的混合溶剂;步骤(3)所述有机溶剂B为乙醚、异丙醚或二甲醚的任意一种;步骤(4)中有机溶剂C为乙醇、甲醇、正丁醇或甲苯中的一种或几种的混合溶剂。
步骤(4)所述缩合反应温度为85℃。
步骤(4)所述双醛氯代环己烯中间体3与含有N-嘧啶基团侧链的2,3,3-三甲基3H吲哚季铵盐(2a,2b)的摩尔比为1:2。
上述尿嘧啶化的吲哚七甲川菁染料在制备检测细胞中线粒体中Hg2+浓度的试剂盒中的应用。
所述应用是尿嘧啶化的吲哚七甲川菁染料作为近红外荧光探针,其发射波长为700-900nm。
所述尿嘧啶化的吲哚七甲川花菁染料分子具有近红外荧光成像、细胞线粒体靶向蓄积和特异性检测Hg2+作用,可用于制备检测细胞中线粒体中Hg2+浓度的试剂盒中的荧光探针。
所述细胞线粒体中Hg2+检测,是指以细胞线粒体Hg2+为靶标,在700-900nm的单光源激光照射下,实现细胞线粒体Hg2+浓度的检测。
本发明所述尿嘧啶化的吲哚七甲川花菁染料是含有不同末端官能团的N-烷基侧链的小分子,具有近红外荧光、细胞线粒体靶向蓄积、特异性检测Hg2+等多功能活性。申请人的实验结果表明,所制备的尿嘧啶化的吲哚七甲川花菁染料,可用于细胞线粒体中Hg2+浓度的检测。
申请人前期合成了一系列的吲哚七甲川花菁染料,其具有良好的细胞线粒体聚集的特点,相关的构效关系研究也表明适宜的亲脂性阳离子结构是其具有线粒体定位的主要原因。另外,嘧啶类汞离子比色传感器的特点是能高选择性地与Hg2+配位,形成稳定的T-Hg-T络合物。据此,将含有嘧啶结构的尿嘧啶功能基团引入至这类线粒体靶向的吲哚七甲川花菁染料,可特异性地结合线粒体中的Hg2+,通过诱导分子内聚集,导致花菁分子的荧光强度改变,从而实现了对线粒体中的Hg2+的检测。本发明采用尿嘧啶化结构,通过分子内F-F键、F-H键,促进T-Hg-T络合物形成和加剧分子内聚集,进一步提高对汞离子检测的灵敏度。
下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。下列实施例中未注明具体条件的实验方法,通常按照常规条件或按照制造厂商所建议的条件。
附图说明
图1为IR-DT(a)及IR-DFT(b)对不同金属离子的荧光淬灭程度;
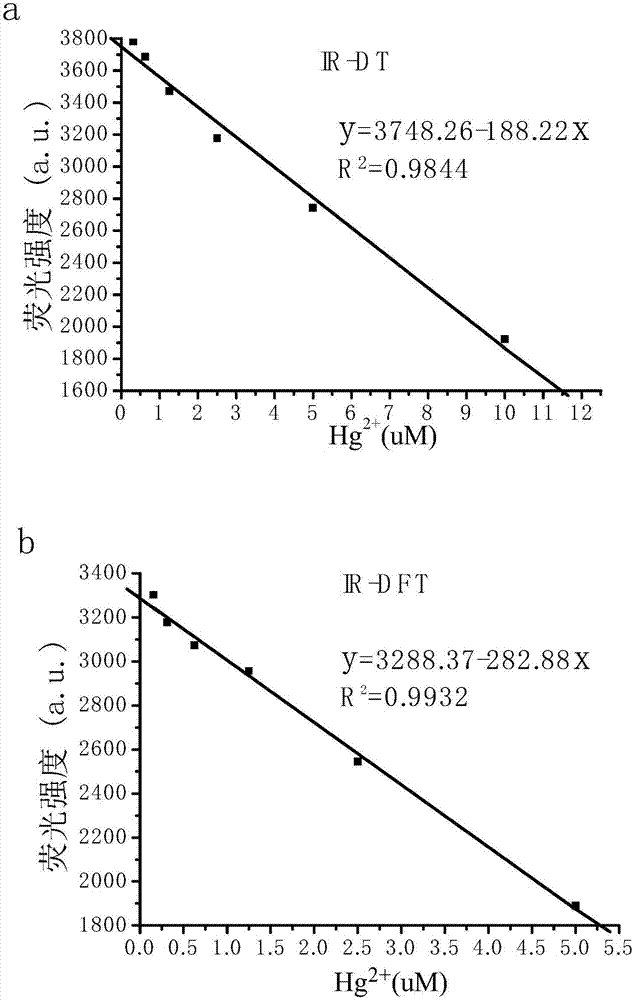
图2为IR-DT(a)及IR-DFT(b)对不同Hg2+浓度的检测;
图3为IR-DFT共聚焦定位实验图(a)和对细胞线粒体中不同浓度Hg2+的荧光成像(b)。
具体实施例
实施例中所采用的试剂:
所述试剂和溶剂均采用市售的分析纯,其中试剂二氯甲烷、甲醇、乙醇、N,N-二甲基甲酰胺、三氯氧磷、三乙胺需经过蒸馏纯化与干燥处理。
实施例中所采用的仪器和设备:
所有反应均以薄层层析跟踪,使用烟台市芝罘黄务硅胶开发试验厂所生产的高效薄层层析硅胶板(型号CF-254),磷钼酸、茚三酮、溴甲酚绿或碘显色。
柱层析用烟台市芝罘黄务硅胶开发试验厂生产的层析硅胶(10-40μ),层析用有机溶剂均为分析纯,且经过重蒸干燥处理。熔点用上海精密科学仪器有限公司生产的WRR熔点仪测定。
所有化合物1HNMR和13CNMR由美国Varian公司生产的MercuryPlus-400核磁共振谱仪测定,TMS作内标,未经特殊说明,均用CDCl3作溶剂,δ值单位为ppm。
质谱由HP5989A型质谱仪测定,IR由Testscan SchimadzuFTIR 8000series测定。
实施例1双醛氯代环己烯(2-氯-3-羟甲烯-1-甲酰基环己烯)的制备
将向盛有60ml无水DMF的反应器中,搅拌下缓慢滴入20ml POCl3,并控制内温不高于5℃。滴毕后加入5ml环己酮,控制内温不超过10℃。滴毕,油欲加热使内温升至80℃,并搅拌反应3.5h。停止反应,反应液倾至水中,搅拌3h后.大量黄色固体析出,抽滤,滤饼用冷水洗至中性。粗品用乙酸乙酯精制得黄色粒状晶体5.2g,收率65.3%,。避光低温(4℃)保存。熔点:130-131℃(文献熔点:130-131℃)薄层层析检测:环己烷:乙酸乙酯(3:1),Rf值约为0.4。UV(甲醇):λmax=408nm[OHC-C=C];
1H NMR(400MHz,DMSO-d):10.85(s,1H),3.35(s,2H),2.36-2.34(t,J=8Hz,4H),1.57(m,2H).MS(ESI+):173.1(M+H+)calcd exactMass:172.03。
实施例2 1-(3-溴丙基)嘧啶-2,4(1H,3H)-二酮(化合物1)的制备
向50mL的反应瓶中加入12.0mmol尿嘧啶或氟尿嘧啶,氮气保护下加入六甲基二硅胺(HMDS,48.0mmol)及0.25mL三甲基氯硅烷,完毕后于126℃下加热搅拌反应。5h后,直接减压浓缩除去溶剂。残留物加入10mL1,3-二溴丙烷,于105℃下加热搅拌反应。5h后直接减压浓缩,残留物用二氯甲烷溶解,水洗,饱和食盐水洗涤,分液,有机层用无水硫酸钠干燥,抽滤,浓缩,柱分离纯化(洗脱条件:CH2Cl2/CH3OH=50/1)得化合物1a或1b。
1a(82%):1H NMR(400MHz,CDCl3):δ11.352(s,1H),7.47-7.45(d,J=8Hz,1H),7.27-7.26(d,J=8Hz,1H),7.04-6.98(m,2H),6.88-6.85(m,1H),5.77-5.75(d,J=8Hz,1H),1.63-1.58(m,2H),1.42(s,3H),1.32-1.28(t,J=6Hz,1H),1.24(s,6H);
1b(76%):1H NMR(400MHz,CDCl3):δ8.41(s,1H),4.09(t,J=2.4Hz,4H),3.39(t,J=2.4Hz,2H),2.86(m,2H).
实施例3N-胸腺嘧啶吲哚季铵溴盐(2a、2b)的制备
取25mL的反应瓶(含冷凝回流装置),加入化合物1a或1b(1.83mmol),吲哚(3.66mmol)。氮气保护,加入无水乙腈(6mL)溶解,于81℃下加热搅拌反应。22h后停止反应,反应液冷却至室温后,直接减压得暗红色粘稠物。将该粘稠物用异丙醚洗涤,干燥得目标化合物粗品(2a、2b)。不需进一步纯化即可进行下一步反应。
实施例4N-嘧啶基团侧链的荧光探针(IR-DT、IR-DFT)的合成
25mL反应瓶中加入500mg吲哚季铵盐(0.71mmol),0.31mmol缩合剂(实施例1产物),及0.71mmol乙酸钠。以无水乙醇(10mL)作溶剂,于80℃下加热回流反应。2h后反应液冷至室温,减压蒸馏除去溶剂得暗红色粘稠物,经硅胶柱层析纯化的墨绿色固体。
IR-DT(38%):1H NMR(600MHz,DMSO-d)δ11.27(s,2H),8.24-8.22(d,J=12Hz,2H),7.69-7.68(d,J=6Hz,2H),7.62-7.61(d,J=6Hz,2H),7.46-7.40(m,4H),7.28-7.26(t,J=6Hz,2H),6.23-6.21(d,J=12Hz,2H),5.57-5.56(s,J-6Hz,2H),4.23(m,4H),3.82-3.80(t,J=6Hz,4H),2.64(m,4H),2.03(m,2H),1.84-1.82(m,2H),1.65(s,12H).MS(ESI+):759.4(M-Br)calcd exactMass:759.3
IR-DFT(30%):1H NMR(400MHz,DMSO-d):δ8.70-8.66(d,J=16Hz,2H),8.58-8.56(d,J=8Hz,2H),8.07-8.05(d,J=8Hz,2H),7.92-7.84(m,4H),7.74-7.70(t,J=8Hz,2H),6.69-6.66(d,J=12Hz,2H),4.70-4.66(m,4H),4.24-4.21(t,J=6Hz,4H),3.82(s,2H),3.09(s,6H),2.10(s,12H).13C NMR(400MHz,DMSO-d6):δ174.223,172.180,171.925,147.948,147.930,142.004,141.021,128.598,126.156,125.134,122.478,111.489,101.573,48.945,43.629,33.402,27.434,26.680,25.788,25.597,24.123,20.971,and 20.339.19F NMR(400MHz,DMSO-d6):δ-168.73ppm.HRMS:795.32(M-Br)calcd exactMass:795.3.
实施例5化合物IR-DT、IR-DFT的近红外荧光特性
在万分之一天平上精确称量样品,配成10mM的DMSO溶液,备用。测试时,先用精密移液枪取2μL此溶液于10mL棕色容量瓶中,然后分别用甲醇和血清稀释至刻度,即得到2μM的染料溶液。最大吸收光谱和发射光谱分别用Shimadzu UV-3600紫外近红外分光光度计和Varian Cary Eclipse Fluorometer荧光光谱仪测定。用朗伯-比尔定律计算化合物的摩尔吸光系数。计算公式为A=εab,式中A代表吸收强度,ε表示摩尔消光系数,a为化合物的浓度(单位为mol/L),b为石英池的厚度(单位为cm)。测试结果表明,所有化合物的最大吸收波长和发射波长均在近红外区(780-820nm),摩尔吸光系数在99000-300000,具有较优良的近红外荧光特性。
实施例6化合物IR-DT、IR-DFT的特异性结合Hg2+
分别称取一定量的AlCl3,CoCl2,Pb(CH3COO)2,KCl,MnSO4,LiCl,ZnCl2,CaCl2,FeCl2,MgSO4,Cu(NO)2,NaCl,HgSO4,用超纯水配成10mM的溶液。称取一定量的柠檬酸三钠,配成10mM的水溶液,同时调节pH到6.65,在柠檬酸三钠的缓冲液中加入5%的无水甲醇,用此溶液将IR-DT或IR-DFT的浓度配成10uM,分别加入不同的金属离子,使金属离子的终浓度为10uM,分别用荧光光谱仪测量溶液的发射光谱。并用不同离子的淬灭系数(1-F0/F)表示IR-DT或IR-DFT对Hg2+的特异性结合能力(参见图1)。其中,F0和F分别为染料加金属离子前和后,发射波长为800nm时的荧光强度。其结果表明IR-DT和IR-DFT对Hg2+都有很好的特异性结合能力。
实施例7化合物IR-DFT对不同Hg2+浓度荧光强度变化
称取一定量的柠檬酸三钠,配成10mM的水溶液,同时调节pH到6.65,在柠檬酸三钠的缓冲液中加入5%的无水甲醇,用此溶液将IR-DT或IR-DFT的浓度配成10uM,分别加入不同量的Hg2+溶液,使Hg2+的浓度分别为0uM,0.32uM,0.63uM,1.25uM,2.5uM,5uM,10uM,20uM,40uM,分别用荧光光谱仪测量溶液的发射光谱。其结果表明当染料浓度为一定时,其荧光强度(发射波长为800nm)随Hg2+浓度的增加而下降,且在一定范围内具有很好的线性关系(参见图2)。
实施例8IR-DFT共聚焦定位实验和细胞线粒体中不同浓度的Hg2+荧光成像
细胞株选用人乳腺癌癌细胞株MCF-7(购自美国ATCC公司),以含10%胎牛血清和1%青霉素/链霉素的DMEM培养基于37℃,5%CO2条件下培养,隔天更换一次培养液。取生长良好,达70-80%融合的细胞,消化离心后接种于35mm共聚焦显微镜观察用的培养皿中,培养过夜。次日弃去培养基,于培养皿中分别加入浓度为5μM、体积为1ml的IR-DFT,于37℃,5%CO2条件下孵育2小时。弃去染液,以PBS缓冲液漂洗三次,以浓度为1:6000的线粒体探针Mito-traker孵育细胞,作用15分钟。弃去染液,以PBS缓冲液漂洗三次后于共聚焦显微镜下观察IR-DFT的荧光信号与Mito-traker的荧光信号的重叠情况(参见图3a)。为了获得MCF-7细胞在加Hg2+和不加Hg2+时的荧光成像,我们将培育好的含IR-DFT(10uM)细胞分别加或不加Hg2+(10uM),并在37℃的培养基中继续孵育1h,弃去染液,以PBS缓冲液漂洗三次后于共聚焦显微镜下观察IR-DFT的荧光信号强度的变化(参见图3b)。结果表明,IR-DF在体外培养条件下可被活体细胞高效摄取,显示出很强的红色荧光信号;红色荧光信号可与来自线粒体的绿色荧光信号完全重合,证实化合物进入细胞后,主要分布于细胞线粒体内;另一方面,IR-DFT对细胞线粒体中不同浓度的Hg2+显示了不同强度的荧光成像,且其淬灭的荧光强度可在加入EDTA后恢复。
- 还没有人留言评论。精彩留言会获得点赞!