着色组合物、喷墨记录用油墨、喷墨记录方法及喷墨打印机墨盒与流程
本发明涉及一种着色组合物、喷墨记录用油墨、喷墨记录方法及喷墨打印机墨盒。
背景技术:
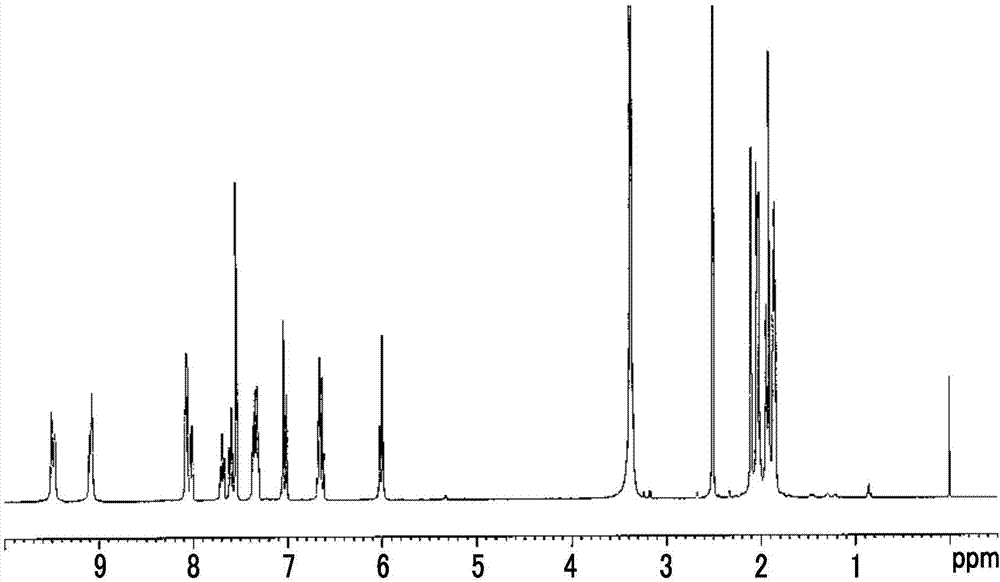
:喷墨记录方法如众所周知是使油墨的小滴飞翔而附着在纸等记录介质上来进行印刷的方法。该印刷方法能够以廉价的装置高速且简便地印刷高分辨率、高品位的图像,尤其是在彩色印刷中,近年来作为可替代照片的图像形成方法而进行了技术开发。例如,专利文献1及专利文献2中记载有一种含有呫吨化合物的喷墨记录用油墨。以往技术文献专利文献专利文献1:日本特开2013-133395号公报专利文献2:国际公开第2015/105108号技术实现要素:发明要解决的技术课题然而,对于染料的领域要求进一步提高性能。本发明的目的在于提供一种能够形成色相、彩度及着色力(印相浓度)优异,且耐光性、耐臭氧性及耐湿性优异的图像,而且喷墨打印中的吐出稳定性也优异的着色组合物、使用了上述着色组合物的喷墨记录用油墨、使用了上述喷墨记录用油墨的喷墨记录方法及填充有上述喷墨记录用油墨的喷墨打印机墨盒。用于解决技术课题的手段本发明人等进行深入研究,发现通过下述机构而能够解决上述课题。本发明中,通过组合通式(1)所表示的化合物和通式(D)所表示的化合物,能够降低(有助于提高油墨的吐出稳定性)着色组合物(油墨)中所含有的染料浓度的同时兼备高着色力(印相浓度)和图像坚牢性(耐光性、耐臭氧性及耐湿性)。优选的理由为如下:通过组合良好的色相及彩度和具有高着色力的不同的色素母核,与单独使用各自的情况相比更能够以高水平满足着色力和图像坚牢性。详细的理由虽不确定,但推定为如下:当混合通式(1)所表示的呫吨系染料和通式(D)所表示的偶氮染料时(例如,喷墨记录用油墨中或利用喷墨记录方法而制成的喷墨印相物:喷墨专用纸上)物理化学的相互作用少,不会引起耐光性降低及油墨的吐出稳定性降低等大的缺点而能够兼备所需性能。〔1〕一种着色组合物,其包含下述通式(1)所表示的化合物和下述通式(D)所表示的化合物。[化学式1]通式(1)通式(1)中,R1、R5、R6及R10各自独立地表示烷基。R4、R9、R11、R12、R13、R14、R15、R16、R17、R18、R19及R20各自独立地表示氢原子或取代基。R2、R3、R7及R8各自独立地表示氢原子、烷基或下述通式(A)所表示的取代基,R2、R3、R7及R8中的至少1个表示下述通式(A)所表示的取代基。[化学式2]通式(A)通式(A)中,X表示下述通式(X1)、通式(X2)或通式(X3)所表示的取代基。*表示与苯环键合的键合键。[化学式3]通式(X1)通式(X1)中,R401、R402、R403、R404及R405各自独立地表示氢原子或取代基。其中,R401、R402、R403、R404及R405满足下述条件(i)或(ii)。*表示与硫原子键合的键合键。条件(i):R401、R402、R403、R404及R405中的至少1个表示羟基,且至少1个表示羧基。条件(ii):R401、R402、R403、R404及R405中的至少2个表示羧基。[化学式4]通式(X2)通式(X2)中,R501、R502、R503、R504、R505、R506及R507各自独立地表示氢原子或取代基。其中,R501、R502、R503、R504、R505、R506及R507满足下述条件(iii)或(iv)。*表示与硫原子键合的键合键。条件(iii):R501、R502、R503、R504、R505、R506及R507中的至少1个表示羟基,且至少1个表示羧基。条件(iv):R501、R502、R503、R504、R505、R506及R507中的至少2个表示羧基。[化学式5]通式(X3)通式(X3)中,R601、R602、R603、R604、R605、R606及R607各自独立地表示氢原子或取代基。其中,R601、R602、R603、R604、R605、R606及R607满足下述条件(v)或(vi)。*表示与硫原子键合的键合键。条件(v):R601、R602、R603、R604、R605、R606及R607中的至少1个表示羟基,且至少1个表示羧基。条件(vi):R601、R602、R603、R604、R605、R606及R607中的至少2个表示羧基。通式(D)[化学式6]通式(D)中,Z1表示哈米特取代基常数σp值为0.20以上的吸电子基团。Z2表示氢原子、脂肪族基团、芳香族基团、酰基或杂环基。R23及R24分别独立地表示氢原子、脂肪族基团、芳香族基团、杂环基、酰基、烷氧基羰基、芳氧基羰基、氨基甲酰基、烷基磺酰基、芳基磺酰基或氨磺酰基。其中,R23及R24不会同时为氢原子。R21及R22分别独立地表示氢原子、卤素原子、脂肪族基团、芳香族基团、杂环基、氰基、羧基、氨基甲酰基、烷氧基羰基、芳氧基羰基、酰基、羟基、烷氧基、芳氧基、甲硅烷氧基、酰氧基、氨基甲酰氧基、杂环氧基、烷氧基羰基氧基、芳氧基羰基氧基、烷基氨基、芳基氨基、杂环氨基、酰氨基、脲基、氨磺酰基氨基、烷氧基羰基氨基、芳氧基羰基氨基、烷基或芳基磺酰基氨基、芳氧基羰基氨基、硝基、烷基或芳基硫基、烷基或芳基磺酰基、烷基或芳基亚磺酰基、氨磺酰基、磺基或杂环硫基。并且,R21与R23或R23与R24可以键合而形成5或6元环。R25及R29分别独立地表示烷基、烷氧基或卤素原子。其中,当R25及R29同时为烷基时,构成该烷基的碳原子数的合计为3以上,它们可以进一步被取代。R26、R27及R28的定义分别独立地与R21及R22相同,R25与R26、或R28与R29可以彼此缩合成环。Q表示氢原子、脂肪族基团、芳香族基团或杂环基。上述Z1、Z2、R21、R22、R23、R24及Q的各基团还可以具有取代基。其中,通式(D)具有至少1个离子性亲水性基团。〔2〕根据〔1〕所述的着色组合物,上述通式(A)中的X表示上述通式(X1)所表示的取代基,且上述通式(X1)中的R401、R402、R403、R404及R405满足上述条件(i)。〔3〕根据〔1〕所述的着色组合物,上述通式(A)中的X表示上述通式(X2)所表示的取代基,且上述通式(X2)中的R501、R502、R503、R504、R505、R506及R507满足上述条件(iii)。〔4〕根据〔1〕所述的着色组合物,上述通式(A)中的X表示上述通式(X3)所表示的取代基,且上述通式(X3)中的R601、R602、R603、R604、R605、R606及R607满足上述条件(v)。〔5〕根据〔1〕至〔4〕中任一项所述的着色组合物,上述通式(1)所表示的化合物与上述通式(D)所表示的化合物的总含量在上述着色组合物中为1.0~5.0质量%。〔6〕根据〔1〕至〔5〕中任一项所述的着色组合物,上述通式(1)所表示的化合物的含量与上述通式(D)所表示的化合物的含量的质量比{通式(1)/通式(D)}为{95/5}~{5/95}。〔7〕一种喷墨记录用油墨,其使用了〔1〕至〔6〕中任一项所述的着色组合物。〔8〕一种喷墨记录方法,其使用了〔7〕所述的喷墨记录用油墨。〔9〕一种喷墨打印机墨盒,填充有〔7〕所述的喷墨记录用油墨。发明效果根据本发明,能够提供一种能够形成色相、彩度及着色力(印相浓度)优异,且耐光性、耐臭氧性及耐湿性优异的图像,而且喷墨打印中的吐出稳定性也优异的着色组合物、使用了上述着色组合物的喷墨记录用油墨、使用了上述喷墨记录用油墨的喷墨记录方法及填充有上述喷墨记录用油墨的喷墨打印机墨盒。附图说明图1为表示例示化合物(1-11)的二甲基亚砜-d6中的1H-NMR(nuclearmagneticresonance:核磁共振)谱的图。图2为表示例示化合物(1-18)的二甲基亚砜-d6中的1H-NMR谱的图。图3为表示例示化合物(1-26)的二甲基亚砜-d6中的1H-NMR谱的图。图4为表示例示化合物(1-30)的二甲基亚砜-d6中的1H-NMR谱的图。具体实施方式以下,对本发明进行说明。首先,将本发明中的取代基的具体例定义为取代基组A。(取代基组A)作为例子,可举出卤原子、烷基、芳烷基、烯基、炔基、芳基、杂环基、氰基、羟基、硝基、烷氧基、芳氧基、甲硅烷氧基、杂环氧基、酰氧基、氨基甲酰氧基、烷氧基羰氧基、芳氧基羰氧基、氨基、酰氨基、氨基羰基氨基、烷氧基羰基氨基、芳氧基羰基氨基、氨磺酰基氨基、烷基或芳基磺酰基氨基、巯基、烷硫基、芳硫基、杂环硫基、氨磺酰基、烷基或芳基亚磺酰基、烷基或芳基磺酰基、酰基、芳氧羰基、烷氧羰基、氨基甲酰基、芳基或杂环偶氮基、酰亚胺基、膦基、氧膦基、氧膦基氧基、氧膦基氨基、甲硅烷基、离子性亲水基团。这些取代基可进一步被取代,作为进一步的取代基,能够举出选自以上说明的取代基组A的基团。作为卤原子,例如可举出氟原子、氯原子、溴原子或碘原子。作为烷基,可举出直链、分支、环状的经取代或未经取代的烷基,还包含环烷基、二环烷基、环结构更多的三环结构等。以下说明的取代基中的烷基(例如,烷氧基、烷硫基的烷基)也表示这种概念的烷基。作为烷基,优选为碳原子数1至30的烷基,例如可举出甲基、乙基、正丙基、异丙基、叔丁基、正辛基、二十烷基、2-氯乙基、2-氰乙基、2-乙基己基等,作为环烷基,优选为碳原子数3至30的经取代或未经取代的环烷基,例如可举出环己基、环戊基、4-正十二环己基等,作为二环烷基,优选为碳原子数5至30的经取代或未经取代的二环烷基即从碳原子数5至30的二环烷烃去除1个氢原子的一价基团,例如可举出二环[1,2,2]庚烷-2-基、二环[2,2,2]辛烷-3-基等。作为芳烷基,可举出经取代或未经取代的芳烷基,作为经取代或未经取代的芳烷基,优选为碳原子数7~30的芳烷基。例如可举出苄基及2-苯乙基。作为烯基,可举出直链、分支、环状的经取代或未经取代的烯基,包含环烯基、二环烯基。作为烯基,优选举出碳原子数2至30的经取代或未经取代的烯基,例如乙烯基、烯丙基、异戊二烯基、香叶基、油烯基等,作为环烯基,优选举出碳原子数3至30的经取代或未经取代的环烯基即从碳原子数3至30的环烯烃去除1个氢原子的一价基团,例如2-环戊烯-1-基、2-环己烯-1-基等,作为二环烯基,可举出经取代或未经取代的二环烯基、优选为碳原子数5至30的经取代或未经取代的二环烯基即去除具有1个双键的二环烯烃的1个氢原子的一价基团,例如二环[2,2,1]庚-2-烯-1-基、二环[2,2,2]辛-2-烯-4-基等。作为炔基,优选举出碳原子数2至30的经取代或未经取代的炔基,例如乙炔基、炔丙基、三甲基甲硅烷基乙炔基等。作为芳基,优选举出碳原子数6至30的经取代或未经取代的芳基,例如苯基、对甲苯基、萘基、间氯苯基、邻十六酰氨基苯基等。作为杂环基,优选举出从5或6元的经取代或未经取代的芳香族或者非芳香族的杂环化合物去除1个氢原子的一价基团,进一步优选为碳原子数3至30的5或6元的芳香族的杂环基,例如2-呋喃基、2-噻吩基、2-嘧啶基、2-苯并噻唑基等。作为非芳香族的杂环基的例子,可举出吗啉基等。作为烷氧基,优选举出碳原子数1至30的经取代或未经取代的烷氧基,例如甲氧基、乙氧基、异丙氧基、叔丁氧基、正辛氧基、2-甲氧基乙氧基等。作为芳氧基,优选举出碳原子数6至30的经取代或未经取代的芳氧基,例如苯氧基、2-甲基苯氧基、4-叔丁基苯氧基、3-硝基苯氧基、2-十四酰基氨基苯氧基等。作为甲硅烷氧基,优选举出碳原子数0至20的经取代或未经取代的甲硅烷氧基,例如三甲基甲硅烷氧基、二苯基甲基甲硅烷氧基等。作为杂环氧基,优选举出碳原子数2至30的经取代或未经取代的杂环氧基,例如1-苯基四唑-5-氧基、2-四氢吡喃基氧基等。作为酰氧基,优选举出甲酰氧基、碳原子数2至30的经取代或未经取代的烷基羰酰氧基、碳原子数6至30的经取代或未经取代的芳基羰酰氧基,例如乙酰氧基、叔戊酰氧基、硬脂酰氧基、苯酰氧基、对甲氧基苯基羰酰氧基等。作为氨基甲酰氧基,优选举出碳原子数1至30的经取代或未经取代的氨基甲酰氧基,例如N,N-二甲基氨基甲酰氧基、N,N-二乙基氨基甲酰氧基、吗啉基羰氧基、N,N-二-正辛基氨基羰氧基、N-正辛基氨基甲酰氧基等。作为烷氧基羰氧基,优选举出碳原子数2至30的经取代或未经取代的烷氧基羰氧基,例如甲氧基羰酰氧基、乙氧基羰酰氧基、叔丁氧基羰酰氧基、正辛基羰酰氧基等。作为芳氧基羰氧基,优选举出碳原子数7至30的经取代或未经取代的芳氧基羰氧基,例如苯氧基羰酰氧基、对甲氧基苯氧基羰酰氧基、对正十六烷氧基苯氧基羰酰氧基等。作为氨基,包含烷基氨基、芳基氨基、杂环氨基,优选举出氨基、碳原子数1至30的经取代或未经取代的烷基氨基、碳原子数6至30的经取代或未经取代的苯胺基,例如甲基氨基、二甲基氨基、苯胺基、N-甲基-苯胺基、二苯基氨基、三嗪基氨基等。作为酰氨基,优选举出甲酰基氨基、碳原子数1至30的经取代或未经取代的烷基羰基氨基、碳原子数6至30的经取代或未经取代的芳基羰基氨基,例如乙酰基氨基、叔戊酰基氨基、月桂酰基氨基、苯甲酰基氨基、3,4,5-三-正辛氧基苯基羰基氨基等。作为氨基羰基氨基,优选举出碳原子数1至30的经取代或未经取代的氨基羰基氨基,例如氨基甲酰基氨基、N,N-二甲基氨基羰基氨基、N,N-二乙基氨基羰基氨基、吗啉羰基氨基等。作为烷氧基羰基氨基,优选举出碳原子数2至30的经取代或未经取代的烷氧基羰基氨基,例如甲氧基羰基氨基、乙氧基羰基氨基、叔丁氧基羰基氨基、正十八烷氧基羰基氨基、N-甲基-甲氧基羰基氨基等。作为芳氧基羰基氨基,优选举出碳原子数7至30的经取代或未经取代的芳氧基羰基氨基,例如苯氧基羰基氨基、对氯苯氧基羰基氨基、间正辛氧基苯氧基羰基氨基等。作为氨磺酰基氨基,优选举出碳原子数0至30的经取代或未经取代的氨磺酰基氨基,例如氨磺酰基氨基、N,N-二甲基氨基磺酰基氨基、N-正辛基氨基磺酰基氨基等。作为烷基或芳基磺酰基氨基,优选举出碳原子数1至30的经取代或未经取代的烷基磺酰基氨基、碳原子数6至30的经取代或未经取代的芳基磺酰基氨基,例如甲基磺酰基氨基、丁基磺酰基氨基、苯基磺酰基氨基、2,3,5-三氯苯基磺酰基氨基、对甲苯基磺酰基氨基等。作为烷硫基,优选举出碳原子数1至30的经取代或未经取代的烷硫基,例如甲基硫基、乙基硫基、正十六烷硫基等。作为芳硫基,优选举出碳原子数6至30的经取代或未经取代的芳硫基,例如苯硫基、对氯苯硫基、间甲氧基苯硫基等。作为杂环硫基,优选举出碳原子数2至30的经取代或未经取代的杂环硫基,例如2-苯并噻唑基硫基、1-苯基四唑-5-基硫基等。作为氨磺酰基,优选举出碳原子数0至30的经取代或未经取代的氨磺酰基,例如N-乙基氨磺酰基、N-(3-十二烷氧基丙基)氨磺酰基、N,N-二甲基氨磺酰基、N-乙酰基氨磺酰基、N-苯甲酰基氨磺酰基、N-(N’-苯基氨基甲酰基)氨磺酰基等。作为烷基或芳基亚磺酰基,优选举出碳原子数1至30的经取代或未经取代的烷基亚磺酰基、碳原子数6至30的经取代或未经取代的芳基亚磺酰基,例如甲基亚磺酰基、乙基亚磺酰基、苯基亚磺酰基、对甲苯基亚磺酰基等。作为烷基或芳基磺酰基,优选举出碳原子数1至30的经取代或未经取代的烷基磺酰基、碳原子数6至30的经取代或未经取代的芳基磺酰基,例如甲基磺酰基、乙基磺酰基、苯基磺酰基、对甲苯基磺酰基等。作为酰基,优选举出甲酰基、碳原子数2至30的经取代或未经取代的烷基羰基、碳原子数7至30的经取代或未经取代的芳基羰基、通过碳原子数2至30的经取代或未经取代的碳原子与羰基键合的杂环羰基,例如乙酰基、新戊酰基、2-氯乙酰基、硬脂酰基、苯甲酰基、对正辛氧基苯基羰基、2-吡啶基羰基、2-呋喃基羰基等。作为芳氧羰基,优选举出碳原子数7至30的经取代或未经取代的芳氧羰基,例如苯氧基羰基、邻苯氯苯氧基羰基、间硝基苯氧基羰基、对叔丁基苯氧基羰基等。作为烷氧羰基,优选举出碳原子数2至30的经取代或未经取代的烷氧羰基,例如甲氧基羰基、乙氧基羰基、叔丁氧基羰基、正十八烷氧基羰基等。作为氨基甲酰基,优选举出碳原子数1至30的经取代或未经取代的氨基甲酰基,例如氨基甲酰基、N-甲基氨基甲酰基、N,N-二甲基氨基甲酰基、N,N-二-正辛基氨基甲酰基、N-(甲基磺酰基)氨基甲酰基等。作为芳基或杂环偶氮基,优选举出碳原子数6至30的经取代或未经取代的芳基偶氮基、碳原子数3至30的经取代或未经取代的杂环偶氮基,例如苯基偶氮基、对氯苯基偶氮基、5-乙硫基-1,3,4-噻二唑-2-基偶氮基等。作为酰亚胺基,优选举出N-琥珀酰亚胺基、N-邻苯二甲酰亚胺基等。作为膦基,优选举出碳原子数0至30的经取代或未经取代的膦基,例如二甲基膦基、二苯基膦基、甲基苯氧基膦基等。作为氧膦基,优选举出碳原子数0至30的经取代或未经取代的氧膦基,例如氧膦基、二辛氧基氧膦基、二乙氧基氧膦基等。作为氧膦基氧基,优选举出碳原子数0至30的经取代或未经取代的氧膦基氧基,例如二苯氧基氧膦基氧基、二辛氧基氧膦基氧基等。作为氧膦基氨基,优选举出碳原子数0至30的经取代或未经取代的氧膦基氨基,例如二甲氧基氧膦基氨基、二甲基氨基氧膦基氨基。作为甲硅烷基,优选举出碳原子数0至30的经取代或未经取代的甲硅烷基,例如三甲基甲硅烷基、叔丁基二甲基甲硅烷基、苯基二甲基甲硅烷基等。作为离子性亲水基团,可举出磺基、羧基、硫代羧基、亚磺基、膦酰基、二羟基膦基、4级铵基等。尤其优选为磺基、羧基。并且,离子性亲水性基团可以包含阳离子或阴离子,将包含阳离子或阴离子的状态称为盐的状态。羧基、膦酰基及磺基可以是盐的状态,形成盐的抗衡阳离子的例子中包含铵离子、碱金属离子(例如,锂离子、钠离子、钾离子)及有机阳离子(例如,四甲基铵离子、四甲基胍离子、四甲基鏻离子),优选为锂盐、钠盐、钾盐、铵盐,更优选为钠盐或以钠盐为主成分的混合盐,最优选为钠盐。另外,本发明中,当化合物为盐时,水溶性油墨中,盐解离在离子中而存在。〔通式(1)所表示的化合物〕对下述通式(1)所表示的化合物进行说明。[化学式7]通式(1)通式(1)中,R1、R5、R6及R10各自独立地表示烷基。R4、R9、R11、R12、R13、R14、R15、R16、R17、R18、R19及R20各自独立地表示氢原子或取代基。R2、R3、R7及R8各自独立地表示氢原子、烷基或下述通式(A)所表示的取代基,R2、R3、R7及R8中的至少1个表示下述通式(A)所表示的取代基。[化学式8]通式(A)通式(A)中,X表示下述通式(X1)、通式(X2)或通式(X3)所表示的取代基。*表示与苯环键合的键合键。[化学式9]通式(X1)通式(X1)中,R401、R402、R403、R404及R405各自独立地表示氢原子或取代基。其中,R401、R402、R403、R404及R405满足下述条件(i)或(ii)。*表示与硫原子键合的键合键。条件(i):R401、R402、R403、R404及R405中的至少1个表示羟基,且至少1个表示羧基。条件(ii):R401、R402、R403、R404及R405中的至少2个表示羧基。[化学式10]通式(X2)通式(X2)中,R501、R502、R503、R504、R505、R506及R507各自独立地表示氢原子或取代基。其中,R501、R502、R503、R504、R505、R506及R507满足下述条件(iii)或(iv)。*表示与硫原子键合的键合键。条件(iii):R501、R502、R503、R504、R505、R506及R507中的至少1个表示羟基,且至少1个表示羧基。条件(iv):R501、R502、R503、R504、R505、R506及R507中的至少2个表示羧基。[化学式11]通式(X3)通式(X3)中,R601、R602、R603、R604、R605、R606及R607各自独立地表示氢原子或取代基。其中,R601、R602、R603、R604、R605、R606及R607满足下述条件(v)或(vi)。*表示与硫原子键合的键合键。条件(v):R601、R602、R603、R604、R605、R606及R607中的至少1个表示羟基,且至少1个表示羧基。条件(vi):R601、R602、R603、R604、R605、R606及R607中的至少2个表示羧基。通式(1)中,R11、R13、R14、R16、R17、R18、R19及R20各自独立地表示氢原子或取代基。当R11、R13、R14、R16、R17、R18、R19及R20表示取代基时,作为取代基可举出选自上述取代基组A中的取代基。优选R11、R13、R14、R16、R17、R18、R19及R20表示氢原子。通式(1)中,R1、R5、R6及R10各自独立地表示烷基,从原材料的获得性和合成的容易性的观点考虑,优选为碳原子数1~6的烷基,更优选为碳原子数1~3的烷基,进一步优选为甲基或乙基。并且,R1、R5、R6及R10所所表示的烷基可以具有取代基,作为取代基可举出选自上述取代基组A中的取代基。通式(1)中,R4、R9、R12及R15各自独立地表示氢原子或取代基。作为R4、R9、R12及R15表示取代基的情况下的取代基,优选为烷基或离子性亲水性基团。作为烷基,优选为碳原子数1~6的烷基,更优选为碳原子数1~3的烷基,进一步优选为甲基或乙基,尤其优选为甲基。作为离子性亲水性基团,优选为羧基、磺基或膦酰基。作为离子性亲水性基团的抗衡阳离子,可举出氢原子(质子)、碱金属阳离子(锂离子、钠离子或钾离子)、铵离子等,但从合成容易性(作为染料粉末的操作容易性)的观点考虑,优选为碱金属阳离子。优选R4、R9、R12及R15中的至少1个表示离子性亲水性基团,更优选2个以上表示离子性亲水性基团。优选R12及R15表示离子性亲水性基团,且R4及R9表示氢原子,或R4及R9表示离子性亲水性基团,且R12及R15表示氢原子,更优选R12及R15表示离子性亲水性基团,且R4及R9表示氢原子。优选R4及R9各自独立地表示氢原子、磺基或羧基,更优选表示氢原子或磺基。优选R12及R15各自独立地表示氢原子、磺基或羧基,更优选表示氢原子或磺基。通式(1)中,R2、R3、R7及R8各自独立地表示氢原子、烷基或上述通式(A)所表示的取代基,R2、R3、R7及R8中的至少1个表示上述通式(A)所表示的取代基。当R2、R3、R7及R8表示烷基时,优选为碳原子数1~6的烷基,更优选为碳原子数1~3的烷基,进一步优选为甲基或乙基。并且,R2、R3、R7及R8所所表示的烷基可以具有取代基,作为取代基可举出选自上述取代基组A中的取代基。优选R2及R7各自独立地表示通式(A)所表示的取代基,且R3及R8表示烷基,或R3及R8各自独立地表示通式(A)所表示的取代基,且R2及R7表示烷基,更优选R2及R7各自独立地表示通式(A)所表示的取代基,且R3及R8表示烷基。通式(A)中,X表示上述通式(X1)、通式(X2)或通式(X3)所表示的取代基。另外,作为通式(X1)、通式(X2)或通式(X3)中的羧基的抗衡阳离子,可举出氢原子(质子)、碱金属阳离子(锂离子、钠离子、或钾离子)、铵离子等,但优选为碱金属阳离子。通式(X1)中,R401、R402、R403、R404及R405各自独立地表示氢原子或取代基。其中,R401、R402、R403、R404及R405满足下述条件(i)或(ii)。条件(i):R401、R402、R403、R404及R405中的至少1个表示羟基,且至少1个表示羧基。条件(ii):R401、R402、R403、R404及R405中的至少2个表示羧基。优选通式(X1)中,R401、R402、R403、R404及R405满足上述条件(i)。即,优选R401、R402、R403、R404及R405中的至少1个表示羟基,且至少1个表示羧基。R401、R402、R403、R404及R405中羟基的数量优选为1~3个,更优选为1~2个,进一步优选为1个。羧基的数量更优选为1~3个,进一步优选为1~2个。优选R403表示羟基,且R402表示羧基,或R401表示羟基,且R402表示羧基,更优选R401表示羟基,且R402表示羧基。作为R401、R402、R403、R404及R405表示取代基的情况下的取代基,可举出选自上述取代基组A中的取代基,优选为烷基或烷氧基,更优选为碳原子数1~6的烷基或烷氧基,进一步优选为碳原子数1~3的烷基或烷氧基,尤其优选为甲基或甲氧基。并且,作为R401、R402、R403、R404及R405表示取代基的情况下的取代基,作为与上述不同的方式,可举出羧基、氯原子、硝基或三氟甲基,更优选为羧基、氯原子或硝基,进一步优选为羧基。尤其,当R401表示羟基,且R402表示羧基时,优选R404表示上述取代基(羧基、氯原子、硝基或三氟甲基)。通式(X1)中,当R401、R402、R403、R404及R405满足上述条件(ii)时,优选R402及R404表示羧基。以下示出通式(X1)所表示的基团的具体例,但并不限定于这些。下述具体的化合物的结构式中,Me表示甲基。*表示与硫原子键合的键合键。[化学式12]通式(X2)中,R501、R502、R503、R504、R505、R506及R507各自独立地表示氢原子或取代基。其中,R501、R502、R503、R504、R505、R506及R507满足下述条件(iii)或(iv)。条件(iii):R501、R502、R503、R504、R505、R506及R507中的至少1个表示羟基,且至少1个表示羧基。条件(iv):R501、R502、R503、R504、R505、R506及R507中的至少2个表示羧基。通式(X2)中,优选R501、R502、R503、R504、R505、R506及R507满足条件(iii)。即,优选R501、R502、R503、R504、R505、R506及R507中的至少1个表示羟基,且至少1个表示羧基。作为R501、R502、R503、R504、R505、R506及R507表示取代基的情况下的取代基,可举出选自上述取代基组A中的取代基,优选为烷基或烷氧基,更优选为碳原子数1~6的烷基或烷氧基,进一步优选为碳原子数1~3的烷基或烷氧基,尤其优选为甲基或甲氧基。R501、R502、R503、R504、R505、R506及R507中羟基的数量优选为1~3个,更优选为1~2个,进一步优选为1个。羧基的数量更优选为1~2个,进一步优选为1个。优选R504表示羟基,且R503表示羧基,或R504表示羟基,且R505表示羧基,更优选为R504表示羟基,且R503表示羧基。以下示出通式(X2)所表示的基的具体例,但并不限定于这些。*表示与硫原子键合的键合键。[化学式13]通式(X3)中,R601、R602、R603、R604、R605、R606及R607各自独立地表示氢原子或取代基。其中,R601、R602、R603、R604、R605、R606及R607满足下述条件(v)或(vi)。*表示与硫原子键合的键合键。条件(v):R601、R602、R603、R604、R605、R606及R607中的至少1个表示羟基,且至少1个表示羧基。条件(vi):R601、R602、R603、R604、R605、R606及R607中的至少2个表示羧基。通式(X3)中,优选R601、R602、R603、R604、R605、R606及R607满足条件(v)。即,优选R601、R602、R603、R604、R605、R606及R607中的至少1个表示羟基,且至少1个表示羧基。作为R601、R602、R603、R604、R605、R606及R607表示取代基的情况下的取代基,可举出选自上述取代基组A中的取代基,优选为烷基或烷氧基,更优选为碳原子数1~6的烷基或烷氧基,进一步优选为碳原子数1~3的烷基或烷氧基,尤其优选为甲基或甲氧基。R601、R602、R603、R604、R605、R606及R607中羟基的数量优选为1~3个,更优选为1~2个,进一步优选为1个。羧基的数量更优选为1~2个,进一步优选为1个。优选R606表示羟基,且R605表示羧基,或R603表示羟基,且R602表示羧基,更优选为R606表示羟基,且R605表示羧基。以下示出通式(X3)所表示的基团的具体例,但并不限定于这些。*表示与硫原子键合的键合键。[化学式14]上述通式(1)所表示的化合物优选为下述通式(2)、通式(3)或通式(4)所表示的化合物。[化学式15]通式(2)通式(2)中,R1、R5、R6及R10各自独立地表示烷基。R4、R9、R11、R12、R13、R14、R15、R16、R17、R18、R19及R20各自独立地表示氢原子或取代基。R3及R8各自独立地表示氢原子或烷基。R401、R402、R403、R404及R405各自独立地表示氢原子或取代基。其中,R401、R402、R403、R404及R405满足下述条件(i-1)或(ii-1)。R406、R407、R408、R409及R410各自独立地表示氢原子或取代基。其中,R406、R407、R408、R409及R410满足下述条件(i-2)或(ii-2)。条件(i-1):R401、R402、R403、R404及R405中的至少1个表示羟基,且至少1个表示羧基。条件(ii-1):R401、R402、R403、R404及R405中的至少2个表示羧基。条件(i-2):R406、R407、R408、R409及R410中的至少1个表示羟基,且至少1个表示羧基。条件(ii-2):R406、R407、R408、R409及R410中的至少2个表示羧基。[化学式16]通式(3)通式(3)中,R1、R5、R6及R10各自独立地表示烷基。R4、R9、R11、R12、R13、R14、R15、R16、R17、R18、R19及R20各自独立地表示氢原子或取代基。R3及R8各自独立地表示氢原子或烷基。R501、R502、R503、R504、R505、R506及R507各自独立地表示氢原子或取代基。其中,R501、R502、R503、R504、R505、R506及R507表示下述条件(iii-1)或(iv-1)。R508、R509、R510、R511、R512、R513及R514各自独立地表示氢原子或取代基。其中,R508、R509、R510、R511、R512、R513及R514满足下述条件(iii-2)或(iv-2)。条件(iii-1):R501、R502、R503、R504、R505、R506及R507中的至少1个表示羟基,且至少1个表示羧基。条件(iv-1):R501、R502、R503、R504、R505、R506及R507中的至少2个表示羧基。条件(iii-2):R508、R509、R510、R511、R512、R513及R514中的至少1个表示羟基,且至少1个表示羧基。条件(iv-2):R508、R509、R510、R511、R512、R513及R514中的至少2个表示羧基。[化学式17]通式(4)通式(4)中,R1、R5、R6及R10各自独立地表示烷基。R4、R9、R11、R12、R13、R14、R15、R16、R17、R18、R19及R20各自独立地表示氢原子或取代基。R3及R8各自独立地表示氢原子或烷基。R601、R602、R603、R604、R605、R606及R607各自独立地表示氢原子或取代基。其中,R601、R602、R603、R604、R605、R606及R607满足下述条件(v-1)或(vi-1)。R608、R609、R610、R611、R612、R613及R614各自独立地表示氢原子或取代基。其中,R608、R609、R610、R611、R612、R613及R614满足下述条件(v-2)或(vi-2)。条件(v-1):R601、R602、R603、R604、R605、R606及R607中的至少1个表示羟基,且至少1个表示羧基。条件(vi-1):R601、R602、R603、R604、R605、R606及R607中的至少2个表示羧基。条件(v-2):R608、R609、R610、R611、R612、R613及R614中的至少1个表示羟基,且至少1个表示羧基。条件(vi-2):R608、R609、R610、R611、R612、R613及R614中的至少2个表示羧基。通式(2)中的R1、R4、R5、R6、R9、R10、R11、R12、R13、R14、R15、R16、R17、R18、R19及R20的定义各自与通式(1)中的R1、R4、R5、R6、R9、R10、R11、R12、R13、R14、R15、R16、R17、R18、R19及R20相同,优选的范围也相同。通式(2)中的R3及R8各自独立地表示氢原子或烷基,优选表示烷基。作为烷基,优选为碳原子数1~6的烷基,更优选为碳原子数1~3的烷基,进一步优选为甲基或乙基。并且,烷基可以具有取代基,作为取代基可举出选自上述取代基组A中的取代基。通式(2)中的R401、R402、R403、R404及R405优选满足上述条件(i-1)。即,优选R401、R402、R403、R404及R405中的至少1个表示羟基,且至少1个表示羧基。R401、R402、R403、R404及R405的优选的范围与各通式(X1)中的R401、R402、R403、R404及R405相同。通式(2)中的R406、R407、R408、R409及R410优选满足上述条件(i-2)。即,优选R406、R407、R408、R409及R410中的至少1个表示羟基,且至少1个表示羧基。R406、R407、R408、R409及R410的优选的范围与各通式(2)中的R401、R402、R403、R404及R405相同。通式(3)中的R1、R4、R5、R6、R9、R10、R11、R12、R13、R14、R15、R16、R17、R18、R19及R20的定义各自与通式(1)中的R1、R4、R5、R6、R9、R10、R11、R12、R13、R14、R15、R16、R17、R18、R19及R20相同,优选的范围也相同。通式(3)中的R3及R8各自独立地表示氢原子或烷基,优选表示烷基。作为烷基,优选为碳原子数1~6的烷基,更优选为碳原子数1~3的烷基,进一步优选为甲基或乙基。并且,烷基可以具有取代基,作为取代基可举出选自上述取代基组A中的取代基。通式(3)中的R501、R502、R503、R504、R505、R506及R507优选满足上述条件(iii-1)。即,优选R501、R502、R503、R504、R505、R506及R507中的至少1个表示羟基,且至少1个表示羧基。R501、R502、R503、R504、R505、R506及R507的优选的范围与各通式(X2)中的R501、R502、R503、R504、R505、R506及R507相同。通式(3)中的R508、R509、R510、R511、R512、R513及R514优选满足上述条件(iii-2)。即,优选R508、R509、R510、R511、R512、R513及R514中的至少1个表示羟基,且至少1个表示羧基。R508、R509、R510、R511、R512、R513及R514的优选的范围与各通式(3)中的R501、R502、R503、R504、R505、R506及R507相同。通式(4)中的R1、R4、R5、R6、R9、R10、R11、R12、R13、R14、R15、R16、R17、R18、R19及R20的定义各自与通式(1)中的R1、R4、R5、R6、R9、R10、R11、R12、R13、R14、R15、R16、R17、R18、R19及R20相同,优选的范围也相同。通式(4)中的R3及R8各自独立地表示氢原子或烷基,优选表示烷基。作为烷基,优选为碳原子数1~6的烷基,更优选为碳原子数1~3的烷基,进一步优选为甲基或乙基。并且,烷基可以具有取代基,作为取代基可举出选自上述取代基组A中的取代基。通式(4)中的R601、R602、R603、R604、R605、R606及R607优选满足上述条件(v-1)。即,优选R601、R602、R603、R604、R605、R606及R607中的至少1个表示羟基,且至少1个表示羧基。R601、R602、R603、R604、R605、R606及R607的优选的范围与各通式(X3)中的R601、R602、R603、R604、R605、R606及R607相同。通式(4)中的R608、R609、R610、R611、R612、R613及R614优选满足上述条件(v-2)。即,优选R608、R609、R610、R611、R612、R613及R614中的至少1个表示羟基,且至少1个表示羧基。R608、R609、R610、R611、R612、R613及R614的优选的范围与各通式(4)中的R601、R602、R603、R604、R605、R606及R607相同。以下举出通式(1)所表示的化合物的具体例,但并不限定于这些。下述具体的化合物的结构式中,Me表示甲基,Et表示乙基。[化学式18][化学式19][化学式20][化学式21][化学式22][化学式23]另外,通过实施例例示通式(1)所表示的化合物的具体的合成法。〔通式(D)所表示的化合物〕[化学式24]通式(D)中,Z1表示哈米特取代基常数σp值为0.20以上的吸电子基团。Z2表示氢原子、脂肪族基团、芳香族基团、酰基或杂环基。R23及R24分别独立地表示氢原子、脂肪族基团、芳香族基团、杂环基、酰基、烷氧基羰基、芳氧基羰基、氨基甲酰基、烷基磺酰基、芳基磺酰基或氨磺酰基。其中,R23及R24不会同时为氢原子。R21及R22分别独立地表示氢原子、卤素原子、脂肪族基团、芳香族基团、杂环基、氰基、羧基、氨基甲酰基、烷氧基羰基、芳氧基羰基、酰基、羟基、烷氧基、芳氧基、甲硅烷氧基、酰氧基、氨基甲酰氧基、杂环氧基、烷氧基羰基氧基、芳氧基羰基氧基、烷基氨基、芳基氨基、杂环氨基、酰氨基、脲基、氨磺酰基氨基、烷氧基羰基氨基、芳氧基羰基氨基、烷基或芳基磺酰基氨基、芳氧基羰基氨基、硝基、烷基或芳基硫基、烷基或芳基磺酰基、烷基或芳基亚磺酰基、氨磺酰基、磺基或杂环硫基。并且,R21与R23或R23与R24可以键合而形成5或6元环。R25及R29分别独立地表示烷基、烷氧基或卤素原子。其中,当R25及R29同时为烷基时,构成该烷基的碳原子数的合计为3以上,它们可以进一步被取代。R26、R27及R28的定义分别独立地与R21及R22相同,R25与R26、或R28与R29可以彼此缩合成环。Q表示氢原子、脂肪族基团、芳香族基团或杂环基。上述Z1、Z2、R21、R22、R23、R24及Q的各基团还可以具有取代基。其中,通式(D)具有至少1个离子性亲水性基团。通式(D)中,Z1表示哈米特取代基常数σp值为0.20以上的吸电子基团。(哈米特取代基常数σp值)对本说明书中所使用的哈米特取代基常数σp值进行说明。哈米特方程为了定量地论述取代基对苯衍生物的反应或平衡造成的影响而在1935年由L.P.Hammett建议的经验法则,其准确性现在被广泛认可。哈米特方程中所求出的取代基常数中有σp值和σm值,这些值能够在许多普通的成书中找到,例如在J.A.Dean编、“Lange’sHandbookofChemistry”第12版、1979年(McGraw-Hill)或“化学领域”增刊、122号、96~103页、1979年(南光堂)中有详细记载。另外,本发明中将各取代基通过哈米特取代基常数σp而限定,或者进行说明,但其并不意味着仅限定于在上述的成书中找到的有已知文献的值的取代基,当然也包括即使其值是未知文献的也在基于哈米特方程进行了测定时包含于该范围内的取代基。Z1的上述吸电子基团为哈米特取代基常数σp值为0.20以上,优选为0.30以上的吸电子基团。作为σp值的上限,优选为1.0以下。作为σp值为0.20以上的吸电子基团的具体例,可举出酰基、酰氧基、氨基甲酰基、烷氧基羰基、芳氧基羰基、氰基、硝基、二烷基膦酰基、二芳基膦酰基、二芳基氧膦基、烷基亚磺酰基、芳基亚磺酰基、烷基磺酰基、芳基磺酰基、磺酰氧基、酰基硫基、氨磺酰基、硫代氰酸酯基、硫代羰基、卤代烷基、卤代烷氧基、卤代芳氧基、卤代烷基氨基、卤代烷基硫基、杂环基、卤素原子、偶氮基、硒基氰酸酯基及经σp值为0.20以上的其它的吸电子性基团取代的芳基。作为Z1,从色相及坚牢性的观点考虑,优选为氰基、硝基或卤素原子,更优选为卤素原子或氰基,最优选为氰基。通式(D)中,Z2表示氢原子、脂肪族基团、芳香族基团、酰基或杂环基。作为脂肪族基团,可举出烷基(直链状或支链状烷基、环烷基)等。作为芳香族基团,可举出芳基等。并且,作为相当于芳香族基团及脂肪族基团的基团,可举出芳烷基。作为烷基,优选为碳原子数为1~12的烷基,更优选为碳原子数1~6的烷基,作为离子,可举出甲基、乙基、丁基、异丙基、叔丁基等。烷基可以具有取代基,作为取代基可举出选自前述取代基组A中的取代基,优选为羟基、烷氧基、氰基、卤素原子及离子性亲水性基团。作为具有取代基的烷基,可举出羟乙基、甲氧基乙基、氰基乙基、三氟甲基、3-磺基丙基及4-磺基丁基等。作为环烷基,优选为碳原子数为5~12的环烷基,作为例子,可举出环己基等。环烷基可以具有取代基,作为取代基可举出选自前述取代基组A中的取代基,优选为离子性亲水性基团。作为芳烷基,优选为碳原子数为7~12的芳烷基,作为例子,可举出苄基、2-苯乙基等。芳烷基可以具有取代基,作为取代基可举出选自前述取代基组A中的取代基,优选为离子性亲水性基团。作为芳基,优选为碳原子数为6~12的芳基,作为例子,可举出苯基、萘基等。芳基可以具有取代基,作为取代基可举出选自前述取代基组A中的取代基及酰胺基、磺酰胺基、酯基等,优选为烷基、烷氧基、卤素原子、烷基氨基、酰胺基、氨基甲酰基、氨磺酰基、磺酰胺基、羟基、酯基或离子性亲水性基团。作为具有取代基的芳基,可举出对甲苯基、对甲氧基苯基、邻氯苯基及间(3-磺基丙基氨基)苯基等。作为杂环基(含杂原子环基),优选为5元或6元环的杂环基,作为例子,可举出2-吡啶基、2-噻嗯基、2-噻唑基、2-苯并噻唑基、2-苯并噁唑基及2-呋喃基等。杂环基可以具有取代基,作为取代基可举出选自前述取代基组A中的取代基及酰胺基、磺酰胺基、酯基等,优选为酰胺基、氨基甲酰基、氨磺酰基、磺酰胺基、羟基、酯基及离子性亲水性基团。作为酰基,优选为碳原子数为1~12的酰基,作为例子,可举出乙酰基、苯甲酰基等。酰基可以具有取代基,作为取代基可举出选自前述取代基组A中的取代基,优选为离子性亲水性基团。作为Z2,优选为烷基或芳基,更优选为碳原子数3~4的烷基(优选为异丙基、叔丁基)、苯基或从吡唑母核侧看在2位、4位或6位中的任一处进一步具有取代基的苯基,进一步优选为叔丁基。通式(D)中,R23及R24分别独立地表示氢原子、脂肪族基团、芳香族基团、杂环基、酰基、烷氧基羰基、芳氧基羰基、氨基甲酰基、烷基磺酰基、芳基磺酰基或氨磺酰基。作为脂肪族基团,可举出烷基、环烷基、烯基、炔基等。作为芳香族基团,可举出芳基等。并且,作为相当于芳香族基团及脂肪族基团的基团,可举出芳烷基。其中,R23及R24不会同时为氢原子。作为烷基、环烷基、芳烷基、芳基、杂环基、酰基,可举出上述Z2中所记载的各基团。各基团还可以具有取代基,取代基的例子也与上述Z2中所记载的例子相同。作为烯基,优选为碳原子数为5~12的烯基,作为例子,可举出乙烯基、烯丙基等。烯基可以具有取代基,作为取代基可举出选自前述取代基组A中的取代基,优选为离子性亲水性基团。作为烷氧基羰基、芳氧基羰基、氨基甲酰基、烷基磺酰基、芳基磺酰基、氨磺酰基、炔基,可举出选自前述取代基组A中的取代基。各基团还可以具有取代基,作为取代基可举出选自前述取代基组A中的取代基。作为R23及R24,从色相的观点考虑,优选分别独立地为氢原子、烷基、环烷基、芳烷基、链烯基、芳香族基团、杂环基、磺酰基、酰基或氨基甲酰基,更优选为氢原子、烷基、芳烷基、芳香族基团、杂环基、磺酰基或酰基,进一步优选为氢原子、芳香族基团或杂环基。尤其优选R23为氢原子或杂环基,R24为芳香族基团。作为杂环基,优选为苯并噁唑基或苯并噻唑基,更具体而言,优选为未经取代或经磺基(还包含盐的状态)取代的苯并噻唑基。作为芳香族基团,优选为经选自烷基及磺基(还包含盐的状态)中的至少1个基团取代的芳基,尤其优选为经选自烷基及磺基中的至少1个基团取代的苯基。上述磺基为盐的状态的情况下的抗衡阳离子的具体例及优选的范围与上述通式(11)所表示的化合物成为盐的情况下的具体例及优选的范围相同。通式(D)中,R21及R22分别独立地表示氢原子、卤素原子、脂肪族基团、芳香族基团、杂环基、氰基、羧基、氨基甲酰基、烷氧基羰基、芳氧基羰基、酰基、羟基、烷氧基、芳氧基、甲硅烷氧基、酰氧基、氨基甲酰氧基、杂环氧基、烷氧基羰基氧基、芳氧基羰基氧基、烷基氨基、芳基氨基、杂环氨基、酰氨基、脲基、氨磺酰基氨基、烷氧基羰基氨基、芳氧基羰基氨基、烷基或芳基磺酰基氨基、芳氧基羰基氨基、硝基、烷基或芳基硫基、烷基或芳基磺酰基、烷基或芳基亚磺酰基、氨磺酰基、磺基或杂环硫基。并且,R21与R23或R23与R24可以键合而形成5或6元环。作为脂肪族基团,可举出烷基、环烷基、烯基、炔基等。作为芳香族基团,可举出芳基等。并且,作为相当于芳香族基团及脂肪族基团的基团,可举出芳烷基。R21及R22所所表示的上述各基团,具体而言可举出选自前述取代基组A中的取代基。各基团还可以具有取代基,作为取代基可举出选自前述取代基组A中的取代基。作为R21及R22,从合成的容易性、耐光性、耐臭氧性的观点考虑,优选为氢原子、烷基、氨基甲酰基或氰基,更优选为氢原子、碳原子数1~4的烷基、氨基甲酰基或氰基。尤其优选R21为氢原子,R22为氢原子或碳原子数1~4的烷基(最优选为甲基)。通式(D)中,R25及R29分别独立地表示烷基、烷氧基或卤素原子。当R25及R29同时为烷基时,构成该烷基的碳原子数的合计为3以上,它们还可以被取代。作为烷基、烷氧基、卤素原子,具体而言,可举出选自前述取代基组A中的取代基。烷基、烷氧基还可以具有取代基,作为取代基可举出选自前述取代基组A中的取代基。从耐光性、耐臭氧性的观点考虑,R25及R29优选为烷基,更优选分别为碳原子数1~3的烷基(优选为甲基、乙基、异丙基)。其中,构成R25及R29的烷基的碳原子数的合计为3以上,优选为碳原子数的合计为3以上且5以下的可以经取代的烷基,更优选为碳原子数的合计为4以上且5以下的未经取代烷基。通式(D)中,R26、R27及R28的定义分别独立地与R21及R22相同,R25与R26、或R28与R29可以彼此缩合成环。R26、R27及R28的具体例与R21及R22的具体例相同,优选的范围也相同,但作为R26、R27及R28,优选为氢原子、烷基或磺基(还包含盐的状态),更优选为氢原子、碳原子数1~4的烷基(最优选为甲基)或磺基。上述磺基为盐的状态的情况下的抗衡阳离子的具体例及优选的范围与上述通式(1)所表示的化合物成为盐的情况下的具体例及优选的范围相同。通式(D)中,Q表示氢原子、脂肪族基团、芳香族基团或杂环基。作为脂肪族基团,可举出烷基、环烷基、烯基等。作为芳香族基团,可举出芳基等。并且,作为相当于芳香族基团及脂肪族基团的基团,可举出芳烷基。作为烷基、环烷基、芳烷基、烯基、芳基、杂环基,具体而言可举出上述R23及R24中所记载的各基团。各基还可以具有取代基,取代基例子也与上述R23及R24中所记载的例子相同。Q优选为经吸电子基团或磺基(还包含盐的状态)取代之芳基或杂环基。上述磺基为盐的状态的情况下的抗衡阳离子的具体例及优选的范围与上述通式(1)所表示的化合物成为盐的情况下的具体例及优选的范围相同。吸电子基团为哈米特取代基常数σp值为0.20以上,优选为0.30以上的吸电子基团。作为σp值的上限,优选为1.0以下。作为σp值为0.20以上的吸电子基团的具体例,可举出上述Z1中所记载的吸电子基团,优选为氰基、硝基、卤素原子。通式(D)所表示的化合物至少具有1个离子亲水性基团。作为上述离子性亲水性基团,从水溶性的观点考虑,优选为选自磺基、羧基、膦酰基及4级铵基中的至少1个基团。作为离子性亲水性基团,优选为选自磺基、羧基及膦酰基中的至少1个基团,其中优选为中羧基、磺基。尤其最优选至少1个为磺基。羧基、膦酰基及磺基可以为盐的状态,形成盐的抗衡离子的例子中包含铵离子、碱金属离子(例,锂离子、钠离子、钾离子)及有机阳离子(例,四甲基铵离子、四甲基胍鎓离子、四甲基鏻离子)。抗衡离子中,优选碱金属盐。碱金属盐中,优选钾离子、钠离子、锂离子,更优选锂离子、钠离子,最优选钠离子。从水溶解性的观点考虑,通式(D)所表示的化合物优选在其分子内具有3个以上且6个以下的离子性亲水性基团,更优选具有3个以上且6个以下的磺基,进一步优选具有3个以上且5个以下的磺基。通式(D)所表示的化合物优选为下述通式(D2)所表示的化合物。[化学式25]通式(D2)中,Z2表示氢原子、脂肪族基团、芳香族基团、酰基或杂环基。R21及R22分别独立地表示氢原子、卤素原子、脂肪族基团、芳香族基团、杂环基、氰基、羧基、氨基甲酰基、烷氧基羰基、芳氧基羰基、酰基、羟基、烷氧基、芳氧基、甲硅烷氧基、酰氧基、氨基甲酰氧基、杂环氧基、烷氧基羰基氧基、芳氧基羰基氧基、烷基氨基、芳基氨基、杂环氨基、酰氨基、脲基、氨磺酰基氨基、烷氧基羰基氨基、芳氧基羰基氨基、烷基或芳基磺酰基氨基、芳氧基羰基氨基、硝基、烷基或芳基硫基、烷基或芳基磺酰基、烷基或芳基亚磺酰基、氨磺酰基、磺基或杂环硫基。R25及R29分别独立地表示烷基、烷氧基或卤素原子。其中,当R25及R29同时为烷基时,构成该烷基的碳原子数的合计为3以上,它们可以进一步被取代。R26、R27及R28的定义分别独立地与R21及R22相同,R25与R26、或R28与R29可以彼此缩合成环。R31、R32、R33、R34、R35、R36、R37、R38、R39、R40、R41、R42及R43分别独立地表示氢原子、脂肪族基团、芳香族基团、杂环基、酰基、烷氧基羰基、芳氧基羰基、氨基甲酰基、烷基磺酰基、芳基磺酰基、氨磺酰基或离子性亲水性基团。M1及M2分别独立地表示氧原子或硫原子。上述Z2、R21、R22的各基团还可以具有取代基。其中,通式(D2)具有至少1个离子性亲水性基团。通式(D2)中,Z2、R21、R22、R25、R26、R27、R28及R29的定义分别与通式(4)中的Z2、R21、R22、R25、R26、R27、R28及R29相同,具体例及优选的范围也相同。通式(D2)中,R31、R32、R33、R34、R35、R36、R37、R38、R39、R40、R41、R42及R43分别独立地表示氢原子、脂肪族基团、芳香族基团、杂环基、酰基、烷氧基羰基、芳氧基羰基、氨基甲酰基、烷基磺酰基、芳基磺酰基、氨磺酰基或离子性亲水性基团。它们的各基团的具体例与通式(D)中的R23及R24中所记载的具体例相同。关于离子性亲水性基团,与前述相同。R31、R32、R33、R34、R35、R36、R37、R38、R39、R40、R41、R42及R43优选为氢原子、烷基或磺基。通式(D2)中,M1及M2分别独立地表示氧原子或硫原子,优选为硫原子。通式(D)所表示的化合物能够通过公知的合成方法(例如日本特开2013-133395号公报中所记载的合成方法)进行合成。以下示出通式(D)所表示的化合物的具体例,但并不限定于下述例子。另外,下述具体例中,磺基可以为盐的状态。[化学式26][化学式27][化学式28][化学式29]〔着色组合物〕本发明的着色组合物包含上述通式(1)所表示的化合物和上述通式(D)所表示的化合物。本发明的着色组合物中所含有的上述通式(1)所表示的化合物可以为一种,也可以为两种以上。并且,本发明的着色组合物中所含有的上述通式(D)所表示的化合物也可以为一种,也可以为两种以上。本发明的着色组合物还能够含有介质,但作为介质而使用了溶剂的情况下尤其作为喷墨记录用油墨而适当。本发明的着色组合物中,作为介质,使用亲油性介质或水性介质,它们中,能够通过对上述通式(1)所表示的化合物进行溶解和/或分散而制作。优选为使用水性介质的情况。本发明的着色组合物中还含有除了介质以外的油墨用组合物。着色组合物中所含有的上述通式(1)所表示的化合物的含量根据所使用的通式(1)所表示的化合物的种类及用于制造着色组合物的溶剂成分的种类等而确定,但着色组合物中的通式(1)所表示的化合物的含量相对于着色组合物的总质量优选包含0.1~20质量%,更优选包含1.0~10质量%,进一步优选包含1.5~10质量%,尤其优选包含2.0~5.0质量%,最优选包含少于2.5~5.0质量。着色组合物中所含有的上述通式(D)所表示的化合物的含量相对于着色组合物的总质量优选包含0.1~3.0质量%,更优选包含0.1~2.5质量%,进一步优选包含0.1~2.0质量%,最优选包含0.1~1.5质量%。着色组合物中所含有的上述通式(1)所表示的化合物与上述通式(D)所表示的化合物的总含量优选为1.0~5.0质量%,更优选为1.0~4.5质量%,进一步优选为1.5~4.0质量%,尤其优选为2.0~4.0质量%,最优选为2.0~3.5质量%。通过将着色组合物中所含有的上述通式(1)所表示的化合物与上述通式(D)所表示的化合物的总含量设为1.0质量%以上,能够使已印刷时的记录介质上的油墨的印相浓度良好。并且,通过将着色组合物中包含的通式(1)所表示的化合物的总计量设为5.0质量%以下,利用喷墨记录方法时,能够使着色组合物的吐出性良好,而且可获得喷墨喷嘴不易堵塞等效果。关于上述通式(1)所表示的化合物的含量与上述通式(D)所表示的化合物的含量的质量比,从色相、彩度、着色力(印相浓度)、耐光性、耐臭氧性及耐湿性的平衡的观点考虑,{通式(1)/通式(D)}优选为{99/1}~{1/99},更优选为{95/5}~{5/95},更优选为{95/5}~{50/50},进一步优选为{90/10}~{60/40},尤其优选为{90/10}~{70/30}。另外,上述通式(1)所表示的化合物的含量与上述通式(D)所表示的化合物的含量的质量比由{通式(1)/通式(D)}表示。更具体而言,由如下质量比表示,即通式(1)所表示的化合物的以质量基准计的含量(W1)与通式(D)所表示的化合物的以质量基准计的含量(WD)的质量比(W1/WD)。本发明的着色组合物可以根据需要而在发挥本发明的效果的范围内含有其他添加剂。本发明的着色组合物作为喷墨记录用油墨而适当使用。[喷墨记录用油墨]喷墨记录用油墨能够通过将通式(1)所表示的化合物及通式(D)所表示的化合物溶解和/或分散于亲油性介质或水性介质中而制作。喷墨记录用油墨优选为使用了水性介质的油墨。喷墨记录用油墨中的通式(1)所表示的化合物的含量、通式(D)所表示的化合物的含量、通式(1)所表示的化合物的含量与通式(D)所表示的化合物的合计的含量的质量比的优选的范围与前述相同。喷墨记录用油墨可以根据需要而在发挥本发明的效果的范围内含有其他添加剂。作为其他添加剂,例如可举出防干燥剂(湿润剂)、防褪色剂、乳化稳定剂、渗透促进剂、紫外线吸收剂、防腐剂、防霉剂、pH调整剂、表面张力调整剂、消泡剂、粘度调整剂、分散剂、分散稳定剂、防锈剂、螯合剂、甜菜碱化合物等公知的添加剂。这些各种添加剂能够在水溶性油墨的情况下直接添加到油墨液中。以分散物形态使用油溶性染料时,通常在制备染料分散物之后添加于分散物,但也可以在制备时添加于油相或水相。防干燥剂是出于防止在喷墨记录方式中所使用的喷嘴的油墨喷射口中因喷墨记录用油墨干燥而引起的堵塞的目的而适当使用。作为防干燥剂,优选蒸汽压比水低的水溶性有机溶剂。作为具体的例子,可列举出以乙二醇、丙二醇、二乙二醇、聚乙二醇、硫二甘醇、二硫二甘醇、2-甲基-1,3-丙二醇、1,2,6-己三醇、乙炔二醇衍生物、甘油、三羟甲基丙烷等为代表的多元醇类、乙二醇单甲基(或乙基)醚、二乙二醇单甲基(或乙基)醚、三乙二醇单乙基(或丁基)醚等多元醇的低级烷基醚类、2-吡咯烷酮、N-甲基-2-吡咯烷酮、1,3-二甲基-2-咪唑啉酮、N-乙基吗啉等杂环类、环丁砜、二甲基亚砜、3-环丁烯砜等含硫化合物、二丙酮醇、二乙醇胺等多官能化合物、脲衍生物。这些中,更优选甘油、二乙二醇等多元醇。另外,上述防干燥剂可以单独使用,也可以同时使用两种以上。这些防干燥剂优选在油墨中含有10~50质量%。渗透促进剂能够以使喷墨记录用油墨更好地渗透到纸中的目的而使用。作为渗透促进剂,能够使用乙醇、异丙醇、丁醇、二(三)乙二醇单丁基醚、1,2-己二醇等醇类或月桂基硫酸钠、油酸钠或非离子性表面活性剂等。只要这些在油墨中含有5~30质量%则通常具有充分的效果,优选在不引起印字的渗洇、印透(printthrough)的添加量的范围内使用。紫外线吸收剂能够以提高图像的保存性的目的而使用。作为紫外线吸收剂,还能够使用日本特开昭58-185677号公报、日本特开昭61-190537号公报、日本特开平2-782号公报、日本特开平5-197075号公报、日本特开平9-34057号公报等中所记载的苯并三唑系化合物、日本特开昭46-2784号公报、日本特开平5-194483号公报、美国专利第3214463号说明书等中所记载的二苯甲酮系化合物、日本特公昭48-30492号公报、日本特公昭56-21141号公报、日本特开平10-88106号公报等中所记载的肉桂酸系化合物、日本特开平4-298503号公报、日本特开平8-53427号公报、日本特开平8-239368号公报、日本特开平10-182621号公报、日本特表平8-501291号公报等中所记载的三嗪系化合物、ResearchDisclosureNo.24239号中所记载的化合物或以芪系、苯并噁唑系化合物为代表的吸收紫外线而发出荧光的化合物、所谓的荧光增白剂。防褪色剂以提高图像的保存性的目的而使用。作为上述防褪色剂,能够使用各种有机系及金属络合物系的防褪色剂。作为有机的防褪色剂,有氢醌类、烷氧基苯酚类、二烷氧基苯酚类、苯酚类、苯胺类、胺类、茚满类、色满类、烷氧基苯胺类、杂环类等,作为金属络合物,有镍络合物、锌络合物等。更具体而言,能够使用ResearchDisclosureNo.17643的第VII的I至J项、ResearchDisclosureNo.15162、ResearchDisclosureNo.18716的650页左栏、ResearchDisclosureNo.36544的527页、ResearchDisclosureNo.307105的872页、ResearchDisclosureNo.15162中引用的专利中所记载的化合物或日本特开昭62-215272号公报的127页~137页中所记载的代表性化合物的通式及化合物例中所包含的化合物。作为防霉剂,可举出脱氢乙酸钠、苯甲酸钠、巯基吡啶-1-氧化钠、对羟基苯甲酸乙酯、1,2-苯并异噻唑啉-3-酮及其盐等。这些在油墨中优选使用0.02~1.00质量%。作为pH调节剂,能够使用上述中和剂(有机碱、无机碱)。关于pH调整剂,以提高喷墨记录用油墨的保存稳定性的目的,优选以喷墨记录用油墨的pH成为6~10的方式来添加,更优选以pH成为7~10的方式来添加。作为表面张力调整剂,可举出非离子、阳离子或阴离子表面活性剂。另外,本发明的喷墨记录用油墨的表面张力优选为25~70mN/m。进一步优选为25~60mN/m。另外,本发明的喷墨记录用油墨的粘度优选为30mPa·s以下。而且更优选调整为20mPa·s以下。作为表面活性剂的例子,优选脂肪酸盐、烷基硫酸酯盐、烷基苯磺酸盐、烷基萘磺酸盐、二烷基磺基琥珀酸盐、烷基磷酸酯盐、萘磺酸福尔马林缩合物、聚氧乙烯烷基硫酸酯盐等阴离子系表面活性剂或聚氧乙烯烷基醚、聚氧乙烯烷基烯丙基醚、聚氧乙烯脂肪酸酯、山梨糖醇苷脂肪酸酯、聚氧乙烯山梨糖醇苷脂肪酸酯、聚氧乙烯烷基胺、甘油脂肪酸酯、氧化乙烯氧化丙烯嵌段共聚物等非离子系表面活性剂。另外,还优选使用乙炔系聚氧乙烯氧化物表面活性剂即SURFYNOLS(AirProducts&Chemicals公司)。另外,还优选N,N-二甲基-N-烷基氧化胺那样的氧化胺型的两性表面活性剂等。而且,还能够使用在日本特开昭59-157,636号的第(37)~(38)页、ResearchDisclosureNo.308119(1989年)中所记载的作为表面活性剂而举出的物质。作为消泡剂,能够根据需要而使用氟系、硅酮系化合物或以EDTA为代表的螯合剂等。甜菜碱化合物能够以防止高湿条件下的图像的渗色为目的而使用。作为甜菜碱化合物,能够优选使用日本特开2004-285269号等中所举出的甜菜碱化合物。这些甜菜碱化合物的添加量根据其种类而优选的范围不同,喷墨记录用油墨中优选使用0.01~10.0质量%,更优选使用0.01~5.0质量%,最优选使用0.01~3.0质量%。水性介质能够使用以水为主成分并根据希望而添加了水混和性有机溶剂的混合物。水混和性有机溶剂的例子中,包括醇(例如、甲醇、乙醇、丙醇、异丙醇、丁醇、异丁醇、仲丁醇、叔丁醇、戊醇、己醇、环己醇、苯甲醇)、多元醇类(例如、乙二醇、二乙二醇、三乙二醇、聚乙二醇、丙二醇、二丙二醇、聚丙二醇、丁二醇、己二醇、戊二醇、甘油、己三醇、硫二甘醇)、甘醇衍生物(例如、乙二醇单甲基醚、乙二醇单乙基醚、乙二醇单丁基醚、二乙二醇单甲基醚、二乙二醇单丁基醚、丙二醇单甲基醚、丙二醇单丁基醚、二丙二醇单甲基醚、三乙二醇单甲基醚、乙二醇二乙酸酯、乙二醇单甲基醚乙酸酯、三乙二醇单甲基醚、三乙二醇单乙基醚、乙二醇单苯基醚)、胺(例如、乙醇胺、二乙醇胺、三乙醇胺、N-甲基二乙醇胺、N-乙基二乙醇胺、吗啉、N-乙基吗啉、乙二胺、二亚乙基三胺、三亚乙基四胺、聚亚乙基亚胺、四甲基亚丙基二胺)及其它的极性溶剂(例如、甲酰胺、N,N-二甲基甲酰胺、N,N-二甲基乙酰胺、二甲基亚砜、环丁砜、2-吡咯烷酮、N-甲基-2-吡咯烷酮、N-乙烯基-2-吡咯烷酮、2-噁唑烷酮、1,3-二甲基-2-咪唑啉酮、乙腈、丙酮)。另外,水混和性有机溶剂可以同时使用两种以上。本发明的喷墨记录用油墨的粘度优选为30mPa·s以下。并且,其表面张力优选为25mN/m以上且70mN/m以下。粘度及表面张力能够通过添加各种添加剂来调整,例如粘度调整剂、表面张力调整剂、比电阻调整剂、皮膜调整剂、紫外线吸收剂、抗氧化剂、褪色防止剂、防霉剂、防锈剂、分散剂及表面活性剂。本发明的喷墨记录用油墨能够使用于各种色调的油墨,优选使用于品红色色调油墨。并且,不仅单色的图像形成,还能够使用于全彩的图像形成中。为了形成全彩图像,能够使用品红色色调油墨、青色色调油墨及黄色色调油墨,并且为了调整色调,还可以使用黑色色调油墨。本发明的喷墨记录用油墨能够使用于印染、复印、标记、笔记、制图、压印等记录方法中,尤其适合于喷墨记录方法中的使用。[喷墨记录方法]关于本发明的喷墨记录方法,对本发明的喷墨记录用油墨供给能量,在公知的图像接收材料、即普通纸、树脂涂布纸、例如日本特开平8-169172号公报、日本特开平8-27693号公报、日本特开平2-276670号公报、日本特开平7-276789号公报、日本特开平9-323475号公报、日本特开昭62-238783号公报、日本特开平10-153989号公报、日本特开平10-217473号公报、日本特开平10-235995号公报、日本特开平10-337947号公报、日本特开平10-217597号公报、日本特开平10-337947号公报等中所记载的喷墨专用纸、薄膜、电子照相共用纸、布帛、玻璃、金属、陶瓷等上形成图像。在形成图像时,以赋予光泽性或耐水性,或者改善耐候性为目的,可以同时使用聚合物微粒分散物(还称为聚合物胶乳)。关于将聚合物胶乳赋予到图像接收材料上的时期,可以是赋予着色剂前,也可以是赋予着色剂后,并且还可以是同时,因此进行添加的地方也既可以是图像接收纸中,也可以是油墨中,或者还可以作为聚合物胶乳单独的液态物而使用。具体而言,能够优选使用日本专利申请2000-363090号、日本专利申请2000-315231号、日本专利申请2000-354380号、日本专利申请2000-343944号、日本专利申请2000-268952号、日本专利申请2000-299465号、日本专利申请2000-297365号等各说明书中所记载的方法。[喷墨打印机墨盒及喷墨记录物]本发明的喷墨记录用墨盒中填充有上述本发明的喷墨记录用油墨。并且,喷墨记录物使用上述本发明的喷墨记录用油墨而在被记录材料上形成着色图像。关于本发明的喷墨记录用油墨,对喷墨的记录方式并无限制,可以用于公知的方式,例如利用静电引力使油墨喷出的电荷控制方式、利用压电元件的振动压力的按需滴落方式(压力脉冲方式)、将电信号转换成声束而对油墨进行照射并利用放射压使油墨喷出的声音喷墨方式及对油墨进行加热而形成气泡并利用所产生的压力的热喷墨方式等。在喷墨记录方式中,包括将称为照片油墨的浓度低的油墨以小的体积而大量喷射的方式、使用实质上为相同的色相且浓度不同的多个油墨来改良图像质量的方式或使用无色透明的油墨的方式。实施例以下,示出实施例对本发明进行详细说明,但本发明并不限定于这些实施例。关于例中的“%”及“份”,除非另有指明,则为质量%及质量份。(合成例)(例示化合物(1-11)的合成)例示化合物(1-11)例如能够按照下述方案而进行合成。[化学式30][化学式31](磺酰荧光素的合成)在室温(20℃)下,向1L的3口烧瓶添加76.4g的糖精、100g的浓硫酸,并将混合液升温至120℃。向其中添加了200g的环丁砜和103.3g的间苯二酚。将添加后的混合液升温至140℃,并在140℃下搅拌了20小时。然后,将所得到的反应液经1小时而冷却至20℃。经30分钟向冷却后的反应液添加500g的水,添加后进一步搅拌了30分钟。对所得到的悬浮液进行过滤,用130mL的水将所得到的晶体喷淋清洗了4次。将喷淋清洗后的晶体在50℃下送风干燥20小时,由此得到了68.5g的磺酰荧光素来作为黄色晶体(产率45%)。(DCSF的合成)向200mL的3口烧瓶添加了36.8g的磺酰荧光素和150g的三氯氧磷。将该混合物升温至105℃,在105℃下搅拌了18小时。然后,经1小时冷却至20℃。向添加有1L的水的2L三口烧瓶,以水温并不超过35℃的方式在20℃的水浴下对烧瓶进行冷却的同时经20分钟添加了所得到的反应液。添加后,在20℃下搅拌了1小时。对所得到的悬浮液进行过滤,将晶体用200mL的水喷淋清洗1次,接着用200mL的乙腈喷淋清洗了2次。将清洗后的晶体在50℃下送风干燥18小时,由此得到了22.7g的二氯磺酞(DCSF)(产率56%)。(中间体(A)的合成)将二氯磺酞(DCSF)30g、2,4,6-三甲基-1,3-亚苯基二胺(TokyoChemicalIndustryCo.,Ltd.制)63g、氯化锌11g添加到乙二醇265g,并在150℃下反应了6小时。将反应液冷却至室温,滴加0.6mol/L盐酸300mL而析出晶体,对所析出的晶体进行过滤,并用水300mL进行了清洗。将所得到的晶体在60℃下干燥12小时而得到了中间体(A)的晶体。产量23g、产率50%、质谱(MS)(m/z)=633([M+1]+、100%)。(中间体(B)的合成)将中间体(A)23.0g添加到10%发烟硫酸420g,并在室温下反应了48小时。将反应液注入到大过量的乙酸乙酯中,并对所析出的晶体进行了过滤。将经过滤的晶体溶解于500mL的甲醇,使用28%甲醇钠甲醇溶液调整为pH7,通过过滤去除了所析出的硫酸钠。使用旋转蒸发器对滤液进行浓缩,并用柱色谱法(填充剂:SephadexLH-20(Pharmacia制)、展开溶剂:甲醇)对所得到的残渣进行纯化而得到了中间体(B)的晶体。产量21.0g、产率68%、质谱(MS)(m/z)=793([M-2Na+H]-、100%)。(例示化合物(1-11)的合成)将中间体(B)3.0g溶解于超纯水15mL,并将内温冷却至10℃以下。以粉体状添加5-氯磺酰水杨酸(用德国专利DE264786号中所记载的方法进行合成)2.55g,在10℃以下的内温下直接使用10%NaOH水溶液而将反应液的pH保持8.0,并直至pH无变化为止持续进行滴加。将所得到的反应液注入到大过量的异丙醇中而对所析出的固体进行了过滤。将所得到的固体溶解于水/甲醇:1/1混合溶剂20mL,用柱色谱法(填充剂:SephadexLH-20(Pharmacia制)、展开溶剂:水/甲醇)纯化之后,使用透析膜(分级分子量3500、Spectra/Por3DialysisMembrane(商品名、SpectrumLaboratories,Inc.)),去除了无机盐及剩余有机溶剂。用稀氢氧化钠水溶液将所得到的水溶液的pH调整为7,并用膜过滤器进行除尘过滤,用旋转蒸发器对所得到的水溶液进行浓缩干燥固化而得到了例示化合物(1-11)的绿色光泽晶体。产量1.5g、产率33%。MS(m/z)=1191([M-1]-、100%)。例示化合物(1-11)的稀释水溶液中的吸收谱的吸收极大波长为532nm,且摩尔吸光系数为87000。将例示化合物(1-11)的二甲基亚砜-d6中的1H-NMR谱示于图1。(例示化合物(1-18)的合成)例示化合物(1-18)例如能够按照下述方案而进行合成。[化学式32]将作为前述例示化合物(1-11)的合成中间体而得到的中间体(B)3.0g溶解于超纯水15mL中,并将内温冷却至10℃以下。以粉体状添加5-氯磺酰基-3-羟基-2-萘甲酸(用德国专利DE264786号中所记载的方法进行合成)2.2g,在10℃以下的内温下直接使用10%NaOH水溶液而将反应液的pH保持7.5,并直至pH无变化为止持续进行滴加。将所得到的反应液注入到大过量的异丙醇中,并对所析出的固体进行了过滤。将所得到的固体溶解于水/甲醇:1/1混合溶剂20mL中,并用柱色谱法(填充剂:SephadexLH-20(Pharmacia制)、展开溶剂:水/甲醇)纯化之后,使用透析膜(分级分子量3500、Spectra/Por3DialysisMembrane(商品名、SpectrumLaboratories,Inc.))去除了无机盐及剩余有机溶剂。使用稀氢氧化钠水溶液将所得到的水溶液的pH调整为7,用膜过滤器进行除尘过滤,并用旋转蒸发器对所得到的水溶液进行浓缩干燥固化而得到了例示化合物(1-18)的绿色光泽晶体。产量1.2g、产率24%。MS(m/z)=1291([M-1]-、100%)。例示化合物(1-18)的稀释水溶液中的吸收谱的吸收极大波长为532nm,且摩尔吸光系数为85000。将例示化合物(1-18)的二甲基亚砜-d6中的1H-NMR谱示于图2。(例示化合物(1-25)的合成)例示化合物(1-25)例如能够按照下述方案进行合成。[化学式33]将作为前述例示化合物(1-11)的合成中间体而得到的中间体(B)3.0g溶解于超纯水15mL中,并将内温冷却至10℃以下。以粉体状添加6-氯磺酰基-2-羟基-1-萘甲酸(用德国专利DE278091号中所记载的方法进行合成)2.2g,在10℃以下的内温下直接使用10%NaOH水溶液而将反应液的pH保持7.5,并直至pH无变化为止持续进行滴加。将所得到的反应液注入到大过量的异丙醇中,并对所析出的固体进行了过滤。将所得到的固体溶解于水/甲醇:1/1混合溶剂20mL中,并用柱色谱法(填充剂:SephadexLH-20(Pharmacia制)、展开溶剂:水/甲醇)纯化之后,使用透析膜(分级分子量3500、Spectra/Por3DialysisMembrane(商品名、SpectrumLaboratories,Inc.))去除了无机盐及剩余有机溶剂。使用稀氢氧化钠水溶液将所得到的水溶液的pH调整为7,用膜过滤器进行除尘过滤,并用旋转蒸发器对所得到的水溶液进行浓缩干燥固化而得到了例示化合物(1-25)的绿色光泽晶体。产量1.3g、产率26%。MS(m/z)=1291([M-1]-、100%)。例示化合物(1-25)的稀释水溶液中的吸收谱的吸收极大波长为532nm,且摩尔吸光系数为83000。(例示化合物(1-26)的合成)例示化合物(1-26)例如能够按照下述方案进行合成。[化学式34]将作为前述例示化合物(1-11)的合成中间体而得到的中间体(B)3.0g溶解于超纯水15mL中,并将内温冷却至10℃以下。以粉体状添加5-氯磺酰基-4-羟基间苯二甲酸(用德国专利DE264786号中所记载的方法进行合成)2.7g,在10℃以下的内温下直接使用10%NaOH水溶液而将反应液的pH保持7.5,并直至pH无变化为止持续进行滴加。将所得到的反应液注入到大过量的异丙醇中,并对所析出的固体进行了过滤。将所得到的固体溶解于水/甲醇:1/1混合溶剂20mL中,并用柱色谱法(填充剂:SephadexLH-20(Pharmacia制)、展开溶剂:水/甲醇)纯化之后,使用透析膜(分级分子量3500、Spectra/Por3DialysisMembrane(商品名、SpectrumLaboratories,Inc.))去除了无机盐及剩余有机溶剂。使用稀氢氧化钠水溶液将所得到的水溶液的pH调整为7,用膜过滤器进行除尘过滤,并用旋转蒸发器对所得到的水溶液进行浓缩干燥固化而得到了例示化合物(1-26)的绿色光泽晶体。产量1.8g、产率36%。MS(m/z)=1279([M-1]-、100%)。例示化合物(1-26)的稀释水溶液中的吸收谱的吸收极大波长为534nm,且摩尔吸光系数为95000。将例示化合物(1-26)的二甲基亚砜-d6中的1H-NMR谱示于图3。(例示化合物(1-30)的合成)例示化合物(1-30)例如能够按照下述方案进行合成。[化学式35]将作为前述例示化合物(1-11)的合成中间体而得到的中间体(B)3.0g溶解于超纯水15mL中。以粉体状添加5-氯磺酰基-间苯二甲酸二甲酯(用德国专利DE278091号中所记载的方法进行合成)2.2g,使用10%NaOH水溶液而将反应液的pH保持5~7,并直至pH无变化为止持续进行滴加。反应结束后,继续添加50%NaOH水溶液3mL,并搅拌了1小时。将所得到的反应液注入到大过量的异丙醇中,并对所析出的固体进行了过滤。将所得到的固体溶解于水/甲醇:1/1混合溶剂20mL中,并用柱色谱法(填充剂:SephadexLH-20(Pharmacia制)、展开溶剂:水/甲醇)纯化之后,使用透析膜(分级分子量3500、Spectra/Por3DialysisMembrane(商品名、SpectrumLaboratories,Inc.))去除了无机盐及剩余有机溶剂。使用稀氢氧化钠水溶液将所得到的水溶液的pH调整为7,用膜过滤器进行除尘过滤,并用旋转蒸发器对所得到的水溶液进行浓缩干燥固化而得到了例示化合物(1-30)的绿色光泽晶体。产量3.7g、产率70%。MS(m/z)=1247([M-1]-、100%)。例示化合物(1-30)的稀释水溶液中的吸收谱的吸收极大波长为532nm,且摩尔吸光系数为82000。将例示化合物(1-30)的二甲基亚砜-d6中的1H-NMR谱示于图4。关于其他例示化合物,能够按照上述方法进行合成。〔实施例1〕向下述成分添加去离子水而使其成为100g之后,在30~40℃下加热的同时搅拌了1小时。然后用10mol/L的氢氧化钠水溶液调整成pH=8.5,用平均孔径0.20μm的微过滤器进行减压过滤而制备了品红色用油墨液1。另外,通式(1)的化合物表示通式(1)所表示的化合物,通式(D)的化合物表示通式(D)所表示的化合物。〔实施例2〕向下述成分添加去离子水而使其成为100g之后,在30~40℃下加热的同时搅拌了1小时。然后用10mol/L的氢氧化钠水溶液调整成pH=8.5,用平均孔径0.20μm的微过滤器进行减压过滤而制备了品红色用油墨液2。(甜菜碱-1)[化学式36]〔实施例3〕向下述成分添加去离子水而使其成为100g之后,在30~40℃下加热的同时搅拌了1小时。然后用10mol/L的氢氧化钠水溶液调整成pH=8.5,用平均孔径0.20μm的微过滤器进行减压过滤而制备了品红色用油墨液3。(甜菜碱-2)[化学式37]〔实施例4〕向下述成分添加去离子水而使其成为100g之后,在30~40℃下加热的同时搅拌了1小时。然后用10mol/L的氢氧化钠水溶液调整成pH=8.5,用平均孔径0.20μm的微过滤器进行减压过滤而制备了品红色用油墨液4。〔实施例5〕向下述成分添加去离子水而使其成为100g之后,在30~40℃下加热的同时搅拌了1小时。然后用10mol/L的氢氧化钠水溶液调整成pH=8.5,用平均孔径0.20μm的微过滤器进行减压过滤而制备了品红色用油墨液5。〔实施例6〕向下述成分添加去离子水而使其成为100g之后,在30~40℃下加热的同时搅拌了1小时。然后用10mol/L的氢氧化钠水溶液调整成pH=8.5,用平均孔径0.20μm的微过滤器进行减压过滤而制备了品红色用油墨液6。〔实施例7〕向下述成分添加去离子水而使其成为100g之后,在30~40℃下加热的同时搅拌了1小时。然后用10mol/L的氢氧化钠水溶液调整成pH=8.5,用平均孔径0.20μm的微过滤器进行减压过滤而制备了品红色用油墨液7。〔实施例8〕向下述成分添加去离子水而使其成为100g之后,在30~40℃下加热的同时搅拌了1小时。然后用10mol/L的氢氧化钠水溶液调整成pH=8.5,用平均孔径0.20μm的微过滤器进行减压过滤而制备了品红色用油墨液8。〔实施例9〕向下述成分添加去离子水而使其成为100g之后,在30~40℃下加热的同时搅拌了1小时。然后用10mol/L的氢氧化钠水溶液调整成pH=8.5,用平均孔径0.20μm的微过滤器进行减压过滤而制备了品红色用油墨液9。〔实施例10〕向下述成分添加去离子水而使其成为100g之后,在30~40℃下加热的同时搅拌了1小时。然后用10mol/L的氢氧化钠水溶液调整成pH=8.5,用平均孔径0.20μm的微过滤器进行减压过滤而制备了品红色用油墨液10。〔实施例11〕替代例示化合物(1-11)而使用了例示化合物(1-18),除此以外,通过与实施例2相同的操作制备了喷墨记录用油墨11。〔实施例12〕替代例示化合物(1-11)而使用了例示化合物(1-19),除此以外,通过与实施例2相同的操作制备了喷墨记录用油墨12。〔实施例13〕替代例示化合物(1-11)而使用了例示化合物(1-20),除此以外,通过与实施例2相同的操作制备了喷墨记录用油墨13。〔实施例14〕替代例示化合物(1-11)而使用了例示化合物(1-25),除此以外,通过与实施例2相同的操作制备了喷墨记录用油墨14。〔实施例15〕替代例示化合物(1-11)而使用了例示化合物(1-26),除此以外,通过与实施例1相同的操作制备了喷墨记录用油墨15。〔实施例16〕替代例示化合物(1-11)而使用了例示化合物(1-26),除此以外,通过与实施例2相同的操作制备了喷墨记录用油墨16。〔实施例17〕替代例示化合物(1-11)而使用了例示化合物(1-29),除此以外,通过与实施例2相同的操作制备了喷墨记录用油墨17。〔实施例18〕替代例示化合物(1-11)而使用了例示化合物(1-30),除此以外,通过与实施例1相同的操作制备了喷墨记录用油墨18。〔实施例19〕替代例示化合物(1-11)而使用了例示化合物(1-30),除此以外,通过与实施例2相同的操作制备了喷墨记录用油墨19。〔实施例20〕替代例示化合物(1-11)而使用了例示化合物(1-34),除此以外,通过与实施例2相同的操作制备了喷墨记录用油墨20。〔实施例21〕替代例示化合物(1-11)而使用了例示化合物(1-35),除此以外,通过与实施例1相同的操作制备了喷墨记录用油墨21。〔实施例22〕替代例示化合物(1-11)而使用了例示化合物(1-35),除此以外,通过与实施例2相同的操作制备了喷墨记录用油墨22。〔实施例23〕替代例示化合物(d-5)而使用了例示化合物(d-3),除此以外,通过与实施例1相同的操作制备了喷墨记录用油墨23。〔实施例24〕替代例示化合物(d-5)而使用了例示化合物(d-3),除此以外,通过与实施例2相同的操作制备了喷墨记录用油墨24。〔实施例25〕替代例示化合物(d-5)而使用了例示化合物(d-4),除此以外,通过与实施例2相同的操作制备了喷墨记录用油墨25。〔实施例26〕替代例示化合物(d-5)而使用了例示化合物(d-9),除此以外,通过与实施例2相同的操作制备了喷墨记录用油墨26。〔实施例27〕替代例示化合物(d-5)而使用了例示化合物(d-17),除此以外,通过与实施例2相同的操作制备了喷墨记录用油墨27。〔实施例28〕向下述成分添加去离子水而使其成为100g之后,在30~40℃下加热的同时搅拌了1小时。然后用10mol/L的氢氧化钠水溶液调整成pH=8.5,用平均孔径0.20μm的微过滤器进行减压过滤而制备了品红色用油墨液28。〔实施例29〕向下述成分添加去离子水而使其成为100g之后,在30~40℃下加热的同时搅拌了1小时。然后用10mol/L的氢氧化钠水溶液调整成pH=8.5,用平均孔径0.20μm的微过滤器进行减压过滤而制备了品红色用油墨液29。〔实施例30〕向下述成分添加去离子水而使其成为100g之后,在30~40℃下加热的同时搅拌了1小时。然后用10mol/L的氢氧化钠水溶液调整成pH=8.5,用平均孔径0.20μm的微过滤器进行减压过滤而制备了品红色用油墨液30。〔实施例31〕向下述成分添加去离子水而使其成为100g之后,在30~40℃下加热的同时搅拌了1小时。然后用10mol/L的氢氧化钠水溶液调整成pH=8.5,用平均孔径0.20μm的微过滤器进行减压过滤而制备了品红色用油墨液31。〔实施例32〕向下述成分添加去离子水而使其成为100g之后,在30~40℃下加热的同时搅拌了1小时。然后用10mol/L的氢氧化钠水溶液调整成pH=8.5,用平均孔径0.20μm的微过滤器进行减压过滤而制备了品红色用油墨液32。〔实施例33〕向下述成分添加去离子水而使其成为100g之后,在30~40℃下加热的同时搅拌了1小时。然后用10mol/L的氢氧化钠水溶液调整成pH=8.5,用平均孔径0.20μm的微过滤器进行减压过滤而制备了品红色用油墨液33。〔实施例34〕向下述成分添加去离子水而使其成为100g之后,在30~40℃下加热的同时搅拌了1小时。然后用10mol/L的氢氧化钠水溶液调整成pH=8.5,用平均孔径0.20μm的微过滤器进行减压过滤而制备了品红色用油墨液34。〔实施例35〕向下述成分添加去离子水而使其成为100g之后,在30~40℃下加热的同时搅拌了1小时。然后用10mol/L的氢氧化钠水溶液调整成pH=8.5,用平均孔径0.20μm的微过滤器进行减压过滤而制备了品红色用油墨液35。〔比较例1〕向下述成分添加去离子水而使其成为100g之后,在30~40℃下加热的同时搅拌了1小时。然后用10mol/L的氢氧化钠水溶液调整成pH=8.5,用平均孔径0.20μm的微过滤器进行减压过滤而制备了品红色用比较油墨液1。〔比较例2〕向下述成分添加去离子水而使其成为100g之后,在30~40℃下加热的同时搅拌了1小时。然后用10mol/L的氢氧化钠水溶液调整成pH=8.5,用平均孔径0.20μm的微过滤器进行减压过滤而制备了品红色用比较油墨液2。〔比较例3〕向下述成分添加去离子水而使其成为100g之后,在30~40℃下加热的同时搅拌了1小时。然后用10mol/L的氢氧化钠水溶液调整成pH=8.5,用平均孔径0.20μm的微过滤器进行减压过滤而制备了品红色用比较油墨液3。〔比较例4〕向下述成分添加去离子水而使其成为100g之后,在30~40℃下加热的同时搅拌了1小时。然后用10mol/L的氢氧化钠水溶液调整成pH=8.5,用平均孔径0.20μm的微过滤器进行减压过滤而制备了品红色用比较油墨液4。〔比较例5〕向下述成分添加去离子水而使其成为100g之后,在30~40℃下加热的同时搅拌了1小时。然后用10mol/L的氢氧化钠水溶液调整成pH=8.5,用平均孔径0.20μm的微过滤器进行减压过滤而制备了品红色用比较油墨液5。〔比较例6〕向下述成分添加去离子水而使其成为100g之后,在30~40℃下加热的同时搅拌了1小时。然后用10mol/L的氢氧化钠水溶液调整成pH=8.5,用平均孔径0.20μm的微过滤器进行减压过滤而制备了品红色用比较油墨液6。〔比较例7〕向下述成分添加去离子水而使其成为100g之后,在30~40℃下加热的同时搅拌了1小时。然后用10mol/L的氢氧化钠水溶液调整成pH=8.5,用平均孔径0.20μm的微过滤器进行减压过滤而制备了品红色用比较油墨液7。〔比较例8〕向下述成分添加去离子水而使其成为100g之后,在30~40℃下加热的同时搅拌了1小时。然后用10mol/L的氢氧化钠水溶液调整成pH=8.5,用平均孔径0.20μm的微过滤器进行减压过滤而制备了品红色用比较油墨液8。〔比较例9〕向下述成分添加去离子水而使其成为100g之后,在30~40℃下加热的同时搅拌了1小时。然后用10mol/L的氢氧化钠水溶液调整成pH=8.5,用平均孔径0.20μm的微过滤器进行减压过滤而制备了品红色用比较油墨液9。〔比较例10〕向下述成分添加去离子水而使其成为100g之后,在30~40℃下加热的同时搅拌了1小时。然后用10mol/L的氢氧化钠水溶液调整成pH=8.5,用平均孔径0.20μm的微过滤器进行减压过滤而制备了品红色用比较油墨液10。〔比较例11〕向下述成分添加去离子水而使其成为100g之后,在30~40℃下加热的同时搅拌了1小时。然后用10mol/L的氢氧化钠水溶液调整成pH=8.5,用平均孔径0.20μm的微过滤器进行减压过滤而制备了品红色用比较油墨液11。〔比较例12〕向下述成分添加去离子水而使其成为100g之后,在30~40℃下加热的同时搅拌了1小时。然后用10mol/L的氢氧化钠水溶液调整成pH=8.5,用平均孔径0.20μm的微过滤器进行减压过滤而制备了品红色用比较油墨液12。〔比较例13〕向下述成分添加去离子水而使其成为100g之后,在30~40℃下加热的同时搅拌了1小时。然后用10mol/L的氢氧化钠水溶液调整成pH=8.5,用平均孔径0.20μm的微过滤器进行减压过滤而制备了品红色用比较油墨液13。〔比较例14〕向下述成分添加去离子水而使其成为100g之后,在30~40℃下加热的同时搅拌了1小时。然后用10mol/L的氢氧化钠水溶液调整成pH=8.5,用平均孔径0.20μm的微过滤器进行减压过滤而制备了品红色用比较油墨液14。〔比较例15〕向下述成分添加去离子水而使其成为100g之后,在30~40℃下加热的同时搅拌了1小时。然后用10mol/L的氢氧化钠水溶液调整成pH=8.5,用平均孔径0.20μm的微过滤器进行减压过滤而制备了品红色用比较油墨液15。[化学式38](图像记录及评价)使用在上述中制备的喷墨记录用油墨,并如下进行图像记录而进行了评价。各实施例及比较例中,通过以下所示的喷墨打印机与记录用纸的组合进行图像记录而进行了评价。关于实施例的喷墨记录用油墨1~27及比较例的喷墨记录用油墨1~11进行了下述评价。将该结果示于表1及表2。另外,表1及表2中,各评价中,将各喷墨记录用油墨装填到墨盒,并用喷墨打印机(SeikoEpsonCorp.;PM-700C)将图像记录到照片用纸(SeikoEpsonCorp.照片纸<光泽>)之后进行了评价。关于实施例的喷墨记录用油墨28~35及比较例的喷墨记录用油墨12~15进行了下述评价。将该结果示于表2。另外,表2中,各评价中,将各喷墨记录用油墨装填到墨盒,并用喷墨打印机(CanonInc.制;PIXUSPro9000MkII)将图像记录到喷墨专用纸(CanonInc.制;照片光泽纸PT-201)之后进行了评价。<色相>用肉眼观察已印相的样品,分三阶段将纯色的品红的情况评价为A,略带红色的接近红色的品红色评价为B,将明显为红紫色的情况评价为C。<彩度>根据颜色特性,并通过下述式对印相物的彩度(C*)进行了计算。关于施加电压50%下的印相图像部分,使用反射浓度计(商品名X-Rite310TR、X-RiteInc.制),测定CIEL*a*b*表色系(国际照明委员会标准(1976年)或JIS(日本工业标准)Z8781-4:2013)中的亮度L*和色度a*及b*,从所得到的值并根据下述算出式求出彩度(C*)而进行评价,并根据下述判定基准进行了评价。[数式1]彩度(C*)=(a*2+b*2)1/2A:C*为90以上时,B:C*为80以上且小于90时C:C*小于80时<印相浓度>通过前述喷墨打印机及记录用纸的组合,并使用各喷墨记录用油墨记录了全面涂布图像(施加电压100%下的印相图像)。使用反射浓度计(商品名X-Rite310TR、X-RiteInc.制)测定所制成的全面涂布图像的印相浓度,分四阶段将印相浓度为2.0以上的情况评价为A,将1.8以上且小于2.0的情况评价为B,将1.7以上且小于1.8的情况评价为C,将小于1.7的情况评价为D。<耐光性>测定刚记录后的图像浓度Ci之后,使用老化试验机(图谱C.165),对图像照射28天氙光(10万勒克斯)之后,再次测定图像浓度Cf1,并从氙光照射前后的图像浓度计算色素残存率而进行了评价。关于图像浓度,使用反射浓度计(商品名X-Rite310TR、X-RiteInc.制)而进行了测定。关于色素残存率,使用初始的图像浓度为1.0±0.2的图像部分而进行了测定。通过下述式求出色素残存率,并根据下述判定基准进行了评价。色素残存率(%)=(Cf1/Ci)×100A:色素残存率为90%以上且小于95%时B:色素残存率为80%以上且小于90%时C:色素残存率小于80%时<耐臭氧性>将干燥空气通入西门子型臭氧发生器的双玻璃管内的同时施加5kV交流电压,使用其在臭氧气体浓度为5±0.1ppm、室温、设定在暗处的箱子内将形成有图像的记录用纸放置3天,使用反射浓度计(商品名X-Rite310TR、X-RiteInc.制)测定臭氧气体下放置后的图像浓度,并从初始的图像浓度Ci和臭氧气体下放置后的图像浓度Cf2计算色素残存率而进行了评价。另外,关于色素残存率,使用初始的图像浓度为1.0±0.2的图像部分进行了测定。关于箱子内的臭氧气体浓度,使用APPLICSCORP.臭氧气体监测器(模型:OZG-EM-01)进行了设定。通过下述式求出色素残存率,并通过下述判定基准进行了评价。色素残存率(%)=(Cf2/Ci)×100A:色素残存率为85%以上且小于90%时B:色素残存率为80%以上且小于85%时C:色素残存率小于80%时<耐湿性>关于高湿条件下的图像的渗色,制作以在正方形彼此之间形成0.5mm的白色背景间隙的方式配置有品红色的1mm×1mm的正方形且3cm×3cm的印刷图案,将该图像样品在45℃相对湿度80%的条件下保存7天之后对白色背景间隙中的品红色染料的渗色进行了观察。具体而言,使用反射浓度计“Spectrilino”(商品名:Gretag公司制)测定暴露于上述条件(45℃、相对湿度80%的条件)之前(刚印刷之后)和在上述条件下保管7天之后的印刷物的OD值,针对刚印刷之后的在上述条件下保管7天之后的白色背景的品红色浓度增加在状态A的绿色过滤器中,将小于0.02的情况设为A,将0.02以上且小于0.05的情况设为B,将0.05以上且小于0.10的情况设为C,将0.10以上的情况设为D。<吐出稳定性>首先,刚制备各喷墨记录用油墨之后,通过前述喷墨打印机及记录用纸的组合,对来自喷墨打印机的所有喷嘴的油墨的吐出进行了确认。然后,输出到各记录用纸100张,并根据以下基准进行了评价,其结果,所有的实施例及比较例中评价结果为“A”。另外,记录用纸的尺寸使用了A4纸。接着,将各喷墨记录用油墨在40℃、相对湿度80%的条件下保持2周之后,再次使用各喷墨记录用油墨并使用与上述相同的组合的喷墨打印机及记录用纸(记录用纸的尺寸为A4),对来自喷墨打印机的所有的喷嘴的油墨的吐出进行了确认。然后,输出到各记录用纸100张,并根据以下基准对吐出稳定性进行了评价。将结果记载在下述表1及表2中。A:从印刷开始至结束为止几乎无印刷错乱B:发生有印刷错乱的输出C:印刷开始至结束为止始终有印刷错乱[表1]色相彩度印相浓度耐光性耐臭氧性耐湿性吐出稳定性备注实施例1AAAAABA本发明实施例2AAAAAAA本发明实施例3AAAAAAA本发明实施例4AAAAAAA本发明实施例5AAAAAAA本发明实施例6AAAAAAA本发明实施例7BBAAAAA本发明实施例8AAAAAAA本发明实施例9AAAAAAA本发明实施例10BBAAAAA本发明实施例11AAAAAAA本发明实施例12AAAAAAA本发明实施例13AAAAAAA本发明实施例14AAAAAAA本发明实施例15AAAAAAA本发明实施例16AAAAAAA本发明实施例17AAAAAAA本发明实施例18AAAAABA本发明实施例19AAAAAAA本发明实施例20AAAAAAA本发明实施例21AAAAABA本发明实施例22AAAAAAA本发明实施例23AAAAABA本发明实施例24AAAAAAA本发明实施例25AAAAAAA本发明实施例26AAAAAAA本发明实施例27AAAAAAA本发明[表2]色相彩度印相浓度耐光性耐臭氧性耐湿性吐出稳定性备注实施例28AAAAAAA本发明实施例29AAAAAAA本发明实施例30AAAAAAA本发明实施例31AAAAAAA本发明实施例32BBAAAAA本发明实施例33BBAAAAA实施例实施例34BBAAAAA实施例实施例35AAAAAAA实施例比较例1BBBAACA比较例比较例2BBBAACA比较例比较例3AACBBBA比较例比较例4AACBBBA比较例比较例5BBCBBCA比较例比较例6AACBBAA比较例比较例7AAACCCA比较例比较例8AAACCCA比较例比较例9CBDBCBB比较例比较例10AAAABCA比较例比较例11AAAABCA比较例比较例12AACBBAA比较例比较例13AACBBAA比较例比较例14BBAABCA比较例比较例15BBAABCA比较例从表1及表2的结果明确可知使用了本发明的化合物的实施例的油墨中,色相、彩度、着色力(印相浓度)、耐光性、耐臭氧性、耐湿性及吐出稳定性均优异。产业上的可利用性根据本发明,能够提供一种能够形成色相、彩度及着色力(印相浓度)优异,且耐光性、耐臭氧性及耐湿性优异的图像,而且喷墨打印机中的吐出稳定性也优异的着色组合物、使用了上述着色组合物的喷墨记录用油墨、使用了上述喷墨记录用油墨的喷墨记录方法及填充有上述喷墨记录用油墨的喷墨打印机墨盒。详细地并参考特定的实施方式对本发明进行了说明,但对于本领域技术人员而言,在不脱离本发明的精神和范围的情况下,可施加各种变更或修正是显而易见的。本申请基于2016年2月24日申请的日本专利申请(特愿2016-032827)、2016年11月9日申请的日本专利申请(特愿2016-219036)及2017年2月21日申请的日本专利申请(特愿2017-030495),并通过参考将其内容编入于此。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1