一种基于半花菁结构测次氯酸根离子的近红外荧光探针、其制备方法及应用与流程
本发明属于有机合成技术领域,具体涉及一种基于半花菁结构测次氯酸根离子的近红外荧光探针以及该探针的制备方法和应用。
背景技术:
作为最重要的内源性活性氧(ros)之一,次氯酸根离子(clo-)不仅具有高度有效的抗菌,杀毒和抗炎,也可以作为适应性免疫的天然佐剂。尽管它对我们的健康有保护作用,但这种体内的强氧化剂的异常水平可以与各种细胞组织反应,并导致组织破坏和细胞损伤,最终导致多种疾病,如关节炎,心血管疾病,肺损伤,肾脏疾病,神经变性,甚至癌症。因此,细胞和生物体中次氯酸根离子的含量应严格控制。
如今,敏感和选择性荧光的可用性荧光探针,可以提供有关生理的重要信息。检测活细胞,组织甚至动物的生化特性,已经开启了生命科学的新视野。荧光成像的优势,包括数据收集的简单性,极好的灵敏度和选择性,空间和时间高分辨率,可视化,实时分析和非破坏性,从而鼓励开发各种化学荧光探针。对于次氯酸根离子具有不同的反应性部分如对甲氧基苯酚,肟,硫酯,硫醚,硫酮,酰肼,硒化物和c=n键。然而,大多数这些探针仍然有一些缺点,如单波长检测,发射波长短,选择性差或交叉敏感性差对其他物种,敏感度低,以及反应时间慢。这些限制激发了我们开发新类型的可用于高灵敏度特异性检测次氯酸根离子,快速响应,以及促进红外或近红外发射在细胞成像中实际应用的荧光探针。在光学传感中方法,比率型荧光探针允许同时检测在两个不同发射波长处的荧光强度,它可以提供内置校准功能来校正多种与分析物无关的因素,例如仪器效率,样品微环境,和探针分子的局部浓度,以及具有精确定量测定的特定分析物的优势。开发用于成像次氯酸根离子的比例荧光探针——特别是与线粒体靶向,是由于次氯酸根离子主要通过细胞内的线粒体产生髓过氧化物酶(mpo)催化还原过氧化氢(h2o2)。
技术实现要素:
本发明目的在于克服现有技术缺陷,本发明提供了一种选择性良好的比率型基于半花菁结构测次氯酸根离子的近红外荧光探针,该探针具有良好的选择性和较高的灵敏度,可适用于待测样品中汞离子含量的荧光检测、目视定性。
本发明还提供了上述基于半花菁结构测次氯酸根离子的近红外荧光探针的制备方法以及应用。
为实现上述目的,本发明采用如下技术方案:
一种反应型测次氯酸根离子的近红外荧光探针,该测次氯酸根离子的近红外荧光探针分子式为c27h26no3+,结构式如下:
上述测次氯酸根离子的近红外荧光探针的制备方法,其包括以下步骤:
1)环己酮与三氯氧磷反应得到化合物1;
2)化合物1与1,3,3-三甲基-2-亚甲基吲哚啉反应得到化合物2;
3)化合物2与化合物3反应得到化合物4;
4)化合物4与二氧化硒反应得到目标产物测次氯酸根离子的近红外荧光探针。
其中,化合物1、化合物2、化合物3和化合物4的结构式分别如下所示:
进一步的,步骤1)具体为:将环己酮、三氯氧磷和溶剂n,n-二甲基甲酰胺于45~55℃加热反应3-5h,反应结束后冰浴静置,析出的黄色固体即为化合物1;三氯氧磷和环己酮的摩尔比为2︰1。
步骤2)具体为:在氮气保护下,将化合物1、1,3,3-三甲基-2-亚甲基吲哚啉、乙酸钠和碘化钾溶于乙酸酐和乙酸组成的混合溶液中,然后于75~85℃加热反应1-2h,反应结束后静置冷却,析出的青铜色固体即为化合物2;化合物1、1,3,3-三甲基-2-亚甲基吲哚啉、乙酸钠和碘化钾的摩尔比为1︰2︰1︰1。
步骤3)具体为:在氮气保护下,将化合物3和k2co3溶于乙腈中获得溶液a,将化合物2溶于乙腈中获得溶液b,将溶液a和溶液b混合后于45~55℃加热反应10-15h,反应结束后,减压蒸除溶剂,并经硅胶柱色谱分离纯化,所得蓝绿色固体即为化合物4;化合物3、k2co3和化合物2的摩尔比为1︰2︰1。
步骤4)具体为:在氮气保护下,将seo2和化合物4加入到乙酸中,并将反应溶液在室温下搅拌0.5~1.5小时,过滤混合物,减压蒸除溶剂,并经硅胶柱色谱分离纯化,所得蓝色固体即为基于半花菁结构测次氯酸根离子的近红外荧光探针;seo2和化合物4的摩尔比为5︰1。
化合物3的合成可参考专利wo2004052314。
本发明还提供了上述基于半花菁结构测次氯酸根离子的近红外荧光探针的应用,具体的,该探针用于生物和环境体系中次氯酸根离子的含量而进行的荧光检测、目视定性检测。检测时,激发波长为335~678nm,荧光响应波长550~750nm。
本发明中所使用的各种原料均为普通市售产品,或者通过本领域技术人员公知的方法或现有技术中公开的方法获得。
本申请合成了一种新的比率型近红外荧光探针用于监测次氯酸根离子的水平。通过次氯酸根离子破坏双键,从而破坏这个分子的共轭程度,发生蓝移。这种双通道响应模式将会实现对次氯酸离子的荧光检测。该探针从蓝色到无色的颜色明显变化,可以通过肉眼直接观察。近红外激发和发射半花菁染料能够避免生物样品的光损伤以及来自天然细胞物种的自体荧光。我们合成了近红外荧光探针,并通过1hnmr,13cnmr和质谱表征分析。探针可以在pbs:乙腈=9:1缓冲液(10mm,ph7.4)中对次氯酸根离子快速响应。这个探针表现出对次氯酸根离子的快速响应和高灵敏度,低检出限。此外,该探针成功应用于滤纸条实验。
本发明是以半花菁为母体,次氯酸根离子使双键断裂,破坏整体共轭结构,荧光强度显著性改变并伴随明显的颜色变化,选取的干扰离子等对检测效果基本没有影响,因而实现了对次氯酸根离子的特应性识别响应,该探针在pbs:乙腈=9:1(10mm,ph7.4)缓冲体系中对次氯酸根离子反应比较迅速,具有良好的选择性和较高的灵敏度,检测限达到52nm,而且成功应用于生物与环境样品中的次氯酸根离子。
附图说明
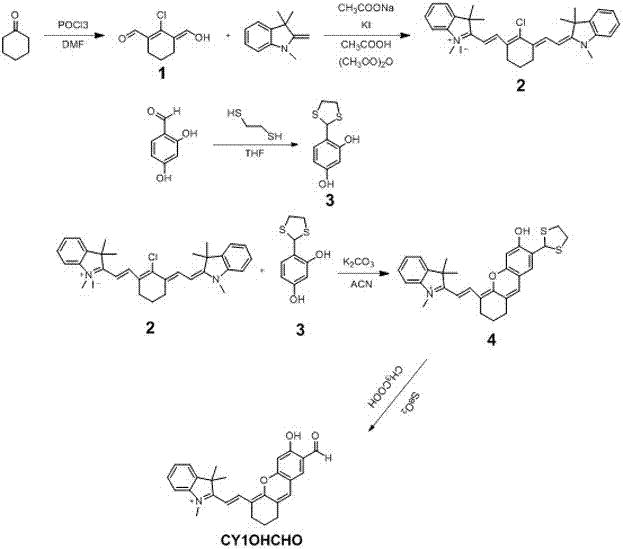
图1:为本发明基于半花菁结构测次氯酸根离子近红外荧光探针的合成路线;
图2:为本发明基于半花菁结构测次氯酸根离子的近红外荧光探针核磁氢谱;
图3:为本发明基于半花菁结构测次氯酸根离子的近红外荧光探针核磁碳谱;
图4:为本发明基于半花菁结构测次氯酸根离子的近红外荧光探针核磁质谱;
图5:为1倍当量的次氯酸根离子加入到本发明近红外荧光探针(10μm)后紫外可见光光谱随时间的变化趋势,插图是可见光下探针的颜色以及探针和次氯酸根离子反应完后的颜色变化;
图6:为1倍当量的次氯酸根离子加入到本发明近红外荧光探针(10μm)后荧光光谱随时间的变化趋势,插图是荧光在335nm做激发波长时荧光强度随时间的变化曲线;
图7:为本发明测次氯酸根离子的近红外荧光探针(10μm)的溶液随次氯酸根离子浓度的增大而呈现的荧光光谱变化,插图是荧光在335nm做激发波长时荧光强度随浓度的变化曲线;
图8:为本发明测次氯酸根离子的近红外荧光探针(10μm)溶液再分别加入10当量的不同离子后荧光光谱在465nm和715nm处取值做荧光强度比(f465/f715)的柱状图,插图是不同离子对探针在465nm和715nm处取值做荧光强度比(f465/f715)的柱状图的放大图;
图9是本发明检出限计算过程中得到的荧光线性关系图。
具体实施方式:
以下通过优选实施例对本发明进一步详细说明,但本发明的保护范围并不局限于此。
实施例:
一种基于半花菁结构测次氯酸根离子的近红外荧光探针,其特征在于,探针分子式为c27h26no3+,结构式如下:
上述基于半花菁结构测次氯酸根离子的近红外荧光探针的制备方法,其合成路线见图1,具体包括以下步骤:
1)化合物1的制备
取n,n-二甲基甲酰胺(10ml),倒入100ml三口烧瓶里,在冰浴中搅拌,并在搅拌条件下缓慢滴加三氯氧磷(4.5ml,0.05mol)和环己酮(2.5g,0.025mol)。然后将混合液在50℃回流反应4h,反应结束后冷却,倒入300g冰中,冰箱内静置冷却过夜,抽滤,得黄色固体2.9g,即为化合物1(收率,52.5%)。
合成路线如下:合成路线如下:
2)化合物2的制备
在氮气保护下,将1,3,3-三甲基-2-亚甲基吲哚啉(0.94g,5.45mmol),化合物1(0.47g,2.72mmol)、乙酸钠(0.22g,2.72mmol)和碘化钾(0.45g,2.72mmol)溶于10ml乙酸酐和10ml乙酸组成的混合溶液中。然后在80℃下加热搅拌1小时,放置冰箱内冷却半个小时,抽滤,滤出物用无水乙醇洗涤后在真空下除去溶剂,再经用柱色谱分离(洗脱剂,v二氯甲烷:v甲醇=100:1),旋蒸出溶剂,真空干燥,得到青铜色固体1.5g,即为化合物2(收率,90%)。化合物2图谱信息如下:
1hnmr(400mhz,cdcl3)δ8.35(d,j=14.1hz,2h),7.44–7.37(m,4h),7.30–7.24(m,2h),7.22(t,j=7.4hz,2h),6.22(d,j=14.1hz,2h),3.76(s,6h),2.75(t,j=6.0hz,4h),2.03–1.91(m,2h),1.73(s,12h).13cnmr(101mhz,cdcl3)δ172.87(s),150.64(s),144.36(s),142.78(s),140.91(s),128.84(s),127.76(s),125.35(s),122.15(s),110.85(s),101.69(s),77.41(s),77.10(s),76.78(s),49.25(s),32.68(s),28.09(s),26.78(s),20.69(s)。
化合物2的合成路线如下:
3)化合物3的制备
在氮气保护下,将1,2-乙二硫醇(0.4ml,4.9mmol)加入到溶有2,4-二羟基苯甲醛(0.5g,3.62mmol)和对甲苯磺酸一水合物(70mg,0.37mmol)的四氢呋喃(10ml)溶液中,室温下搅拌30分钟后,加入无水硫酸镁(1.0g),继续搅拌反应4小时,减压除去溶剂,得到黄色油状粗产物。然后通过硅胶柱色谱(洗脱剂,v乙酸乙酯:v己烷=1:1)进一步分离纯化,得到淡黄色油状液体0.7g,即为化合物3(收率,86%)。
化合物3的合成路线如下:
4)化合物4的制备
在氮气保护下,将化合物3(70mg,0.33mmol)和k2co3(45mg,0.33mmol)加入到25ml乙腈中,在室温下搅拌30min获得溶液a。将化合物2(100mg,0.16mmol)溶于10ml乙腈获得溶液b。通过注射器将溶液b加入到上述溶液a中,然后在50℃条件下加热回流反应10小时。反应结束后,减压蒸除溶剂,通过硅胶柱色谱(洗脱剂,v二氯甲烷:v甲醇=50:1)进一步分离纯化,得到蓝绿色固体57mg,即为目标化合物4(收率,71%)。化合物4图谱信息如下:
1hnmr(400mhz,cdcl3)δ8.07(d,j=13.3hz,1h),7.65(s,1h),7.36(s,1h),7.30(s,1h),7.27(d,j=2.3hz,1h),7.05(t,j=7.4hz,1h),6.84(d,j=7.8hz,1h),6.66(s,1h),6.07(s,1h),5.59(d,j=13.4hz,1h),3.36(s,3h),3.34–3.30(m,4h),2.67(t,j=5.9hz,2h),2.61(t,j=5.8hz,2h),1.94–1.84(m,2h),1.67(s,6h).13cnmr(101mhz,cdcl3)δ179.68(s),165.47(s),159.40(s),158.83(s),143.98(s),140.16(s),139.55(s),138.47(s),131.57(s),128.06(s),126.24(s),122.06(s),116.55(d,j=4.1hz),116.19(s),107.57(s),103.25(s),94.09(s),77.36(s),77.04(s),76.72(s),49.95(s),47.26(s),38.89(s),29.97(s),28.61(s),27.96(s),24.58(s),21.42(s).hrms(m/z):found488.1712[m+h]+,calculated488.1705forc29h30no2s2+。
化合物4的合成路线如下:
(5)目标化合物基于半花菁结构测次氯酸根离子的近红外荧光探针的制备
在氮气保护下,将seo2(114mg,1.05mm)和化合物4(100mg,0.21mm)加入到乙酸(5ml)溶液中,并将反应混合物在室温下搅拌1小时,过滤混合物,减压蒸发溶剂,并通过硅胶柱色谱法(洗脱剂,v二氯甲烷:v甲醇=30:1)进一步分离纯化,得到蓝色固体71mg,即为目标化合物基于半花菁结构测次氯酸根离子的近红外荧光探针(收率,83.5%)。
对制备所得目标化合物基于半花菁结构测次氯酸根离子的近红外荧光探针进行核磁氢谱、核磁碳谱和质谱分析,结果如下(详见图2、3和4):
1hnmr(400mhz,meod)δ10.07(s,1h),8.74(d,j=15.3hz,1h),7.83(s,1h),7.70(d,j=7.3hz,1h),7.64(d,j=7.9hz,1h),7.58(t,j=7.1hz,1h),7.52(t,j=7.3hz,1h),7.24(s,1h),6.88(s,1h),6.65(d,j=15.2hz,1h),3.94(s,3h),2.79–2.67(m,4h),1.97–1.89(m,2h),1.83(s,6h).13cnmr(100mhz,meod)δ177.84(s),161.63(s),159.83(s),154.41(s),145.30(s),142.41(s),141.79(s),134.32(s),128.76(s),127.10(s),126.83(s),126.50(s),123.81(s),122.19(s),114.47(s),114.25(s),112.17(s),103.20(s),101.52(s),99.45(s),50.36(s),31.25(s),28.62(s),26.79(s),26.41(s),23.65(s),19.54(s).hrms(m/z):found412.1910[m+h]+,calculated412.1907forc27h26no3+.
目标化合物的合成路线如下:
荧光检测应用试验
下文中,为描述简便,将本发明制备所得目标化合物“基于半花菁结构测次氯酸根离子的近红外荧光探针”统一简称为“探针cy1ohcho”。
1)检测用储备液的配制:
a.测次氯酸根离子的近红外荧光探针样品溶液(1.00×10-3mol·l-1)的配制:
取0.00412g(m=412.19)探针cy1ohcho溶于10ml乙腈中,配成浓度为1.00×10-3mol·l-1,记为探针cy1ohcho样品溶液;
b.各种阴离子均用去离子水配置成为浓度为1.00×10-4mol·l-1或1.00×10-3mol·l-1或1.00×10-2mol·l-1的溶液;
c.pbs缓冲溶液(0.01mol·l-1,ph=7.4)的配制:
母液配置:0.2mol·l-1k2hpo4:称取78gk2hpo4·12h2o溶于1000ml水中;0.2mol·l-1kh2po4:称取27.2gkh2po4·2h2o,溶于1000ml水中。
0.2mol·l-1pbs母液(ph=7.4):取19ml的0.2mol·l-1kh2po4,81ml0.2mol·l-1k2hpo4,即可。然后取50ml0.2mol·l-1pbs溶液,加水稀释至1000ml即可。
本文实验中使用的缓冲溶液均为pbs(0.01mol·l-1,ph=7.4,10%乙腈),实验用水均为去离子水。
2)检测分析
取3ml缓冲溶液,加入30μl探针cy1ohcho样品溶液(1.00×10-3mol·l-1),再加入探针cy1ohcho样品溶液(1.00×10-3mol·l-1)30μl,于25℃反应,然后进行紫外-可见光光谱扫描,结果如图5所示。由图5可以看出:随着时间的增加,探针cy1ohcho和次氯酸根离子反应,使吸光度降到最低。图5插图为反应前后可见光下的照片,图中肉眼可见次氯酸根离子可以使探针cy1ohcho溶液发生明显的颜色变化,颜色由蓝色变为无色透明溶液。
取3ml缓冲溶液,加入30μl探针cy1ohcho样品溶液(1.00×10-3mol·l-1),再加入次氯酸根离子储备液(1.00×10-3mol·l-1)0-30μl,于25℃反应,然后进行荧光检测,结果如图6所示。从图6中可以看出:在715nm处荧光强度立马降到最低。实验结果表明,探针cy1ohcho加入次氯酸根离子后响应非常迅速,反应时间小于1秒,从而进一步说明此探针的效果非常好。图6插图为在335nm作为激发波长狭缝:2.5/10nm,荧光强度随时间的变化曲线,图中可以看出:在465nm处荧光强度立马增强。
取3ml缓冲溶液,加入30μl探针cy1ohcho样品溶液(1.00×10-3mol·l-1),再加入次氯酸根离子储备液(1.00×10-4mol·l-1)0-30μl,于25℃反应1分钟,然后进行荧光检测,激发波长为678nm,狭缝:2.5/10nm,结果如图7所示。由图7可以看出:随着次氯酸根离子加入当量的增加,探针和次氯酸根离子反应,使荧光强度逐渐降低。图7插图为在335nm作为激发波长,狭缝:10/10nm,荧光强度随次氯酸根离子浓度的变化曲线,由图中可以看出:随着次氯酸根离子加入当量的增加,探针和次氯酸根离子反应,使荧光强度逐渐增加。
取3ml缓冲溶液,加入30μl测次氯酸根离子的近红外荧光探针样品溶液(1.00×10-3mol·l-1),再加入1空白,2100μmonoo-,3100μm1o2,4100μmo2-,5100μm·oh,6100μmno·,7100μmh2o2,8100μms2o32-,9100μmch3coo-,10100μmco32-,11100μms2o32-,12100μmso42-,13100μmhco3-,14100μmhso32-,15100μmcl-,16100μmi-,17100μmf-,18100μmgsh,19100μmcys,20100μmhs-,21100μms2-,22100μmclo-,反应混匀后进行荧光光谱扫描,在25℃下在pbs/acn溶液(v/v=9/1,ph=7.4),我们分别以335nm和678nm处做激发,然后分别在465nm和715nm处取值做荧光强度比(f465/f715),结果如图8所示。由图8中可以看出:我们发现比率型探针对次氯酸根有很好的选择性,荧光强度比是其它离子的大约4200倍。插图:1-21不同离子荧光强度比率(f465/f715)的放大图。
3)检出限
取3ml缓冲溶液,分别每次加入30μl探针cy1ohcho样品溶液(1.00×10-3mol·l-1),分别反应30分钟后进行紫外-可见光光谱扫描,测吸光度,直到吸光度没有明显变化为止,以浓度的倒数为横坐标,吸光度之比为纵坐标进行做图,得如图9所述的线性方程。经计算(3σ/k)得出该探针对次氯酸根的检出限为52nm。
- 还没有人留言评论。精彩留言会获得点赞!