超细气泡发生剂和超细气泡产生方法与流程
文档序号:31999191发布日期:2022-11-02 10:21阅读:131来源:国知局
bubble technology”,arc报告,2016年11月。
11.https://arc.asahi-kasei.co.jp/report/arc_report/pdf/rs-1007.pdf
技术实现要素:
12.技术问题
13.如上所述,用于在不使用气泡产生装置的情况下产生与超细气泡相对应的细气泡的方法尚不是已知的。因此,本发明的一个目的是提供能够产生对应于超细气泡的细气泡的超细气泡发生剂。
14.本发明还旨在提供用于产生超细气泡的方法。此外,本发明旨在提供含超细气泡的液体和所述液体的生产方法。
15.技术方案
16.本发明人进行了广泛的研究以解决以上问题,并且发现,除气体发生组分之外,通过使用(a)包含质量比为78:22至100:0的酸型槐糖脂和内酯型槐糖脂的槐糖脂和(b)脂肪酸或其盐,可以在水中产生对应于超细气泡的细气泡。
17.本发明是作为基于这些发现的进一步研究的结果而完成的,并且包括以下实施方案。
18.对应于超细气泡的细气泡和槐糖脂在下面有时可以分别缩写为“ufb”和“sl”。
19.(i)ufb发生剂
20.(i-1)
21.一种ufb发生剂,包含以下(a)、(b)和(c)的组合:
22.(a)包含比率(质量比)为78:22至100:0的酸型sl和内酯型sl的sl,
23.(b)游离脂肪酸或其盐,和
24.(c)气体发生组分。
25.(i-2)
26.根据项(i-1)所述的ufb发生剂,其中(c)为选自以下的至少一者:二氧化碳气体发生组分、氧气发生组分、氢气发生组分、和氯气发生组分。
27.(i-3)
28.根据项(i-2)所述的ufb发生剂,其中所述二氧化碳气体发生组分为碳酸盐或碳酸氢盐,或者与其对应物的组合;所述氧气发生组分为过氧化氢或与其对应物的组合;所述氢气发生组分为氢化盐、硼氢化盐或盐酸,或者与其对应物的组合;或者所述氯气发生组分为次氯酸盐或与其对应物的组合。
29.(i-4)
30.根据项(i-1)至(i-3)中任一项所述的ufb发生剂,其中所述游离脂肪酸(b)为具有12至20个碳原子的脂肪酸。
31.(i-5)
32.根据项(i-1)至(i-4)中任一项所述的ufb发生剂,所述ufb发生剂为(a)、(b)和(c)的组合物或者其中至少(c)与(a)和(b)分开包装的产品组合。
33.(i-6)
34.根据项(i-1)至(i-5)中任一项所述的ufb发生剂,所述ufb发生剂在向硬度为
30mg/l至200mg/l、并且优选为50mg/l至200mg/l的水中添加时使用。
35.(i-7)
36.根据项(i-6)所述的ufb发生剂,其中使用(a)和(b)使得相对于水,(a)的浓度为0.005质量%或更大、并且优选为0.005质量%至0.04质量%,以及(b)的浓度为0.0001质量%或更大、并且优选为0.0001质量%至0.3质量%。
37.(i-8)
38.根据项(i-7)所述的ufb发生剂,其中使用(c)使得相对于水,(c)的浓度以气体发生体的浓度计为0.1质量%或更大、并且优选为0.1质量%至20质量%。
39.(i-9)
40.根据项(i-1)至(i-8)中任一项所述的ufb发生剂,所述ufb发生剂在硬度为30mg/l至200mg/l的水中产生具有10000cps或更大、并且优选30000cps或更大的散射强度和小于1000nm、并且优选500nm或更小的平均个数粒径(average number particle size)的细气泡。
41.(i-10)
42.根据项(i-1)至(i-9)中任一项所述的ufb发生剂,所述ufb发生剂为洗涤剂、浴用添加剂、化妆品、漱口剂、含漱剂、质地改良剂、食品或饮料、植物生长促进剂、海鲜生长促进剂、或消毒剂。
43.(ii)ufb产生方法
44.(ii-1)
45.一种用于产生ufb的方法,包括:
46.(a)向硬度为30mg/l至200mg/l、并且优选为50mg/l至200mg/l的水中添加以下(a)、(b)和(c)以使这三者共存于所述水中的步骤;以及
47.(b)在所述水中产生细气泡的步骤,
48.(a)包含比率(质量比)为78:22至100:0的酸型sl和内酯型sl的sl,
49.(b)游离脂肪酸或其盐,和
50.(c)气体发生组分。
51.(ii-2)
52.根据项(ii-1)所述的用于产生ufb的方法,其中步骤(b)中产生的所述细气泡为具有10000cps或更大、并且优选30000cps或更大的散射强度和小于1000nm、并且优选500nm或更小的平均个数粒径的细气泡。
53.(ii-3)
54.根据项(ii-1)或(ii-2)所述的用于产生ufb的方法,其中(c)为选自以下的至少一者:二氧化碳气体发生组分、氧气发生组分、氢气发生组分、和氯气发生组分。
55.(ii-4)
56.根据项(ii-3)所述的用于产生ufb的方法,其中所述二氧化碳气体发生组分为碳酸盐或碳酸氢盐,或者与其对应物的组合;所述氧气发生组分为过氧化氢或与其对应物的组合;所述氢气发生组分为氢化盐、硼氢化盐或盐酸,或者与其对应物的组合;或者所述氯气发生组分为次氯酸盐或与其对应物的组合。
57.(ii-5)
58.根据项(ii-1)至(ii-4)所述的用于产生ufb的方法,其中在步骤(a)中向所述水中添加(a)和(b),使得在所述水中(a)的浓度和(b)的浓度分别为0.005质量%或更大、并且优选为0.005质量%至0.4质量%,以及0.0001质量%或更大、并且优选为0.0001质量%至0.3质量%。
59.(ii-6)
60.根据项(ii-4)至(ii-5)所述的用于产生ufb的方法,其中在步骤(a)中向所述水中添加(c),使得在所述水中(c)的浓度以气体发生体的浓度计为0.1质量%或更大,并且优选为0.1质量%至20质量%。
61.(ii-7)
62.根据项(ii-1)至(ii-6)中任一项所述的用于产生ufb的方法,其中步骤(b)是在不从外部引入气体的情况下在水中产生细气泡的步骤。
63.(iii)含ufb的液体
64.(iii-1)
65.一种含ufb的液体,包含以下(a)、(b)、(c)和(d):
66.(a)包含比率(质量比)为78:22至100:0的酸型sl和内酯型sl的sl,
67.(b)游离脂肪酸或其盐,
68.(c)细气泡,所述细气泡由选自二氧化碳气体、氧气、氢气和氯气中的至少一种气体形成,并且所述细气泡的平均个数粒径小于1000nm;和
69.(d)水。
70.(iii-2)
71.根据项(iii-1)所述的含ufb的液体,其中所述细气泡具有500nm或更小的平均个数粒径和10000cps或更大、并且优选30000cps或更大的散射强度。
72.(iii-3)
73.根据项(iii-1)或(iii-2)所述的含ufb的液体,其中(a)的浓度为0.005质量%或更大、并且优选为0.005质量%至0.4质量%,以及(b)的浓度为0.0001质量%或更大、并且优选为0.0001质量%至0.3质量%。
74.(iii-4)
75.根据项(iii-1)或(iii-3)中任一项所述的含ufb的液体,其中(d)是硬度为30mg/l至200mg/l、并且优选为50mg/l至200mg/l的水。
76.(iv)用于生产含ufb的液体的方法
77.(iv-1)
78.一种用于生产含ufb的液体的方法,包括:
79.(a)向硬度为30mg/l至200mg/l、并且优选为50mg/l至200mg/l的水中添加以下(a)、(b)和(c)以使这三者共存于所述水中的步骤;以及
80.(b)在所述水中产生细气泡的步骤,
81.(a)包含比率(质量比)为78:22至100:0的酸型sl和内酯型sl的sl,
82.(b)游离脂肪酸或其盐,和
83.(c)气体发生组分。
84.(iv-2)
85.根据项(iv-1)所述的生产方法,其中步骤(b)中产生的所述细气泡为具有10000cps或更大、并且优选30000cps或更大的散射强度和小于1000nm、并且优选500nm或更小的平均个数粒径的细气泡。
86.(iv-3)
87.根据项(iv-1)或(iv-2)所述的生产方法,其中(c)为选自以下的至少一者:二氧化碳气体发生组分、氧气发生组分、氢气发生组分、和氯气发生组分。
88.(iv-4)
89.根据项(iv-3)所述的生产方法,其中所述二氧化碳气体发生组分为碳酸盐或碳酸氢盐,或者与其对应物的组合;所述氧气发生组分为过氧化氢或与其对应物的组合;所述氢气发生组分为氢化盐、硼氢化盐或盐酸,或者与其对应物的组合;或者所述氯气发生组分为次氯酸盐或与其对应物的组合。
90.(iv-5)
91.根据项(iv-1)至(iv-4)所述的生产方法,其中在步骤(a)中向所述水中添加(a)和(b),使得在所述水中(a)的浓度和(b)的浓度分别为0.005质量%或更大、并且优选为0.005质量%至0.4质量%,以及0.0001质量%或更大、并且优选为0.0001质量%至0.3质量%。
92.(iv-6)
93.根据项(iv-4)或(iv-5)所述的生产方法,其中在步骤(a)中向所述水中添加(c),使得在所述水中(c)的浓度以气体发生体的浓度计为0.1质量%或更大,并且优选为0.1质量%至20质量%。
94.(iv-7)
95.根据项(iv-1)至(iv-6)中任一项所述的生产方法,其中步骤(b)是在不从外部引入气体的情况下在水中产生细气泡的步骤。
96.有益效果
97.根据本发明的ufb发生剂和ufb产生方法,可以在不使用气泡产生装置的情况下在水中产生ufb。根据本发明的ufb产生方法和用于生产含ufb的液体的方法,可以在不使用气泡产生装置的情况下生产并获得含ufb的液体。
98.由于由此获得的含ufb的液体在液体中具有平均个数粒径小于1000nm的细气泡,因此可以在相对长的时间段内实现由超细气泡引起的效果。
附图说明
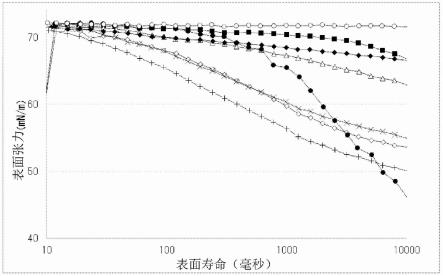
99.图1示出了以0.01质量%的表面活性剂浓度进行的实验例13的结果。图1中的各条线与所使用的表面活性剂的关系如下(这同样适用于图2):
100.―
■
―:含sl的组合物1,
101.―
△
―:烷基聚氧乙烯硫酸钠,
102.―
◇
―:二甲基二癸基氯化铵,
103.―
◆
―:苯扎氯铵,
104.―
×
―:月桂基二甲基氨基乙酸甜菜碱,
105.―+―:月桂基二甲胺氧化物,
106.―
●
―:poe月桂基醚,以及
107.―〇―:poe硬脂基醚(6eo)。
108.图2示出了以0.05质量%的表面活性剂浓度进行的实验例13的结果。
具体实施方式
109.ufb的定义和测量方法
110.超细气泡被定义为气泡尺寸小于1μm的气泡(iso 20480-1:2017细气泡技术)。
111.作为本发明的目标的ufb为具有上述气泡尺寸的细气泡。细气泡的气泡尺寸可以使用基于动态光散射原理的测量仪器(动态光散射分光光度计)来测量。具体地,当测量测试样品(液体)中包含的气泡的粒径时,如果平均个数粒径小于1000nm,则可以确定测试样品包含ufb。ufb的平均个数粒径可以小于1000nm,并且下限没有特别限制。ufb可以分类为平均个数粒径为50nm至小于200nm的细气泡、平均个数粒径为200nm至小于500nm的细气泡和平均个数粒径为500nm至小于1000nm的细气泡。ufb优选为平均个数粒径为500nm或更小的细气泡。根据基于气泡尺寸的功能,这些样品(液体)可以用于各种领域(例如环境领域、工业领域、农业领域、渔业领域、医学和药学领域、化妆品领域、食品和饮料领域)。下面,本说明书中的术语“粒径”或“气泡尺寸”表示平均个数粒径。
112.为了使包含气泡尺寸小于1000nm的细气泡(ufb)的液体有效地表现其功能,优选的是ufb以预定的浓度比包含在液体中。液体中的ufb进行粒径相关的布朗运动。因此,通过用激光(he-ne模式)照射含ufb的液体以用动态光散射分光光度计检测发射的散射光,可以测量取决于ufb颗粒的布朗运动的散射强度。因此,可以通过测量含ufb的液体中ufb的散射强度(cps)来评估液体中ufb的比率(浓度)。具体的测量方法和条件如实验例1中所述。如下所述,可以通过从含ufb的液体的散射强度减去除ufb之外的颗粒的散射强度来评估含ufb的液体中ufb的散射强度。ufb的散射强度没有限制,并且优选为5000cps或更大,更优选为10000cps或更大,并且特别优选为30000cps或更大。ufb的散射强度没有特别限制,只要ufb的散射强度的上限为100000000cps即可。
113.由通过以上方法获得的散射光,使用光子相关法获得自相关函数。表示布朗运动速度的扩散系数、以及粒径和粒径分布可以通过使用累积量分析和直方图分析来获得。在本发明中,ufb粒径可以根据以下实验例1中所示的方法和条件来测量和评估。
114.与快速上升至液体的表面并破裂的毫气泡和缓慢漂浮并消失的微气泡不同,已知ufb一旦在液体中形成,就会在通过布朗运动在液体中扩散的同时漂浮并保持长的时间段而不上升。同样在本发明中,还期望散射强度持续长的时间段。时间段没有限制,并且例如可以持续:按天计,例如一天至数天;按月计,例如一个月至数个月;或按年计,例如一年至数年。虽然时间段没有限制,但是目标时间段为6个月或更长,优选为一年或更长,更优选为两年或更长,并且特别优选为三年或更长。
115.在本发明的以下实施方案中,ufb的粒径和散射强度通过在大气压和室温(25℃)下在以下条件下使用动态光散射分光光度计(dls 6500-hl:由otsuka electronics co.,ltd生产)来确定。
116.激光模式:he-ne激光
117.积算次数:400次
118.采样时间:10微秒
119.测量通道:1024ch
120.测量角度:30
°
121.针孔1:0.5,
122.针孔2:0.2。
123.(i)ufb发生剂
124.将本发明的ufb发生剂添加至目标液体中以在液体中产生ufb。目标液体没有限制,只要其在添加本发明的ufb发生剂时产生ufb即可。目标液体优选为水性溶剂。更优选硬度在30mg/l至200mg/l的范围内的水性溶剂,并且特别优选硬度在50mg/l至200mg/l的范围内的水性溶剂。可以适当地使用硬度在该范围内的水。
125.在本文中,硬度(mg/l)意指美国硬度(或日本硬度),其可以具体地通过根据以下式1将钙和镁的量换算为碳酸钙(caco3)的量来确定。
126.硬度[mg/l]=(钙含量[mg/l]
×
2.5)+(镁含量[mg/l]
×
4.1)
[0127]
ufb发生剂包含以下(a)、(b)和(c)的组合:
[0128]
(a)包含比率(质量比)为78:22至100:0的酸型槐糖脂和内酯型槐糖脂的槐糖脂,
[0129]
(b)游离脂肪酸或其盐,和
[0130]
(c)气体发生组分。
[0131]
(a)槐糖脂(sl)
[0132]
槐糖脂(sl)通常是由槐糖或者其一个或更多个羟基被乙酰化或酯化的槐糖、和羟基脂肪酸组成的糖脂。槐糖是由通过β1
→
2键结合的两个葡萄糖分子组成的糖。羟基脂肪酸是具有羟基的脂肪酸。sl大致分类为酸型sl和内酯型sl。酸型sl是其中羟基脂肪酸的羧基是游离的槐糖脂。内酯型sl是其中羟基脂肪酸的羧基与分子中的槐糖结合的槐糖脂。酸型sl的实例包括由下式(1)表示的sl,以及内酯型sl的实例包括由下式(2)表示的sl。由产生sl的酵母通过发酵获得的sl通常为酸型sl和内酯型sl的混合物,并且获得为30种或更多种类型的结构同系物(例如具有不同脂肪酸链长度(r2)的那些,在槐糖的6'位置(r3)和6”位置(r4)处被乙酰化或质子化的那些,以及在槐糖的3'位置、4'位置、2”位置、3”位置和4”位置中的一者(r5)处被酯化的那些)的集合。
[0133][0134]
(在式(1)中,r1表示氢原子或甲基;
[0135]
r3和r4相同或不同,并且独立地表示氢原子或乙酰基;全部r5为氢原子,或者五个
r5中的一者为可以具有羟基的饱和或不饱和脂肪酸残基,并且余者全部为氢原子;r2为饱和脂族烃链或具有至少一个双键的不饱和脂族烃链,其可以具有一个或更多个取代基;以及
[0136]
r6为羟基)。
[0137][0138]
(在式(2)中,r1至r4如式(1)中所限定)。
[0139]
本发明所针对的sl可以包含这样的二聚体(二聚体sl),在所述二聚体中,由式(1)表示的酸型sl中的为其中一个r5基团可以具有羟基并且其余四个r5可以具有氢原子的饱和或不饱和脂肪酸残基的酸型sl的c-1位置处的r6结合至由式(3)表示的酸型sl中的一个r7以形成单键。
[0140][0141]
(在式(3)中,r
1'
为氢原子或甲基;
[0142]r3'
和r
4'
相同或不同,并且表示氢原子或乙酰基;
[0143]r2'
为饱和脂族烃链或具有至少一个双键的不饱和脂族烃链,并且可以具有一个或更多个取代基;以及
[0144]
一个r7结合至由式(1)表示的酸型sl的r6以形成单键,并且其余r7全部为氢原子。)
[0145]
在式(1)至(3)中,由r2或r
2'
表示的饱和或不饱和脂族烃链中的碳数没有限制,但通常为9至20,优选为9至18,更优选为11至16,并且特别优选为14至16。饱和脂族烃链可以
apicola)、嗜石油假丝酵母(candida petrophilum)、candida bogoriensis、巴蒂斯塔假丝酵母(candida batistae)等。
[0150]
本发明中的这样的产生sl的酵母的培养物使用包含糖(例如葡萄糖)(亲水性底物)以及脂肪酸、脂肪酸酯(例如脂肪酸甘油三酯)或者油和脂肪(例如包含脂肪酸作为组分的植物油)(疏水性底物)作为碳源的培养基。培养基的其他组分没有特别限制,并且可以适当地选自通常用于酵母的培养基组分。
[0151]
本发明中使用的sl是指其中基于酸型sl和内酯型sl的总量(100质量%),由式(1)表示的酸型sl以78质量%或更大的比率存在以及由式(2)表示的内酯型sl以22质量%或更小的比率存在的组合物;优选其中酸型sl以85质量%或更大的比率存在以及内酯型sl以15质量%或更小的比率存在的组合物;更优选其中酸型sl以90质量%或更大的比率存在以及内酯型sl以10质量%或更小的比率存在的组合物;甚至更优选其中酸型sl以95质量%或更大的比率存在以及内酯型sl以5质量%或更小的比率存在的组合物。sl可以为不含内酯型sl的sl,具体地为其中酸型sl的比率为100质量%的sl。
[0152]
在例如产生sl的酵母培养物或其加工产物中的含sl的组合物中酸型sl与内酯型sl的比率可以通过例如在wo2015/020114中描述的测量方法来确定,其内容在此通过引用并入。具体地,可以使用以下方法:使通过将酸型sl和内酯型sl的混合物(含sl的组合物)与等体积的50体积%乙醇溶液混合而制备的溶液经受如下所述的反相柱色谱,并使获得的部分进一步经受高效液相色谱(hplc)以定量分析各洗脱级分的sl含量。
[0153]
通过反相柱色谱进行分馏
[0154]
(1)使通过将600g含sl的组合物与等体积的50体积%乙醇溶液混合而获得的溶液在以下条件下经受反相柱色谱。
[0155]
固定相:c
18
柱(cosmosil 40c18-prep,由nacalai tesque,inc.生产,7.5kg)
[0156]
流动相:乙醇浓度为50体积%至95体积%的乙醇水溶液
[0157]
(2)具体地,依次使10l的50体积%乙醇水溶液、10l的80体积%乙醇水溶液、15l的90体积%乙醇水溶液和15l的95体积%乙醇水溶液经受固定相,并收集用80体积%乙醇水溶液、90%乙醇水溶液和95%乙醇水溶液洗脱的级分。
[0158]
(3)将各洗脱级分蒸发至干燥,然后溶解在乙醇中。使用这些溶液作为测试样品并在以下条件下经受hplc。
[0159]
通过hplc进行定量分析
[0160]
条件
[0161]
装置:shimadzu corporation lc-10 ad-vp
[0162]
柱:inertsil ods-3(4.6mm
×
250mm)
[0163]
柱温:40℃
[0164]
流动相:[a]蒸馏水,
[0165]
[b]包含0.1体积%甲酸的甲醇
[0166]
梯度:0分钟
→
60分钟:[b]70体积%
→
100体积%
[0167]
60分钟
→
70分钟:[b]100体积%
→
70体积%。
[0168]
流量:1.0ml/分钟
[0169]
进样体积:10μl
[0170]
检测器:蒸发光散射检测器(elsd-ltii,由shimadzu corporation生产)
[0171]
检测器温度:40℃
[0172]
增益:5
[0173]
气体压力:350kpa(n2气)
[0174]
用80体积%乙醇水溶液洗脱的级分包含由式(1)表示的酸型sl中的由下式(1a)表示的酸型sl。在由式(1)表示的酸型sl中,这种类型的酸型sl为由式(1)表示的其中所有r5都为氢原子的酸型sl。在以上条件下的hplc中,酸型sl(1a)在10分钟至25分钟的保留时间区中洗脱。
[0175][0176]
(在式(1a)中,r1至r4与式(1)中的限定相同。)
[0177]
用80体积%乙醇水溶液洗脱的级分不仅包含酸型sl(1a),而且还包含由上式(2)表示的内酯型sl。在以上条件下的hplc中,内酯型sl(2)在25分钟至40分钟的保留时间区中洗脱。
[0178]
用90体积%乙醇水溶液洗脱的级分包含酸型sl(1b),其为由式(1)表示的酸型sl中的其中一个r5为可以具有羟基的饱和或不饱和脂肪酸残基并且其余r5均为氢原子的一种酸型sl。在以上条件下的hplc中,酸型sl(1b)在45分钟至60分钟的保留时间区中洗脱。
[0179]
用95体积%乙醇溶液洗脱的级分包含由式(3)表示的二聚体sl。在以上条件下的hplc中,二聚体sl(3)在60分钟至70分钟的保留时间区中洗脱。
[0180]
因此,包含在含sl的组合物中的酸型sl与内酯型sl的比率,具体地基于酸型sl和内酯型sl的总量(100质量%)的各sl的比率可以由在以下条件下的hplc中的各保留时间区中检测到的峰的面积比确定。
[0181]
本发明中的sl在形式上没有特别限制并且可以呈液体、乳液或固体的形式。固体形式的实例包括:干固体,例如冷冻干燥产品、喷洒干燥产品和蒸发干燥产品;片剂;丸剂;散剂;颗粒剂;和胶囊剂。本发明的ufb发生剂中的酸型sl和内酯型sl的比率可以从基于组分(a)、(b)和(c)的总量(100质量%)的1质量%至80质量%的范围中适当地选择,只要可以获得本发明的效果即可。
[0182]
(b)游离脂肪酸或其盐
[0183]
作为本发明的目标的游离脂肪酸可以为饱和或不饱和脂肪酸,只要可以实现本发明的效果即可。饱和脂肪酸的实例包括c
12-20
脂肪酸(月桂酸、肉豆蔻酸、十五酸、棕榈酸、十
七酸、硬脂酸、和花生酸),优选c
14-20
脂肪酸,更优选c
16-20
脂肪酸,甚至更优选c
16-18
脂肪酸,并且特别优选c
16
棕榈酸。不饱和脂肪酸的实例包括具有1至3个双键的c
12-20
脂肪酸。双键的数目优选为1个至2个,并且更优选为1个。碳原子数优选为16至20,更优选为16至18,并且特别优选为18。不饱和脂肪酸的优选实例包括具有一个双键的c
16
棕榈油酸;具有一个双键的c
18
油酸或异油酸(优选油酸);具有两个双键的c
18
亚油酸;具有三个双键的c
18
亚麻酸(9、12、15)、亚麻酸(6、9、12)和桐酸;以及具有两个双键的c
20
亚麻酸(9、12、15)、亚麻酸(6、9、12)和桐酸。更优选地,不饱和脂肪酸为具有一个双键的c
16
棕榈油酸或c
18
油酸,并且特别优选为油酸。
[0184]
这些脂肪酸的盐没有特别限制,只要其不损害本发明的效果即可。这些脂肪酸的盐优选为不损害游离脂肪酸在水中的溶解度的那些。具体实例包括碱金属例如钠和钾的盐、和碱土金属例如钙和镁的盐,并且优选碱金属盐。
[0185]
本发明中的游离脂肪酸或其盐在形式上没有特别限制,并且可以呈液体、乳液或固体的形式。固体形式的实例包括干固体、片剂、丸剂、散剂、颗粒剂、和胶囊剂。本发明的ufb发生剂中的组分(b)的比率可以从基于组分(a)、(b)和(c)的总量(100质量%)的0.0001质量%至10质量%的范围中适当地选择,只要可以实现本发明的效果即可。
[0186]
(c)气体发生组分
[0187]
作为本发明的目标的气体发生组分是在水的存在下反应以产生气体的组分。只要气体发生组分为在水的存在下反应以产生气体的组分即可,其可以由单一组分或者两种或更多种组分的组合组成。气体发生组分可以包含气体发生体与其对应物的组合,如下所述。
[0188]
目标气体(气体)包括但不限于二氧化碳气体、氧气、氢气和氯气。优选的实例包括二氧化碳气体、氧气和氢气。
[0189]
二氧化碳气体发生组分可以为在水的存在下反应以产生二氧化碳气体(碳酸气)的任何组分。实例包括碳酸盐或碳酸氢盐。当将碳酸盐或碳酸氢盐置于包含组分(a)的水溶液中时,产生碳酸气。已知碳酸氢盐在水中加热时产生碳酸气。碳酸盐的优选实例包括碱金属盐例如碳酸钠和碳酸钾。碳酸氢盐的优选实例包括碱金属盐例如碳酸氢钠和碳酸氢钾。
[0190]
碳酸盐或碳酸氢盐也可以与在水的存在下使碳酸盐或碳酸氢盐分解以产生碳酸气的组分组合使用。在本发明中,使气体发生体例如碳酸盐分解的组分或者通过促进气体发生体的分解而有助于气体产生的组分作为与气体发生体组合使用的组分被称为“对应物”。与碳酸盐或碳酸氢盐(气体发生体)组合使用的对应物的实例包括酸和酸式盐。
[0191]
本文中使用的酸没有特别限制,只要其在水的存在下与碳酸盐或碳酸氢盐反应以产生碳酸气,并且其不损害本发明的效果即可。实例包括:无机酸,例如盐酸和硫酸;以及有机酸,例如琥珀酸、富马酸、己二酸、酒石酸、苯甲酸、柠檬酸、吡咯烷酮羧酸、水杨酸、马来酸、邻苯二甲酸、戊二酸、和草酸。这些可以单独使用或者以两者或更多者的组合使用。酸式盐的优选实例包括具有碱金属例如钠和钾的盐。
[0192]
氧气发生组分可以为在水的存在下反应以产生氧气的任何组分。实例包括作为氧气产生体的过氧化氢。过氧化氢也可以与在水的存在下使过氧化氢分解以产生氧气的组分(对应物)组合使用。与过氧化氢组合使用的对应物的实例包括过氧化氢降解酶例如过氧化氢酶、和催化剂例如二氧化锰。
[0193]
氢气发生组分可以为在水的存在下反应以产生氢气的任何组分。实例包括作为氢
气产生体的氢化盐、硼氢化盐或盐酸。氢化盐或硼氢化盐中的盐可以为任何盐,只要它们发挥以上作用即可。实例包括诸如钠和钾的碱金属盐、以及诸如钙和镁的碱土金属盐。具体地,氢化盐的实例包括氢化钠、氢化钾、氢化钙和氢化镁。硼氢化盐的实例包括硼氢化钠。
[0194]
盐酸也可以与在水的存在下使盐酸分解以产生氢气的组分(对应物)组合使用。与盐酸组合使用的对应物的实例包括金属例如铁、锌或镁。
[0195]
氯气发生组分可以为任何组分,只要其在水的存在下反应以产生氯气即可。实例包括作为氯气产生体的次氯酸盐例如次氯酸钠。次氯酸盐也可以与在水的存在下使次氯酸盐分解以产生氯气的组分(对应物)组合使用。与次氯酸盐组合使用的对应物的实例包括酸。酸没有特别限制,并且实例包括:无机酸,例如盐酸和硫酸;以及有机酸,例如琥珀酸、富马酸、己二酸、酒石酸、苯甲酸、柠檬酸、吡咯烷酮羧酸、水杨酸、马来酸、邻苯二甲酸、戊二酸、和草酸。这些酸可以单独使用或者以两者或更多者的组合使用。
[0196]
在本发明的ufb发生剂中,气体发生组分的形式没有特别限制,只要气体发生组分被配置成当其与水接触时首次产生气体即可。气体产生产品优选呈固体形式。固体形式的实例包括干固体、片剂、丸剂、散剂、颗粒剂、和胶囊剂。如上所述,气体发生组分可以与气体发生体与其对应物组合使用,在这种情况下,优选将气体发生体与其对应物以分离的状态组合,使得仅在它们与水接触时发生反应。本发明的ufb发生剂中的组分(c)的比率可以从每100质量%的组分(a)、(b)和(c)的总和0.1质量%至98.9999质量%的范围中适当地选择,只要可以获得本发明的效果即可。
[0197]
(d)其他组分
[0198]
本发明的ufb发生剂可以包含除了(a)、(b)和(c)之外的组分,只要不损害本发明的效果即可。这样的其他组分可以根据ufb发生剂的应用和应用领域来适当地选择。以下仅为实例并不是限制性的。
[0199]
口腔清洗剂(例如,漱口剂和含漱剂)
[0200]
实例包括润湿剂(例如,甘油、丙二醇、乙醇和异丙醇)、甜味剂(例如,甜菊苷、山梨糖醇、赤藓糖醇和糖精钠)、消毒剂(例如,甘草酸二钾、氯化十六烷基吡啶氨甲环酸、异丙基甲基苯酚、聚乙烯吡咯烷酮碘、苯扎氯铵、和葡萄糖酸氯己定乙醇)、和氟化钠。
[0201]
化妆品
[0202]
实例包括乙醇、甘油、丁二醇、二丙二醇、丙二醇、凡士林、矿物油、角鲨烷、高级脂肪酸、高级醇(例如,硬脂醇、山嵛醇和鲸蜡醇)、脂肪(例如,橄榄油、椰子油、乳木果油、荷荷巴籽油、和马油)、蜡(例如,蜂蜡和羊毛脂)、植物提取物、乙基己酸十六烷基酯、三乙基己酮、肉豆蔻酸异丙酯、聚二甲基硅氧烷、环戊硅氧烷等。
[0203]
浴用添加剂
[0204]
实例包括无机盐(例如,碳酸钾、碳酸钙、倍半碳酸钠、氯化钠、氯化钾、硫酸钠、硫酸镁、和偏硅酸钠)、草药和植物提取物(例如,茴香、黄芩根、黄柏皮、洋甘菊、木兰皮、鱼腥草、菖蒲、蛇床子根茎、蜜柑皮(citrus unshiu peel)、日本当归根、苦橙皮、辣椒、人参、柚子、苦艾、防风根和根茎、薄荷草、生姜、甘草、和肉桂皮);酶(例如,木瓜蛋白酶、胰酶和蛋白水解酶)、酸(例如,富马酸、琥珀酸、苹果酸、柠檬酸、马来酸、酒石酸、和乳酸)、保湿剂、植物油(例如,荷荷巴油、橄榄油、大豆油和稻米油)、异黄酮、羊毛脂、甘油、酪蛋白、硬脂醇、液体石蜡、白凡士林、丙二醇、脱脂奶粉、角鲨烷、蜂蜜、聚乙二醇、着色剂(例如,核黄素、胡萝卜
素、叶绿素、黄色#202、黄色#4、蓝色#1、绿色#201、和绿色#204)、无水硅酸、樟脑、水杨酸甲酯、萜品油、薄荷醇、糊精、氧化钛、和调味剂。
[0205]
食品和饮料
[0206]
实例包括氨基酸(例如,精氨酸、赖氨酸和谷氨酰胺)、矿物质(例如,铁、钾和钙)、必需脂肪酸(例如,亚麻酸、dha和epa)、维生素、胶原蛋白、肽、芝麻素、软骨素、和膳食纤维。
[0207]
植物生长促进剂
[0208]
实例包括硝酸盐(例如,硝酸铵、硝酸镁和硝酸钾)、硫酸盐(例如,硫酸铵、硫酸镁和硫酸钾)、磷酸盐或磷酸氢盐(例如,磷酸铵、磷酸镁、磷酸钾和磷酸氢二钾)、氯化物(例如,氯化铵、氯化镁和氯化钾)、尿素、镁、钙、锰、柠檬酸、酒石酸、草酸、乙酸、和乙底酸。
[0209]
海鲜生长促进剂
[0210]
实例包括:蛋白质和碳水化合物,例如大豆粉、鱼粉、肉、骨粉、氨基酸、玉米、和面粉;维生素,例如抗坏血酸;以及矿物质和微量元素。
[0211]
洗涤剂和消毒剂
[0212]
实例包括阴离子表面活性剂(例如,烷基聚氧乙烯硫酸盐、线性烷基苯磺酸盐和α-烯烃磺酸盐)、阳离子表面活性剂(例如,二烷基二甲基氯化铵和烷基苯扎氯铵)、两性表面活性剂(例如,烷基甜菜碱、烷基二亚乙基三氨基乙酸和烷基胺氧化物)、非离子表面活性剂(例如,聚氧乙烯烷基醚、甘油脂肪酸酯和聚氧乙烯聚氧丙烯二醇)、碱性化合物(例如,有机碱化合物例如烷醇胺和烷基胺;以及碱金属的氢氧化物,例如氢氧化钠、氢氧化钾、碳酸钠、碳酸钾、碳酸氢钠、碳酸氢钾、硅酸钠、硅酸钾、磷酸钠、和磷酸钾)、溶剂(例如,乙醇、丙二醇和甘油)、水溶助剂(例如,对甲苯磺酸和二甲苯磺酸或其盐)、螯合剂(例如,edta、nta和мdga)、酶(例如,蛋白酶、淀粉酶、脂肪酶、和纤维素酶)、消毒剂(例如,聚六亚甲基双胍盐酸盐、氯己定及其盐、异丙基甲基苯酚、烷基二氨基乙基甘氨酸盐酸盐、苯扎氯铵、异丙醇、乙醇、聚乙烯吡咯烷酮碘、次氯酸钠、邻苯二甲醛、戊二醛和过氧乙酸)、分散剂(例如,聚丙烯酸钠和聚乙烯吡咯烷酮)、抗氧化剂(例如,丁基羟基甲苯、亚硫酸钠和亚硫酸氢钠)、ph调节剂(例如,柠檬酸、葡萄糖酸、苹果酸、琥珀酸和乙酸)、增稠剂、粘度调节剂、调味剂、着色剂、防腐剂、漂白剂、漂白活化剂,等等。
[0213]
(f)形式、比例、剂量等
[0214]
本发明的ufb发生剂的形式包括包含组分(a)、(b)和(c)的组合物(一种试剂)以及其中至少组分(c)相对组分(a)和(b)分开包装并且这些组分在使用时进行组合的产品组合(试剂盒或试剂套)。此外,组分(c)也可以是其中气体发生体与其对应物分开包装并且在使用时进行组合的产品组合(试剂盒或试剂套)。在组合物(一种试剂)的情况下,形式没有特别限制,只要其被配置成在将组合物添加至水中时首次产生气体即可。所述形式优选为固体形式。这样的固体形式的实例包括干固体、片剂、丸剂、散剂、颗粒剂、胶囊剂。
[0215]
在本发明的ufb发生剂中,组分(a)、(b)和(c)的比例没有特别限制,只要不损害本发明的效果即可。组分(a)和(b)优选以这样的方式制备,即当被添加至水中以供使用时,组分(a)的浓度为0.005质量%或更大,以及组分(b)的浓度为0.0001质量%或更大。考虑到上述浓度,也可以确定在添加并混合在水中时ufb发生剂与水的比例。
[0216]
在水中,组分(a)的浓度优选为0.01质量%或更大,更优选为0.01质量%至0.4质量%;以及组分(b)的浓度优选为0.0005质量%或更大,并且更优选为0.0005质量%至0.3
质量%。本文中所指的水包括各种各样的水,例如水性溶剂和水溶液。
[0217]
在被添加至水中以供使用的组分(c)中,气体发生体的浓度可以为0.1质量%或更大。特别地,当组分(c)为二氧化碳气体发生组分时,优选以使得二氧化碳气体发生体(碳酸盐、碳酸氢盐)在水中的浓度为0.1质量%或更大的方式制备并使用。气体发生体在水中的浓度优选为0.1质量%或更大,更优选为0.1质量%至20质量%,并且特别优选为0.5质量%至1质量%。
[0218]
(ii)用于产生ufb的方法
[0219]
本发明的ufb产生方法可以通过向硬度为30mg/l至200mg/l、并且优选为50mg/l至200mg/l的水中添加组分(a)、(b)和(c),并使这三种组分共存于水中来进行。本发明的ufb产生方法是能够在不特别从外部引入气体的情况下在水中产生ufb的方法。
[0220]
水的温度没有特别限制,只要其为不损害ufb的产生的温度即可。水的温度优选为50℃或更小。组分(a)、(b)和(c)可以以预先混合的状态(以单一组合物的形式)使用。还可以在添加至水中之前将其中至少组分(c)与组分(a)和(b)分开包装的产品(试剂套或试剂盒)混合,或者在使用时将这三种组分同时添加至水中。具体地,可以通过使用如上所述的本发明的ufb发生剂(组合剂),以简单的方式简单地产生期望的ufb。
[0221]
硬度为30mg/l至200mg/l的水包括自来水以及包含多种组分的水溶液,这取决于用途或应用领域(例如环境领域、工业领域、农业领域、渔业领域、医学和药学领域、化妆品领域、以及食品和饮料领域)。这样的组分的实例包括但不限于如上所述的组分(d)。
[0222]
在一个实例中,通过将上述组分(a)、(b)和(c)或本发明的ufb发生剂与硬度为30mg/l至200mg/l的洗剂混合,可以在洗剂中产生期望的ufb以制备并获得含ufb的洗剂。含ufb的洗剂可以在每次使用时制备,或者其可以在首次使用时制备并继续使用,因为ufb稳定地保持在水中。
[0223]
在另一个实例中,通过将上述组分(a)、(b)和(c)或本发明的ufb发生剂与硬度为30mg/l至200mg/l的包含杀菌成分的水溶液(例如,消毒剂和农用化学品)混合,可以在水溶液中产生期望的ufb以制备并获得含ufb的消毒剂或农用化学品。通过将组分(a)、(b)和(c)或本发明的ufb发生剂与硬度为30mg/l至200mg/l的包含诸如肥料或生长剂的组分的水溶液混合,可以在水溶液中产生期望的ufb以制备并获得含ufb的肥料或生长剂。这些含ufb的液体也可以在每次使用时制备,或者它们可以在首次使用时制备并继续使用。
[0224]
本发明的ufb产生方法中使用的组分(a)、(b)和(c)如部分(i)中所述。可以参考部分(i)中的包括当与水混合时所使用的组分(a)、(b)和(c)的量(在水中的浓度)、所使用的水的硬度、待产生的ufb的散射强度、和粒径的描述。
[0225]
(iii)含ufb的液体及其生产方法
[0226]
本发明的含ufb的液体包含以下(a)、(b)、(c)和(d):
[0227]
(a)包含比率(质量比)为78:22至100:0的酸型sl和内酯型sl的sl;
[0228]
(b)游离脂肪酸或其盐;
[0229]
(c)细气泡,所述细气泡由选自二氧化碳气体、氧气、氢气和氯气中的至少一种气体形成,并且所述细气泡的平均个数粒径小于1000nm;和
[0230]
(d)水。
[0231]
组分(a)、(b)和(c)的类型和量(浓度)如部分(i)中所说明的,并且描述可以在此
参考。组分(d)是硬度为30mg/l至200mg/l、并且优选为50mg/l至200mg/l的水。所述水可以与溶解的组分(d)一起使用,只要其不偏离30mg/l至200mg/l的硬度范围即可。组分(d)可以根据用途或应用领域(例如环境领域、工业领域、农业领域、渔业领域、医学和药学领域、化妆品领域、以及食品和饮料领域)适当地使用。本发明的含ufb的液体可以根据组分(d)用于上述各种领域中。
[0232]
本发明的含ufb的液体中ufb的粒径可以小于1000nm。ufb包括粒径为50nm至小于200nm的细气泡、粒径为200nm至小于500nm的细气泡、以及粒径为500nm至小于1000nm的细气泡。ufb优选为粒径为500nm或更小的细气泡。根据基于ufb粒径的功能,含ufb的液体可以用于各种领域(例如环境领域、工业领域、农业领域、渔业领域、医学和药学领域、化妆品领域、以及食品和饮料领域)中。
[0233]
在本发明的含ufb的液体中,如通过上述方法所测量的散射强度没有限制,并且优选为5000cps或更大,更优选为10000cps或更大,并且特别优选为30000cps或更大。
[0234]
本发明的含ufb的液体可以通过以下方法来生产,即,用于生产含ufb的液体的方法,包括:
[0235]
(a)向硬度为30mg/l至200mg/l、并且优选为50mg/l至200mg/l的水中添加以下(a)、(b)和(c)以使这三者共存于水中的步骤;以及
[0236]
(b)在水中产生气泡的步骤,
[0237]
(a)包含比率(质量比)为78:22至100:0的酸型sl和内酯型sl的sl,
[0238]
(b)游离脂肪酸或其盐,和
[0239]
(c)气体发生组分。
[0240]
根据该方法,可以在不特别从外部引入气体的情况下在水中产生ufb,并且可以制备并获得本发明的含ufb的液体。
[0241]
本说明书中的术语“包含”和“含有”包括由......组成和基本上由......组成的含义。
[0242]
实施例
[0243]
为了帮助理解本发明的结构和效果,以下参照实验例描述了本发明。然而,本发明不限于这些实验例。除非另有说明,否则以下实验均在室温(25
±
5℃)和大气压条件下进行。除非另有说明,否则以下描述的“%”意指“质量%”,以及以下描述的“份”意指“质量份”。
[0244]
参照生产例1:含sl的组合物2的制备
[0245]
(1)使用每升包含10g水性葡萄糖(由nihon shokuhin kako co.,ltd.生产,产品名称:nisshoku gansui kessho budoto)、10g蛋白胨(由oriental yeast co.,ltd.生产,产品名称:peptone cb90m)和5g酵母提取物(由asahi food&healthcare co.,ltd.生产,产品名称:meast powder n)的液体培养基作为培养基。在30℃下摇动的同时将熊蜂生假丝酵母atcc222142在培养基中培养2天。将其用作液体预培养物。
[0246]
(2)将液体预培养物以4%的比例接种到置于5升发酵罐中的主培养基(3l)中,然后在30℃下以0.6vvm的充气量培养6天以进行发酵。主培养基每升包含100g水性葡萄糖、50g棕榈油精(由nof corporation生产,产品名称:palmary 2000)、50g油酸(由acid chem生产,产品名称:palmac 760)、1g氯化钠、10g磷酸二氢钾、10g七水硫酸镁、2.5g酵母提取物
(由asahi food&healthcare co.,ltd.生产,产品名称:meast powder n)和1g尿素(灭菌之前的ph为4.5至4.8)。
[0247]
从培养开始后第六天,停止发酵。将从发酵罐中取出的液体培养物加热,然后回到室温并使其静置2至3天。结果,液体培养物从底部依次分成以下三层:液体褐色沉淀物层、推测主要包含真菌细胞的乳白色固体层、和上清液。在除去上清液之后,以等于除去的上清液的量的量添加工业用水或地下水。在搅拌所得混合物的同时,逐渐添加48质量%氢氧化钠水溶液以将ph调节成6.5至6.9,从而使包含在液体培养物中的sl溶解。将所得产物用台式离心机(westfalia,由westfalia separator ag生产)离心以使乳白色固体沉淀,并收集上清液。在搅拌收集的上清液的同时,逐渐添加62.5质量%硫酸以将ph调节成2.5至3.0,从而再次使sl不溶解。在使所得混合物静置2天之后,通过倾析尽可能多地除去上清液。获得剩余物作为含sl的组合物2(水含量为约50%)。
[0248]
参照生产例2:含sl的组合物1的制备
[0249]
向以上在参照生产例1中获得的含sl的组合物2中添加氢氧化钠水溶液以将ph调节成14,并在80℃下进行处理2小时以进行水解(碱水解)。然后,使所得物回到室温,并使用硫酸(9.8m水溶液)将ph调节成10。通过过滤除去产生的不溶性物质,并获得滤液作为含sl的组合物1(水含量为约30%)。
[0250]
参照生产例3:含sl的组合物3的制备
[0251]
基于wo2015/034007的实施例1对以上在参照生产例2中制备的含sl组合物1进行纯化,并获得所得粉末作为含sl的组合物3。
[0252]
实验例1:由二氧化碳气体(co2气体)组成的细气泡的产生(1)
[0253]
实验例1中使用的起始材料如下。
[0254]
含sl的组合物1:包含34%的sl(酸型sl:内酯型sl=100:0(质量比))和2.5%的油酸的含sl的组合物(参见参照生产例2)
[0255]
含sl的组合物2:包含58%的sl(酸型sl:内酯型sl=78:22(质量比))和4.3%的油酸的含sl的组合物(参见参照生产例1)
[0256]
烷基聚氧乙烯硫酸钠:taycapol ne1230(包含27%的烷基聚氧乙烯硫酸钠)(由tayca corporation生产)
[0257]
烷基聚糖苷:cg-50(包含50%的烷基聚糖苷)(由dow chemical生产)
[0258]
月桂基二甲基氨基乙酸甜菜碱:rikabion a-100(包含30%的月桂基二甲基氨基乙酸甜菜碱)(由new japan chemical co.,ltd.生产)
[0259]
在将所述组分混合使得在水中的最终浓度满足表1至3中所示的比率(最终浓度:质量%)之后,将所得混合物添加至置于玻璃烧杯中的1l自来水(硬度:100mg/l)(室温)中,并通过用搅拌棒和搅拌器搅拌来溶解(ph:8.3),并使所述组分反应(产生二氧化碳气体)。
[0260]
使所得物在室温下静置,并且在12小时之后,测量散射强度和平均个数粒径(在下文中,也简称为“粒径”)。关于散射强度和粒径的测量,使用动态光散射分光光度计(dls 6500-hl:由otsuka electronics co.,ltd.生产)。具体地,使用10ml注射器将以上制备的水溶液通过0.45μm孔尺寸的过滤器过滤以除去固体杂质,将滤液收集在直径为21mm的圆柱形测量池中,并使其作为测量样品在以下条件下经受动态光散射分光光度计。
[0261]
动态光散射分光光度计的测量条件
[0262]
测量温度:25℃,
[0263]
积算次数:400次,
[0264]
采样时间:10微秒,
[0265]
测量通道:1024ch,
[0266]
测量角度:30
°
,
[0267]
针孔1:0.5,
[0268]
针孔2:0.2。
[0269]
表1至3示出了结果。
[0270]
散射强度通过从其中溶解有所有组分的水溶液(测试样品)的散射强度减去其中溶解有组分a和b(含sl的组合物1或2)或表面活性剂的水溶液(对照样品1)的散射强度和其中溶解有组分c(c1:气体发生体,c2:对应物)的水溶液(对照样品2)的散射强度来计算,如下式2中所示。关于各组分的溶解,使用散射强度为585cps的自来水(硬度:100mg/l)。
[0271]
式2:
[0272]
散射强度=[测试样品的散射强度]-[对照样品1的散射强度]-[对照样品2的散射强度]
[0273]
表1至3中示出的评估基于以下标准。
[0274]
散射强度
[0275]
◎
:30000cps或更大
[0276]
○
:10000cps或更大且小于30000cps
[0277]
△
:5000cps或更大且小于10000cps
[0278]
×
:小于5000cps
[0279]
平均个数粒径
[0280]
◎
:50nm或更大且小于200nm
[0281]
○
:200nm或更大且小于500nm
[0282]
△
:500nm或更大且小于1000nm
[0283]
×
:1000nm或更大
[0284]
由于当散射强度为8000cps或更小时,无法测量粒径,因此评估栏中描述了
“‑”
。
[0285]
[表1]
[0286][0287]
[表2]
[0288][0289]
[表3]
[0290]
小时之后,其仍稳定地保持在水中。此外,从其粒径和散射强度来看,确定气泡为对应于超细气泡的细气泡。在产生细气泡(ufb)的水溶液中,sl浓度为0.005%或更大,并且优选为0.01%或更大,游离脂肪酸浓度为0.0004%或更大,以及气体发生体的浓度为0.1%或更大。从表3中所示的结果来看,即使当气体发生体的浓度高达20质量%时,也获得了稳定的细气泡(ufb)。因此认为,气体发生体的浓度的上限没有特别限制,只要其可溶于水即
可。
[0291]
这证实了至少使浓度为0.005%或更大的sl、浓度为0.0004%或更大的游离脂肪酸和浓度为0.1%或更大的气体发生体共存于水中,从而产生了细气泡(ufb)。
[0292]
另一方面,确定当仅包含气体发生体并且不包含sl或游离脂肪酸时或者当将气体发生体与代替含sl的组合物的表面活性剂组合时,产生气泡co2,而未产生ufb(表2)。
[0293]
实验例2:由co2气体组成的细气泡的产生(2)
[0294]
评估了游离脂肪酸在反应体系中的影响。
[0295]
实验例2中使用的起始材料如下。
[0296]
含sl的组合物1:包含34%的sl(酸型sl:内酯型sl=100:0(质量比))和2.5%的油酸的含sl的组合物(参见参照生产例2)
[0297]
含sl的组合物3:包含99.8%的sl(酸型sl:内酯型sl=100:0(质量比))和0.2%的油酸的含sl的组合物(参见参照生产例3)
[0298]
在将所述组分混合使得在水中的最终浓度满足表4中所示的比率(质量%)之后,将所得混合物添加至置于玻璃烧杯中的1l自来水(硬度:100mg/l)(室温)中,并通过用搅拌棒和搅拌器搅拌来溶解(ph:8.3),并使所述组分反应(产生co2气体)。
[0299]
使所得物在室温下静置,并且在12小时之后,以与实验例1中相同的方式测量散射强度和粒径。散射强度通过从其中溶解有所有组分的水溶液(测试样品)的散射强度减去其中溶解有含sl的组合物1或3的水溶液(对照样品1)的散射强度和其中溶解有组分b和c的水溶液(对照样品2)的散射强度来计算,如上式2中所示。
[0300]
表4示出了结果。
[0301]
[表4]
[0302][0303]
表4的结果证实了除了sl和气体发生体之外,对应于超细气泡的细气泡的产生和在静置至少12小时之后其在水中的稳定保留还需要预定量的游离脂肪酸的存在。在水溶液
中产生和保持细气泡(ufb)所需的游离脂肪酸的浓度被认为是至少0.0001%。
[0304]
实验例3:由co2气体组成的细气泡的产生(3)
[0305]
使用ptl 4(jp2013-207122a)中公开的sl或hlb为6至12的非离子表面活性剂作为表面活性剂,以与实验例1中相同的方式在水中产生co2气体,并评估产生的气泡。
[0306]
实验例3中使用的起始材料如下。
[0307]
含sl的组合物1:与实验例1相同
[0308]
四油酸poe山梨糖醇(40eo):rheodol 440v(由kao corporation生产)
[0309]
聚氧乙烯硬化蓖麻油(25eo):emanon ch―25(由kao corporation生产)
[0310]
poe月桂基醚:emulgen 103(由kao corporation生产)
[0311]
脱水山梨糖醇单油酸酯(6eo):rheodol tw―o106v(由kao corporation生产)
[0312]
poe硬脂基醚(6eo):emulgen 306p(由kao corporation生产)
[0313]
在将所述组分混合使得在水中的最终浓度满足表5中所示的比率(质量%)之后,将所得混合物添加至置于玻璃烧杯中的1l自来水(硬度:100mg/l)(室温)中,并通过用搅拌棒和搅拌器搅拌来溶解(ph:8.3),并使所述组分反应(产生二氧化碳气体)。
[0314]
使所得物在室温下静置,并且在12小时之后,以与实验例1中相同的方式测量散射强度和粒径。散射强度通过从其中溶解有所有组分的水溶液(测试样品)的散射强度减去其中溶解有含sl的组合物1或表面活性剂的水溶液(对照样品1)的散射强度和其中溶解有组分c的水溶液(对照样品2)的散射强度来计算,如上式2中所示。
[0315]
表5示出了结果。
[0316]
[表5]
[0317][0318]
如表5中所示,当使用表面活性剂(非离子表面活性剂)代替含sl的组合物1(sl和游离脂肪酸)时,未发现对应于超细气泡的细气泡的产生。这证实了除了气体发生体之外,细气泡(ufb)的产生还需要sl和游离脂肪酸的存在。
[0319]
实验例4:由氧气、氢气或氯气组成的细气泡的产生
[0320]
代替co2气体,在水中产生o2气体、h2气体或cl2气体,并评估产生的气泡。
[0321]
实验例4中使用的起始材料如下。
[0322]
含sl的组合物1:与实验例1相同
[0323]
过氧化氢酶:asc super 25(由mgc advance co.,ltd.生产)
[0324]
在将所述组分混合使得在水中的最终浓度满足表6中所示的比率(质量%)之后,
将所得混合物添加至置于玻璃烧杯中的1l自来水(硬度:100mg/l)(室温)中,并通过用搅拌棒和搅拌器搅拌来溶解(ph:8.0),使所述组分反应(产生气体)。
[0325]
使所得物在室温下静置,并且在12小时之后,以与实验例1中相同的方式测量散射强度和粒径。散射强度通过从其中溶解有所有组分的水溶液(测试样品)的散射强度减去其中溶解有含sl的组合物1的水溶液(对照样品1)的散射强度和其中溶解有组分c(c1:气体发生体,c2:对应物)的水溶液(对照样品2)的散射强度来计算,如上式2中所示。
[0326]
表6示出了结果。
[0327]
[表6]
[0328]
[0329]
如表6中所示,确定当使sl、游离脂肪酸和各种气体发生组分(c1:气体发生体,c2:对应物)共存于水中时,各种气体(氧气、氢气和氯气)的气泡得以产生并且稳定地保持在水中。此外,从它们的粒径和散射强度来看,确定气泡为对应于超细气泡的细气泡。
[0330]
实验例5:漱口剂的制备和评估
[0331]
根据表7中所示的配方,将所述组分混合并溶解在纯化水(硬度:80mg/l)中以制备漱口剂(本发明的漱口剂1和2以及比较漱口剂1至3)(ph:6.5)。具体地,在根据需要将表7中所示的组分1至3混合之后,将所得混合物添加并溶解在通过预先混合而制备的溶液中(组分4至6和组分8),并用ph调节剂(组分7)将ph调节至6.5,从而制备漱口剂。
[0332]
对于制备的漱口剂,以以下方式评估超细气泡的产生和去污性。
[0333]
(1)超细气泡的产生的评估
[0334]
使漱口剂在室温下静置,并且在12小时之后,以与实验例1中相同的方式测量散射强度和粒径,并根据与实验例1中相同的标准进行评估。
[0335]
(2)去污性的评估
[0336]
将2%黏蛋白水溶液滴加至hap盘(apatite pellet app-100,10mm
×
10mm
×
2mm)中,并干燥以生产假口腔污渍测试片。将测试片在各漱口剂(本发明的漱口剂1和2以及比较漱口剂1至3)(37℃)中浸没3分钟。在浸没之后,将测试片用流动水冲洗30秒,干燥,并进行目视观察。使用power quick residual protein detector(由saraya co.,ltd.生产)对无法目视确定污渍的片进行染色。再次目视观察染色程度,并根据以下标准评估去污性。
[0337]
去污性评估
[0338]
◎
:没有残留污渍(在未进行可视化处理的情况下),并且即使在可视化处理之后也几乎未观察到污渍。
[0339]
○
:几乎没有残留污渍(在未进行可视化处理的情况下),但在可视化处理之后残留一些污渍。
[0340]
△
:残留少许污渍(在未进行可视化处理的情况下)。
[0341]
×
:残留许多污渍(在未进行可视化处理的情况下)。
[0342]
表7也示出了结果。
[0343]
[表7]
[0344][0345]
如表7中所示,对于本发明的漱口剂,确定了将组分1和2添加并溶解在水溶液中,从而产生了细气泡(ufb),并且确定了其气泡稳定地保持在水中。还确定了与细气泡(ufb)的产生未得到证实的比较漱口剂相比,本发明的漱口剂具有优异的去污性。
[0346]
实验例6:含漱剂的制备和评估
[0347]
根据表8中所示的配方,将所述组分混合并溶解在纯化水(硬度:80mg/l)中以制备含漱剂(本发明的含漱剂1和2以及比较含漱剂1至3)(ph:6.5)。具体地,在根据需要将表8中所示的组分1至3混合之后,将所得混合物添加并溶解在通过预先混合而制备的水溶液中(组分4、5和7),并用ph调节剂(组分6)将ph调节成6.5,从而获得含漱剂。
[0348]
对于制备的含漱剂,以以下方式评估超细气泡的产生和抗菌特性。
[0349]
(1)超细气泡的产生的评估
[0350]
使含漱剂在室温下静置,并且在12小时之后,以与实验例1中相同的方式测量散射强度和粒径,并根据与实验例1中相同的标准进行评估。
[0351]
(2)抗菌特性的评估
[0352]
将调节成30℃的各含漱剂(本发明的含漱剂1和2以及比较含漱剂1至3)和细菌液(变形链球菌(streptococcus mutans):atcc25175)(107cfu/ml)以9:1的质量比混合。1分钟之后,用灭活剂(包含4%聚山梨醇酯80、0.3%卵磷脂吐温80(nof corporation)和大豆来源的卵磷脂(fujifilm wako pure chemical corporation))停止反应。将获得的反应液连续稀释,并与培养基(胰蛋白胨大豆琼脂培养基)混合,然后在37℃下培养24小时。然后,对菌落数目进行计数。将计数的菌落数目与初始细菌计数(107cfu/ml)进行比较,以计算对数减少值。由计算的对数减少值,根据以下标准评估各含漱剂的抗菌特性。
[0353]
抗菌特性的评估
[0354]
◎
:对数减少值为2.0或更大
[0355]
○
:对数减少值小于1.5
[0356]
△
:对数减少值小于1.0
[0357]
×
:对数减少值小于0.5
[0358]
表8也示出了结果。
[0359]
[表8]
[0360][0361]
如表8中所示,对于本发明的含漱剂,确定了将组分1和2添加并溶解在水溶液中,从而产生了细气泡(ufb),并且确定了其气泡稳定地保持在水中。还确定了与细气泡(ufb)的产生未得到证实的比较含漱剂相比,本发明的含漱剂具有优异的抗菌能力。
[0362]
实验例7:洗剂的制备和评估
[0363]
根据表9中所示的配方,将所述组分混合并溶解在纯化水(硬度:80mg/l)中以制备洗剂(本发明的洗剂1和2以及比较洗剂1至3)(ph:5.0)。具体地,在根据需要将表9中所示的组分1至3混合之后,将所得混合物添加并溶解在通过预先混合而制备的溶液中(组分4、5和7),并用ph调节剂(组分6)将ph调节成5.0,从而获得洗剂。
[0364]
对于制备的洗剂,测量在应用于皮肤期间超细气泡的产生和使用中的感觉(水分和刺激感),并以以下方式评估水分保留和刺激性。
[0365]
(1)超细气泡的产生的评估
[0366]
使洗剂在室温下静置,并且在12小时之后,以与实验例1中相同的方式测量散射强度和粒径,并根据与实验例1中相同的标准进行评估。
[0367]
(2)使用中的皮肤感觉的测量
[0368]
要求五名专家小组成员在洗脸之后将各洗剂(本发明的洗剂1和2以及比较洗剂1至3)施加至他们的面部(施加至面部的洗剂的量:5ml),并根据以下标准评估水分和刺激感。
[0369]
水分(水分保留)
[0370]
在施加之后1小时,通过将施加洗剂的皮肤(面部上)与未施加洗剂的皮肤(对照皮肤)进行比较来评估接触皮肤时的水分。
[0371]
◎
:比对照皮肤更湿润
[0372]
○
:比对照皮肤略微湿润
[0373]
△
:比对照皮肤不太湿润
[0374]
×
:不比对照皮肤更湿润
[0375]
刺激感(刺激性)
[0376]
评估了施加期间的皮肤刺激性。
[0377]
○
:无刺激性
[0378]
△
:轻微的刺激性
[0379]
×
:相当大的刺激性
[0380]
表9也示出了结果。
[0381]
[表9]
[0382][0383]
如表9中所示,对于本发明的洗剂,确定了将组分1和2添加并溶解在水溶液中,从而产生了细气泡(ufb),并且确定了其气泡稳定地保持在水中。还确定了与细气泡(ufb)的产生未得到证实的比较洗剂相比,本发明的洗剂具有更小的刺激性和优异的水分保留。
[0384]
实验例8:浴用添加剂的制备和评估
[0385]
根据表10中所示的配方,对所述组分进行粉末混合并根据标准方法模制成散剂或片剂,从而制备固体浴用添加剂(本发明的浴用添加剂1和2以及比较浴用添加剂1和2)。
[0386]
(1)超细气泡的产生的评估
[0387]
将50g制备的各浴用添加剂放入10l 38℃的温水(硬度:100mg/l)中(ph:8.2),并评估超细气泡的产生。具体地,将温水按原样静置,并且在12小时之后,以与实验例1中相同的方式测量散射强度和粒径,并根据与实验例1中相同的标准进行评估。
[0388]
(2)沐浴效果的评估
[0389]
将50g制备的各浴用添加剂放入38℃的温水(硬度:100mg/l)中(ph:8.2),并由三名小组成员评估沐浴效果(身体温暖度和持续温暖度)。
[0390]
(a)温暖度
[0391]
在将50g本发明的各浴用添加剂或比较浴用添加剂放入38℃的浴水(150l)中之后,要求小组成员立即沐浴10分钟,其中水最高至他们的肩部,并在沐浴之后立即评估温暖度。与同样在38℃的不含浴用添加剂的普通热水中沐浴10分钟之后的温暖度相比,根据以下标准评估温暖度。
[0392]
温暖度的评估
[0393]
◎
:比普通热水温暖得多
[0394]
○
:比普通热水更温暖
[0395]
△
:比普通热水略微温暖
[0396]
×
:与普通热水的温暖程度相同
[0397]
(b)持续温暖度
[0398]
在24℃的房间中,将5g本发明的各浴用添加剂或比较浴用添加剂放入置于恒温装置中的38℃的温水(10l)中,然后小组成员将他们的双脚放入水中持续15分钟。15分钟之后,他们将他们的脚从温水中取出,擦去水滴,并将他们的脚在室温下裸露静置20分钟。此后,用热成像仪(thermo shot f30s:由nippon avionics co.,ltd.生产)对脚的表面进行拍照。根据捕获的屏幕的颜色,根据以下标准评估皮肤表面上的持续温暖度。
[0399]
持续温暖度的评估
[0400]
◎
:整个捕获的屏幕是红色的(持续温暖度被评估为非常优异)。
[0401]
○
:整个捕获的屏幕是红色和黄色的(持续温暖度被评估为良好)。
[0402]
△
:整个捕获的屏幕是黄色的(持续温暖度在某种程度上得到认可)。
[0403]
×
:大部分的捕获的屏幕是蓝色的(持续温暖度与普通热水一样)。
[0404]
表10也示出了结果。
[0405]
[表10]
[0406][0407]
如表10中所示,确定了将本发明的浴用添加剂添加并溶解在温水中,从而产生了细气泡(ufb),并且确定了其气泡稳定地保持在水中。还确定了与即使在将其添加至温水中
时细气泡(ufb)的产生也未得到证实的比较浴用添加剂相比,本发明的浴用添加剂具有优异的温暖度和持续温暖度。
[0408]
实验例9:医疗装置洗涤剂的制备和评估
[0409]
根据表11中所示的配方,对所述组分进行粉末混合,并根据标准方法模制成散剂或片剂,从而制备固体医疗装置洗涤剂(本发明的医疗装置洗涤剂1至3以及比较医疗装置洗涤剂1至3)。
[0410]
将0.5g制备的各医疗装置洗涤剂放入置于烧杯中的100ml 20℃的水(硬度:100mg/l)中(ph:9.0),并评估超细气泡的产生和针对血迹的去污性。
[0411]
(1)超细气泡的产生的评估
[0412]
将各医疗装置洗涤剂放入水中并静置。12小时之后,以与实验例1中相同的方式测量散射强度和平均个数粒径,并根据与实验例1中相同的标准进行评估。
[0413]
(2)针对血迹的去污性的评估
[0414]
使用用血液污染的清洁效率指示剂(tosi,由pereg生产)评估去污性。将指示剂在各医疗装置洗涤剂(本发明的医疗装置洗涤剂1至3和比较医疗装置洗涤剂1至3)(20℃)中浸没120分钟。在浸没之后,将指示剂用流动水冲洗30秒,干燥,并进行目视观察。使用power quick residual protein detector(由saraya co.,ltd.生产)对无法确定污渍的指示剂进行染色。再次目视观察染色程度,并根据以下标准评估去污性。
[0415]
去污性评估
[0416]
◎
:没有残留污渍(在未进行可视化处理的情况下),并且即使在可视化处理之后也几乎未观察到污渍。
[0417]
○
:几乎没有残留污渍(在未进行可视化处理的情况下),但在可视化处理之后残留一些污渍。
[0418]
△
:残留少许污渍(在未进行可视化处理的情况下)。
[0419]
×
:残留许多污渍(在未进行可视化处理的情况下)。
[0420]
表11也示出了结果。
[0421]
[表11]
[0422][0423]
如表11中所示,确定了将本发明的医疗装置洗涤剂添加并溶解在水中,从而产生了细气泡(ufb),并且确定了其气泡稳定地保持在水中。还确定了与即使在将其添加至水中时细气泡(ufb)的产生也未得到证实的比较医疗装置洗涤剂相比,本发明的医疗装置洗涤剂具有优异的针对血迹的去污性。
[0424]
实验例10:餐具洗涤剂的制备和评估
[0425]
根据表12中所示的配方,对所述组分进行粉末混合,并根据标准方法模制成散剂
或片剂,从而制备固体餐具洗涤剂(本发明的餐具洗涤剂1至3以及比较餐具洗涤剂1至3)。
[0426]
将50g制备的各餐具洗涤剂放入置于浸没槽中的10l 40℃的水(硬度:100mg/l)中(ph:8.2),并评估超细气泡的产生和针对淀粉的去污性。
[0427]
(1)超细气泡的产生的评估
[0428]
将各餐具洗涤剂放入40℃的水中并静置。12小时之后,以与实验例1中相同的方式测量散射强度和粒径,并根据与实验例1中相同的标准进行评估。
[0429]
(2)针对淀粉污渍的去污性的评估
[0430]
将包装的稻米(s&b foods inc.)在微波炉中加热,并将约100g稻米铺在直径19cm的瓷盘的中心上。在使稻米静置10分钟之后,将其从盘中取出,并将盘在室温下干燥1小时。然后,将盘在包含各餐具洗涤剂(本发明的餐具洗涤剂1至3以及比较餐具洗涤剂1至3)的浸没槽中的水(40℃)中浸没5分钟。将盘拉起并立即使用商业洗碗机(zanussi 520)用60℃的热水洗涤1分钟,然后干燥。在干燥之后,将盘的整个内部用碘溶液染色。在染色之后,目视观察染色程度以评估去污性。
[0431]
去污性评估
[0432]
○
:几乎没有污渍(残留污渍)
[0433]
△
:少许污渍(残留污渍)
[0434]
×
:许多污渍(残留污渍)
[0435]
表12也示出了结果。
[0436]
[表12]
[0437][0438]
如表12中所示,确定了将本发明的餐具洗涤剂添加并溶解在水中,从而产生了细气泡(ufb),并且确定了气泡稳定地保持在水中。还确定了与比较餐具洗涤剂(即使其被添加至水中也未确认产生细气泡(ufb))相比,本发明的餐具洗涤剂具有优异的去污性,特别是针对淀粉污渍的去污性。
[0439]
实验例11:衣物洗涤剂的制备和评估
[0440]
根据表13中所示的配方,对所述组分进行粉末混合,并根据标准方法模制成散剂或片剂,从而制备固体衣物洗涤剂(本发明的衣物洗涤剂1至3以及比较衣物洗涤剂1至3)。
[0441]
将1g制备的各衣物洗涤剂放入置于烧杯中的1l 30℃的温水(硬度:100mg/l)中
(ph:8.2或11.1),并评估超细气泡的产生和针对人工污染衣物的去污性。表13也示出了结果。
[0442]
(1)超细气泡的产生的评估
[0443]
将各衣物洗涤剂放入30℃的温水中并静置。12小时之后,以与实验例1中相同的方式测量散射强度和粒径,并根据与实验例1中相同的标准进行评估。
[0444]
(2)针对人工污染布的去污性的评估
[0445]
使用模拟衣领污渍的湿的人工污染布和洗净力试验机(tergotometer,
ターゴトメーター
)进行评估。将1l自来水放入洗净力试验机(tm-8,由daiei kagaku seiki mfg.co.,ltd.生产)的测试杯中,并将5g各衣物洗涤剂(本发明的衣物洗涤剂1至3以及比较衣物洗涤剂1至3)和人工污染布放入其中。在120rpm和30℃下将布清洁10分钟。然后,将布用1l30℃的自来水冲洗3分钟,然后排水两次。将布用手轻轻挤压并熨烫以完成干燥。使用反射率计(cm-600d,minolta)确定污染布在清洁之前和之后的白度,通过下式3计算清洁率。
[0446]
式3
[0447]
清洁率(%)=(污染布在清洁之后的白度-污染布在清洁之前的白度)/(参考白布的白度-污染布在清洁之前的白度)
×
100
[0448]
去污性评估
[0449]
○
:60%或更大的清洁率
[0450]
△
:50%或更大的清洁率
[0451]
×
:40%或更小的清洁率。
[0452]
表13也示出了结果。
[0453]
[表13]
[0454][0455]
如表13中所示,确定了将本发明的衣物洗涤剂添加并溶解在温水中,从而产生了细气泡(ufb),并且确定了气泡稳定地保持在水中。还确定了与即使在将其添加至温水中时细气泡(ufb)的产生也未得到证实的比较衣物洗涤剂相比,本发明的衣物洗涤剂具有优异的针对衣领污渍的去污性。
[0456]
实验例12:由co2气体组成的细气泡的稳定性
[0457]
使用实验例1中所示的测试样品1-2(参见表1)进行稳定性测试。
[0458]
具体地,在将所述组分混合使得在水中的最终浓度满足表1(测试样品1-2)中所示的比率(最终浓度:质量%)之后,将所得混合物添加至置于玻璃烧杯中的1l自来水(硬度:
100mg/l)(室温)中,并通过用搅拌棒和搅拌器搅拌来溶解(ph:8.2),并使所述组分反应(产生co2气体)。
[0459]
将所得物置于50ml玻璃瓶中,并在室温下在黑暗中储存1个月、6个月和12个月。然后,以与实验例1中相同的方式测量散射强度和粒径。
[0460]
表14示出了结果。表14中所示的评估结果基于与实验例1中相同的标准。
[0461]
[表14]
[0462][0463]
如表14中所示,散射强度和平均个数粒径二者在长达一年的时间段内均是稳定的。这证实了通过本发明的方法在水中产生的细气泡(ufb)在长时间段内稳定地保持在水中。
[0464]
实验例13:动态表面张力的测量
[0465]
使用sl或表15和表16中所示的各种表面活性剂中的每一者作为表面活性剂,以与实验例1中相同的方式在水中产生co2气体,并评估产生的气泡。此外,测量制备的水溶液随时间的动态表面张力,并检查产生的气泡的状态与动态表面张力之间的关系。
[0466]
用于实验例13中使用的表面活性剂的起始材料如下。括号中示出了图1和图2中的线的符号。
[0467]
测试样品13-a1和13-b1:含sl的组合物1:与实验例1中相同(―
■
―)
[0468]
测试样品13-a2和13-b2:烷基聚氧乙烯硫酸钠:taycapol ne1230(由tayca corporation生产)(―
△
―)
[0469]
测试样品13-a3和13-b3:二甲基二癸基氯化铵:阳离子ddc-80t(由sanyo chemical industries,ltd.生产)(―
◇
―)
[0470]
测试样品13-a4和13-b4:苯扎氯铵:白蛋白1214(由taiwan surfactant生产)(―
◆
―)
[0471]
测试样品13-a5和13-b5:月桂基二甲基氨基乙酸甜菜碱:rikabion a-100(由new japan chemical co.,ltd.生产)(―
×
―)
[0472]
测试样品13-a6和13-b6:月桂基二甲胺氧化物:amphitol 20n(由kao corporation生产)(―+―)
[0473]
测试样品13-a7和13-b7:poe月桂基醚:emulgen 103(由kao corporation生产)(―
●
―)
[0474]
测试样品13-a8和13-b8:poe硬脂基醚(6eo):emulgen 306(由kao corporation生产)(―〇―)
[0475]
(1)测试样品的制备
[0476]
在添加所述组分使得在水中的最终浓度满足表15和表16中所示的比率(质量%)
之后,将所得混合物添加至置于玻璃烧杯中的1l自来水(硬度:100mg/l)(室温)中,并通过用搅拌棒和搅拌器搅拌来溶解(ph:8.2),并使所述组分反应(产生co2气体)。
[0477]
(2)气泡的散射强度和粒径的测量
[0478]
将以上制备的测试样品各自在室温下静置,并且在12小时之后,以与实验例1中相同的方式测量散射强度和粒径。散射强度通过从其中溶解有所有组分的水溶液(测试样品)的散射强度减去其中溶解有含sl的组合物1或各表面活性剂的水溶液(对照样品1)的散射强度和其中溶解有组分c的水溶液(对照样品2)的散射强度来计算,如上式2中所示。
[0479]
(3)动态表面张力的测量
[0480]
测量用于制备测试样品的表面活性剂的动态表面张力。关于动态表面张力的测量,使用气泡压力动态表面张力计(bp-100:由kurss生产)。具体地,将各表面活性剂的水溶液(0.01%和0.05%)置于专用的培养皿中,并在以下条件下经受动态表面张力。表面寿命意指从界面形成开始到最大压力的时间。
[0481]
测量温度:25℃,
[0482]
表面寿命:10毫秒至10000毫秒。
[0483]
表15和图1示出了当表面活性剂浓度为0.01%时的结果,以及表16和图2示出了当表面活性剂浓度为0.05%时的结果。
[0484]
[表15]
[0485][0486]
[表16]
[0487][0488]
如表15和表16以及图1和图2中所示,确定了使碳酸氢盐与各表面活性剂共存于水中,从而产生了co2气体;然而,从散射强度和粒径来看,在12小时之后产生超细气泡(ufb)
仅在使用含sl的组合物的测试样品13-a1和13-b1(各图中的“―
■
―”)中得到证实。确定了与使用除poe硬脂基醚之外的表面活性剂的测试样品13-a2至13-a7、13-b2至13-b7的表面张力相比,其表面张力降低得更慢,并且确定了它们容易被吸收到水中。具体地,测试样品13-a1(sl浓度:0.01%)的表面张力即使在1秒之后也保持在70mn/m或更大;然而,测试样品13-a2至13-a7的表面张力降低至小于70mn/m。此外,测试样品13-b1(sl浓度:0.05%)的表面张力即使在10秒之后也保持在60mn/m或更大;然而,测试样品13-b2至13-b7的表面张力显著降低至小于60mn/m。
[0489]
另一方面,即使使用poe硬脂基醚(6eo)作为表面活性剂的测试样品13-a8和13-b8(各图中的―〇―)的动态表面张力缓慢下降,它们也未产生超细气泡(ufb)。其原因是例如poe硬脂基醚(6eo)为非离子表面活性剂。
[0490]
由本发明所针对的气体发生组分产生的细气泡带有负电荷。因此,带有正电荷的物质在其周围聚集以形成正/负双电层。由于sl在亲水基团中的负电荷,因此认为sl被吸引至细气泡的双电层的正电荷并且被吸附至细气泡以稳定化。另一方面,由于亲水基团中没有电荷,因此认为poe硬脂基醚(6eo)不被吸引至细气泡的双电层并且不被吸附至细气泡。从这些结果来看,虽然没有限制,但是认为在水中细气泡的产生及其稳定性(保留)受含sl的组合物的表面张力特性(阴离子性和慢的动态表面张力)影响。
- 该技术已申请专利。仅供学习研究,如用于商业用途,请联系技术所有人。
- 技术研发人员:谢花喜史 熊野亘 荒木道阳 尾田友香 川向惠美子 平田善彦
- 技术所有人:莎罗雅株式会社
- 我是此专利的发明人
- 该领域下的技术专家
- 如您需求助技术专家,请点此查看客服电话进行咨询。
- 1、平老师:1.功能涂层设计与应用 2.柔性电子器件设计与应用 3.结构动态参数测试与装置研发 4.智能机电一体化产品研发 5.3D打印工艺与设备
- 2、郝老师:1. 先进材料制备 2. 环境及能源材料的制备及表征 3. 功能涂层的设计及制备 4. 金属基复合材料制备
- 如您是高校老师,可以点此联系我们加入专家库。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1
精彩留言,会给你点赞!
专利分类正在加载中....