沸石内部原位合成钙钛矿量子点复合物材料的制备方法
1.本发明属于发光材料技术领域,具体涉及一种沸石内部原位合成钙钛矿量子点复合物材料的制备方法。
背景技术:
2.近年来,铅卤钙钛矿作为一类“明星材料”,受到了人们的广泛关注。由于其具有载流子扩散长度长、消光系数高和缺陷密度低等优点,在光电领域呈现出十分广阔的应用前景。自2009年首个无机—有机杂化钙钛矿太阳能电池诞生至今,其能量转换效率已经从最初的3.8%跃升至23.2%。钙钛矿在太阳能电池方面取得的巨大成功也进一步刺激了研究者们对钙钛矿材料在其他相关领域的应用探索,如光电探测,激光,发光二极管(light emitting diode,led),x
‑
射线成像等。其中,由于钙钛矿具有发射谱线窄、带隙易调控、量子效率高、价格低廉及合成便捷等特点,被看作是发光领域理想的替代材料。使用铅卤钙钛矿为发光层,取代传统的发光材料如cdse量子点,制备钙钛矿型led(peled)也成为了该领域的研究热点。
3.冲击peled效率是当前的研究主流,但目前制约其应用最大障碍却是器件的工作寿命。目前3d结构钙钛矿多是由ch3nh3pbx3或其衍生物制备而成,但这些材料在~60%湿度的空气氛围中保存数周即分解。2d钙钛矿的稳定性优于3d的材料,但其疏水的有机长链胺也极大程度地阻挡了载流子的注入,影响了器件效率。稳定性是所有钙钛矿相关领域的阻碍,稳定性的提升对于如太阳能电池、激光、光电探测器等均具有重要的意义。与上述应用不同的是,led内部有较强的电压和电流,即使在恒定低电压下工作,器件亮度仍会出现明显的衰减。目前而言,通过良好的技术处理和封装工艺来提升器件的性能和寿命是不可避免的,但是这些仪器造价昂贵,工艺复杂,因此材料科学家更希望着眼于通过材料设计提升内在稳定性,从根本上解决这一问题。
4.为了提升钙钛矿的稳定性,研究者们投入了大量的工作,并取得一定的成功。最早期的铅卤钙钛矿放置在空气里半个小时就完全失去了光学活性,现在的材料在放置在空气里长达一个星期也没有明显的衰减,因为大家对钙钛矿的制备过程也有了越来越深入的了解。钙钛矿遇水容易分解,而放在空气里快速分解是因为在烘干时,溶剂n,n
‑
二甲基甲酰胺(dmf)会残留在晶体当中,dmf是一种吸水性很强的物质,如果残留比较多的话,大量吸水会迅速破坏晶格。研究者们开拓了一种真空退火技术,使材料中残余的dmf完全挥发,从而大大提高了钙钛矿的稳定性。目前,提升材料稳定性的方法较多,例如掺杂,表面钝化,高分子或无机物的包覆。
技术实现要素:
5.本发明的目的在于解决钙钛矿遇水容易分解、在空气里快速分解、物理和化学性质不稳定等问题,提供一种沸石内部原位合成钙钛矿量子点复合物材料的制备方法。
6.本发明的目的通过如下技术方案来实现:包括以下步骤:
7.步骤1:将0.188mmol氯化铅、2.0ml油酸、2.0ml油胺和10ml十八烯溶液置于烧瓶中,真空120℃下搅拌30min后,通入氮气升温至150℃并维持10min;
8.步骤2:将2.5ml油酸铯快速注入烧瓶中,反应5s后快速通过冰水浴将烧瓶中的热溶液冷却至室温;
9.步骤3:对烧瓶中的溶液进行离心分离,通过异丙醇洗涤沉淀物2
‑
3次后,将沉淀物置于真空干燥箱35℃烘干12h,获得中间产物cs4pbcl6纳米晶;
10.步骤4:将0.3mmol溴化锌或者碘化锌、200μl油胺、10ml正己烷或辛烷或氯仿置于烧杯中搅拌12h,获得znm2(m=br,i)溶液;
11.步骤5:向cs4pbcl6纳米晶加入znm2(m=br,i)溶液,室温条件下cs4pbcl6纳米晶快速转化成cspbx3量子点;
12.步骤6:将1.0g沸石zeolite
‑
y和0.0021g溴化铯分散在10ml去离子水中,在水浴60℃中搅拌24h,将产物离心并用去离子水洗涤,然后在80℃空气中干燥12h获得cs
+
‑
y;
13.步骤7:将0.376mmol氯化铅、2.0ml油酸、2.0ml油胺与10ml十八烯混合,将混合物在120℃真空搅拌下干燥30min;之后,往混合物通入氮气直到氯化铅完全溶解,得到氯化铅溶液;
14.步骤8:将1gcs
+
‑
y与10ml十八烯混合,将混合物在真空和120℃下干燥30min,在氮气氛围下将反应温度升至150℃并再保持30min;将步骤7中制备好的氯化铅溶液注入热反应混合物中,搅拌10min后使用冰水浴冷却;将所得产物用异丙醇洗涤两次,然后离心,在40℃下干燥12h,得到cs4pbcl6@zeolite复合材料;
15.步骤9:向cs4pbcl6@zeolite复合材料加入50
‑
1000μl的znm2(m=br,i)溶液,在室温条件下cs4pbcl6@zeolite转化为cspbx3@zeolite,完成制备。
16.本发明的有益效果在于:
17.本发明采用离子交换法结合非极性有机引发剂成功制备了立方相cspbx3(x=br,i)纳米晶,将一定量的znm2(m=br,i)溶液滴入不发光的中间产物cs4pbcl6纳米晶体中,形成了明亮的、稳定的cspbx3纳米晶体。通过沸石无机物包覆可以使cspbx3@zeolite复合材料的稳定性极大提升。本发明操作简单,反应条件温和,在室温下溶液中即可反应完成,所使用设备简单,对制备高效的、拥有潜在应用性的钙钛矿量子点提供了一种路径,解决了钙钛矿遇水容易分解、在空气里快速分解、物理和化学性质不稳定等问题。
附图说明
18.图1是cs4pbcl6单相x射线粉末衍射(x
‑
raydiffraction,xrd)图谱。
19.图2是cs4pbcl6单相透射电子显微镜(transmissionelectronmicroscope,tem)图谱。
20.图3(a)是cspbbr3单相xrd衍射图谱。
21.图3(b)是cspbi3单相xrd衍射图谱。
22.图4(a)是cspbbr3单相tem图谱。
23.图4(b)是cspbi3单相tem图谱。
24.图5是cs4pbcl6纳米晶向cspbx3纳米晶转化的过程(0
‑
15min)。
25.图6是获得的cspbbr3和cspbi3纳米晶的吸收和发射光谱,插图显示了在紫外光(λ
=365nm)下的强烈绿光和红光发射。
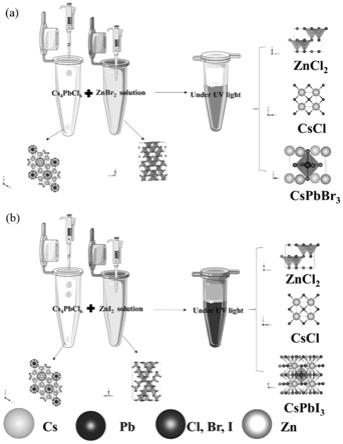
26.图7是cspbx3纳米晶的整个形成过程示意图。
27.图8(a)是cspbbr3纳米晶在不同溶剂中的发射光谱。
28.图8(b)是cspbi3纳米晶在不同溶剂中的发射光谱。
29.图8(c)是cspbbr3纳米晶在不同溶剂中的照片。
30.图8(d)是cspbi3纳米晶在不同溶剂中的照片。
31.图9是na
+
‑
y,cs
+
‑
y,cs4pbx6@zeolite,cspbbr3@zeolite和cspbi3@zeolite复合材料xrd衍射图谱。
32.图10是cspbbr3@zeolite复合材料tem图谱。
33.图11(a)是cspbbr3@zeolite复合材料的添加不同量的znbr2的发射图谱。
34.图11(b)是cspbi3@zeolite复合材料的添加不同量的zni2的发射图谱。
35.图12(a)是cspbbr3@zeolite复合材料温度相关的发射光谱。
36.图12(b)是cspbi3@zeolite复合材料。
具体实施方式
37.下面结合附图对本发明做进一步描述。
38.本发明涉及发光材料领域,具体涉及沸石(zeolite
‑
y)内部原位合成钙钛矿量子点cspbx3(x=br,i)发光材料。本发明采用离子交换法结合非极性有机引发剂成功制备了立方相cspbx3(x=br,i)纳米晶。将一定量的znm2(m=br,i)溶液滴入不发光的中间产物cs4pbcl6纳米晶体中,形成了明亮的、稳定的cspbx3纳米晶体。
39.本发明的目的是这样实现的
40.1、0.188mmol氯化铅,2.0ml油酸,2.0ml油胺和10ml十八烯溶液于100ml的三口圆底烧瓶中,真空120℃下搅拌30min后,通入氮气升温至150℃并维持10min。将预先制备好的2.5ml油酸铯快速注入该热溶液中。反应时间大概5s快速将热溶液通过冰水浴冷却至室温。最后以转速为9500转/分离心5min,用异丙醇洗涤沉淀离心2
‑
3次。真空干燥箱35℃烘干12h获得中间产物cs4pbcl6纳米晶。
41.2、0.3mmol溴化锌或者碘化锌和200μl油胺和10ml正己烷(辛烷或者氯仿)于20ml小烧杯中搅拌12h获得znm2(m=br,i)溶液。
42.3、不同znm2溶液的量(50,100,200,300,500,750,1000μl)滴加入cs4pbcl6纳米晶,室温条件下cs4pbcl6纳米晶快速转化成cspbx3量子点。
43.4、1.0g沸石(zeolite
‑
y)和0.0021g溴化铯分散在10ml去离子水并转移至单口圆底烧瓶中。该混合物在水浴60℃中搅拌24h。将产物离心并用去离子水洗涤,然后在80℃空气中干燥12h获得cs
+
‑
y。
44.5、通过在100ml三口圆底烧瓶中将0.376mmol氯化铅、2.0ml油酸、2.0ml油胺与10ml十八烯混合制备氯化铅溶液。将混合物在120℃真空搅拌下干燥30min。之后,往混合物通入氮气直到氯化铅完全溶解。为了制备cs4pbcl6@zeolite复合材料,将cs
+
‑
y(1g)与10ml十八烯一起装入100ml三口圆底烧瓶中。将混合物在真空和120℃下干燥30min。在氮气氛围下将反应温度升至150℃并再保持30min。将制备好的氯化铅溶液迅速注入热反应混合物中。将混合物搅拌约10min。然后使用冰水浴冷却混合物。最后,所得产物用异丙醇洗涤两
次,然后离心。cs4pbcl6@zeolite复合材料在40℃下干燥12h。
45.6、在cs4pbcl6@zeolite复合材料中加入不同量(50
‑
1000μl)的znm2(m=br,i)溶液,在室温条件下cs4pbcl6@zeolite转化为cspbx3@zeolite。
46.本发明针对现有材料稳定性制备所面临的技术难题,提出适用于近紫外/蓝光激发的钙钛矿量子点及制备方法,其化学组成为:cspbx3,其中卤素x为br,i中的一种。材料结构简单,合成方法简化,材料物理化学性能提升。材料发不同的光因卤素x的不同而不同,
47.(1)当x为br时,材料发绿光;
48.(2)当x为i时,材料发红光;
49.材料的合成采用易得廉价的化学品作为原材料,合成方法简单,其合成制备步骤如下:
50.步骤1、中间产物cs4pbcl6纳米晶的合成:
51.0.188mmol氯化铅,2.0ml油酸,2.0ml油胺和10ml十八烯溶液于100ml的三口圆底烧瓶中,真空120℃下搅拌30min后,通入氮气升温至150℃并维持10min。将预先制备好的2.5ml油酸铯快速注入该热溶液中。反应时间大概5s快速将热溶液通过冰水浴冷却至室温。最后9500转/分的转速下离心5min,用异丙醇洗涤沉淀离心2
‑
3次。真空干燥箱35℃烘干12h,x射线粉末衍射图谱表明其为纯相cs4pbcl6纳米晶。
52.步骤2、
53.(1)znm2(m=br,i)溶液的制备:
54.0.3mmol溴化锌或者碘化锌和200μl油胺和10ml正己烷(辛烷或者氯仿)转移至20ml小烧杯中搅拌12h。
55.(2)cspbx3量子点的合成:
56.不同的量(50,100,200,300,500,750,1000μl)znm2溶液滴加入cs4pbcl6纳米晶,室温条件下cs4pbcl6纳米晶快速转化成cspbx3量子点。转化过程可以书写为
57.2cs4pbcl6+3znbr2→
2cspbbr3+6cscl+3zncl2ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(1)
58.2cs4pbcl6+3zni2→
2cspbi3+6cscl+3zncl2ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(2)
59.步骤3、
60.(1)cs
+
‑
y的制备:
61.1.0g沸石(zeolite
‑
y)和0.0021g溴化铯分散在10ml去离子水并转移到单口圆底烧瓶中。该混合物在水浴60℃中搅拌24h。将产物离心并用去离子水洗涤,然后在80℃空气中干燥12h。cs
+
‑
y的形成可由以下化学方程式表示
62.na
+
‑
y+cs
+
→
→
cs
+
‑
y+na
+
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(3)
63.(2)cs4pbcl6@zeolite复合材料的合成:
64.通过在100ml三口圆底烧瓶中将0.376mmol氯化铅、2.0ml油酸、2.0ml油胺与10ml十八烯混合制备氯化铅溶液。将混合物在120℃真空和搅拌下干燥30min。之后,往混合物通入氮气直到氯化铅完全溶解。为了制备cs4pbcl6@zeolite复合材料,将cs
+
‑
y(1g)与10ml十八烯一起装入100ml三口圆底烧瓶中。将混合物在真空和120℃下干燥30min。在氮气氛围下将反应温度升至150℃并再保持30min。将制备好的氯化铅溶液迅速注入热反应混合物中。将混合物搅拌约10min。然后使用冰水浴冷却混合物。最后,所得产物用异丙醇洗涤两次,然后离心。cs4pbcl6@zeolite复合材料在40℃下干燥12h。该反应对应的化学方程式可以表示
为:
65.4cs
+
‑
y+pb
2+
+6x
‑
→
cs4pbx6‑
y
ꢀꢀꢀꢀꢀꢀꢀꢀ
(4)
66.(3)cspbx3@zeolite复合材料的合成:
67.在cs4pbcl6@zeolite复合材料中加入不同量(50,100,200,300,500,750,1000μl)的znm2(m=br,i)溶液,在室温条件下cs4pbcl6@zeolite转化为cspbx3@zeolite。该反应对应的化学方程式可以表示为:
68.2cs4pbcl6@zeolite+3znbr2→
2cspbbr3@zeolite+6cscl+3zncl2ꢀꢀꢀꢀꢀ
(5)
69.2cs4pbcl6@zeolite+3zni2→
2cspbi3@zeolite+6cscl+3zncl2ꢀꢀꢀꢀꢀ
(6)
70.本发明的有益效果是:
71.(1)材料结构组成简单,易于合成制备。解决了钙钛矿遇水容易分解、在空气里快速分解、物理和化学性质不稳定等问题。
72.(2)沸石无机物包覆可以使cspbx3@zeolite复合材料的稳定性极大提升。
73.(3)本发明所述制备方法操作简单,反应条件温和,在室温下溶液中即可反应完成,所使用设备简单。该方法对制备高效的、拥有潜在应用性的钙钛矿量子点提供了一种路径。
74.本发明所使用的原料是沸石na
+
‑
zeolite
‑
y(sio2/al2o3=5.1)、纯度为99.9%的csbr、znbr2、zni2、pbcl2、90%的油酸、十八烯和油胺、97%的正己烷、大于等于95%的辛烷和氯仿等。所有的试剂均直接使用,未经进一步处理和纯化。
75.实施例1:中间产物cs4pbcl6纳米晶的合成:
76.如图1所示为实施例1中cs4pbcl6单相xrd衍射图谱。如图2显示实施例1的cs4pbcl6单相tem图谱。
77.实施例2:cspbx3量子点的合成:
78.图3显示实施例2的(a)cspbbr3和(b)cspbi3单相xrd衍射图谱。
79.图4显示实施例2的(a)cspbbr3和(b)cspbi3单相tem图谱。
80.所得产物的xrd谱图如图3所示。衍射峰与立方相cspbbr3(pdf#84
‑
0464)非常吻合,进一步证实了成功的转变。使用tem表征产物。如tem图像(图4)所示,可以观察到具有立方形钙钛矿晶体结构的cspbbr3和cspbi3纳米晶。
81.图5照片显示实施例2的cs4pbcl6纳米晶向cspbx3纳米晶转化的过程(0
‑
15min)。
82.图6获得的cspbbr3和cspbi3纳米晶的吸收和发射光谱。插图显示了在紫外光(λ=365nm)下的强烈绿光和红光发射。
83.图7cspbx3纳米晶的整个形成过程示意图。
84.如图6所示,在吸收光谱中可以观察到505和660nm处的峰,它们归属于cspbx3纳米晶。相应的发射光谱显示亮绿色发射(511nm)和红色发射(678nm),半峰全宽分别为20和37nm。测得所得产品的量子效率为92%和50%。
85.图8(a)相应的cspbbr3纳米晶在不同溶剂中的发射光谱。(b)相应的cspbi3纳米晶在不同溶剂中的发射光谱。(c)cspbbr3纳米晶在不同溶剂中的照片。(d)cspbi3纳米晶在不同溶剂中的照片。
86.图8a
‑
b不同溶剂合成的量子点的发射强度也不同(正己烷>辛烷>氯仿)。图8c
‑
d显示了在紫外光照射下具有不同溶剂的cspbx3纳米晶的照片。
87.实施例3:cspbx3@zeolite复合材料的合成:
88.图9显示实施例3的na
+
‑
y,cs
+
‑
y,cs4pbx6@zeolite,cspbbr3@zeolite和cspbi3@zeolite复合材料xrd衍射图谱。
89.图10显示实施例3的cspbbr3@zeolite复合材料tem图谱。
90.图9xrd证实了cspbx3@zeolite复合材料的成功合成。cs4pbcl6@zeolite转化后cspbbr3@zeolite的tem如图10所示。我们可以清楚地看到,量子点位于沸石内部,其中一些不可避免地在外部合成。由于反应时间长且不受沸石内部骨架的限制,外部合成的量子点的尺寸大于内部合成的量子点的尺寸。
91.图11(a)显示实施例3的cspbbr3@zeolite复合材料的添加不同量的znbr2的发射图谱。(b)cspbi3@zeolite复合材料的添加不同量的zni2的发射图谱。
92.图12(a)cspbbr3@zeolite(b)cspbi3@zeolite复合材料温度相关的发射光谱。
93.制备的cspbx3@zeolite复合材料在紫外光激发下表现出强烈的绿光和红光发射。如图11所示,相应的发射光谱在519和689nm处显示了一个峰值。测得所得产物的量子效率分别为83%和46%。cspbx3@zeolite复合材料在空气中的稳定性大大提升。cspbx3@zeolite复合材料在高温下仍保持稳定的发光性能,这对其实际应用非常重要。因此,我们通过结合沸石封装来提高钙钛矿量子点的发光稳定性。图12显示实施例3的热衰减曲线。cspbx3@zeolite复合材料的温度依赖性发射光谱如图12。如图所示,发射强度随温度升高而降低,在100℃时发射强度仍为原始强度的40%。然而,当淬火温度为60℃时,未封装的钙钛矿量子点的发射强度已经低于原始强度的40%。
94.以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1