一种表面无机金属离子介导靶向作用的纳米材料及其应用的制作方法
1.本发明属于靶向纳米技术领域,具体是指一种表面无机金属离子介导靶向作用的纳米材料及其应用。
背景技术:
2.无机纳米材料因其良好的生物安全性、丰富的物理化学性质、比表面积大、表面易功能化修饰等优势,所构建的靶向纳米探针在肿瘤、心脑血管疾病的诊断与治疗等领域展现了广阔的应用前景。目前,纳米材料的靶向性主要通过在其表面偶联具有靶向功能的抗体、多肽、核酸等配体分子,与特定生物分子特异性结合,实现靶向作用。因此,配体的特异性对于纳米探针的靶向效率以及诊疗效果至关重要。提高纳米材料的靶向效率一直以来都是一大难题,为此,多篇文章以及专利等文件【theranostics,2016,6(11):1780.cn202110697471.2,cn202011534812.6,cn202010872013.3】都公开了在纳米材料表面修饰配体分子,实现提高配体介导的纳米探针靶向效率。
3.尽管通过配体分子表面修饰纳米材料可以实现靶向作用,但是现有的配体分子介导的靶向作用因非定向偶联技术常导致配体分子靶向结合位点难以有效暴露,配体分子在靶向过程中的利用度不足,影响其靶向效率。近年来,随着配体分子的定向偶联技术的发展,配体靶向位点得以充分暴露,但是定向偶联技术工艺较为复杂且制备成本较高,限制了其推广应用。
4.针对纳米材料生物医学应用中靶向效率不足的问题,本发明提供了一种表面无机金属离子介导靶向的纳米材料,与现有配体分子介导的靶向作用均不同,本发明利用纳米材料表面的无机金属离子和该离子对应的转运蛋白之间的选择性结合作用,在不修饰靶向配体的情况下,通过调控纳米材料中无机金属离子的含量以及表面无机金属离子的暴露量,实现了高效的靶向作用。本发明提供的一种表面金属离子介导靶向的纳米材料,为高特异性纳米探针的设计与构建提供了新思路。
技术实现要素:
5.为了满足生物医学应用对靶向纳米材料的需求,本发明提供一种表面无机金属离子介导靶向的纳米材料,通过调控纳米材料中无机金属离子的含量以及表面无机金属离子的暴露量,来进一步提高纳米颗粒靶向性的方法,并将其应用于磁共振成像、细胞示踪、磁颗粒成像以及靶向药物递送等领域。
6.为了实现上述功能,本发明采取的技术方案如下:一种表面无机金属离子介导靶向作用的纳米材料,所述纳米材料表面具有无机金属离子,其可以和细胞膜上的特定受体蛋白特异性结合,从而实现纳米材料对特定组织的靶向富集,纳米材料是对人体无害的纳米材料,如铁氧体纳米颗粒,量子点,上转换纳米材料,贵金属纳米颗粒等等。
7.优选的,所述纳米材料表面的无机金属离子是人体所含微量元素中的过渡金属元素中的至少一种,所述无机金属离子在所述纳米材料中的质量百分比为12%-60%。
8.优选的,所述纳米材料尺寸范围是1.5nm-5.5nm,所述的纳米材料形貌为球形、立方体、颗粒状、线状和片状中的至少一种,优选颗粒状。
9.优选的,所述纳米材料通过高温热分解法、共沉淀法、水热法或溶胶-凝胶法中的至少一种制备,并且通过配体交换或配体加成法进行表面修饰以使所述纳米材料能够分散于水相中。
10.本发明还提供了上述一种表面无机金属离子介导靶向的纳米材料的应用,所述纳米材料与细胞表达离子通道蛋白或金属离子转运蛋白特异性结合,实现纳米材料对特定组织的靶向富集,并通过调控所述纳米材料中所述无机金属离子的含量以及表面无机金属离子在纳米材料表面的暴露量,来调控其对所述特定组织的靶向富集的程度,可以应用于磁共振成像、细胞示踪、磁颗粒成像以及靶向药物递送等领域;其中,所述细胞表达离子通道蛋白包括:钠离子通道蛋白,钾离子通道蛋白,钙离子通道蛋白和镁离子通道蛋白中的至少一种;所述金属离子转运蛋白包括二价金属离子转运蛋白家族和溶质载体家族蛋白中的至少一种。
11.优选的,所述表达离子通道蛋白或金属离子转运蛋白的细胞包括正常或病变的体细胞或肿瘤细胞,所述正常细胞包括肝细胞、胆管细胞、胰腺细胞、结直肠细胞、乳腺细胞、肾细胞、胃细胞、甲状腺细胞和成骨细胞中的至少一种;所述肿瘤细胞包括肝癌细胞、胆管癌细胞、胰腺癌细胞、结直肠癌细胞、乳腺癌细胞、肾癌细胞、胃癌细胞、甲状腺癌细胞和骨肿瘤细胞中的至少一种。
12.优选的,所述特定组织为病灶组织或正常组织。
13.本发明采取上述方案取得有益效果如下:本发明的一种表面金属离子介导靶向作用的纳米材料,通过调控纳米材料中无机金属离子的含量以及表面无机金属离子在纳米材料表面的暴露量,来调控其对所述特定组织的靶向富集的程度,可实现纳米材料的靶向效率的提高,因而能够更好的应用于磁共振成像、细胞示踪、磁颗粒成像以及靶向药物递送等领域。
附图说明
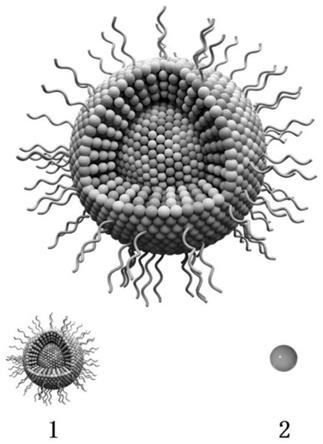
14.图1为根据本发明的一些实施例所示的一种表面无机金属离子介导靶向作用的纳米材料结构示意图;
15.图2为根据本发明的一些实施例所示的纳米探针的制备流程图;
16.图3为本发明实施例1的锰铁氧体纳米颗粒透射电镜图;
17.图4是本发明实施例1的锰铁氧体纳米颗粒金属元素分析图;
18.图5是本发明实施例1的锰铁氧体纳米颗粒尺寸分布图;
19.图6为本发明实施例1的锰铁氧体纳米颗粒和肝细胞表面slc39a14蛋白特异性结合的超分辨结构光显微成像图;
20.图7为本发明实施例2的定量表征肝细胞特异性内吞不同锰含量的锰铁氧体纳米颗粒;
21.图8是本发明实施例3中定量锰铁氧体纳米颗粒活体肝细胞特异性磁共振成像;
22.图9是本发明实施例3中铜铁氧体纳米颗粒活体骨组织特异性磁共振成像。
23.其中,1为纳米颗粒,2为表面金属离子,a为前驱体,a为肝脏,b为胆囊。
具体实施方式
24.下面对本发明的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
25.图1是根据本发明的一些实施例所示的一种表面金属离子介导靶向作用的纳米材料结构示意图,如图1所示,纳米材料表面具有无机金属离子,纳米材料为对人体无害的纳米材料,例如:铁氧体纳米颗粒,量子点,上转换纳米材料,贵金属纳米颗粒等等;无机金属离子为人体所含的微量元素中的过渡金属元素,具体的,无机金属离子可以是铁、锌、铜、锰、镁等中的至少一种;该纳米材料可以将物质向目标组织递送,物质可以是对比剂或者药物等类似物或其组合,而目标组织可以是病灶组织(如肿瘤)或正常组织;而表面无机金属离子可以与目标组织中细胞表面的特定蛋白结合,以实现所述纳米材料向目标组织靶向富集。
26.细胞表达离子通道蛋白包括:离子通道蛋白,金属离子转运蛋白,离子通道蛋白包括:钠离子通道蛋白,钾离子通道蛋白,钙离子通道蛋白(transient receptor potential vanilloid subfamily)和镁离子通道蛋白至的至少一种;金属离子转运蛋白包括:二价金属离子转运蛋白家族(divalent metal transport,dmt)和溶质载体家族蛋白(solute carrier family 39(metal ion transporter))中的至少一种;
27.表达离子通道蛋白或金属离子转运蛋白的细胞包括正常或病变的体细胞或肿瘤细胞,正常细胞包括肝细胞、胆管细胞、胰腺细胞、结直肠细胞、乳腺细胞、肾细胞、胃细胞、甲状腺细胞、成骨细胞等;肿瘤细胞包含肝癌细胞、胆管癌细胞、胰腺癌细胞、结直肠癌细胞、乳腺癌细胞、肾癌细胞、胃癌细胞、甲状腺癌细胞、骨肿瘤细胞等。
28.在一些实施例中,所述纳米材料可以是具有成像功能的纳米材料,其可以使得所述对比剂或显影剂在正常组织或病灶组织上富集以实现对所述正常或病灶组织的靶向成像。在一些实施例中,所述纳米材料1可以是携带药物的纳米探针,其可以使得所述药物在肿瘤组织上富集以实现对所述肿瘤组织靶向治疗。
29.在一些实施例中,通过改变纳米材料表面的无机金属离子的含量,可以调控所述靶向富集的程度。
30.图2是该纳米材料的制备流程图,制备纳米材料通过步骤一s1,采用前驱体制备含有无机金属离子的纳米颗粒,并在进行表面修饰使其可以分散在水相中。在一些实施例中,步骤一中通过热分解法制备表面含有无机金属离子的纳米材料,并且通过表面修饰亲水性配体使其可以分散在水相中;在另一些实施例中,步骤一是直接在水相中合成表面含有无机金属离子的纳米材料。
31.实施例1:小于5nm的锰铁氧体纳米颗粒的制备及其肝细胞特异性研究,超小铁氧体纳米颗粒的制备可以通过热分解法、共沉淀法、微波辅助法等进行制备,本实施例主要以热分解为例。
32.(1)称量1.07g芥酸铁,0.62g油酸锰,1.61g油醇,0.56g油酸,加入10g苄醚中,置于50ml三口烧瓶内,进行热分解反应,在265℃反应30min反应结束;
33.(2)降温至50℃以下,采用氯仿分散-离心的方式对产物进行三次清洗。最终产物分散于10ml氯仿中;
34.(3)取1ml(2)中所得产物,50mg磷酸化的聚乙二醇(mpeg),加入15ml氯仿,在氩气保护下升温至50℃,进行配体交换反应;
35.(4)将(3)中所得产物分散在水相中,研究其表面锰离子介导的和肝细胞表面slc39a14蛋白的特异性作用。
36.对所制备的锰铁氧体纳米颗粒表面锰离子介导的肝细胞特异性进行一系列表征,具体是将所制备的超小氧化铁纳米颗粒分散在水中,取分散有纳米颗粒的水溶液滴在镀有碳膜的cu网上,自然干燥后做表征。
37.图3为磷酸化聚乙二醇修饰后的锰铁氧体纳米颗粒的透射电镜图,从图中可以看出,锰铁氧体纳米颗粒大小、形貌均一,尺寸在3nm左右;
38.图4是磷酸化聚乙二醇修饰后的锰铁氧体纳米颗粒的元素分析,可见该纳米颗粒含有锰铁两种无机金属元素;
39.图5是磷酸化聚乙二醇修饰后的锰铁氧体纳米颗粒的尺寸分布图,横坐标是颗粒尺寸,纵坐标是对应的颗粒数量,从图中可以看出纳米颗粒的尺寸主要分布范围是1.5-5.5纳米,优选分布范围为2.5-3.5纳米之间;
40.图6是将具有绿色荧光分子fitc标记的锰铁氧体纳米颗粒和肝细胞相互作用(slc39a14蛋白标记蓝色荧光),采用结构光超分辨显微镜成像图,图中绿色荧光是锰铁氧体纳米颗粒,蓝色荧光是slc39a14蛋白,图6-2到6-5是图6-1局部放大的图示;结果显示蓝色和绿色荧光重叠,表明锰铁氧体纳米颗粒可以特异性结合肝细胞膜上的slc39a14蛋白。
41.实施例2:锰铁氧体纳米颗粒肝细胞特异性随锰含量的变化规律
42.在相同条件下,将所制备的不同锰含量的锰铁氧体纳米颗粒和肝细胞共培养相同的时间,将细胞清洗干净后消解进行icp测试锰铁元素在细胞中的含量,定量表征肝细胞特异性内吞锰铁氧体颗粒的规律,表征该纳米颗粒表面锰离子依赖的肝细胞特异性;
43.图7是定量表征肝细胞内吞不同锰含量的锰铁氧体纳米颗粒的图,图中纵坐标是平均每个细胞的内吞量,横坐标是“1”,“2”,“3”,“4”,“5”,“6”分别代表纳米颗粒中锰的质量百分比含量为5%,12%,24%,31%,60%和70%的锰铁氧体纳米颗粒,结果显示随着锰含量增加肝细胞内吞量先增加后降低,5%锰含量的颗粒在每个细胞的平均内吞量仅有1.72pg,12%锰含量的颗粒在每个细胞的平均内吞量是5%锰含量颗粒内吞量的3.96倍,显示较好的特异性,随后内吞量随含量的增加而缓慢增加,当锰含量在70%是细胞的内吞量急剧降低,可能是因为较高的锰含量引起细胞毒性导致内吞量较低,因此锰含量范围在12%-60%的特异性较好。
44.实施例3:
45.1)锰铁氧体纳米颗粒肝细胞特异性磁共振成像
46.采用实施例1合成锰铁氧体纳米颗粒,将锰铁氧体纳米颗粒静脉注射至动物体内后,进行磁共振成像,肝细胞特异性的磁共振成像探针可以增强肝脏信号(箭头a),当探针被肝细胞清除至胆囊时,胆囊信号也会增强(箭头b)。
47.图8是锰铁氧体纳米颗粒进行肝细胞特异性成像,可以看出肝脏信号变亮、胆囊信号变量,胆囊信号变亮表明锰铁氧体纳米颗粒经肝细胞代谢至胆道系统,表明锰铁氧体纳米颗粒可以特异性靶向肝细胞,并且可以进行磁共振肝胆成像应用。
48.2)铜铁氧体纳米颗粒表面的铜离子介导的靶向骨组织磁共振成像
49.成骨细胞表面含有二价金属离子转运蛋白(divalent metal transport 1,dmt1),该蛋白可以特异性结合铁、铜、锌等离子,并转运进细胞。图9采用实施例1的中的热分解法制备超小铜铁氧体纳米颗粒与活体骨组织特异性磁共振成像图,超小铜铁氧体纳米颗粒表面修饰聚乙二醇,具体合成方法如下:称量1.07g芥酸铁,0.62g油酸铜,1.61g油醇,0.56g油酸,加入10g苄醚中,置于50ml三口烧瓶内,进行热分解反应,在265℃反应30min反应结束;待反应体系降温至50℃以下,采用氯仿分散-离心的方式对产物进行三次清洗,最终产物分散于10ml氯仿中;取1ml氯仿分散的纳米颗粒,50mg磷酸化的聚乙二醇(mpeg),加入15ml氯仿,在氩气保护下升温至50℃,进行配体交换反应;可得到聚乙二醇表面修饰的铜铁氧体纳米颗粒,通过调控芥酸铁和油酸铜的比例,铜离子在纳米颗粒中的含量可以调控。本实施例中铜铁氧体纳米颗粒经icp测试后铜离子和铁离子的比例为1:2。将铜铁氧体纳米颗粒静脉注射至动物体内后,进行磁共振成像,如图9所示,箭头是骨骼,可以看到骨骼信号被增强,且信号呈现中间低周围高,显示是骨骼增强而不是骨髓。
50.以上对本发明及其实施方式进行了描述,这种描述没有限制性,实施例中所示的也只是本发明的实施方式之一,实际的实施方式并不局限于此。总而言之如果本领域的普通技术人员受其启示,在不脱离本发明创造宗旨的情况下,不经创造性的设计出与该技术方案相似的工艺流程以及实施例,均应属于本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1