一种乳化低共熔溶剂及其在提取枸杞色素中的方法
1.本发明涉及食品深加工领域,具体涉及一种提取枸杞色素的方法。
背景技术:
2.枸杞是茄科枸杞属蔓生灌木植物,国内外各地均有分布,我国宁夏、青海、陕西、甘肃、内蒙古等地为枸杞的主要生产区。枸杞全身是宝,传统上,枸杞叶、花、果实和根等均可入药,是典型的药食两用植物。目前,枸杞果实和根依然被收录于《中华人民共和国药典》,分别称为枸杞子和地骨皮。
3.枸杞还具有免疫调节、抗氧化、抗衰老、抗疲劳、抗肿瘤、抗福射损伤、降血脂、降血糖、降血压、保肝、健脑、补肾、排毒、养颜和保护生殖系统等多项功能。现代医药研究表明,枸杞具有多种生物活性,甜菜碱、枸杞色素和枸杞多糖为其主要活性物质。枸杞色素是枸杞浆果中各种呈色物质的总称,主要成分是疏水性的类胡萝卜素及其酯。枸杞色素有消炎、抗疲劳、抗氧化、延缓衰老和预防肿瘤等重要的生物学功能,在医药保健领域有较好应用前景。枸杞色素性质较稳定,具安全可靠,无不良反应,颜色自然和富含营养成分等优点,是食品和化妆品行业常用的天然着色剂。随着枸杞色素的应用越来越广泛,如何提取得到质优价廉的高纯度枸杞色素已成为重要课题。
4.目前枸杞色素的提取方法主要有水浴法、索氏提取、微波辅助提取法、超声辅助提取法、超临界流体萃取等,这些提取工艺多以有机溶剂做提取剂,而有机溶剂提取时普遍存在提取耗时长,消耗溶剂量大,提取效率低,对设备造成了一定的损害,对环境造成污染等问题。
5.现有技术中也存在一些改进的枸杞色素提取方法。例如,中国专利文献cn102850820a公开了一种锐孔法制备枸杞色素微胶囊的方法,采用酸性乙醇浸提与微波提取枸杞色素,酸性乙醇浸提12-20小时,微波提取20-30分钟,重复提取2-3次,该方法具有提取时间过长、温度高、微波能耗大等问题;中国专利文献cn107459838b公开了一种亚临界萃取与膜分离纯化浓缩相结合制备枸杞类胡萝卜素色素的方法,该方法使用液态丁烷作为萃取剂,虽可循环使用,但液态丁烷是易燃易爆物,存在一定的危害性;中国专利文献cn106543769a公开了一种超声提取枸杞中玉米黄质为主的类胡萝卜素类单体色素的方法,该方法使用了乙醇、氢氧化钾、磷酸、盐酸、四氢呋喃、二氯甲烷等大量有机溶剂,不仅不可回收循环使用,而且生产成本高,安全性低,污染环境;中国专利文献cn107312354a公开了一种天然染料敏化剂枸杞色素的提取及其酰化的方法,该方法使用了乙醇、石油醚、乙醚等有机溶剂,不仅易燃易爆,而且污染环境;中国专利文献cn112142636b公开了一种提取分离枸杞果实中玉米黄质及其棕榈酸酯色素单体的方法,该方法使用了正己烷、二氯甲烷、乙腈等有机溶剂,不仅消耗溶剂量大,而且对设备具有一定的损害。
6.综上所述,目前从枸杞中提取色素的技术多使用有机溶剂,存在着溶剂耗量大、效率低、成本高、污染环境等各种问题。因此,需要寻找一种绿色环保且高效提取色素的新型绿色溶剂来提取枸杞色素,具有广阔的应用前景和重要的现实意义。
7.近年来,低共熔溶剂(deep eutectic solvent,des)作为一种新型绿色的溶剂在各种生物活性物质的萃取分离方面得到广泛应用,已被公认为是传统溶剂的替代品。低共熔溶剂大多由有机盐和有机分子通过氢键、共价键等相互作用组合而成。des具有合成简单、纯度高、制备成本低、毒性低和可生物降解等优点。此外,大多数des与水不反应,在室温下为液态。des在萃取过程中用作溶剂的方法取决于其粘度、密度和极性等物理性质,而选择低粘度的溶剂混合,有利于相分离。随着对des研究的不断深入,发现其在生物活性物质的萃取和分离领域也有广泛的应用,如dna提取,木质素提取、蛋白质的提取和酚酸的萃取等。
8.低共熔溶剂在枸杞有效成分提取中的应用较少,主要体现在枸杞多糖的提取方面。例如,中国专利文献cn113698506a公开了一种温度响应型低共熔溶剂及提取枸杞多糖的方法,该低共熔溶剂由氢键供体和氢键受体混合形成,氢键供体为正辛酸、正癸酸、月桂酸、十四酸中的一种,氢键受体为丁卡因、利多卡因、普鲁卡因中的一种;中国专利文献cn112457426a公开了一种同时提取不同枸杞多糖组分的方法,是将枸杞与低共熔溶剂水溶液混合,进行脱脂,得到枸杞渣,然后加水进行均质提取,该低共熔溶剂为薄荷醇和乳酸的混合物。
9.随着公众对于“天然”、“环保”和“绿色”的要求不断提高,绿色化学成为近年的研究热点之一,低共熔溶剂作为一种无毒可降解的绿色溶剂,在各个领域都有广阔的应用前景。
技术实现要素:
10.本发明为了克服传统有机溶剂和低共熔溶剂的缺陷,提供一种绿色环保且高效的新型乳化低共熔溶剂来提取色素的方法,能够改善传统溶剂的一系列弊端,所得枸杞色素提取率和纯度显著高于传统溶剂提取法。该方法具有效率高、能耗低、操作便利、新型绿色、无三废排放、溶剂可循环使用等优点。
11.本发明提供了一种提取枸杞色素的方法,包括以下步骤:
12.步骤1:利用乳化剂将低共熔溶剂进行乳化;所述乳化剂优选为吐温20;
13.步骤2:利用乳化后的低共熔溶剂对枸杞原料进行提取,得到枸杞浸提液,其中,所述低共熔溶剂由氢键供体和氢键受体组成;
14.步骤3:利用大孔树脂吸附法将步骤2得到的枸杞浸提液中的枸杞色素吸附,经乙酸乙酯洗脱后蒸发,然后干燥得到枸杞色素。
15.优选的是,所述低共熔溶剂乳化的步骤包括:将低共熔溶剂、蒸馏水以及乳化剂混合,经涡旋后,加热搅拌得到乳化后的低共熔溶剂。
16.上述任一项优选的是,步骤1中,所述乳化的步骤包括:将所述低共熔溶剂、蒸馏水和乳化剂混合,经涡旋后,在55~80℃下搅拌15min,得到乳化后的低共熔溶剂。优选的,所述乳化剂为吐温20;进一步优选的,所述低共熔溶剂、蒸馏水和乳化剂的体积比(1~9)ml:(1~9)ml:(0.15~0.75)ml,优选为5ml:5ml:0.3ml;进一步优选的,所述涡旋时间为1~2min,加热方式为水浴加热,水浴温度为55℃~80℃,搅拌时间为15min,在此条件下,乳化效果更好。
17.进一步地,所述乳化剂为吐温20,步骤(1)中,所述低共熔溶剂与蒸馏水的混合液
和乳化剂吐温20的体积比为10:(0.15~0.75)ml。例如,低共熔溶剂与蒸馏水的混合液和乳化剂吐温20的体积比可以为:10ml:0.15ml,10ml:0.30ml,10ml:0.45ml,10ml:0.60ml,10ml:0.75ml。在此条件下,优化乳化剂吐温20的添加量,使低共熔溶剂和蒸馏水能很好的混合在一起,提高了枸杞色素的提取效果。
18.进一步地,所述低共熔溶剂和蒸馏水的体积比(1~9)ml:(1~9)ml。例如,低共熔溶剂和蒸馏水的体积比可以为:1ml:9ml,2ml:8ml,3ml:7ml,4ml:6ml,5ml:5ml,6ml:4ml,7ml:3ml,8ml:2ml,9ml:1ml。在此条件下,减少低共熔溶剂的用量,不仅使得枸杞色素提取效果较优,且不会造成浪费。
19.上述任一项优选的是,步骤2中,所述氢键供体为乳酸,所述氢键受体为薄荷醇,所述薄荷醇和乳酸摩尔比为(1~2):(1~8),进一步的优选为1:1,1:2,1:3,1:5,1:6,1:7,1:8。所述薄荷醇和乳酸摩尔比优选为1:4,在该比例下的低共熔溶剂更为澄清、透明且粘度小,更适合用于枸杞色素的提取。
20.上述任一项中优选的是,所述低共熔溶剂的制备方法包括以下步骤:将所述薄荷醇和乳酸混合,于75~95℃搅拌至澄清,得到所述低共熔溶剂。例如,搅拌时的温度可以为75℃,76℃,77℃,78℃,79℃,80℃,81℃,82℃,83℃,84℃,85℃,86℃,87℃,88℃,89℃,90℃,91℃,92℃,93℃,94℃,95℃。搅拌时的温度优选为80~90℃,在此范围下的低共熔溶剂更为澄清、透明且粘度小,更适合用于枸杞色素的提取。
21.上述任一项优选的是,所述薄荷醇和乳酸混合后以氢键形式结合到一起,形成低共熔混合物。两者的纯度需要大于95%。
22.上述任一项优选的是,步骤2中,所述提取的步骤包括:将枸杞原料、乳化后的低共熔溶剂混合,经搅拌、离心,得到枸杞浸提液,优选的,所述枸杞原料和乳化后的低共熔溶剂的质量体积比1g:(10~140)ml,进一步优选为1g:100ml;进一步优选的,所述搅拌为在20~40℃下搅拌0.5~3.0h,例如,搅拌温度可以为20℃,25℃,30℃,35℃,40℃,搅拌时间可以为0.5h,1.0h,1.5h,2.0h,2.5h,3.0h,优选为在30℃下搅拌2.5h;进一步优选为在30℃下搅拌2.5h;进一步优选的,所述离心为在10000~12000rpm转速下离心10~15min,离心2次。优选在12000rpm转速下离心10min,离心2次。
23.上述任一项优选的是,所述枸杞原料为枸杞粉。
24.上述任一项优选的是,所述枸杞粉的制备方法包括:将枸杞果经干燥、粉碎、过筛,得到枸杞粉。
25.上述任一项优选的是,枸杞果干燥为将所述枸杞果干燥至水分含量为5~10%;枸杞果经干燥、粉碎后,过60~100目筛。例如,可以将枸杞果经烘箱60℃过夜干燥。
26.进一步地,所述枸杞原料为枸杞粉,步骤(2)中,所述枸杞粉和乳化后低共熔溶剂的质量体积比为1g:(10~140)ml。例如,枸杞粉和乳化后低共熔溶剂的质量体积比可以为:1.0g:10ml,1.0g:20ml,1.0g:40ml,1.0g:60ml,1.0g:80ml,1.0g:100ml,1.0g:120ml,1.0g:140ml。在此条件下,减少枸杞粉的用量,不仅减少枸杞原料的浪费,还使枸杞色素提取效果较优。
27.上述任一项优选的是,步骤3中,所述吸附的步骤包括:将所述枸杞浸提液用大孔吸附树脂ab-8进行吸附,然后用乙酸乙酯进行洗脱,得到的洗脱液再经过旋转蒸发即可得到枸杞色素样品。
28.上述任一项优选的是,所述提取枸杞色素的方法还包括:将步骤2中离心得到的枸杞渣重复步骤2至3进行二次提取分离。
29.上述任一项优选的是,所述提取枸杞色素的方法还包括:将步骤2中枸杞浸提液用树脂ab-8吸附后,经乙酸乙酯洗脱,得到的洗脱液再经过旋蒸,分别回收低共熔溶剂和乙酸乙酯,并将回收得到的低共熔溶剂和乙酸乙酯循环使用。
30.用乳化后的薄荷醇-乳酸体系从枸杞中提取枸杞色素,主要是利用该体系具有对生物大分子(枸杞色素)很好的萃取效果的特性,在整个提取过程中,枸杞色素溶于乳化后低共熔溶剂中,并且枸杞色素在乳化后低共熔溶剂中具有较高的溶解度,因此,当枸杞色素被大孔吸附树脂吸附后,低共熔溶剂中不溶解大量的溶质(枸杞色素),仍具有继续萃取枸杞色素的能力,即已提取过枸杞色素并利用大孔树脂吸附后的回收的低共熔溶剂仍可用于枸杞色素的提取。
31.本发明技术方案,具有如下优点:
32.1、本发明利用乳化后低共熔溶剂法提取枸杞色素,是利用薄荷醇、乳酸以及乳化剂结合到一起形成乳化后低共熔溶剂,基于该乳化后低共熔溶剂对枸杞色素具有高度溶解和特异性作用的能力,实现枸杞中色素的高效提取。具体而言,本发明利用乳化后低共熔溶剂提取枸杞色素,使其有效地溶解于溶剂中,然后利用大孔树脂吸附枸杞色素,经乙酸乙酯洗脱后旋转蒸发,然后干燥得到枸杞色素。
33.2、与传统的有机溶剂法提取枸杞色素相比,利用乳化后低共熔溶剂提取枸杞中的枸杞色素不需要使用大量的有毒或低毒有机溶剂,不会造成浪费和污染。因此,本发明提供的方法克服了传统有机溶剂提取枸杞色素的方法所存在污染环境、效率低、能耗高等一系列问题。有利于降低能耗,提高效率,同时本发明提取的枸杞色素提取率和产物纯度均比传统有机溶剂提取法得到大幅提高。
34.3、本发明提供的方法中所使用的低共熔溶剂和乙酸乙酯可回收利用,回收后的低共熔溶剂仍表现为均匀液体状态,无固态沉淀,重复利用性好,回收后仍可作为溶剂来提取枸杞色素,仍有较高的提取率,具有无废液、废物排放,绿色环保的优点。
附图说明
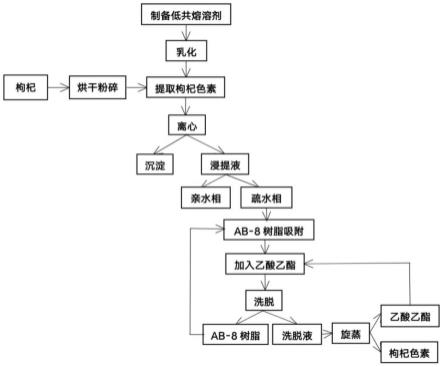
35.图1为本发明实施例7提取枸杞色素的工艺流程图;
36.图2为本发明实施例1制备的枸杞粉;
37.图3为本发明实施例3制备的低共熔溶剂;
38.图4为本发明的β-胡萝卜素标准品在220nm~600nm的波长扫描图;
39.图5为本发明的β-胡萝卜素标准品的标准曲线;
40.图6为本发明实施例1中不同低共熔溶剂(辛酸-癸酸、辛酸-月桂酸、薄荷醇-癸酸、薄荷醇-乳酸、辛酸-癸酸-乙酸)乳化前后对枸杞色素的提取含量。
具体实施方式
41.本发明通过以下实施例进行更加清晰、完整的描述,但所描述的实例仅是本发明一部分实施例,并非全部。所述实施例为帮助理解本发明,不应依此来局限本发明的保护范围。
42.实施例中所用的枸杞果为红色枸杞品种,购自宁夏中宁县。
43.实施例中各指标的检测和计算方法如下:
44.低共熔溶剂的色素提取含量:
45.利用紫外分光光度法测定枸杞浸提液中的色素含量,色素提取含量按照下式进行计算:
46.色素提取含量(mg/g)=浸提液中的色素质量/样品质量
47.样品(枸杞粉)中色素含量采用紫外分光光度计进行检测。
48.采用紫外分光光度计法测定色素含量的方法如下:
49.(1)枸杞色素最大吸收波长的测定:精密称取5.0mgβ-胡萝卜素标准品,以无水乙醇溶解并定容至50ml容量瓶中,制成0.1mg/ml的β-胡萝卜素标准溶液。以无水乙醇为空白对照,在220nm~600nm波长范围内进行全波长扫描,确定枸杞色素最大吸收波长的测定波长。
50.(2)以β-胡萝卜素为标准品制作标准曲线:分别取(1)制备好的0.1mg/ml的β-胡萝卜素标准溶液用无水乙醇稀释为0.005,0.025,0.05,0.075mg/ml,然后分别用0.005、0.025、0.05、0.075、0.1mg/ml一系列浓度的β-胡萝卜素的标准溶液,在最大吸收波长处测其吸光度。以β-胡萝卜素浓度为横坐标,吸光度为纵坐标,作标准曲线,并进行线性拟合,求得回归方程。样品同标曲之操作,测定吸光值,代入标准曲线,即可得色素含量。如图4所示,为本发明的β-胡萝卜素标准品在220nm~600nm的波长扫描图;如图5所示,为本发明的β-胡萝卜素标准品的标准曲线。
51.实施例1
52.与其他低共熔溶剂乳化前后的对比
53.对比不同低共熔溶剂(辛酸-癸酸、辛酸-月桂酸、薄荷醇-癸酸、薄荷醇-乳酸、辛酸-癸酸-乙酸)乳化前后对枸杞色素的提取效果,具体方法如下:
54.按照如下步骤制备枸杞粉:
55.将枸杞果放置在阴凉、干燥通风处自然风干,在烘箱中60℃温度下烘至枸杞果水分含量约10%,再用粉碎机将其粉碎,过80目筛,得到枸杞粉,如图2所示。
56.按照如下步骤制备低共熔溶剂:
57.辛酸-癸酸:将辛酸和癸酸按照摩尔比3:1:混合,于85℃搅拌至澄清;辛酸-月桂酸:将两者按照摩尔比3:1混合,于85℃搅拌至澄清;薄荷醇-癸酸:将两者按照摩尔1:1混合,于85℃搅拌至澄清;薄荷醇-乳酸:将两者按照摩尔比1:2混合,于85℃搅拌至澄清;辛酸-癸酸-乙酸:将辛酸、癸酸和乙酸按照摩尔比2:1:1混合,于85℃搅拌至澄清。
58.低共熔溶剂不进行乳化的操作如下:
59.称取枸杞粉1.0g置于试管中,加入10ml低共熔溶剂,在30℃水浴条件下磁力搅拌1.5h后,在12000rpm转速下离心10min,离心2次,得到枸杞色素的浸提液。以蒸馏水为空白对照,在最大吸收波长452nm下测浸提液吸光度,确定枸杞色素的提取含量。
60.低共熔溶剂进行乳化的操作如下:
61.(1)准确吸取7ml低共熔溶剂,3ml蒸馏水于试管中,再加入0.5ml吐温20,在55℃-80℃水浴下搅拌15min,得到乳化后的低共熔溶剂;
62.(2)称取枸杞粉1.0g置于试管中,加入(1)步乳化好的低共熔溶剂,在30℃水浴条
件下磁力搅拌1.5h后,在12000rpm转速下离心10min,离心2次,得到枸杞色素的浸提液。以蒸馏水为空白对照,在最大吸收波长452nm下测浸提液吸光度,确定枸杞色素的提取含量。
63.计算各低共熔溶剂乳化前后的枸杞色素提取含量。
64.各低共熔溶剂乳化前后对枸杞色素的提取含量如图6所示,在相同条件下,乳化后的薄荷醇-乳酸低共熔溶剂体系对枸杞色素具有较高的提取效果,可以用于枸杞色素的提取。
65.实施例2
66.低共熔溶剂在不同乳化剂吐温20添加量下提取枸杞色素
67.按照如下步骤制备枸杞粉:
68.将枸杞果放置在阴凉、干燥通风处自然风干,在烘箱中60℃温度下烘至枸杞果水分含量约10%,再用粉碎机将其粉碎,过80目筛,得到枸杞粉。
69.按照如下步骤制备低共熔溶剂:
70.将薄荷醇和乳酸按照摩尔比1:2混合,于85℃搅拌至澄清,得到低共熔溶剂。
71.按照如下步骤提取枸杞色素:
72.(1)分别准确吸取7ml低共熔溶剂,3ml蒸馏水于试管中,再加入0.15ml、0.30ml、0.45ml、0.60ml、0.75ml吐温20,在55℃-80℃水浴下搅拌15min,得到乳化后的低共熔溶剂;
73.(2)分别称取若干份1.0g枸杞粉,加入(1)步乳化好的低共熔溶剂,在30℃水浴条件下磁力搅拌1.5h后,在12000rpm转速下离心10min,离心2次,得到枸杞色素的浸提液。以蒸馏水为空白对照,在最大吸收波长452nm下测浸提液吸光度,确定最佳的乳化剂吐温20添加量。
74.本实施例不同吐温20添加量下得到的色素提取含量如表1所示。
75.表1不同吐温20添加量下的色素提取含量
76.吐温20添加量(ml)0.150.300.450.600.75色素提取含量(mg/g)8.9310.199.636.515.64
77.如表1所示,当吐温20添加量在0.30ml时枸杞色素的提取含量最高,为10.19mg/g。
78.实施例3
79.低共熔溶剂在不同摩尔比下提取枸杞色素
80.按照如下步骤制备枸杞粉:
81.将枸杞果放置在阴凉、干燥通风处自然风干,在烘箱中60℃温度下烘至枸杞果水分含量约10%,再用粉碎机将其粉碎,过80目筛,得到枸杞粉。
82.按照如下步骤制备低共熔溶剂:
83.将薄荷醇和乳酸分别按照摩尔比2:1,1:2,1:4,1:6,1:8混合,于85℃搅拌至澄清,得到低共熔溶剂,如图3所示。
84.按照如下步骤提取枸杞色素:
85.(1)分别准确吸取7ml低共熔溶剂,3ml蒸馏水于试管中,再加入0.30ml吐温20,在55℃-80℃水浴下搅拌15min,得到乳化后的低共熔溶剂;
86.(2)分别称取若干份1.0g枸杞粉,加入(1)步乳化好的低共熔溶剂,在30℃水浴条件下磁力搅拌1.5h后,在12000rpm转速下离心10min,离心2次,得到枸杞色素的浸提液。以蒸馏水为空白对照,在最大吸收波长452nm下测浸提液吸光度,确定最佳的低共熔溶剂的摩
尔比。
87.本实施例低共熔溶剂的不同摩尔比下得到的色素提取含量如表2所示。
88.表2低共熔溶剂的不同摩尔比下的色素提取含量
89.薄荷醇:乳酸(mol)2:11:21:41:61:8色素提取含量(mg/g)5.8810.6112.999.348.53
90.如表2所示,当低共熔溶剂的摩尔比为1:4时枸杞色素的提取含量最高,为12.99mg/g。
91.实施例4
92.低共熔溶剂在不同料液比下提取枸杞色素
93.按照如下步骤制备枸杞粉:
94.将枸杞果放置在阴凉、干燥通风处自然风干,在烘箱中60℃温度下烘至枸杞果水分含量约10%,再用粉碎机将其粉碎,过80目筛,得到枸杞粉。
95.按照如下步骤制备低共熔溶剂:
96.将薄荷醇和乳酸按照摩尔比1:4混合,于85℃搅拌至澄清,得到低共熔溶剂。
97.按照如下步骤提取枸杞色素:
98.(1)分别准确吸取7ml低共熔溶剂,3ml蒸馏水于试管中,再加入0.30ml吐温20,在55℃-80℃水浴下搅拌15min,得到乳化后的低共熔溶剂;
99.(2)将枸杞粉和乳化后的低共熔溶剂按照质量体积比分别为1.0g:10ml,1.0g:20ml,1.0g:40ml,1.0g:60ml,1.0g:80ml,1.0g:100ml,1.0g:120ml,1.0g:140ml,称取若干份枸杞粉加入第(1)步乳化的低共熔溶剂,在30℃水浴条件下磁力搅拌1.5h后,在12000rpm转速下离心10min,离心2次,得到枸杞色素的浸提液。以蒸馏水为空白对照,在最大吸收波长452nm下测浸提液吸光度,确定最佳的料液比。
100.本实施例不同料液比下得到的色素提取含量如表3所示。
101.表3不同料液比下的色素提取含量
102.料液比(g:ml)1:101:201:401:601:801:1001:1201:140色素提取含量(mg/g)11.5814.1316.2217.7518.9421.4719.1518.77
103.如表3所示,当料液比为1:100时枸杞色素的提取含量最高,为21.47mg/g。
104.实施例5低共熔溶剂在不同加水量下提取枸杞色素
105.枸杞粉和低共熔溶剂的制备方法同实施例3。
106.按照如下步骤提取枸杞色素:
107.(1)将蒸馏水按照10%,20%,30%,40%,50%,60%,70%,80%,90%加入低共熔溶剂中于试管中溶解均匀,再加入0.30ml吐温20,在55℃-80℃水浴下搅拌15min,得到乳化后的低共熔溶剂;
108.(2)分别称取若干份1.0g枸杞粉,加入(1)步乳化好的低共熔溶剂,在30℃水浴条件下磁力搅拌1.5h后,在12000rpm转速下离心10min,离心2次,得到枸杞色素的浸提液。以蒸馏水为空白对照,在最大吸收波长452nm下测浸提液吸光度,确定最佳的加水量。
109.本实施例不同加水量下得到的色素提取含量如表4所示。
110.表4不同加水量下的色素提取含量
111.加水量(%)1020304050607080色素提取含量(mg/g)9.7414.4619.3019.7928.2932.9746.0264.53
112.如表4所示,随加水量的增加,枸杞色素提取效果越好。但是也随着水量的增加,水量达到一定程度,低共熔溶剂很难和水分开,且当水量为100%时,提取效果最差,所以找到低共熔溶剂和水分离效果最好且色素提取效率好的点,作为最佳加水量点。从而选取加水量为50%时,枸杞色素提取含量为28.29mg/g。
113.实施例6
114.低共熔溶剂在不同温度下提取枸杞色素
115.枸杞粉和低共熔溶剂的制备方法同实施例3。
116.按照如下步骤提取枸杞色素:
117.(1)分别准确吸取5ml低共熔溶剂,5ml蒸馏水于试管中,再加入0.30ml吐温20,在55℃-80℃水浴下搅拌15min,得到乳化后的低共熔溶剂;
118.(2)称取若干份1.0g枸杞粉,加入(1)步乳化好的低共熔溶剂,分别在20℃,25℃,30℃,35℃和40℃水浴条件下磁力搅拌1.5h后,在12000rpm转速下离心10min,离心2次,得到枸杞色素的浸提液。以蒸馏水为空白对照,在最大吸收波长452nm下测浸提液吸光度,确定最佳的提取温度。
119.本实施例不同提取温度下得到的色素提取含量如表5所示。
120.表5不同提取温度下的色素提取含量
121.温度(℃)2025303540色素提取含量(mg/g)26.9327.9029.1128.4523.74
122.如表5所示,当提取温度在30℃时枸杞色素的提取含量最高,为29.11mg/g。
123.实施例7
124.低共熔溶剂在不同提取时间下提取枸杞色素
125.枸杞粉和低共熔溶剂的制备方法同实施例3。
126.按照如下步骤提取枸杞色素,工艺流程如图1所示:
127.(1)分别准确吸取5ml低共熔溶剂,5ml蒸馏水于试管中,再加入0.30ml吐温20,在55℃-80℃水浴下搅拌15min,得到乳化后的低共熔溶剂;
128.(2)称取若干份1.0g枸杞粉,加入(1)步乳化好的低共熔溶剂,在30℃水浴条件下分别磁力搅拌0.5h,1.0h,1.5h,2.0h,2.5h和3.0h后,在12000rpm转速下离心10min,离心2次,得到枸杞色素的浸提液。以蒸馏水为空白对照,在最大吸收波长452nm下测浸提液吸光度,确定最佳的提取时间。
129.本实施例不同提取时间下得到的色素提取含量如表6所示。
130.表6不同提取时间下的色素提取含量
131.提取时间(h)0.51.01.52.02.53.0色素提取含量(mg/g)27.5528.3329.5829.9332.0928.37
132.如表6所示,当提取时间在2.5h时枸杞色素的提取含量最高,为32.09mg/g。
133.实施例8
134.低共熔溶剂提取枸杞色素的可重复利用性
135.枸杞粉和低共熔溶剂的制备方法同实施例3。
136.按照如下步骤提取枸杞色素:
137.(1)准确吸取5ml低共熔溶剂,5ml蒸馏水于试管中,再加入0.30ml吐温20,在55℃-80℃水浴下搅拌15min,得到乳化后的低共熔溶剂;
138.(2)称取1.0g枸杞粉,加入(1)步乳化好的低共熔溶剂,在30℃水浴条件下磁力搅拌2.5h后,在12000rpm转速下离心10min,离心2次,得到枸杞色素的浸提液。
139.(3)将步骤(2)中离心后得到的枸杞浸提液收集,利用大孔树脂吸附法将枸杞色素吸附,经乙酸乙酯洗脱后旋转蒸发,然后干燥得到枸杞色素。在这一过程中分别回收低共熔溶剂和乙酸乙酯,并将回收得到的低共熔溶剂和乙酸乙酯循环使用。
140.(4)再次称取枸杞粉1.0g置于试管中,重复步骤(2)再次得到枸杞浸提液,在此过程中使用步骤(3)回收的低共熔溶剂。
141.利用大孔树脂吸附法分离回收低共熔溶剂,通过旋蒸收集乙酸乙酯,回收的处理方法几乎未造成溶剂损失,需要说明的是,在收集过程中有操作的原因如挂壁等现象会导致极为微量的损失,因此回收率约为100%。在包括色素的提取、利用大孔树脂吸附法分离回收低共熔溶剂以及利用旋蒸的方式回收乙酸乙酯在内的整个工艺流程中,均未发现有乳酸或者薄荷醇晶体析出,同时也未出现低共熔溶剂凝固现象,说明低共熔溶剂体系未发生改变,可以重复用于枸杞色素的提取。
142.重复使用回收的低共熔溶剂所具有的提取效果说明低共熔溶剂在提取色素的过程中,以及大孔树脂吸附色素的过程中,只是利用物理法吸附枸杞色素,溶剂体系未被破坏,所以仍可用于枸杞色素的提取。
143.实验例9
144.与传统有机溶剂提取枸杞色素的方法对比
145.将本发明提供的低共熔溶剂提取枸杞色素的方法与传统有机溶剂提取枸杞色素的方法进行效果对比,得出的效果数据如表7所示。
146.低共熔溶剂提取枸杞色素的操作如下:
147.(1)准确吸取5ml低共熔溶剂,5ml蒸馏水于试管中,再加入0.30ml吐温20,在55℃-80℃水浴下搅拌15min,得到乳化后的低共熔溶剂;
148.(2)称取1.0g枸杞粉,加入(1)步乳化好的低共熔溶剂,在30℃水浴条件下磁力搅拌2.5h后,在12000rpm转速下离心10min,离心2次,得到枸杞色素的浸提液。以蒸馏水为空白对照,在最大吸收波长452nm下测浸提液吸光度,确定枸杞色素的提取含量。
149.传统有机溶剂提取枸杞色素的操作如下:
150.准确称取若干份1.0g枸杞粉,分别加入10ml不同的传统有机溶剂(无水乙醇、乙酸乙酯、异丙醇、丙酮、正己烷、乙醚),在30℃水浴条件下磁力搅拌2.5h后,在12000rpm转速下离心10min,离心2次,得到枸杞色素的浸提液。以蒸馏水为空白对照,在最大吸收波长452nm下测浸提液吸光度,确定枸杞色素的提取含量。
151.利用紫外分光光度法测定枸杞浸提液中的色素含量,色素提取含量按照下式进行计算:
152.色素提取含量(mg/g)=浸提液中的色素质量/样品质量
153.本实施例将本发明提供的低共熔溶剂提取枸杞色素的方法与传统有机溶剂提取
枸杞色素的方法进行效果对比,得出的效果数据如表7所示。
154.表7本发明低共熔溶剂提取和传统有机溶剂提取枸杞色素方法的效果对比
155.提取剂低共熔溶剂无水乙醇乙酸乙酯异丙醇丙酮正己烷乙醚色素提取含量(mg/g)32.091.034.991.515.515.485.65
156.如表7所示,本发明提供的低共熔溶剂提取法能够得到高提取的枸杞色素,并且相较于传统有机溶剂提取法显著提高了色素提取含量。
157.显然,上述实施例仅仅是为清楚地说明所作的举例,而并非对实施方式的限定。对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动。这里无需也无法对所有的实施方式予以穷举。而由此所引伸出的显而易见的变化或变动仍处于本发明创造的保护范围之中。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1