一种负性液晶化合物及其制备方法与应用与流程
1.本发明涉及液晶材料技术领域,尤其涉及一种负性液晶化合物及其制备方法与应用。
背景技术:
2.近年来,液晶显示装置发展越来越迅速,也发展出不同类型,如车载小型液晶显示装置、便携式液晶显示装置、超薄型液晶显示装置等等。以电视为例,其特点是重量轻、占据空间小、移动方便等,此外还有笔记本型个人电脑、手机等。
3.液晶材料作为环境材料在信息显示材料、有机光电子材料等领域中具有极大的研究价值和美好的应用前景。目前,tft-lcd产品技术已经成熟,成功地解决了视角、分辨率、色饱和度和亮度等技术难题,大尺寸和中小尺寸tft-lcd显示器在各自的领域已逐渐占据平板显示器的主流地位。但是对显示技术的要求一直在不断的提高,要求液晶显示器实现更快速的响应,降低驱动电压以降低功耗等,也就要求液晶材料具有低电压驱动、快速响应、宽的温度范围和良好的低温稳定性。
4.液晶材料本身对改善液晶显示器的性能发挥着重要的作用,为了改善材料的性能使其适应新的要求,新型结构液晶化合物的合成及结构-性能关系的研究成为液晶领域的一项重要工作。
5.鉴于此,特提出本发明。
技术实现要素:
6.本发明目的是提供目的在于提供一种新型结构的负性液晶化合物,通过对其结构进行优化,能够有效改善显示品质,使液晶材料达到低功耗和宽视角、高对比度的优良性能,具有重要的应用价值。
7.具体地,本发明提供以下技术方案:
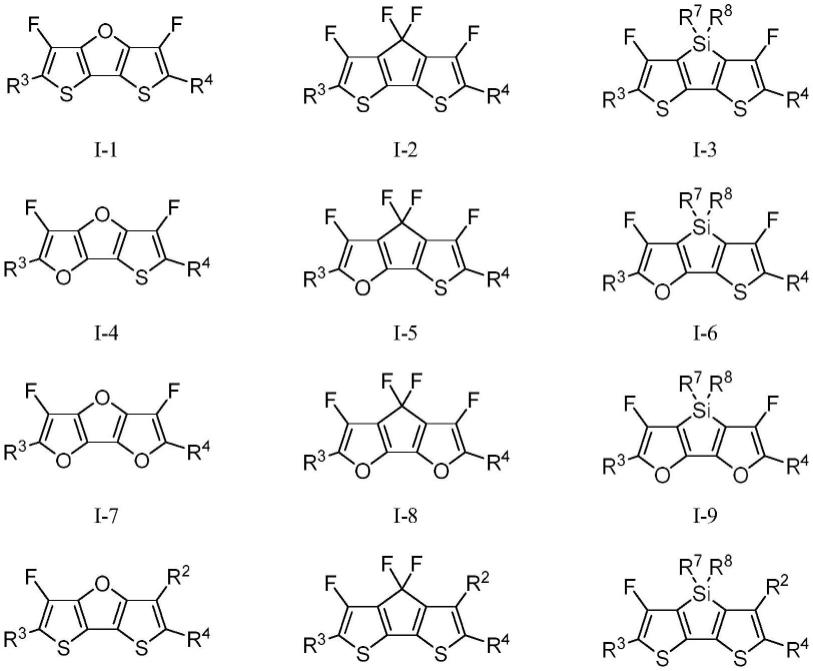
8.本发明提供一种液晶化合物,其具有如通式i所示的结构:
[0009][0010]
式i中,
[0011]
x1、x2各自独立地选自o或s;
[0012]
z选自o、c(r5r6)或si(r7r8);
[0013]
r1、r2、r3、r4、r5、r6、r7、r8各自相同或不同地选自由氢、氘、氟、氰基、c
1-c
40
的直链烷基、c
1-c
40
的直链烷氧基、c
1-c
40
的直链杂烷基、c
1-c
40
的直链杂烷氧基、c
3-c
40
的支链或环状的烷基、c
3-c
40
的支链或环状的烷氧基、c
3-c
40
的支链或环状的杂烷基、c
3-c
40
的支链或环状的杂烷氧基、c
2-c
40
的烯基或炔基、c
6-c
80
的芳基和c
2-c
60
的杂芳基组成的群组;且r1、r2、r3、
r4、r5、r6、r7、r8中的一个或多个氢原子可任选地被氟原子代替。
[0014]
作为优选,所述r1、r2、r3、r4、r5、r6、r7、r8各自相同或不同地含有如下基团:甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、2-甲基丁基、正戊基、仲戊基、新戊基、环戊基、正己基、新己基、环己基、正庚基、环庚基、正辛基、环辛基、2-乙基己基、环己烯基、庚烯基、环庚烯基、辛烯基、环辛烯基、乙炔基、丙炔基、丁炔基、戊炔基、己炔基、庚炔基或辛炔基。
[0015]
作为优选,所述r1、r2、r3、r4、r5、r6、r7、r8各自相同或不同地含有如下基团:甲氧基、三氟甲氧基、乙氧基、正丙氧基、异丙氧基、正丁氧基、异丁氧基、仲丁氧基、叔丁氧基、正戊氧基、仲戊氧基、2-甲基丁氧基、正己氧基、环己氧基、正庚氧基、环庚氧基、正辛氧基、环辛氧基、2-乙基己氧基、五氟乙氧基或2,2,2-三氟乙氧基。
[0016]
作为优选,在所述r1、r2、r3、r4、r5、r6、r7、r8中,所述c
1-c
40
的直链杂烷基与c
3-c
40
的支链或环状的杂烷基均是指其中单独的氢原子或-ch
2-基团能被氧、硫、卤素原子取代的基团。更优选地,所述r1、r2、r3、r4、r5、r6、r7、r8各自相同或不同地含有如下基团:烷氧基、烷硫基、氟代的烷氧基、氟代的烷硫基。最优选地,所述r1、r2、r3、r4、r5、r6、r7、r8各自相同或不同地含有如下基团:甲氧基、乙氧基、正丙氧基、异丙氧基、正丁氧基、异丁氧基、仲丁氧基、叔丁氧基、甲硫基、乙硫基、正丙硫基、异丙硫基、正丁硫基、异丁硫基、仲丁硫基、叔丁硫基、三氟甲硫基、三氟甲氧基、五氟乙氧基、五氟乙硫基、2,2,2-三氟乙氧基、2,2,2-三氟乙硫基、乙烯氧基、乙烯硫基、丙烯氧基、丙烯硫基、丁烯硫基、丁烯氧基、戊烯氧基、戊烯硫基、环戊烯氧基、环戊烯硫基、己烯氧基、己烯硫基、环己烯氧基、环己烯硫基、乙炔氧基、乙炔硫基、丙炔氧基、丙炔硫基、丁炔氧基、丁炔硫基、戊炔氧基、戊炔硫基、己炔氧基或己炔硫基。
[0017]
作为优选,所述r1、r2、r3、r4、r5、r6、r7、r8各自相同或不同地含有如下基团:环丙基、环丁基、环戊基、环己基、环丁烯基、环戊烯基、环己烯基、环庚基或环庚烯基,其中,一个或多个-ch
2-基团可被上述基团代替;此外,一个或多个氢原子还可被氘原子、卤素原子或氰基代替。
[0018]
作为优选,所述c
6-c
80
的芳基为c
6-c
60
的芳基。
[0019]
作为优选,所述芳基包括简单的芳族环,如苯或联苯,也包括稠合的芳族环,如蒽或菲。
[0020]
作为优选,所述c
2-c
60
的杂芳基含有2-60个碳原子和至少一个杂原子,碳原子和杂原子的总和至少是5。
[0021]
作为优选,所述杂原子选自n、o或s。
[0022]
作为优选,所述杂芳基包括简单的杂芳族环,如吡啶、嘧啶或噻吩,也包括稠合的杂芳族环,如喹啉或异喹啉。
[0023]
本发明中,所述芳基或杂芳基上的氢通过简单的替换或取代形成取代的芳基或取代的杂芳基,例如氟苯、二氟苯、三氟苯、四氟苯、环己基苯、环己基氟苯等。
[0024]
作为优选,所述r1、r2、r3、r4、r5、r6、r7、r8各自相同或不同地含有上述基团组成的群组。
[0025]
进一步地,所述r1、r2在每次出现时,各自独立地选自氢、甲基、乙基、氰基、三氟甲基、三氟乙基、五氟乙基、甲氧基或三氟甲氧基。
[0026]
作为优选,所述r1、r2各自独立地选自氢、氟、甲基、乙基、氰基、三氟甲基或三氟甲氧基,并且r1和r2至少有一者为氟。
[0027]
进一步地,所述r5、r6为氢或氟。
[0028]
进一步地,所述r7、r8各自独立地选自甲基或乙基。
[0029]
进一步地,所述x1、x2为s。
[0030]
作为优选,所述液晶化合物为以下所示结构中的任一种:
[0031][0032]
[0033]
进一步地,所述r1、r2在每次出现时,各自独立地选自氢、甲基、乙基、氰基、三氟甲基、三氟乙基、五氟乙基、甲氧基或三氟甲氧基。
[0034]
作为优选,所述液晶化合物选自式i-1、i-2、i-3、i-10、i-11、i-12、i-22或i-24。
[0035]
作为优选,所述式i的液晶化合物选自如下任一结构:
[0036][0037]
其中,r、r’各自独立地选自由氢、氟、氯、氰基、c
1-c7的烷基、c
3-c6的环烷基或c
2-c
12
的烯基,其中任意一个或多个不相邻的*-ch
2-*任选的被*-c≡c-*、*-coo-*、*-ooc-*、*-o-*、或*-s-*取代,任意一个或多个氢原子任选的被氟原子或氯原子取代。
[0038]
*—和—*指示取代基键合的位置。
[0039]
作为优选,所述液晶化合物为如下所示结构ls01-ls222中任一所示结构:
[0040]
[0041]
[0042]
[0043]
[0044]
[0045]
[0046]
[0047]
[0048]
[0049][0050]
其中,z为o、si(ch3)2或cf2。
[0051]
本发明还提供以上所述的液晶化合物的制备方法,其中:
[0052]
z为o的合成路线如下:
[0053][0054]
z为si(ch3)2或cf2的合成路线如下:
[0055][0056]
在本发明中,合成通式i所示液晶化合物的原料能够通过商业途径购买而得。
[0057]
本发明所述的合成方法,其原理、操作过程、常规后处理、过柱纯化、重结晶提纯等手段是本领域合成人员所熟知的,完全可以实现合成过程,得到目标产物。
[0058]
在本发明中,上述所有反应均在溶剂中进行,所述溶剂选自四氢呋喃、2-甲基四氢呋喃、n,n-二甲基甲酰胺、二甲基亚砜、1-甲基吡咯烷-2-酮、乙醇、甲醇、二氯甲烷、丙酮、甲苯和去离子水的一种或几种。
[0059]
本发明同时提供一种液晶介质,其包含一种或多种以上所述的液晶化合物。
[0060]
作为优选,所述液晶介质还包含一种或多种结构式为ii的化合物,作为第二组份:
[0061][0062]
其中,
[0063]
r7、r8各自独立地选自由以下a、b、c所定义的基团组成的群组:
[0064]
a:具有c
1-c7的直链烷基或具有c
1-c7的直链烷氧基;
[0065]
b:所述a中的任一基团中的一个或多个*-ch
2-*被*-o-*、*-coo-*、*-ooc-*或*-ch=ch-*代替后形成的基团;
[0066]
c:所述a中的任一基团中的一个或多个氢原子被f、cl、*-ch=ch2或*-ch=ch-ch3代替后形成的基团;
[0067]
环b、环c、环d、环e各自独立地选自由如下基团组成的群组:
[0068][0069]
并且在所述环b、环c、环d、环e中至少有一个选自中的一种;
[0070]
m、n、o各自独立地为0或1;
[0071]
z1、z2、z3各自独立地选自由单键、*-c2h
4-*、*-ch=ch-*、*-c≡c-*、*-coo-*、*-ooc-*、*-ch2o-*、*-och
2-*、*-cf2o-*和*-ocf
2-*组成的群组,其中任意的h可以被f代替;
[0072]
作为优选,所述液晶介质还包含一种或多种结构式为iii的化合物:
[0073][0074]
其中,
[0075]
r9、r
10
各自独立地选自由具有c
1-c
10
的烷基和具有c
2-c
10
的烯基组成的群组,其中任意的*-ch
2-*可以被*-ch2o-*、*-och
2-*和*-c≡c-*代替,任意的氢原子可以被氟原子代替;
[0076]
环f、环g、环i、环j各自独立地选自由如下基团组成的群组:
[0077][0078]
p、q、r各自独立地为0或1;
[0079]
z4、z5、z6各自独立地选自由单键、*-c2h
4-*、*-ch=ch-*、*-c≡c-*、*-coo-*、*-ooc-*、*-ch2o-*、*-och
2-*、*-cf2o-*和*-ocf
2-*组成的群组,其中任意的氢原子可以被氟原子代替。
[0080]
*—和—*指示取代基键合的位置。
[0081]
作为优选,在所述液晶介质中,所述液晶化合物的质量百分含量为1~24%,结构式为ii的化合物的质量百分含量为35~58%,结构式为iii的化合物的质量百分含量为30~46%。
[0082]
作为优选,所述结构式为ii的化合物为如下式ii-1~式ii-15所示的化合物中的任一种:
[0083][0084][0085]
其中,
[0086]
r7、r8各自独立地选自由以下a、b、c所定义的基团组成的群组:
[0087]
a:具有c
1-c7的直链烷基或具有c
1-c7的直链烷氧基;
[0088]
b:所述a中的任一基团中的一个或多个*-ch
2-*被*-o-*、*-coo-*、*-ooc-*或*-ch=ch-*代替后形成的基团;
[0089]
c:所述a中的任一基团中的一个或多个h被f、cl、*-ch=ch2或*-ch=ch-ch3代替后形成的基团;
[0090]
上述环h1、环h2各自独立地选自由如下基团组成的群组:
[0091][0092]
*—和—*指示取代基键合的位置。
[0093]
作为优选,所述结构式为iii的化合物为如下式iii-1~式iii-16所示的任一种:
[0094][0095][0096]
其中,r9、r
10
各自独立地选自由具有c
1-c
10
的烷基或具有c
2-c
10
的烯基组成的群组,其中任意的*-ch
2-*可以被*-ch2o-*、*-och
2-*和*-c≡c-*代替,任意的h可以被f代替;(f)各自独立地表示f或h。
[0097]
作为优选,所述液晶介质还包含功能性添加剂;所述功能性添加剂包含抗氧化剂、手性剂、光稳定剂、紫外线吸收剂的一种或多种。
[0098]
本发明还提供一种消费型产品,其包含以上所述的液晶介质。
[0099]
本发明中,所述的消费型产品包括但并不限于平板显示器、计算机监视器、医疗监视器、电视机、告示牌、用于内部或外部照明和/或发信号的灯、平视显示器、全透明或部分透明的显示器、柔性显示器、激光打印机、电话、蜂窝电话、平板电脑、平板手机、个人数字助
理(pda)、可佩戴装置、膝上型计算机、数码相机、摄像机、取景器、对角线小于2英寸的微型显示器、3-d显示器、虚拟现实或增强现实显示器、交通工具、包含多个平铺在一起的显示器的视频墙、剧院或体育馆屏幕、光疗装置和指示牌。
[0100]
如无特殊说明,本发明中所用原料均可通过市售商购获得,本发明所记载的任何范围包括端值以及端值之间的任何数值以及端值或者端值之间的任意数值所构成的任意子范围。
[0101]
基于上述技术方案,本发明的有益效果如下:
[0102]
由于二苯并呋喃或二苯并噻吩或芴分子的大平面共轭刚性结构,使此类化合物的响应速度和溶解性较差,限制其应用。令人惊奇的是,本发明的二噻吩并呋喃或二噻吩并芴平面共轭能力减弱,溶解性变好,使得液晶化合物表现出更好的互溶性和更快的响应速度,故利用本发明提供的式i所示化合物可改善液晶化合物的互溶性和响应速度,改善混晶低温稳定性,拓展液晶混合物的应用范围,具有重要的应用价值。
具体实施方式
[0103]
以下实施例用于说明本发明,但不用来限制本发明的范围。
[0104]
实施例中未注明具体技术或条件者,按照本领域内的文献所描述的技术或条件,或者按照产品说明书进行。所用试剂或仪器未注明生产厂商者,均为可通过正规渠道商购买得到的常规产品。
[0105]
本发明中,制备方法如无特殊说明则均为常规方法。所用的原料如无特别说明均可从公开的商业途径获得,所述百分比如无特殊说明均为质量百分比。本发明提供的一系列新型液晶化合物,所有的反应都是在众所周知的适合条件下进行,有些涉及到简单的有机制备,例如苯硼酸的制备均能通过熟练的操作技能合成,在本发明中没有详细描述。
[0106]
实施例1
[0107]
化合物ls11(z为o)的制备,包括如下步骤:
[0108]
第一步:化合物int-1的制备
[0109][0110]
在氮气保护下,30.0mmol的镁屑和80ml干燥的乙基叔丁基醚混合,加入1粒碘,升温回流至红色消失,滴加入20.0mmol的5-丙基-4-氟-2-溴噻吩溶于乙基叔丁基醚的溶液,继续回流反应2小时至镁屑消失,加入0.6mmol的nicl2(dppp)和36.0mmol的无水溴化锂,再加入24.0mmol的5-戊基-4-氟-2-溴噻吩,升温回流反应12小时,降到室温,加入50ml的2n稀盐酸水溶液,分出有机相干燥,过滤,滤液减压浓缩干,用硅胶柱分离纯化,乙醇重结晶,得到化合物int-1,收率:75%。
[0111]
第二步:化合物int-2的制备
[0112][0113]
在氮气保护下,20.0mmol的int-1溶于50ml的dmf中,加入42.0mmol的nbs,于室温搅拌反应12小时,将反应液倒入250ml的水中,用乙酸乙酯萃取,有机相用饱和盐水洗,分出有机相干燥,过滤,滤液减压浓缩干,用硅胶柱分离纯化,乙醇重结晶,得到化合物int-2,收率:87%。
[0114]
第三步:化合物int-3的制备
[0115][0116]
在氮气保护下,20.0mmol的int-2溶于50ml干燥的thf中,用液氮降温至-78℃,滴加入22.0mmol的1.5m正丁基锂正己烷溶液,搅拌反应1小时,再滴加入25.0mmol的硼酸三甲酯,升到室温搅拌反应1小时,加入50ml的2n稀盐酸水溶液,搅拌反应30分钟,用乙酸乙酯萃取,有机相干燥,过滤,滤液减压浓缩干,加入石油醚分散,过滤,得到化合物int-3和int-3’混合物,收率:78%。
[0117]
第四步:化合物int-4的制备
[0118][0119]
20.0mmol的int-3和int-3’混合物溶于60ml的二氯甲烷中,降温至0℃,加入10.0ml的30%过氧化氢,搅拌反应12小时,过滤,滤液分出有机相用5%的维生素c水溶液洗,有机相干燥,过滤,滤液减压浓缩干,硅胶柱分离纯化,得到化合物int-4和int-4’混合物,收率:87%。
[0120]
第五步:化合物ls11(z为o)的制备
[0121][0122]
20.0mmol的int-4和int-4’混合物溶于50ml的dmf中,加入40.0mmol的碳酸铯和2.0mmol的氧化铜,升温至120℃,搅拌反应12小时,降到室温,过滤,将滤液倒入150ml的水中,用乙酸乙酯萃取,有机相用饱和盐水洗,干燥,过滤,滤液减压浓缩干,硅胶柱分离纯化,得到化合物ls11(z为o),灰白色固体,收率:74%,hrms,m/z:329.0783[m+h]。1hnmr(δ、cdcl3):2.75~2.68(4h,m);1.66~1.60(4h,m);1.37~1.22(4h,m);1.08(3h,t);0.90(3h,t)。
[0123]
参照上述实施例1类似的合成方法,制备化合物ls01~ls138中z为o的化合物。
[0124]
实施例2
[0125]
化合物ls47(z为cf2)的制备,包括如下步骤:
[0126]
第一步:化合物int-5的制备
[0127][0128]
参照实施例1的合成方法,仅将实施例1中第一步的5-丙基-4-氟-2-溴噻吩替换为5-乙氧基-4-氟-2-溴噻吩,将5-戊基-4-氟-2-溴噻吩替换为5-戊氧基-4-氟-2-溴噻吩制备获得化合物int-5,收率:77%。
[0129]
第二步:化合物int-6的制备
[0130][0131]
参照实施例1的合成方法,仅将实施例1中第二步的int-1替换为int-5制备获得化合物int-6,收率:90%。
[0132]
第三步:化合物int-7的制备
[0133][0134]
在氮气保护下,30.0mmol的int-6溶解于60ml干燥的thf中,液氮降温到-78℃,滴加入66.0mmol的2.5m正丁基锂正己烷溶液,搅拌反应1小时,再滴加入33.0mmol的二甲氨基甲酰氯,升至室温搅拌反应12小时,加入20ml的饱和氯化铵水溶液,分出有机相,水相用乙酸乙酯萃取,有机相合并干燥,过滤,滤液减压浓缩干,用硅胶柱分离纯化,乙醇重结晶,得到化合物int-7,收率:76%。
[0135]
第四步:化合物ls47(z为cf2)的制备
[0136][0137]
在氮气保护下,20.0mmol的int-7溶解于40ml干燥的二氯甲烷中,降温到0℃,滴加入50.0mmol的dast,搅拌反应2小时,升到室温搅拌反应12小时,滴加入50ml的冰水,分出有机相,水用用二氯甲烷萃取,收集有机相再用饱和盐水洗,有机相干燥,过滤,滤液减压浓缩干,用硅胶柱分离纯化,乙醇重结晶,得到化合物ls47,浅黄色固体,收率:92%,hrms,m/z:381.0612[m+h]。1hnmr(δ、cdcl3):4.04~3.79(4h,m);1.75~1.68(2h,m);1.39~1.34(7h,m);0.87(3h,t)。
[0138]
参照上述实施例2类似的合成方法,制备化合物ls01~ls222中z为cf2的化合物。
[0139]
实施例3
[0140]
化合物ls125(z为sime2)的制备:
[0141][0142]
在氮气保护下,20.0mmol的int-8溶解于60ml干燥的thf中,液氮降温到-78℃,滴加入44.0mmol的2.5m正丁基锂正己烷溶液,搅拌反应1小时,再滴加入22.0mmol的二甲二氯化硅,升至室温搅拌反应1小时,加入20ml的饱和氯化铵水溶液,分出有机相,水相用乙酸乙酯萃取,有机相合并干燥,过滤,滤液减压浓缩干,用硅胶柱分离纯化,乙醇重结晶,得到化合物ls125,白色固体,收率:79%,hrms,m/z:499.1906[m+h]。1hnmr(δ、cdcl3):3.94~3.91(2h,t);3.75~3.73(2h,d);1.92~1.78(3h,m);1.52~1.39(7h,m);1.32~1.13(8h,m);1.08~0.96(2h,m);0.90~0.85(6h,m);0.12(6h,s)。
[0143]
参照上述实施例3类似的合成方法,制备化合物ls01~ls138中z为sime2的化合物。
[0144]
混合物实施例
[0145]
实施例4-11:
[0146]
实施例4-11列出了不同液晶介质的制备方法,其中,各实施例具体化合物的单体结构、用量(重量百分含量)、所得的液晶介质的性能参数测试结果分别如下表1-8所示。
[0147]
各实施例中所涉及的温度单位为℃,其他符号的具体意义及测试条件如下:
[0148]
c.p.表示液晶的清亮点(℃),测试仪器:mettler-toledo-fp system显微热分析仪;
[0149]
γ1为旋转粘度(mpa
·
s),测试条件为:25℃、instec:alct-ir1、18微米垂直盒;
[0150]k11
为扭曲弹性常数,k
33
为展曲弹性常数,测试条件为:25℃、instec:alct-ir1、18微米垂直盒;
[0151]
δε表示介电各向异性,δε=ε∥-ε
⊥
,其中,ε∥为平行于分子轴的介电常数,ε
⊥
为垂直于分子轴的介电常数,测试条件:25℃、instec:alct-ir1、18微米垂直盒;
[0152]
δn表示光学各向异性,δn=n
o-ne,其中,no为寻常光的折射率,ne为非寻常光的折射率,测试条件:589nm、25
±
0.2℃。
[0153]
本发明中,分别按比例称取通式i、ii和iii的化合物,制备得到液晶介质,其中液晶介质的制备所用的设备和仪器为:
[0154]
(1)电子精密天平(精确度0.1mg);
[0155]
(2)不锈钢烧杯:用于称量化合物原料;
[0156]
(3)勺子:用于加入原料;
[0157]
(4)磁力转子:用于搅拌;
[0158]
(5)控温电磁搅拌器。
[0159]
液晶介质的制备方法包括以下步骤:
[0160]
(1)将所用原料按顺序摆放整齐;
[0161]
(2)把不锈钢烧杯放置在天平上,用小勺将式i的化合物盛入不锈钢烧杯中;
[0162]
(3)依次按所需重量添加其他化合物原料;
[0163]
(4)把加好料的不锈钢烧杯放置在磁力搅拌仪器上加热融化;
[0164]
(5)待不锈钢烧杯中混合物大部份融化后,往不锈钢烧杯中加入一颗磁力转子,将液晶混合物搅拌均匀,冷却到室温后即得液晶介质。
[0165]
将所得的液晶介质填充于液晶显示器两基板间进行性能测试。
[0166]
实施例4的液晶介质的组分配比及其性能参数表1;
[0167]
表1
[0168]
[0169]
实施例5的液晶介质的组分配比及其性能参数表2;
[0170]
表2
[0171][0172][0173]
实施例6的液晶介质的组分配比及其性能参数表3;
[0174]
表3
[0175][0176][0177]
实施例7的液晶介质的组分配比及其性能参数表4;
[0178]
表4
[0179][0180][0181]
实施例8的液晶介质的组分配比及其性能参数表5;
[0182]
表5
[0183][0184][0185]
实施例9的液晶介质的组分配比及其性能参数表6;
[0186]
表6
[0187][0188][0189]
实施例10的液晶介质的组分配比及其性能参数表7;
[0190]
表7
[0191][0192]
实施例11的液晶介质的组分配比及其性能参数表8;
[0193]
表8
[0194]
[0195][0196]
对比例1
[0197]
配方如下表9所示,其组分中不包含结构式为式i的化合物,而包含式v的化合物。
[0198]
表9
[0199][0200][0201]
结论:由实施例9和对比例1对比可知,将二苯并噻吩液晶替换为本发明的二噻吩并呋喃和二噻吩并芴液晶后表现出良好的互溶性和低温稳定性,并且具有更大的负性介电常数。
[0202]
对比例2
[0203]
配方如下表10所示,其组分中不包含结构式为式i的化合物,而包含式为v的化合物。
[0204]
表10
[0205][0206]
结论:由实施例10和对比例2对比可知,将二噻吩并噻吩液晶替换为本发明的二噻吩并呋喃和二噻吩并芴液晶后表现出良好的互溶性和低温稳定性,并且具有更大的负性介电常数。
[0207]
由实施例4至实施例11的液晶组合物的性能参数可知,本发明提供的液晶组合物具有良好的互溶性和较大的负性介电常数,故利用本发明提供的式i所示的化合物可改善液晶化合物的互溶性,拓展液晶混合物的应用范围,具有重要的应用价值。
[0208]
虽然,上文中已经用一般性说明及具体实施方案对本发明作了详尽的描述,但在本发明基础上,可以对之作一些修改或改进,这对本领域技术人员而言是显而易见的。因此,在不偏离本发明精神的基础上所做的这些修改或改进,均属于本发明要求保护的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1