一种有机红色长余辉材料及其制备方法和应用与流程
1.本发明涉及有机长余辉材料技术领域,尤其涉及一种有机红色长余辉材料及其制备方法和应用。
背景技术:
2.长余辉发光材料简称长余辉材料(long persistent luminescence,长余辉)是一种光致发光材料。它是一类吸收能量并在激发停止后仍可继续发出光的物质,是一种具有应用前景的材料。长余辉发光材料,就是能够储存外界光辐照能量,在一定温度下(一般为室温),缓慢地以可见光的形式释放这些储存能量的材料。其发光原理属光致发光,即当受到光源激发时在激发态存储激发能,当激发停止后,再将能量以光的形式缓慢释放出来。1996年matsuzawa等发表了铕(eu)和镝(dy)掺杂的铝酸锶(sral2o4)体系,余辉衰减时间可长达10小时并具有很高的耐久性;随后这种稀土激活的铝酸盐长余辉材料就成为发光涂料的基础,获得了商业界的青睐,广泛应用在仪表显示、光电子器件、夜间应急指示以及国防军事等领域。然而这种基于无机体系的长余辉材料不仅需要昂贵的稀有元素,而且制造温度高达1000℃以上,能耗较高。为了解决这些问题,很多目光又集中在基于有机体系的长余辉材料之上。
3.目前,有机分子呈现出的室温磷光行为还比较少见,发光效率也比较低,导致磷光强度低和磷光持续时间短的问题,并且因为三线态激子会受到自旋耦合的限制,同时会被空气中的氧气所猝灭。
技术实现要素:
4.本发明的目的在于克服现有技术中的不足,提供一种有机红色长余辉材料及其制备方法和应用,该有机红色长余辉材料具有很好的柔性和透明性,在室温紫外灯下照射,能够产生肉眼可见的红色荧光,关闭激发光源,能够产生肉眼可见的红色余辉发光;并且该有机红色长余辉材料同时实现了室温条件下的荧光发射和磷光发射,具有高度的隐蔽性,使用方便,容易识别,从而实现更高级别的防伪功能,在有机光电材料以及防伪加密等领域具有很好的应用前景。
5.本发明是通过以下技术方案实现的:提供了一种有机红色长余辉材料,包括含有蒽醌胺的客体分子,含有阳离子季鏻自由基的主体分子,所述客体分子与所述主体分子以质量比为1:100熔融。
6.通过上述技术方案,本发明基于含有蒽醌胺的客体分子,以及含有阳离子季鏻自由基的主体分子,使得主体分子和客体分子之间通过光诱导电荷转移、电荷分离以及电荷重组,以产生有机长余辉材料;其具体实现机理为对于aeaq:ppt体系,当微量的aeaq分子分散并且嵌入到ppt结构中时,通过光诱导电子或空穴产生电荷分离态aeaq
·
+-(ppt)
n-ppt
·-,产生的ppt
·-可以在ppt晶体中发生电子转移,并最终达到与aeaq
·
+
高效分离的结果,产生电荷分离态。由于电荷分离(cs)态的能量高于aeaq三重态能量,允许从电荷分离态转换为
aeaq三重态。与aeaq从单重态到三重态占比23%的系间窜越过程相比,占比77%的电荷转移(et)过程可以有效生成长寿命cs态,长寿命cs态可以在水氧条件下诱导产生aeaq三重态,这一过程可以抑制aeaq由于氧等其他分子引起的激子猝灭现象,从而实现长寿命余辉现象。
7.本发明限定主体分子与客体分子以质量比为1:100熔融,在光激发期间,在主体分子和客体分子之间形成电荷转移态。然后,生成的主体分子自由基阴离子ppt
·-通过ppt体分子之间的电荷跳跃扩散,将1-氨基乙基氨基-9,10-蒽醌(aeaq)自由基阳离子aeaq
·
+
与主体分子的反自由基阴离子分离并形成稳定的电荷分离状态aeaq
·
+-(ppt)
n-ppt
·-。最后主体分子自由基阴离子和1-氨基乙基氨基-9,10-蒽醌(aeaq)自由基阳离子逐渐复合,并产生激发复合物发射,在光激发停止后很长时间仍会持续;故所得有机红色长余辉材料在紫外灯的照射下,能够产生肉眼可见的红色荧光,关闭激发光源,能够产生肉眼可见的红色余辉发光。
8.其具体实现机理如下:紫外光激发后使客体分子由单线态变成三线态,产生能量并回落发光。
9.掺杂主客体的荧光和磷光发射主要来自于客体分子。在主体的结构中客体分子可以吸收能量通过系间窜越从单线态转换为三线态;电荷分离态能量高于客体分子三线态能量,允许电荷从cs态转移到客体三线态,得出体系的长余辉发射主要来源于客体分子的室温磷光和伴随电荷分离态的延迟荧光。掺杂体系的长余辉发光包含客体分子的磷光发射波段和弱延迟荧光两个来源。
10.进一步地,优选地,所述客体分子为1-氨基乙基氨基-9,10-蒽醌(aeaq),具体结构式如上式;
11.通过上述技术方案,本发明限定1-氨基乙基氨基-9,10-蒽醌(aeaq)与主体分子以质量比为1:100熔融,在光激发期间,在1-氨基乙基氨基-9,10-蒽醌(aeaq)和主体分子之间形成电荷转移态。然后,生成的主体分子自由基阴离子通过主体分子之间的电荷跳跃扩散,将1-氨基乙基氨基-9,10-蒽醌(aeaq)自由基阳离子与主体分子的反自由基阴离子分离并形成稳定的电荷分离状态。最后主体分子自由基阴离子和1-氨基乙基氨基-9,10-蒽醌(aeaq)自由基阳离子逐渐复合,并产生激发复合物发射,在光激发停止后很长时间仍会持续;故所得有机红色长余辉材料在紫外灯的照射下,能够产生肉眼可见的红色荧光,关闭激发光源,能够产生肉眼可见的红色余辉发光。
12.进一步地,优选地,所述主体分子为1,5-二氨基蒽醌,具体结构式如下:
13.[0014][0015]
通过上述技术方案,本发明限定1,5-二氨基蒽醌与主体分子以质量比为1:100熔融,在光激发期间,在1,5-二氨基蒽醌和主体分子之间形成电荷转移态。然后,生成的主体分子自由基阴离子通过主体分子之间的电荷跳跃扩散,将1,5-二氨基蒽醌自由基阳离子与主体分子的反自由基阴离子分离并形成稳定的电荷分离状态。最后主体分子自由基阴离子和1,5-二氨基蒽醌自由基阳离子逐渐复合,并产生激发复合物发射,在光激发停止后很长时间仍会持续;故所得有机红色长余辉材料在紫外灯的照射下,能够产生肉眼可见的红色荧光,关闭激发光源,能够产生肉眼可见的红色余辉发光。
[0016]
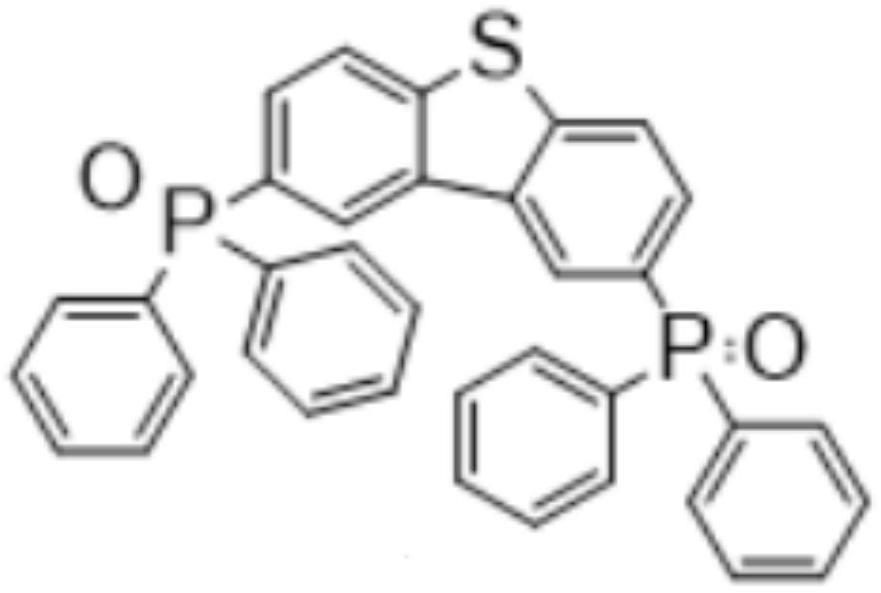
进一步地,优选地,所述主体分子为二苯并噻吩衍生物2,8-二(二苯基氧膦基)二苯并噻吩(ppt),具体结构式如下:
[0017][0018]
通过上述技术方案,本发明限定客体分子与二苯并噻吩衍生物2,8-二(二苯基氧膦基)二苯并噻吩(ppt)以质量比为1:100熔融,在光激发期间,在客体分子和二苯并噻吩衍生物2,8-二(二苯基氧膦基)二苯并噻吩(ppt)之间形成电荷转移态。然后,生成的二苯并噻吩衍生物2,8-二(二苯基氧膦基)二苯并噻吩(ppt)自由基阴离子通过二苯并噻吩衍生物2,8-二(二苯基氧膦基)二苯并噻吩(ppt)之间的电荷跳跃扩散,将1-氨基乙基氨基-9,10-蒽醌(aeaq)自由基阳离子与二苯并噻吩衍生物2,8-二(二苯基氧膦基)二苯并噻吩(ppt)的反自由基阴离子分离并形成稳定的电荷分离状态。最后二苯并噻吩衍生物2,8-二(二苯基氧膦基)二苯并噻吩(ppt)自由基阴离子和1-氨基乙基氨基-9,10-蒽醌(aeaq)自由基阳离子逐渐复合,并产生激发复合物发射,在光激发停止后很长时间仍会持续;故所得有机红色长余辉材料在紫外灯的照射下,能够产生肉眼可见的红色荧光,关闭激发光源,能够产生肉眼
可见的红色余辉发光;优选地,aeaq与ppt掺杂的效果最好,其表征是通过关闭光源后红色余辉的持续时间来判定。
[0019]
同时,提供一种制备上述有机红色长余辉材料的方法,包括以下具体步骤:
[0020]
步骤s1.将客体分子和主体分子以质量比为1:100混合均匀,放入耐火材料制成的坩埚或池窑中,加热熔融;
[0021]
步骤s2.向步骤s1内充入氮气,升温至250℃使得客体分子达到熔融态;
[0022]
步骤s3.将步骤s2所得熔融态快速冷却至室温,制成无定形透明薄膜状的有机红色长余辉材料。
[0023]
步骤s4:用365w紫外光照射薄膜60s后,关闭光源,可以观测到10s左右的红色余辉光。
[0024]
具体地,对比细节如下:
[0025]
步骤s1.将客体分子和主体分子以质量比为1:100混合均匀,放入耐火材料制成的坩埚或池窑中,加热熔融;
[0026]
步骤s2.向步骤s1内充入空气,升温至250℃使得客体分子达到熔融态;
[0027]
步骤s3.将步骤s2所得熔融态快速冷却至室温,制成无定形透明薄膜状的有机红色长余辉材料。
[0028]
步骤s4:用365w紫外光照射薄膜60s后,关闭光源,可以观测到1s左右的红色余辉光。
[0029]
通过观察发现当所处环境为有氧有水环境中,红色余辉仅能维持1s。
[0030]
步骤s1.将客体分子和主体分子以质量比为10:100混合均匀,放入耐火材料制成的坩埚或池窑中,加热熔融;
[0031]
步骤s2.向步骤s1内充入氮气,升温至250℃使得客体分子达到熔融态;
[0032]
步骤s3.将步骤s2所得熔融态快速冷却至室温,制成无定形透明薄膜状的有机红色长余辉材料。
[0033]
步骤s4:用365w紫外光照射薄膜60s后,关闭光源,可以观测到5s左右的红色余辉光。
[0034]
步骤s1.将客体分子和主体分子以质量比为1:1000混合均匀,放入耐火材料制成的坩埚或池窑中,加热熔融;
[0035]
步骤s2.向步骤s1内充入氮气,升温至250℃使得客体分子达到熔融态;
[0036]
步骤s3.将步骤s2所得熔融态快速冷却至室温,制成无定形透明薄膜状的有机红色长余辉材料。
[0037]
步骤s4:用365w紫外光照射薄膜60s后,关闭光源,可以观测到2s左右的红色余辉光。
[0038]
通过上述实验对比发现,仅仅当比例为1:100时效果最好。
[0039]
进一步地,在步骤s1中,所述客体分子的蒽醌胺作为电子给体,所述主体分子的阳离子季鏻自由基作为有机陷阱。
[0040]
通过上述技术方案,基于现有的长余辉发光机理是通过电子或空穴俘获机制来实现长效持久发光,在电子陷阱中,提出了在激发(ex)之后,被激发的电子穿过导带到达电子接受陷阱;在空穴陷阱中,电子通过价带传递而填充了空穴;在这两种情况下,弛豫都被阻
止,这是因为激发的电子已经迁移,或者是空穴已被填充;热干扰会恢复电子或空穴,从而产生余辉发射(em);
[0041]
类似上述长余辉发光机理,本发明以阳离子季鏻自由基作为有机陷阱,蒽醌胺作为电子给体,首先会在给体和受体分子之间发生光诱导的电荷转移,然后进行电荷分离,在最后进行电荷重组之前,可能会发生多个电荷分离,从而导致有机长余辉持续发光。
[0042]
基于现有的红色长余辉材料的制备条件苛刻,缺少生物相容性,不能实现柔性制备;而本发明的有机红色长余辉材料制备条件温和,柔性良好,且具有较好的生物相容性。
[0043]
此外,提供一种上述的有机红色长余辉材料的应用,作为荧光探针用于生物成像。
[0044]
提供一种上述的有机红色长余辉材料的应用,应用于数据加密和防伪标识。
[0045]
通过上述技术方案,本发明的有机红色长余辉材料具有在室温紫外灯下照射,能够产生肉眼可见的红色荧光,关闭激发光源,能够产生肉眼可见的红色余辉发光的优点,故便于将该材料同时实现室温条件下的荧光发射和磷光发射,可作为荧光探针用于生物成像;基于有机红色长余辉材料还具有高度的隐蔽性,使用方便,容易识别,从而能够实现更高级别的防伪功能,在有机光电材料、防伪标识、数据加密等领域具有很好的应用前景。
[0046]
本发明的有益效果在于:本发明的有机红色长余辉材料具有在室温紫外灯下照射,能够产生肉眼可见的红色荧光,关闭激发光源,能够产生肉眼可见的红色余辉发光的优点,故便于将该材料同时实现室温条件下的荧光发射和磷光发射,可作为荧光探针用于生物成像;基于有机红色长余辉材料还具有高度的隐蔽性,使用方便,容易识别,从而能够实现更高级别的防伪功能,在有机光电材料、防伪标识、数据加密等领域具有很好的应用前景。
具体实施方式
[0047]
下面结合具体实施例进一步说明本发明的内容,但不应理解为对本发明的限制。若未特别指明,实施例中所用的技术手段为本领域技术人员所熟知的常规手段;除非特别说明,本发明采用的试剂和设备如下所示;
[0048]
表1购买药品和药品来源
[0049][0050][0051]
表2下述实施例中测试所涉及的仪器以及型号:
[0052][0053]
实施例1
[0054]
一种有机红色长余辉材料,其原料包括含有蒽醌胺的客体分子,含有阳离子季鏻自由基的主体分子,客体分子与主体分子以质量比为1:100熔融;具体步骤如下:
[0055]
步骤s1.将主体分子和客体分子以质量比为1:100混合均匀,放入耐火材料制成的坩埚或池窑中,加热熔融;
[0056]
步骤s2.向步骤s1内充入氮气,升温至250℃使得客体分子达到熔融态;
[0057]
步骤s3.将步骤s2所得熔融态快速冷却至室温,制成无定形透明薄膜状的有机红色长余辉材料。
[0058]
效果检测
[0059]
将所得有机红色长余辉材料在室温紫外灯下照射,能够产生肉眼可见的红色荧光,关闭激发光源,能够产生肉眼可见的红色余辉发光。
[0060]
实施例2
[0061]
一种有机红色长余辉材料,包括客体分子1-氨基乙基氨基-9,10-蒽醌(aeaq),主体分子二苯并噻吩衍生物2,8-二(二苯基氧膦基)二苯并噻吩(ppt),aeaq与ppt以质量比为1:100熔融,具体步骤如下:
[0062]
步骤s1.将客体分子aeaq和主体分子ppt以质量比为1:100混合均匀,具体是称量原料aeaq(1mg)和ppt(100mg),并将其混合均匀;
[0063]
步骤s2.向步骤s1内充入氮气,升温至250℃使得ppt达到熔融态;
[0064]
步骤s3.将步骤s2所得熔融态快速冷却至室温,制成无定形透明薄膜状的有机红色长余辉材料。
[0065]
效果检测
[0066]
将所得有机红色长余辉材料在室温紫外灯下照射,能够产生肉眼可见的红色荧光,关闭激发光源,能够产生肉眼可见的红色余辉发光。
[0067]
实施例3
[0068]
一种有机红色长余辉材料,包括客体分子1,5-二氨基蒽醌,主体分子二苯并噻吩衍生物2,8-二(二苯基氧膦基)二苯并噻吩(ppt),1,5-二氨基蒽醌与ppt以质量比为1:100熔融,具体步骤如下:
[0069]
步骤s1.将客体分子1,5-二氨基蒽醌和主体分子ppt以质量比为2:200混合均匀,具体是称量原料1,5-二氨基蒽醌(2mg)和ppt(200mg),并将其混合均匀;
[0070]
步骤s2.向步骤s1内充入氮气,升温至250℃使得ppt达到熔融态;
[0071]
步骤s3.将步骤s2所得熔融态快速冷却至室温,制成无定形透明薄膜状的有机红色长余辉材料。
[0072]
效果检测
[0073]
将所得有机红色长余辉材料在室温紫外灯下照射,能够产生肉眼可见的红色荧光,关闭激发光源,能够产生肉眼可见的红色余辉发光。
[0074]
实施例4
[0075]
一种有机红色长余辉材料,包括客体分子1-氨基乙基氨基-9,10-蒽醌(aeaq),主体分子二苯并噻吩衍生物2,8-二(二苯基氧膦基)二苯并噻吩(ppt),aeaq与ppt以质量比为1:100熔融,具体步骤如下:
[0076]
步骤s1.将客体分子aeaq和主体分子ppt以质量比为1:10混合均匀,具体是称量原料aeaq(1mg)和ppt(10mg),并将其混合均匀;
[0077]
步骤s2.向步骤s1内充入氮气,升温至250℃使得ppt达到熔融态;
[0078]
步骤s3.将步骤s2所得熔融态快速冷却至室温,制成透明薄膜状的有机红色长余辉材料。
[0079]
效果检测
[0080]
将所得有机红色长余辉材料在室温紫外灯下照射,能够产生肉眼可见的红色荧光,关闭激发光源,能够产生肉眼可见的红色余辉发光。
[0081]
综上所述,实施例4与实施例2相比,实施例2效果更好;在光激发期间,在aeaq和ppt之间形成电荷转移态;然后,生成的ppt自由基阴离子通过ppt分子之间的电荷跳跃扩散,将aeaq自由基阳离子与ppt的反自由基阴离子分离并形成稳定的电荷分离状态;最后ppt自由基阴离子和aeaq自由基阳离子逐渐复合,并产生激发复合物发射,在光激发停止后很长时间仍会持续。
[0082]
最后应说明的是:以上所述仅为本发明的优选实施例而已,并不用于限制本发明,尽管参照前述实施例对本发明进行了详细的说明,对于本领域的技术人员来说,其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1