一种诱导聚苯胺负载石墨烯修饰电极反应器应用及除刚果红方法
本发明属于微生物电化学技术水处理领域,特别涉及一种诱导聚苯胺负载石墨烯修饰电极反应器及除刚果红方法,进而对染料厂工业废水中刚果红进行高效快速的去除。
背景技术:
随着工业的发展,染料作为一种重要的化学原料,大量出现在各种工业生产中。染料废水具有成分复杂、水量大、色度高、可生化程度低以及含有较多有毒有机污染物等特点。如果处理不达标排入,会对生态环境造成巨大的危害,并严重影响人类健康。刚果红(c32h22n6na2o6s2)是一种应用广泛易溶于水的联苯胺基偶氮染料,在生产和使用过程中流失率高,易进入水体,而且存在易损失、易污染、可降解性差等问题。刚果红在进入环境之后,它会被代谢为联苯胺,而联苯胺是已知的人体致癌物。所以刚果红污染成为了亟待解决的环境问题。目前废水中刚果红的去除方法依据其应用原理的不同可以划分为物理修复、化学修复以及生物修复。
物理法是通过物理作用对水中的刚果红进行分离,在处理过程中不改变污染物的化学性质。常用的物理法包括吸附法、膜分离法、磁分离技术、离子浮选、溶剂分离和吸附胶质浮选法等。其中,吸附法是应用最多的物理处理方法,是利用吸附剂本身的多孔道结构和表面的官能基团与染料分子形成稳固的化学键,对废水中的染料分子进行富集从而达到净化水体的目的。常用的吸附剂有活性炭、硅藻土、天然蒙脱土以及煤渣等。但是,不同种类的吸附剂对染料的吸附具有选择性,并且饱和吸附剂在再生过程中易产生二次污染此外还存在吸附效率低,分离困难等问题。
常用的化学法有混凝法、氧化法等。混凝法指在偶氮染料废水中添加混凝剂,通过减弱分子间排斥力,使染料废水中悬物和胶体的稳定性下降,相互之间发生碰撞且附聚,使刚果红从废水中分离出来以达到脱色且处理偶氮染料废水的目的。但此方法费用高、使用范围窄。化学氧化法是指使用强氧化剂、高温、光照等方法处理染料分子,使其结构中的发色基团被断键破坏的方法。常见的氧化法有电化学氧化法、芬顿氧化法、臭氧氧化法和光催化氧化法等。化学法虽然能够达到处理的目的,但是仍然存在一些缺点,例如耗能大、成本高、会产生二次污染等。
生物法是通过向废水中加入能降解染料的微生物,利用微生物的新陈代谢作用对废水中的污染物进行氧化降解。根据微生物的呼吸方式分为好氧生物处理法和厌氧生物处理法。好氧生物处理法只适用于处理低浓度的染料废水,并且难以有效处理人工合成的染料类大分子有机物质,同时会产生大量的剩余污泥;厌氧生物处理法能够处理中高浓度的染料废水,并且不会产生剩余污泥,但在厌氧条件下,生物代谢速度慢,水力停留时间长,某些染料还可能产生苯胺类致癌物质。此外,微生物对于营养物质、ph、温度等条件要求高,难以适应染料废水成分复杂、水质波动大、毒性高的特点。
微生物电化学系统作为一种新兴的技术,可以在对刚果红进行有效降解的同时解决以上问题,该技术是以电活性微生物为核心,通过氧化还原反应,将化学能转化成其他有价值的能源或物质的一种技术。微生物电化学系统产电性能、污染物降解能力与电活性微生物的氧化还原活性密切相关,然而,由于产电微生物和电极间以胞外电子传递的方式进行电子转移,其转移率较低,因而性能受到很大的限制。在体系整个反应过程中,产电微生物与电极之间的电子传递是反应发生的关键一步,因此电极修饰成为提高微生物电化学系统对污染物的降解性能最直接、最普遍、最简单的方法。
技术实现要素:
本发明目的是解决现有微生物电化学技术存在的电子转移效率低、电活性微生物以及降解性微生物在电极上富集效果差的问题,提供一种利用修饰电极的方法以实现微生物的快速富集以及电子的高效传递,进而实现水体中刚果红高效快速降解。
本发明的技术方案是一种诱导聚苯胺负载石墨烯修饰电极反应器应用,去除刚果红。
本发明的第二个技术方案是一种诱导聚苯胺负载石墨烯修饰电极反应器除刚果红方法,包括如下步骤:
1)具有电活性的降解微生物膜的培养
使用与步骤1)相同的电化学反应器,向其中加入溶液为刚果红染料厂污水与磷酸缓冲溶液的混合液体,加入乙酸钠1g/l作为碳源,采用计时电流法进行具有电活性的降解微生物膜的富集培养,运行3-4个周期(5–10天)以形成具有厚度为80-90μm的降解微生物膜;
2)微生物电化学技术对水体中刚果红降解效果的检测与计算
微生物膜成熟之后,向反应器中加入刚果红溶液,在不同的时间点进行取样,用离心机以10000–12000rpm/min转速对样品进行离心5–10min,将上清液过滤膜除去杂质,使用紫外分光光度计在497nm下对样品进行测试,结合标准曲线,利用公式计算出待测水体中的刚果红浓度。
所述刚果红染料厂污水与磷酸缓冲溶液的混合体积比例为2–1:1。
所述刚果红溶液的添加,需要在溶液中同步加入1g/l的乙酸钠以提供碳源。
本发明的优点和有益效果:本发明和现有技术相比,通过修饰电极,促进了系统中微生物在电极表面成膜,缩短启动时间,强化电子传递,为加速反应器启动以及提高微生物电化学系统高效处理刚果红染料污染水体提供了新方法。
附图说明
图1是实施例1、对比例1和对比例2的时间-电流图像。
图2是实施例1、对比例1和对比例2的刚果红去除率随时间变化的图像。
图3是实施例1、对比例1和对比例2的剩余刚果红浓度随时间变化的图像。
具体实施方式
下面将结合本发明中的实施例,对本发明中的技术方案进行清楚、完整地描述。显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
实施例1
设置使用聚苯胺和石墨烯修饰电极的微生物电化学系统对水体中刚果红进行降解的实验组pg+me
1)石墨棒电极的修饰
电化学反应器为直径5cm、高5cm的包括石墨棒工作电极、铂片对电极和ag/agcl参比电极的三电极系统,在反应器中加入100ml蒸馏水,0.8%浓硫酸,4.0ml苯胺溶液,1500rpm/min高速搅拌10min使苯胺均匀分散在溶液中。使苯胺均匀分散在溶液中。使用电化学工作站施加0.8v电位100s,之后加入0.03g石墨烯进行循环伏安法扫描,扫描速度为0.05v/s,扫描电位范围为-0.3–1.2v,最后将修饰的电极在25℃温度下干燥;
2)具有电活性的降解微生物膜的培养
使用与步骤1)相同的电化学反应器,向其中加入溶液为刚果红染料厂污水与磷酸缓冲溶液2:1的混合液体,加入乙酸钠1g/l作为碳源,采用计时电流法进行具有电活性的降解微生物膜的富集培养,运行8天以形成具有厚度为80-90μm的降解微生物膜;
3)修饰电极的生物电化学系统对水体中刚果红降解效果的检测与计算
微生物膜成熟之后,向电活性反应器中加入200mg/l的刚果红溶液和1g/l的乙酸钠,在不同的时间点(0、6、18、30、42、54、66、78、90h)进行取样,用离心机对样品进行离心5分钟,转速为10000rpm;将上清液过0.45μm滤膜除去杂质,之后使用紫外分光光度计在497nm下对样品进行测试,结合标准曲线,公式为y=0.011x+0.0134,r2=0.976,利用公式计算出待测水体中的刚果红浓度。
对比例1
设置仅修饰聚苯胺的石墨棒电极作为对照组p+me:
1)石墨棒电极的修饰
电化学反应器为直径5cm、高5cm的包括石墨棒工作电极、铂片对电极和ag/agcl参比电极的三电极系统,在反应器中加入100ml蒸馏水,0.8%浓硫酸,4.0ml苯胺溶液,1500rpm/min高速搅拌10min使苯胺均匀分散在溶液中。使苯胺均匀分散在溶液中。使用电化学工作站施加0.8v电位100s,之后进行循环伏安法扫描,扫描速度为0.05v/s,扫描电位范围为-0.3–1.2v,最后将修饰的电极在25℃温度下干燥;
2)具有电活性的降解微生物膜的培养
使用与步骤1)相同的电化学反应器,向其中加入溶液为刚果红染料厂污水与磷酸缓冲溶液2:1的混合液体,加入乙酸钠1g/l作为碳源,采用计时电流法进行具有电活性的降解微生物膜的富集培养,运行8天以形成具有厚度为80-90μm的降解微生物膜;
3)修饰电极的生物电化学系统对水体中刚果红降解效果的检测与计算
微生物膜成熟之后,向电活性反应器中加入200mg/l的刚果红溶液和1g/l的乙酸钠,在不同的时间点(0、6、18、30、42、54、66、78、90h)进行取样,用离心机对样品进行离心5分钟,转速为10000rpm;将上清液过0.45μm滤膜除去杂质,之后使用紫外分光光度计在497nm下对样品进行测试,结合标准曲线,公式为y=0.011x+0.0134,r2=0.976,利用公式计算出待测水体中的刚果红浓度。
对比例2
设置使用未处理的石墨棒作为对照组me:
1)具有电活性的降解微生物膜的培养
使用与步骤1)相同的电化学反应器,向其中加入溶液为刚果红染料厂污水与磷酸缓冲溶液2:1的混合液体,加入乙酸钠1g/l作为碳源,采用计时电流法进行具有电活性的降解微生物膜的富集培养,运行8天以形成具有厚度为80-90μm的降解微生物膜;
2)修饰电极的生物电化学系统对水体中刚果红降解效果的检测与计算
微生物膜成熟之后,向电活性反应器中加入200mg/l的刚果红溶液和1g/l的乙酸钠,在不同的时间点(0、6、18、30、42、54、66、78、90h)进行取样,用离心机对样品进行离心5分钟,转速为10000rpm;将上清液过0.45μm滤膜除去杂质,之后使用紫外分光光度计在497nm下对样品进行测试,结合标准曲线,公式为y=0.011x+0.0134,r2=0.976,利用公式计算出待测水体中的刚果红浓度。
测试例1:聚苯胺和石墨烯修饰电极的微生物电化学系统电流变化情况:
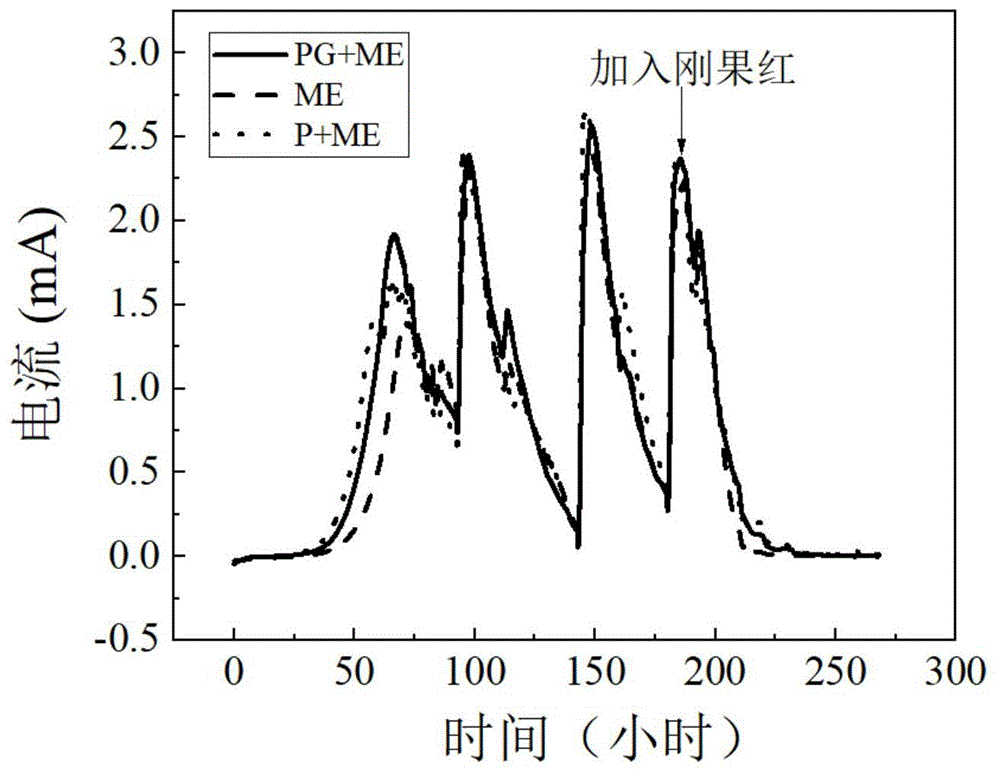
实施例1(pg+me组)与对比例1(p+me组)和对比例2(me组)中的电流产出采用恒电位仪实时采集。电化学反应器两端的电流通过连接在电脑上的恒电位仪每100s进行采集记录1次,并由电脑进行自动记录和保存,之后进行绘图(图1),图中实线的为pg+me组的电流,较短虚线的为me组的电流,较长虚线为p+me组的电流。
根据图1,在加入刚果红之前,三组均在65h左右出现峰值电流,而pg+me组的电流则达到了1.92ma左右,分别是p+me组和me组的1.2倍和1.4倍。系统中电流产生主要是阳极附近微生物的代谢活动产生,并由产电微生物将电子导出到电极;电流的增加表明产电微生物易富集在修饰后的石墨棒上。
测试例2:聚苯胺和石墨烯修饰电极的微生物电化学系统刚果红去除情况:
将实施例1与对比例2~3修复不同时间(0、6、18、30、42、54、66、78、90h)的刚果红溶液;用离心机对样品进行离心3分钟,转速为10000rpm;将上清液过0.45μm滤膜除去杂质,之后使用紫外分光光度计在497nm下对样品进行测试;结合标准曲线计算待测水体中的刚果红浓度。得到实施例1与对比例2~3各样品点的刚果红浓度(图2),得到刚果红的去除率并绘图(图3)。
根据图3,经过90h的修复,实施例1与对比例2~3反应器中刚果红的去除量表现为pg+me>p+me>me,表明在使用修饰了聚苯胺和石墨烯的微生物电化学系统中对溶液中刚果红的去除达到了最优的效果,刚果红的去除率达到95%;p+me相对与me组,刚果红的去除率降低了,这表明修饰电极对于刚果红的去除率更多的是聚苯胺和石墨烯的联合作用;此外,pg+me组对刚果红的去除率在第54个小时的时候就达到了最大,此时p+me组和me组的去除率仅为67%和78%,这说明聚苯胺和石墨烯的量和作用进一步促进了系统中的电子转移,从而加速了水体中刚果红的去除。
以上所述的实施例是本发明的优选方式,需要注意,在不脱离本发明所述原理的情况下所做的一切改进和润饰,都属于本发明保护的范畴。
- 还没有人留言评论。精彩留言会获得点赞!