一种六价铬的化学-微生物协同修复方法及处理液
1.本发明属于六价铬污染修复技术领域,具体涉及一种六价铬的化学-微生物协同修复方法及处理液。
背景技术:
2.我国土壤重金属污染问题突出,铬(cr)是主要无机污染物之一。我国商品种类中铬化合物产品占比约为15%,其中铬化工、电镀和制革是最主要的行业,占铬消耗总量的70%以上,三大涉铬行业企业数量达万个。随着近年来我国产业结构调整,大量企业被关停搬迁。长达几年至几十年的粗放生产导致这些遗留场址地块受到严重污染,威胁人体健康和生态安全,大量受污染地块亟需治理。cr(vi)迁移能力强、毒性高且易致癌,是国家重点控制的五大重金属之一。cr(iii)水溶性低、迁移能力弱,且不能穿过细胞膜,毒性相对较低。因此,将cr(vi)还原为毒性较低的cr(iii)是环境铬污染治理的重要途径。
3.土壤化学还原稳定化技术近年来被广泛应用。常用的土壤铬污染修复化学药剂包括硫酸亚铁、含铁矿物和硫系材料(如硫化氢和亚硫酸盐)等。化学还原稳定化技术具有处理效率高和可操作性强等优点,但试剂消耗量大、易产生二次污染,且显著改变土壤理化性质。此外,化学药剂失效及还原产物再氧化影响土壤铬还原稳定化的长效性,导致单一铬化学还原稳定化技术难以达到我国建设用地土壤六价铬风险管控要求。
4.微生物参与可形成亚纳米级三价铬,降低三价铬再氧化机率,但其对复杂环境中铬的耐受能力较低。微生物与化学修复技术联合有望突破化学还原产物再氧化及微生物低适应性的局限,构建绿色、经济、长效的土壤铬还原稳定化技术体系。
5.纳米技术在多个工业应用领域中具有可持续竞争力。纳米颗粒的独特性在于是它们具有更大的比表面积和高反应活性等。其中,纳米零价铁(nzvi)在土壤及溶液中六价铬修复方面展现出巨大潜力。纳米零价铁是一种环境友好型材料,反应寿命优异、流动性良好、毒性较低、粒径可控且表面活性位点丰富,是铬污染土壤及地下水修复的理想材料。但相关研究表明,纳米零价铁颗粒本身易团聚、表面易氧化,且铬铁沉淀物附着在颗粒表面阻碍六价铬的还原,使纳米零价铁反应活性大大降低。因此,亟需解决纳米零价铁在修复六价铬污染溶液及土壤时易钝化失活的问题,提供一种可溶解铬铁沉淀,且可再生二价铁以延长材料反应寿命的铬污染溶液及土壤的协同修复方法。
技术实现要素:
6.本发明的目的在于克服现有技术不足,并提供一种六价铬的化学-微生物协同修复方法及处理液。
7.本发明所采用的具体技术方案如下:
8.第一方面,本发明提供一种六价铬的化学-微生物协同修复方法,具体在于,将草酸青霉sl2孢子悬液或草酸青霉sl2菌丝球中的一种与纳米零价铁颗粒混合后获得的处理液添加至待修复的六价铬污染物中。
9.作为优选,上述草酸青霉sl2孢子悬液的制备方法如下:将草酸青霉sl2接种至马铃薯葡萄糖琼脂培养基中,进行黑暗条件培养后接种至无菌triton x溶液中,过滤菌丝后得到草酸青霉sl2孢子悬液。
10.作为优选,上述草酸青霉sl2菌丝球的制备方法如下:将所述的草酸青霉sl2孢子悬液接种至马铃薯葡萄糖液体培养基中进行预培养,预培养结束后用无菌水冲洗得到草酸青霉sl2菌丝球。
11.作为优选,上述黑暗条件培养温度为30℃,时间为7d。
12.作为优选,上述预培养时间为48h。
13.作为优选,上述纳米零价铁颗粒的制备方法如下:在氮气气氛条件下,将通过硼氢化钾还原氯化铁法制备得到的颗粒分散于无水乙醇中,进行氮吹处理,获得纳米零价铁颗粒。
14.作为优选,上述六价铬污染物为土壤,修复方法如下:
15.s1:采集原始六价铬污染土壤,经风干、研磨过2.0mm筛后经伽马射线照射预处理达到灭菌目的,得到待处理六价铬污染土壤;
16.s2:在上述待处理六价铬污染土壤中喷洒含草酸青霉sl2孢子悬液和纳米零价铁颗粒的处理液,混合均匀后于30℃条件下修复180~360d;草酸青霉sl2孢子悬液中孢子的添加量为108个孢子/g土壤;纳米零价铁颗粒的添加量为4.0g/kg土壤。
17.作为优选,上述六价铬污染物为水体,修复方法如下:
18.向六价铬污染物水体中加入葡萄糖液体培养基以提供碳源,随后加入含草酸青霉sl2菌丝球和纳米零价铁颗粒的处理液进行修复;上述草酸青霉sl2菌丝球的添加量为9g/l;上述纳米零价铁颗粒的添加量为0.2g/l,修复在180rpm、30℃条件下进行24h。
19.进一步的,上述葡萄糖液体培养基中葡萄糖浓度为4.5~20g/l。
20.第二方面,本发明提供一种用于修复六价铬污染物的处理液,处理液为草酸青霉sl2孢子悬液或草酸青霉sl2菌丝球中的一种和纳米零价铁混合所得。
21.本发明相对于现有技术而言,具有以下有益效果:
22.(1)本发明提供的化学-微生物协同修复方法在水体和土壤中均具备良好的修复效果,在含六价铬污染的水体中,本发明提供的草酸青霉sl2与纳米零价铁颗粒协同修复可在1d内将水体中初始浓度为200mg/l的六价铬完全还原;本发明提供的修复方法可将土壤六价铬浓度降至3.4mg/kg,低于中国ii类建设用地土壤污染风险筛选值(5.7mg/kg,参见生态环境部《土壤环境质量建设用地土壤污染风险管控标准gb36600-2018》)。为了评估修复后六价铬污染土壤中重金属浸出率,采用tclp法进行提取,结果表明修复180d后土壤中tclp提取态六价铬浓度从7.7mg/l下降至0.09mg/l(低于中国地表水v类环境质量标准限值0.1mg/l,参见原国家环境保护总局《地表水环境质量标准gb3838-2002》),说明修复后的土壤对地下水和地表水危害显著降低;
23.(2)本发明提供的化学-微生物协同修复方法通过功能微生物草酸青霉sl2(penicillium oxalicum sl2)参与还原稳定六价铬,减少了纳米零价铁颗粒的用量。此外,草酸青霉sl2可溶解纳米零价铁表面铬铁沉淀,使纳米零价铁反应充分,且可将三价铁还原,活化纳米零价铁,充分延长纳米零价铁的使用寿命。降低处理成本同时提升六价铬还原稳定化效率,更绿色环保,同时可避免土壤理化性质的显著改变,避免二次污染的发生;
24.(3)本发明提供的化学-微生物协同修复方法的还原产物稳定,仅由化学药剂参与的土壤铬还原产物易再氧化,而本发明提供的修复方法在修复360d后仍较为稳定,土壤中六价铬的浓度低于5.7mg/kg,说明了该修复药剂及三价铬产物的长效稳定性。
附图说明
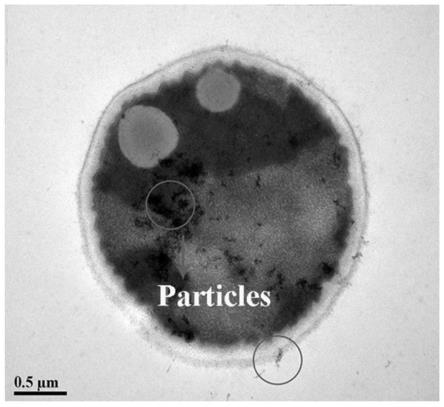
25.图1为实施例1中化学-微生物协同修复下草酸青霉sl2的透射电镜图。
26.图2为实施例1和对比例1、2测定的溶液中六价铬还原率。
27.图3为实施例1和对比例2测定的溶液中总铁与二价铁浓度。
28.图4为实施例2、实施例3和对比例3~5测定的土壤中六价铬浓度。
29.图5为实施例2、对比例3和对比例5中测定的土壤二价铁浓度。
具体实施方式
30.下面结合附图和具体实施方式对本发明做进一步阐述和说明。本发明中各个实施方式的技术特征在没有相互冲突的前提下,均可进行相应组合。
31.本发明下述实施例所用的草酸青霉penicillium oxalicum sl2菌株保存于中国典型培养物保藏管理中心,保藏号为cctcc no:m 2014505,菌株名称:penicillium oxalicum sl2,保藏日期:2014年10月22日。下述实施例中其余的试剂均可采用市售分析纯及以上的商业产品。
32.实施例1
33.本实施例提供一种水体中六价铬的化学-微生物协同修复方法,具体如下:
34.(1)将200g马铃薯煮沸30min后经无菌纱布过滤取上清液,加入20g葡萄糖后定容至1000ml,将上述混合液于115℃高压灭菌20min获得马铃薯葡萄糖液体(pdl)培养基;将上述pdl培养基中加入1.8%(w/v)的琼脂获得马铃薯葡萄糖琼脂(pda)培养基,用于培养草酸青霉sl2(penicillium oxalicum sl2);将2g葡萄糖加入100ml去离子水中115℃高压灭菌20min即可制得葡萄糖液体培养基。
35.上述pdl培养基、pda培养基和葡萄糖液体培养基中葡萄糖浓度均为20g/l。通过实验测定,培养过程中微生物实际消耗的葡萄糖浓度为4.5-5.0g/l,因此在实际应用中,直接在水体中加入浓度为4.5g/l的葡萄糖液体培养基也可满足草酸青霉sl2的生长需求。
36.(2)称取烘干的重铬酸钾(k2cr2o7)5.66g于100ml烧杯中,加50ml去离子水完全溶解后定容至100ml容量瓶中,得到浓度为20g/l的重铬酸钾标准液。
37.(3)将草酸青霉sl2接种至马铃薯葡萄糖琼脂(pda)培养基中,置于30℃黑暗条件下培养7d,收获新鲜孢子;将上述新鲜孢子提取至0.05%无菌triton x溶液中经无菌玻璃棉过滤菌丝后,获得浓度为108个孢子/ml的草酸青霉sl2孢子悬液。
38.(4)将1ml上述草酸青霉sl2孢子悬液接种至99ml pdl培养基,使得草酸青霉sl2孢子的添加量为106个孢子/ml。置于30℃环境中进行预培养48h后用无菌去离子水冲洗3遍获得草酸青霉sl2菌丝球。
39.(5)在氮气(n2)气氛条件下通过硼氢化钾(kbh4)还原氯化铁(fecl3·
6h2o)法制备颗粒分散于无水乙醇中,进行氮吹处理,获得纳米零价铁颗粒(nzvi)。纳米零价铁颗粒密封并于-70℃超低温冰箱中保存备用。
40.(6)量取上述重铬酸钾标准液1ml于250ml锥形瓶中,加入99ml葡萄糖液体培养基模拟六价铬污染水体,其中六价铬的浓度为200mg/l。将草酸青霉sl2菌丝球和纳米零价铁颗粒加入上述模拟六价铬污染水体中(其中草酸青霉sl2菌丝球的添加量为9g/l,纳米零价铁颗粒的添加量为0.2g/l),用透气膜封口,放入恒温摇床(180rpm,30℃)修复24h。
41.(7)在超净工作台中定期取步骤(6)中的上清液,采用二苯碳酰二肼分光光度法(参见生态环境部《水质六价铬的测定二苯碳酰二肼分光光度法gb/t7467-1987》)测定上清液中的六价铬浓度,采用邻菲啰啉分光光度法(参见原国家环境保护总局《水质铁的测定邻菲啰啉分光光度法hj/t 345-2007》)测定溶液总铁和二价铁浓度。
42.实施例2
43.本实施例提供一种土壤中六价铬的化学-微生物协同修复方法(记作sl2+nzvi组),具体如下:
44.(1)将200g马铃薯煮沸30min后经无菌纱布过滤取上清液,加入20g葡萄糖后定容至1000ml,将上述混合液于115℃高压灭菌20min获得马铃薯葡萄糖液体(pdl)培养基;将上述pdl培养基中加入1.8%(w/v)的琼脂获得马铃薯葡萄糖琼脂(pda)培养基,用于培养草酸青霉sl2。
45.上述pdl培养基和pda培养基中葡萄糖浓度均为20g/l。
46.(2)将草酸青霉sl2接种至pda培养基中,置于30℃黑暗条件下培养7d,收获新鲜孢子;将上述新鲜孢子于0.05%无菌triton x溶液中经无菌玻璃棉过滤菌丝后,获得浓度为10
10
个孢子/ml的草酸青霉sl2孢子悬液浓缩液。
47.(3)在氮气(n2)气氛条件下通过硼氢化钾(kbh4)还原氯化铁(fecl3·
6h2o)法制备颗粒分散于无水乙醇中,进行氮吹处理,获得纳米零价铁颗粒(nzvi)。纳米零价铁颗粒密封并于-70℃超低温冰箱中保存备用。
48.(4)采集原始六价铬污染土壤(其中总铬浓度为314.1mg/kg,六价铬的浓度为187.1mg/kg),经风干、研磨过2.0mm筛后经伽马射线(50kgy)照射预处理得到待处理六价铬污染土壤,伽马射线照射可在减少对土壤基本理化性质扰动的前提下达到灭菌的目的,以降低土著微生物的影响,从而更利于外源功能微生物草酸青霉sl2的定殖。
49.(5)称取上述待处理六价铬污染土壤50g于250ml烧杯中,通过30ml塑料喷瓶将草酸青霉sl2孢子悬液浓缩液和纳米零价铁颗粒加入到50%的pdl培养基中并均匀喷洒至六价铬污染土壤中(最终土壤中草酸青霉sl2孢子悬液中孢子的添加量为108个孢子/g土壤,纳米零价铁颗粒的添加量为4.0g/kg),边喷洒边搅拌,用透气膜将烧杯封口,放入人工气候室中(30℃)修复180d。每隔30d向土壤中补充草酸青霉sl2孢子悬液和50%的pdl培养基。含水率控制在15%(v/m),并每周补充去离子水对样品进行补偿,以保持在修复期间所需要的水分。
50.上述50%的pdl培养基为pdl培养基与灭菌去离子水按1:1(v/v)的比例稀释而成。
51.(6)定期取步骤(5)中的土壤样品,采用火焰原子吸收分光光度法(参见生态环境部《土壤和沉积物六价铬的测定碱溶液提取-火焰原子吸收分光光度法hj 1082-2019》)测定土壤中六价铬浓度;土壤样品经0.5mol/l的hcl提取后采用邻菲啰啉分光光度法(参见原国家环境保护总局《水质铁的测定邻菲啰啉分光光度法hj/t 345-2007》)测定土壤二价铁浓度。
52.实施例3
53.本实施例提供一种土壤中六价铬的化学-微生物协同修复方法(记作sl2+nzvi 360d组),具体如下:
54.(1)将200g马铃薯煮沸30min后经无菌纱布过滤取上清液,加入20g葡萄糖后定容至1000ml,将上述混合液于115℃高压灭菌20min获得马铃薯葡萄糖液体(pdl)培养基;将上述pdl培养基中加入1.8%(w/v)的琼脂获得马铃薯葡萄糖琼脂(pda)培养基,用于培养草酸青霉sl2。
55.上述pdl培养基和pda培养基中葡萄糖浓度均为20g/l。
56.(2)将草酸青霉sl2接种至pda培养基中,置于30℃黑暗条件下培养7d,收获新鲜孢子;将上述新鲜孢子于0.05%无菌triton x溶液中经无菌玻璃棉过滤菌丝后,获得浓度为10
10
个孢子/ml的草酸青霉sl2孢子悬液浓缩液。
57.(3)在氮气(n2)气氛条件下通过硼氢化钾(kbh4)还原氯化铁(fecl3·
6h2o)法制备颗粒分散于无水乙醇中,进行氮吹处理,获得纳米零价铁颗粒(nzvi)。纳米零价铁颗粒密封并于-70℃超低温冰箱中保存备用。
58.(4)采集原始六价铬污染土壤(其中总铬浓度为314.1mg/kg,六价铬的浓度为187.1mg/kg),经风干、研磨过2.0mm筛后经伽马射线(50kgy)照射预处理得到待处理六价铬污染土壤,伽马射线照射可在减少对土壤基本理化性质扰动的前提下达到灭菌的目的,以降低土著微生物的影响,从而更利于外源功能微生物草酸青霉sl2的定殖。
59.(5)称取上述待处理六价铬污染土壤50g于250ml烧杯中,通过30ml塑料喷瓶将草酸青霉sl2孢子悬液浓缩液和纳米零价铁颗粒加入到50%的无菌pdl培养基中并均匀喷洒至六价铬污染土壤中(其中草酸青霉sl2孢子悬液中孢子的添加量为108个孢子/g土壤,纳米零价铁颗粒的添加量为4.0g/kg),边喷洒边搅拌,用透气膜将烧杯封口,放入人工气候室中(30℃)修复360d。每隔30d向土壤中补充草酸青霉sl2孢子悬液和50%的pdl培养基。含水率控制在15%(v/m),并每周补充去离子水对样品进行补偿,以保持在修复期间所需要的水分。
60.上述50%的pdl培养基为pdl培养基与灭菌去离子水按1:1(v/v)的比例稀释而成。
61.(6)定期取步骤(5)中的土壤样品,采用火焰原子吸收分光光度法(参见生态环境部《土壤和沉积物六价铬的测定碱溶液提取-火焰原子吸收分光光度法hj 1082-2019》)测定土壤中六价铬浓度;土壤样品经0.5mol/l的hcl提取后采用邻菲啰啉分光光度法(参见原国家环境保护总局《水质铁的测定邻菲啰啉分光光度法hj/t 345-2007》)测定土壤二价铁浓度。
62.对比例1
63.本对比例与实施例1相比,提供一种不添加纳米零价铁颗粒的一种水体中六价铬的化学-微生物协同修复方法,具体如下:
64.(1)将200g马铃薯煮沸30min后经无菌纱布过滤取上清液,加入20g葡萄糖后定容至1000ml,将上述混合液于115℃高压灭菌20min获得马铃薯葡萄糖液体(pdl)培养基;将上述pdl培养基中加入1.8%(w/v)的琼脂获得马铃薯葡萄糖琼脂(pda)培养基,用于培养草酸青霉sl2;将2g葡萄糖加入100ml去离子水中115℃高压灭菌20min即可制得葡萄糖液体培养基。
65.上述pdl培养基、pda培养基和葡萄糖液体培养基中葡萄糖浓度均为20g/l。
66.(2)称取烘干的重铬酸钾(k2cr2o7)5.66g于100ml烧杯中,加50ml去离子水完全溶解后定容至100ml容量瓶中,得到浓度为20g/l的重铬酸钾标准液。
67.(3)将草酸青霉sl2接种至马铃薯葡萄糖琼脂(pda)培养基中,置于30℃黑暗条件下培养7d,收获新鲜孢子;将上述新鲜孢子提取至0.05%无菌triton x溶液中经无菌玻璃棉过滤菌丝后,获得浓度为108个孢子/ml的草酸青霉sl2孢子悬液。
68.(4)将1ml上述草酸青霉sl2孢子悬液接种至99ml pdl培养基,使得草酸青霉sl2孢子的添加量为106个孢子/ml。置于30℃环境中进行预培养48h后用无菌去离子水冲洗3遍获得草酸青霉sl2菌丝球。
69.(5)量取上述重铬酸钾标准液1ml于250ml锥形瓶中,加入99ml葡萄糖液体培养基模拟六价铬污染水体,其中六价铬的浓度为200mg/l。将草酸青霉sl2菌丝球加入上述模拟六价铬污染水体中,草酸青霉sl2菌丝球的添加量为9g/l,用透气膜封口,放入恒温摇床(180rpm,30℃)修复24h。
70.(6)在超净工作台中定期取步骤(5)中的上清液,采用二苯碳酰二肼分光光度法(参见生态环境部《水质六价铬的测定二苯碳酰二肼分光光度法gb/t7467-1987》)测定上清液中的六价铬浓度,采用邻菲啰啉分光光度法(参见原国家环境保护总局《水质铁的测定邻菲啰啉分光光度法hj/t 345-2007》)测定溶液总铁和二价铁浓度。
71.对比例2
72.本对比例与实施例1相比,提供一种不添加草酸青霉sl2菌丝球的一种水体中六价铬的化学-微生物协同修复方法,具体如下:
73.(1)将2g葡萄糖加入100ml去离子水中115℃高压灭菌20min即可制得葡萄糖液体培养基,葡萄糖液体培养基中葡萄糖浓度为20g/l。
74.(2)称取烘干的重铬酸钾(k2cr2o7)5.66g于100ml烧杯中,加50ml去离子水完全溶解后定容至100ml容量瓶中,得到浓度为20g/l的重铬酸钾标准液。
75.(3)在氮气(n2)气氛条件下通过硼氢化钾(kbh4)还原氯化铁(fecl3·
6h2o)法制备颗粒分散于无水乙醇中,进行氮吹处理,获得纳米零价铁颗粒(nzvi)。纳米零价铁颗粒密封并于-70℃超低温冰箱中保存备用。
76.(4)量取上述重铬酸钾标准液1ml于250ml锥形瓶中,加入99ml葡萄糖液体培养基模拟六价铬污染水体,其中六价铬的浓度为200mg/l,将纳米零价铁颗粒加入上述模拟六价铬污染水体中(其中纳米零价铁颗粒的添加量为0.2g/l),用透气膜封口,放入恒温摇床(180rpm,30℃)修复24h。
77.(5)在超净工作台中定期取步骤(3)中的上清液,采用二苯碳酰二肼分光光度法(参见生态环境部《水质六价铬的测定二苯碳酰二肼分光光度法gb/t7467-1987》)测定上清液中的六价铬浓度,采用邻菲啰啉分光光度法(参见原国家环境保护总局《水质铁的测定邻菲啰啉分光光度法hj/t 345-2007》)测定溶液总铁和二价铁浓度。
78.如图2所示,采用本实施例提供的化学-微生物协同修复方法修复水体中的六价铬时,由测得的六价铬浓度计算得到相应的去除率。结果表明,实施例1中溶液六价铬还原率在24h时可达100.0%,而对比例1和对比例2中的六价铬还原率在24h仅分别为63.1%和58.4%。表明草酸青霉sl2和纳米零价铁颗粒协同修复方法具有出色的六价铬还原效率,其
可在24h内将200mg/l的六价铬完全还原,修复后溶液中六价铬含量小于0.05mg/l,低于地表水环境质量ii类水标准(参见原国家环境保护总局《地表水环境质量标准gb3838-2002》)。
79.如图3所示,在反应24h时,实施例1水体中总铁浓度和二价铁浓度分别高达156.1mg/l和43.7mg/l,其中二价铁占总铁比例为28.0%。而对比例2溶液中总铁浓度和二价铁浓度分别为79.7mg/l和6.5mg/l。这说明草酸青霉sl2可将纳米零价铁颗粒中的铁较多地溶解出来,并参与到氧化还原反应过程中,草酸青霉sl2还可将溶液中的三价铁还原为二价铁,具有较强的促进三价铁/二价铁循环及活化纳米零价铁的能力。如图1所示,从草酸青霉sl2的透射电镜图可以看出,细胞中的颗粒为摄取转运的铁,证明草酸青霉sl2和纳米零价铁颗粒联合作用具有摄取并还原三价铁的能力。
80.对比例3
81.本对比例相对于实施例2,提供一种不添加草酸青霉sl2和纳米零价铁颗粒的土壤中六价铬的化学-微生物协同修复方法(记作control组),具体如下:
82.(1)采集原始六价铬污染土壤(其中总铬浓度为314.1mg/kg,六价铬的浓度为187.1mg/kg),经风干、研磨过2.0mm筛后经伽马射线(50kgy)照射预处理得到待处理六价铬污染土壤,伽马射线照射可在减少对土壤基本理化性质扰动的前提下达到灭菌的目的,以降低土著微生物的影响,从而更利于外源功能微生物草酸青霉sl2的定殖。
83.(2)称取上述待处理六价铬污染土壤50g于250ml烧杯中,用由透气膜将烧杯封口,放入人工气候室中(30℃)修复180d。含水率控制在15%(v/m),并每周补充去离子水对样品进行补偿,以保持在修复期间所需要的水分。
84.(3)定期取步骤(3)中的土壤样品,采用火焰原子吸收分光光度法(参见生态环境部《土壤和沉积物六价铬的测定碱溶液提取-火焰原子吸收分光光度法hj 1082-2019》)测定土壤中六价铬浓度;土壤样品经0.5mol/l的hcl提取后采用邻菲啰啉分光光度法(参见原国家环境保护总局《水质铁的测定邻菲啰啉分光光度法hj/t 345-2007》)测定土壤二价铁浓度。
85.对比例4
86.本对比例相对于实施例2,提供一种不添加纳米零价铁颗粒的土壤中六价铬的化学-微生物协同修复方法(记作sl2组),具体如下:
87.(1)将200g马铃薯煮沸30min后经无菌纱布过滤取上清液,加入20g葡萄糖后定容至1000ml,将上述混合液于115℃高压灭菌20min获得马铃薯葡萄糖液体(pdl)培养基;将上述pdl培养基中加入1.8%(w/v)的琼脂获得马铃薯葡萄糖琼脂(pda)培养基,用于培养草酸青霉sl2。
88.上述pdl培养基和pda培养基中葡萄糖浓度均为20g/l。
89.(2)将草酸青霉sl2接种至pda培养基中,置于30℃黑暗条件下培养7d,收获新鲜孢子;将上述新鲜孢子于0.05%无菌triton x溶液中经无菌玻璃棉过滤菌丝后,获得浓度为10
10
个孢子/ml的草酸青霉sl2孢子悬液浓缩液。
90.(3)采集原始六价铬污染土壤(其中总铬浓度为314.1mg/kg,六价铬的浓度为187.1mg/kg),经风干、研磨过2.0mm筛后经伽马射线(50kgy)照射预处理得到待处理六价铬污染土壤,伽马射线照射可在减少对土壤基本理化性质扰动的前提下达到灭菌的目的,以
降低土著微生物的影响,从而更利于外源功能微生物草酸青霉sl2的定殖。
91.(4)称取上述待处理六价铬污染土壤50g于250ml烧杯中,通过30ml塑料喷瓶将草酸青霉sl2孢子悬液浓缩液加入到50%的无菌pdl培养基中并均匀喷洒至六价铬污染土壤中,土壤中草酸青霉sl2孢子悬液中孢子的添加量为108个孢子/g土壤,边喷洒边搅拌,用透气膜将烧杯封口,放入人工气候室中(30℃)修复180d。每隔30d向土壤中补充草酸青霉sl2孢子悬液和50%的pdl培养基。含水率控制在15%(v/m),并每周补充去离子水对样品进行补偿,以保持在修复期间所需要的水分。
92.上述50%的pdl培养基为pdl培养基与灭菌去离子水按1:1(v/v)的比例稀释而成。
93.(5)定期取步骤(4)中的土壤样品,采用火焰原子吸收分光光度法(参见生态环境部《土壤和沉积物六价铬的测定碱溶液提取-火焰原子吸收分光光度法hj 1082-2019》)测定土壤中六价铬浓度;土壤样品经0.5mol/l的hcl提取后采用邻菲啰啉分光光度法(参见原国家环境保护总局《水质铁的测定邻菲啰啉分光光度法hj/t 345-2007》)测定土壤二价铁浓度。
94.对比例5
95.本对比例相对于实施例2,提供一种不添加草酸青霉sl2孢子悬液的土壤中六价铬的化学-微生物协同修复方法(记作nzvi组),具体如下:
96.本实施例提供一种土壤中六价铬的化学-微生物协同修复方法,具体如下:
97.(1)在氮气(n2)气氛条件下通过硼氢化钾(kbh4)还原氯化铁(fecl3·
6h2o)法制备颗粒分散于无水乙醇中,进行氮吹处理,获得纳米零价铁颗粒(nzvi)。纳米零价铁颗粒密封并于-70℃超低温冰箱中保存备用。
98.(2)采集原始六价铬污染土壤(其中总铬浓度为314.1mg/kg,六价铬的浓度为187.1mg/kg),经风干、研磨过2.0mm筛后经伽马射线(50kgy)照射预处理得到待处理六价铬污染土壤,伽马射线照射可在减少对土壤基本理化性质扰动的前提下达到灭菌的目的,以降低土著微生物的影响,从而更利于外源功能微生物草酸青霉sl2的定殖。
99.(3)称取上述待处理六价铬污染土壤50g于250ml烧杯中,通过30ml塑料喷瓶将纳米零价铁颗粒加入到50%的无菌pdl培养基中并均匀喷洒至六价铬污染土壤中,纳米零价铁颗粒的添加量为4.0g/kg,边喷洒边搅拌,用由塑料及棉片组成的透气组培封瓶膜将烧杯封口,放入人工气候室中(30℃)修复180天。每隔30d向土壤中补充50%的pdl培养基。含水率控制在15%(v/m),并每周补充去离子水对样品进行补偿,以保持在修复期间所需要的水分。
100.上述50%的pdl培养基为pdl培养基与灭菌去离子水按1:1(v/v)的比例稀释而成。
101.(4)定期取步骤(3)中的土壤样品,采用火焰原子吸收分光光度法(参见生态环境部《土壤和沉积物六价铬的测定碱溶液提取-火焰原子吸收分光光度法hj 1082-2019》)测定土壤中六价铬浓度;土壤样品经0.5mol/l的hcl提取后采用邻菲啰啉分光光度法(参见原国家环境保护总局《水质铁的测定邻菲啰啉分光光度法hj/t 345-2007》)测定土壤二价铁浓度。
102.如图4所示,实施例2中草酸青霉sl2和纳米零价铁颗粒协同修复180d后,土壤六价铬浓度可降低至3.4mg/kg,在实施例3中修复360d后土壤六价铬含量为4.1mg/kg(低于5.7mg/kg),达到中国ii类建设用地筛选值标准。而在对比例4和5中单独添加草酸青霉sl2
和纳米零价铁的处理组中土壤六价铬浓度分别为104.7mg/kg和31.6mg/kg。这表明两者联合处理时的修复效果优于单独添加条件下的修复效果,在土壤铬还原稳定化过程中亦具有显著的协同修复作用。
103.如图5所示,实施例2中草酸青霉sl2和纳米零价铁颗粒协同修复180d后,土壤二价铁浓度为186.2mg/kg,而对比例3中不添加草酸青霉sl2和纳米零价铁颗粒的对照组中检测得到的土壤二价铁浓度为39.0mg/kg,对比例4中仅添加纳米零价铁颗粒的处理组土壤二价铁浓度为105.5mg/kg。土壤中二价铁含量与溶液体系中的变化情况类似,联合处理组中土壤二价铁浓度相对较高,这进一步表明草酸青霉sl2的添加延长了纳米零价铁颗粒的反应活性,验证了两者可协同修复六价铬污染的溶液和土壤。
104.此外,草酸青霉sl2不仅具有高效的六价铬还原能力,还可溶解铬铁沉淀、驱动三价铁还原,活化纳米零价铁,显著提升纳米零价铁的反应活性。草酸青霉sl2和纳米零价铁协同修复可在降低处理成本的同时提高六价铬还原稳定化效率,具有广阔的应用前景。
105.以上所述的实施例只是本发明的一种较佳的方案,然其并非用以限制本发明。有关技术领域的普通技术人员,在不脱离本发明的精神和范围的情况下,还可以做出各种变化和变型。因此凡采取等同替换或等效变换的方式所获得的技术方案,均落在本发明的保护范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1