低温高效抗中毒催化甲酸制氢的铱催化剂及其制法与应用的制作方法
本发明涉及一种均相催化剂,特别是一种低温高效抗中毒催化甲酸制氢的铱催化剂、其制备方法及应用,属于能源催化材料、氢气制造技术领域。
背景技术:
氢气作为一种高化学活性和广泛用途的物质,在国民生产和科研领域占有重要地位,氢气作为高效清洁能源也吸引了越来越多的关注。但是氢气的应用面临三大难题:制氢、储氢、广泛经济的应用形式。
近几年来直接甲酸燃料电池以其具有燃料来源广、能量转化率高、低污染、储存和运输方便等优点,在便携式电源、电动机车等领域具有广阔的应用前景,己经得到了世界范围的关注和重视。
目前基于化学过程的液体移动制氢已成为当前燃料电池领域的热门话题之一,甲酸因其高含氢量等优点而成为移动制氢的研究热点,目前所面临的问题就是如何在温和条件下连续催化甲酸分解获得氢气。
JP2005-289742、CN101541668B、CN103240108A公开了由甲酸分解产生H2和CO2的方法,但反应条件均较为苛刻,对于燃料电池、便携性用氢设备等实际应用是不可行的。
近年来有一些研究中利用一些均相催化剂在常温下实现了高效的甲酸制氢反应,但是反应介质是有机相,在实际应用,比如燃料电池的制作使用过程中,极易发生火灾危险。
综述,之前的各项技术普遍存在氢气转化率低、含有毒气体、反应温度较高、所需压力较大等缺陷。
Bi等人(J.Am.Chem.Soc.,2012,134,8926-8933)公开了用氧化锆负载纳米金颗粒、团簇在温和条件下催化分解甲酸生成氢气的方法。中科院长春应化所的邢魏等人,使用纳米钯碳、纳米钯银催化剂,也可以高效的分解甲酸制氢。但是贵金属单质的催化剂,对很多物质容易中毒,例如,极少量的甲醛、大部分蛋白质类的物质和巯基类物质都会导致催化剂中毒。因此使用此类贵金属非均相催化剂,必须在甲酸分解反应之前,将甲酸中少量的毒害物质除去,但这样会大大增加制取氢气的成本。
技术实现要素:
本发明的主要目的在于提供一种低温高效抗中毒催化甲酸制氢的铱催化剂及其制备方法与应用,从而克服现有技术中的不足。
为实现前述发明目的,本发明采用的技术方案包括:
一种常温抗中毒甲酸制氢铱催化剂,其选自具有下式(I)所示结构的金属络合物:
其中,X为能够与Ir络合的配体,并至少选自或其衍生物、或其衍生物、Cl、H2O,n选自1、2或3。
本发明还提供了一种制备所述低温高效抗中毒催化甲酸制氢的铱催化剂的方法,包括:
1)将铱离子与五甲基环戊二烯在极性有机溶剂中混合并充分回流反应后,经后处理获得第一中间产物;
2)将步骤(1)所获第一中间产物与Ag离子在非极性溶剂中混合并在室温黑暗条件下充分反应,再经后处理获得第二中间产物;
3)将步骤(2)所获第二中间产物与选定配体在水中混合并在室温下充分反应,再经后处理获得目标产物。
其中,所述选定配体至少选自2,2’-联吡啶或其衍生物、2,2’-联嘧啶或其衍生物、H2O或氯离子。
本发明还提供了所述铱催化剂的用途。
例如,在一实施方案之中提供了一种甲酸制氢方法,其包括:采用所述的铱催化剂使甲酸在低温,例如温度为-20℃~100℃的条件下分解,从而获得氢气。
在一较为优选的实施方案之中,所述的甲酸制氢方法包括:将所述铱催化剂溶于水相体系中,并使甲酸在所述水相体系中被所述铱催化剂催化分解,从而获得氢气。
在一更为优选的实施方案之中,所述的甲酸制氢方法包括:将所述铱催化剂溶于水相体系中,并直接将甲酸连续加入所述水相体系,从而连续获得氢气。
进一步的,在所述的甲酸制氢方法之中,甲酸在所述铱催化剂的催化作用下分解生成 的物质仅含体积比为1:1的氢气和二氧化碳。
在一尤为优选的实施方案之中,所述的甲酸制氢方法包括:在温度为-20℃~100℃的条件下,以水作为所述铱催化剂的溶剂,使甲酸被催化分解,从而获得氢气。较佳的,反应温度为50℃以下,更佳的,反应温度为常温,例如28℃~35℃,最佳的,反应温度为33℃。
进一步的,所述铱催化剂催化甲酸分解的TOF大于400h-1。
进一步的,所述铱催化剂催化甲酸分解的TOF大于400h-1,而小于或等于430h-1。
与现有技术相比,本发明的优点包括:
(1)提供的铱催化剂在低温、常压、水相条件下能高效催化甲酸分解分解成体积比为1:1的氢气和二氧化碳,TOF可达430h-1,且所获得的气体混合物中不含任何CO等对于燃料电池有毒成分,工艺简单,所得氢气纯度高并且易于和CO2分离,可直接供给发动机、燃料电池等;
(2)提供的铱催化剂对大部分常见的催化剂毒物均有很好的抗中毒效果;
(3)提供的铱催化剂在长期连续使用后,无需分离便可继续再次用于甲酸催化分解反应,且仍保持较高稳定性和活性,可大幅降低应用成本。
附图说明
图1是本发明实施例1所获的一种铱催化剂催化甲酸的核磁共振图谱;
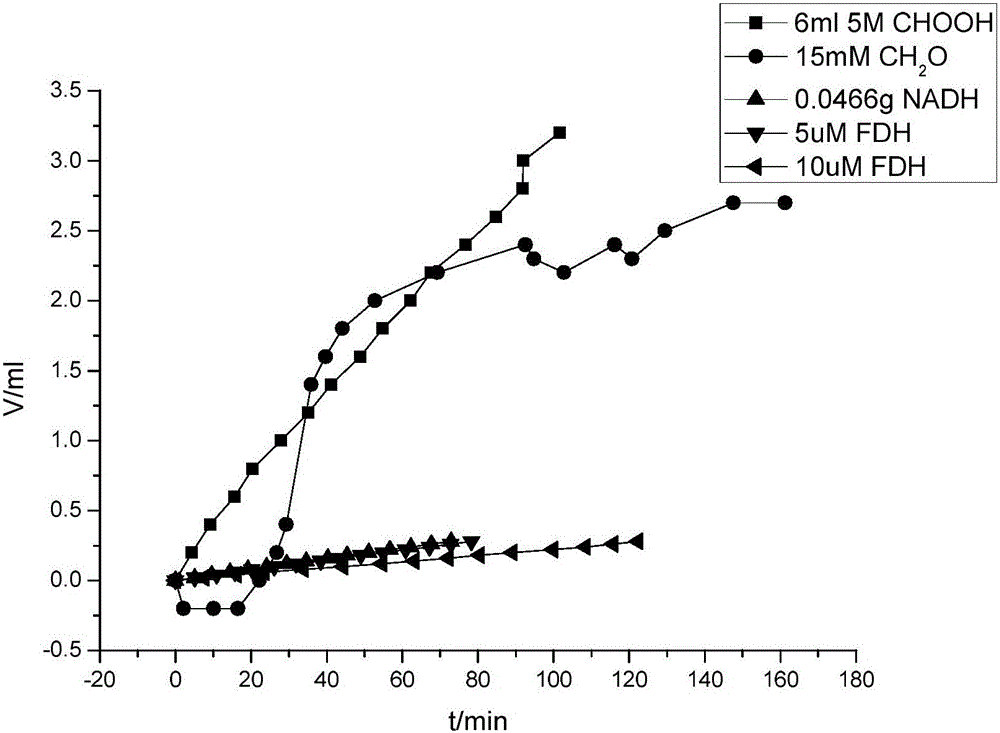
图2是本发明实施例1所获铱催化剂催化甲酸的抗中毒测试图。
具体实施方式
如前所述,鉴于现有技术的诸多缺陷,本案发明人经长期深入的研究和大量实践,得以提出本发明的技术方案,如下具体说明。
本发明的一个方面提供了一种铱催化剂,其可以由原位生成的催化剂、金属源和配体,或预先处理的金属络合物构成。
本发明的另一个方面提供了所述铱催化剂的制备方法。
本发明的又一个方面提供了基于所述铱催化剂的甲酸催化制氢方法。
在一些实施例之中,所述铱催化剂选自具有下式(I)所示结构的金属络合物:
其中,X至少选自或其衍生物、或其衍生物、Cl、H2O,n选自1、2或3。
进一步的,所述铱催化剂的活性组分为铱,可以溶于水。
更为具体的,在一些实施案例之中,所述催化剂可以具有如下所示的结构:
其中,R、R1至少选自OH、H和NO2。
进一步的,所述铱催化剂在低温、常压、水相条件下即可高效的催化甲酸分解生成氢气和二氧化碳,且所获得的气体混合物中不含任何CO等对于燃料电池有毒成分。
进一步的,本发明的铱催化剂能够在空气中长期稳定存在,并保持良好的活性和稳定性。
进一步的,所述铱催化剂可以使甲酸分解并按照1:1的比率(H2:CO2=50:50体积%)释放出H2和CO2。因而,藉由该催化剂,可以在较低温度范围内获得H2/CO2混合物。
较为优选的,基于所述铱催化剂的甲酸催化制氢方法的反应温度为-20℃~100℃。
进一步的,所述铱催化剂在温度不高于50℃的条件,例如常温条件下可以长时间持续稳定的催化甲酸制氢,例如在甲酸溶液中连续催化制氢20天后,依旧具有很好的催化性能。
更进一步的,基于所述铱催化剂的甲酸催化制氢方法的反应温度最佳为33℃,在此条 件下TOF大于400,最高可达430h-1,且不需要再添加其他添加剂。
进一步的,所述铱催化剂的溶剂优选水。
进一步的,甲酸可以连续加入到溶有所述铱催化剂的水相反应器中,并可源源不断的产生氢气。且在一阶段反应结束后催化剂无需分离便可直接进行到下一阶段的反应中。
进一步的,由于所述铱催化剂抗中毒能力好,特别是对甲醛、蛋白质、氨基酸等常见毒性物质有非常好的抗中毒特性。因此对甲酸的纯度要求不高,使用工业纯的甲酸也具有好的催化效果。
以下结合若干实施例对本发明的技术方案作进一步的说明。
实施例1:铱催化剂的制备。
1)将铱离子(例如氯铱酸)与五甲基环戊二烯(Cp*)溶解在少量极性溶剂(例如甲醇)中,回流37h,冷却至0℃,过滤,使用乙醚洗涤,得到黄棕色中间产物。
2)将步骤(1)所获黄棕色产物与1,10-菲罗啉或2,2’-联嘧啶或邻菲罗啉溶解在非极性溶剂(例如二氯甲烷)中,在室温黑暗下搅拌5h,浓缩干燥得到黄色粉末,即式(Ⅰ)所示的铱催化剂。其中一种典型催化剂的核磁氢谱如图1所示。
实施例2:催化剂酸分解制备氢气的过程
将10-3mmol实施例1所获铱催化剂溶解在1ml 5mol/L甲酸中,通入N2,在33℃油浴搅拌下反应,通过U型管监测气体值变化,可得到连续的气体,该气体由体积比1:1的氢气和二氧化碳组成。
实施例3:催化剂酸分解甲酸抗中毒测试。
1)向反应了约3h的实施例2的反应液中加入10ul甲醛,吹N2,通过U型管监测气体值变化,仍可得到连续的由体积比1:1的氢气和二氧化碳组成的气体,说明该催化剂可抗甲醛中毒。
2)向步骤(1)最终所获反应液中加入约20Mm NAD+,吹N2,通过U型管监测气体值变化,仍可得到连续的由体积比1:1的氢气和二氧化碳组成的气体,说明该催化剂可抗NAD+中毒。
3)向步骤(2)最终所获反应液中加入约20Mm NADH,吹N2,通过U型管监测气体值变化,仍可得到连续的由体积比1:1的氢气和二氧化碳组成的气体,说明该催化剂可抗NADH中毒。
4)向步骤(3)最终所获反应液中加入约5ul甲酸脱氢酶,吹N2,通过U型管监测气体值变化,仍可得到连续的由体积比1:1的氢气和二氧化碳组成的气体,说明该催化剂可抗甲酸脱氢酶中毒。其测试结果详见图2。
式(I)所示的其它化合物的合成步骤与实施例1中铱催化剂的制备过程相似。而参照实施例2-3对这些催化剂进行测试,可以发现其具有与实施例1所获催化剂相近的性能。
以上所述仅是本发明的优选实例之一,应当指出,对于本技术领域的普通技术人员,在不脱离本发明原理的前提下,还可以做出若干细节变化,这些细节变化也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!