在中性条件下用于电化学H2O2生产的高选择性N-和O-掺杂的碳的制作方法
陈光需、陆之毅和崔屹
发明领域
本发明涉及过氧化氢在中性溶液中的电化学生产。
背景
过氧化氢(h2o2)是在化学工业、食品、能量和环境保护等许多领域中非常有价值的化学品。因为过氧化氢的常规生产是能源密集型工艺,所以,最近人们致力于生产h2o2的高效方法。用于h2o2生产的一种安全、有吸引力且有前途的策略是通过双电子途径的电化学氧还原。
一定程度上获得了具有高选择性的催化剂,以通过该电化学方法生产h2o2。用于氧还原反应生成h2o2的催化剂的活性高度依赖于电解质的ph值,迄今为止的工作证实了仅在酸性或碱性电解质中具有良好结果。因此,由于缺乏高效催化剂,在中性条件下选择性产生h2o2仍然是极大挑战。由于大多数废水的ph值都接近7,ph中性工艺可以提供现场产生h2o2用于水消毒,因此可以消除由h2o2的运输和储存所导致的潜在危险。因此,迫切需要开发一种催化剂,用于在中性条件下生产h2o2。
概述
我们报道了一种n-和o-掺杂的碳催化剂的简易一锅合成法,所述n-和o-掺杂的碳催化剂在中性介质中具有高氧还原活性(在相对于rhe(可逆氢电极)的0.6v下,6.6mamg-1)和最高的h2o2产率(96%)。在一个实例中,n-和o-掺杂的碳催化剂源自乙二胺四乙酸(edta)碳化,所述乙二胺四乙酸(edta)是低成本的,且包含适度氮含量(9.6%)。n-和o-掺杂的碳催化剂对于电化学生成h2o2的这种史无前例的催化活性和选择性归因于氮和氧物质对催化剂的协同作用。该n-和o-掺杂的碳催化剂显示出在中性电解质中对于生成h2o2的最佳活性和选择性。
该n-和o-掺杂的碳催化剂的主要应用为用于在中性电解质中由氧还原反应进行h2o2的电化学生成。所产生的h2o2可以用于环境保护和水或食物消毒。
提供了显著的优点。1)该n-和o-掺杂的碳催化剂可以源自乙二胺四乙酸(edta)在熔融的氢氧化钾中碳化,其是非常便宜且简单的。2)该n-和o-掺杂的碳催化剂在中性电解质中显示出h2o2电化学生成的最佳活性和选择性。
可采取多种变化形式。1)前体,包括乙二胺四乙酸或其类似结构(即,碳前体)以及氢氧化钾或其类似碱(即,碱前体)。参见下文替代的碳前体和碱前体。2)碳前体和碱前体之间的前体质量比值。3)反应温度范围为400℃至1000℃。4)反应气氛通常为在氮气或氩气下。5)催化剂中氮和氧的含量。
重要特征包括如下:n-和o-掺杂的碳催化剂的结构。n和o两者都用于催化剂,并且n-和o-掺杂的碳催化剂对于h2o2电化学生成的这种史无前例的催化活性和选择性归因于氮和氧物质对催化剂的协同作用。
附图简要说明
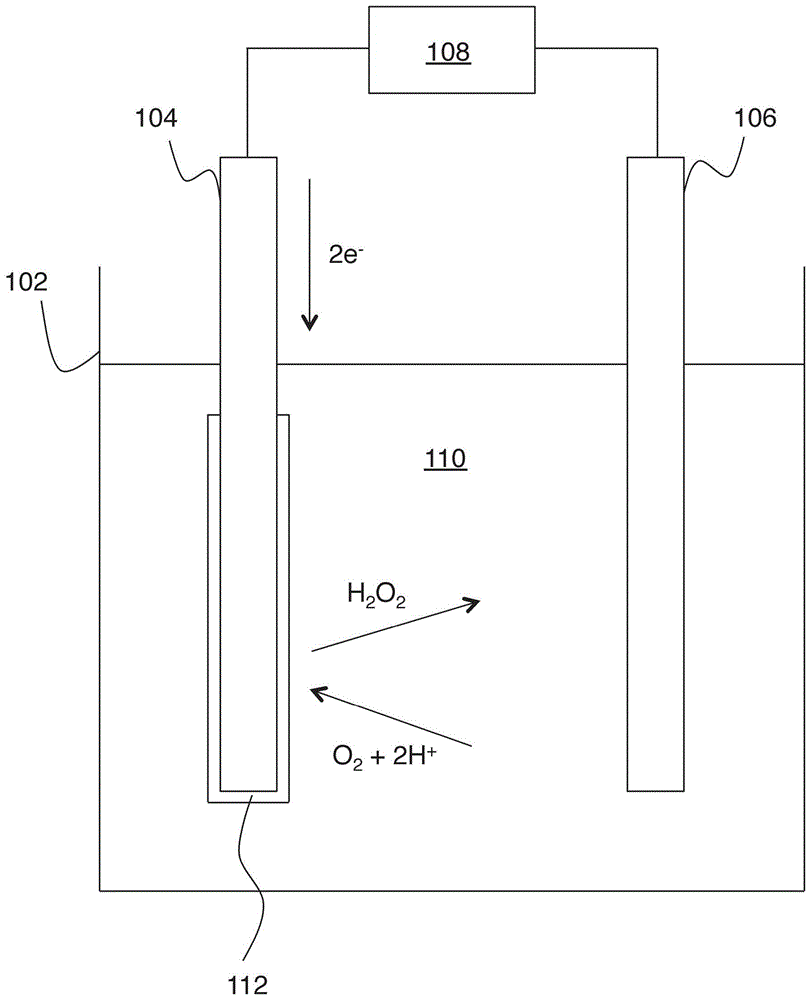
图1显示示例性电化学池(cell)。
图2a示意性显示过氧化氢生产的催化。
图2b-d显示来自该研究的催化剂的图像和表征结果。
图3a-c显示来自示例性实验的过氧化氢生产结果。
图4a-b显示来自该研究的催化剂的xps结果。
图4c-f显示来自其它实验的过氧化氢生产结果。
图5a-b显示来自示例性实验的消毒结果。
图6显示n-和o-掺杂的碳微片的横截面sem图像。
图7显示n-和o-掺杂的碳催化剂的xrd分析。
图8显示在n-和o-掺杂的碳上的xps测量谱。
图9显示用于orr的n-和o-掺杂的碳催化剂的稳定性测试结果。
图10a-c显示具有不同n/c比值的n-和o-掺杂的碳催化剂的n1s的高分辨率xps。
图11a-c显示与以三聚氰胺作为前体的n-和o-掺杂的碳催化剂有关的结果。
详细描述
a节描述了与本发明多个实施方式有关的一般原理。b节详细描述了本发明原理的实验演示。
a)一般原理
图1显示了适用于实施本发明实施方式的电化学池。更具体地说,电化学池102包括电解质110、第一电极104和第二电极106。如图所示,电源108驱动电流流动以产生h2o2。虽然此处所示的特定反应是双电子氧还原反应,但是也可以进行同样产生h2o2的其它电化学反应。该设置的两个方面特别重要。第一方面是电解质110是ph中性的,本文限定为具有6至8的ph。第二方面是催化剂112构造成在该中性电解质的情况下高效催化产生h2o2。与催化剂有关的其它细节见述于下文和b节。
因此,本发明的一个实施方式是一种在ph中性的溶液中产生过氧化氢的方法。此处,所述方法包括:
a)提供电化学反应池;
b)在电化学反应池中提供同时包括氮掺杂和氧掺杂的介孔碳催化剂;以及
c)为电化学反应池提供电流,以驱动产生过氧化氢的氧还原反应。
此处,氧还原反应由介孔碳催化剂进行催化,所述介孔限定为具有直径为2nm至50nm的孔的多孔结构。
该方法的应用包括产生h2o2以提供对环境水的处理。该处理可以是污染物的化学降解和/或消毒的任意组合。
本发明的另一实施方式是一种制备用于电化学产生过氧化氢的催化剂的方法。此处,所述方法包括:
a)提供含氮有机前体;以及
b)用碱使含氮有机前体碳化,以提供同时包括氮掺杂和氧掺杂的介孔碳催化剂。
含氮有机前体可以具有下式给出的化学结构:
其中,n≥1、m≥1、x≥1、y≥1、z≥1,并且各r独立地选自下组:h、烃基、碱金属(li、na、k、rb、cs)离子和碱土金属(be、mg、ca、sr、ba)离子。
本发明的实践并不严格依赖于用于使前体碳化的碱。合适的碱包括但不限于:氢氧化钾(koh)、氢氧化钠(naoh)、氢氧化锂(lioh)、氢氧化铷(rboh)、氢氧化铯(csoh)、氢氧化铵(nh4oh)、氢氧化铍(beoh)、氢氧化镁(mg(oh)2)和氢氧化钙(ca(oh)2)。
用碱使含氮有机前体碳化优选在600℃至900℃的温度下进行。
本发明的另一实施方式是同时包括氮掺杂和氧掺杂的介孔碳催化剂,其中,所述催化剂构造成对电化学氧还原反应进行催化,从而在ph中性的溶液中产生过氧化氢。另一实施方式是包含该催化剂的电化学池(例如,如图1所示)。
该催化剂优选构造为包括石墨化纳米级域(nano-scalegraphitizeddomain)的无定形碳的多孔微片。此处,微片定义为一个维度为1微米或更小而其他两个维度为5微米或更大的结构,并且纳米级域定义为最大尺寸为1微米或更小。
催化剂的氮含量和氧含量皆优选大于1%。优选在介孔碳催化剂中不含过渡金属(第21-29号、第39-47号、第57-79号元素)。
氮掺杂能以各种化学构型包括在介孔碳催化剂中,所述化学构型包括但不限于吡咯(pyrrolic)和吡啶(pyridinic)构型及其组合。此处,如果nh基团是五元芳环的一部分,则氮原子为吡咯构型,例如,在吡咯(c4h4nh)中。如果n原子替代六元芳环的ch基团,则氮原子为吡啶构型,例如,在吡啶(c5h5n)中。在n1s的xps光谱中,吡啶型氮的峰在398.5ev处,并且吡咯型氮的峰在400.1ev处。
b)实验实施例
b1)引言
过氧化氢(h2o2)是在化学工业、食品、能量和环境保护等许多领域中非常有价值的化学品。此外,h2o2是强氧化剂,并且其利用的唯一降解作用是水,这使其广泛用于水体环境中难降解污染物的降解以及水消毒。在工业中,h2o2的需求通过经取代的蒽醌的氢化和氧化的相继过程来满足,这是一个能源密集型过程,并且几乎不能视为环境友好的方法。近年来,人们大力致力于开发产生h2o2的高效方法。通过在非均相反应中使单质氢和氧在多种催化剂上转化为h2o2来实现h2o2的直接合成。然而,该工艺将会涉及潜在的爆炸危险。用于h2o2生产的另一种安全、有吸引力且有前途的策略是通过双电子途径(orr,氧还原反应)的电化学氧还原。在文献中,在使用理论模拟和复杂的合成技术的情况下,一定程度上已经获得了对h2o2生产具有高选择性的催化剂。
实际上,催化剂对orr产生h2o2的活性高度依赖于电解质的ph值。已确定贵金属基催化剂(例如,pd-au、pt-hg)主要在酸性条件下实现双电子途径,并且选择性超过90%,但稀缺性和高成本可能会阻碍其大规模应用。并且,还需要考虑催化剂本身的重金属污染。碳基材料最近作为低成本且高活性的催化剂出现,用于在碱性或酸性电解质中的氧还原。此外,氧还原的反应途径(双电子途径或四电子途径)可以通过结构调整或用杂原子(例如,fe、n、s)对碳进行选择性掺杂来进行微调。尽管有该进展,但是由于缺乏高效催化剂,在中性条件下选择性产生h2o2仍然是极大挑战。由于大多数废水的ph值都接近7,因此该工艺可以提供在现场产生h2o2用于水消毒,并且因此可以消除由h2o2的运输和储存所导致的潜在危险。因此,迫切需要开发一种新型碳基催化剂,其在中性条件下对于h2o2产生具有高活性和选择性。
b2)技术途径
本文中,我们报道了一种n-和o-掺杂碳催化剂的简易一锅合成法,其在中性介质中具有高氧还原活性(在相对于rhe的0.6v下,6.6mamg-1)和最高的h2o2产率(96%)(图1和图2a)。n-和o-掺杂的碳催化剂源自乙二胺四乙酸(edta)碳化,所述乙二胺四乙酸(edta)是低成本的,且包含适度氮含量(9.6%)。n-和o-掺杂的碳催化剂对于电化学生成h2o2的这种史无前例的催化活性和选择性归因于氮和氧物质对催化剂的协同作用。此外,我们演示了一种用于水消毒的h2o2现场电化学生成系统,其具有>99.999%的出色效率。
图2a显示使用n-和o-掺杂的碳催化剂的h2o2的电化学生成方案。图2b显示n-和o-掺杂的碳微片的代表性sem图像。图2c显示n-和o-掺杂的碳微片的tem和hrtem图像。图2d显示iv型氮吸附等温线。插图是通过巴雷特-乔伊纳-哈伦达(barrett–joyner–halenda,bjh)模型的n-和o-掺杂碳的孔径特征。
b3)催化剂制备和表征
通过在氩气气氛中,使乙二胺四乙酸(edta)在熔融的氢氧化钾中碳化,来进行n-和o-掺杂的碳催化剂的简易一锅合成法(详情参见下文)。通过离心来收集所得产物,并用稀硝酸和去离子水洗涤产物数次。所制备的n-和o-掺杂的碳催化剂首先通过扫描电子显微镜(sem)进行表征。如图2b中sem图像所示,产物主要由碳微片形成。较高放大倍数下的sem图像(图2b插图和图6)表明,微片是高度多孔的。透射电子显微镜(tem)研究(图2c)揭示了碳微片的无定形结构,这与x射线衍射(xrd)的分析一致(图7)。但是,高分辨率tem(hrtem)图像(图2c插图)表明,n-和o-掺杂的碳包括许多纳米尺寸的石墨化碳域,这表明n-和o-掺杂的碳会具有高表面积。
使用布伦纳-埃米特-特勒(brunauer–emmett–teller)方法对n-和o-掺杂的碳进行n2吸附-解吸等温分析,确认了约494m2g-1的高比表面积(图2d)。观察到iv型等温线在较高相对压力(p/p0>0.5)下具有滞后现象,这是介孔材料的指示(图2d)。通过巴雷特-乔伊纳-哈伦达(bjh)方法的孔径分布分析揭示出n-和o-掺杂的碳的主要孔径为约3.9nm(图2d插图),与tem观察良好对应。由于氮含量与n-和o-掺杂的碳催化剂的催化性能直接对应,因此进行x射线光电子能谱(xps)和元素分析(ea)测量以确定n-和o-掺杂的碳微片的氮含量和氧含量。来自xps测量的n-和o-掺杂的碳微片的氮含量为约1.8%,与ea(2.0%)分析略有不同。该值的变化主要是由于xps测定的表面特异性。氧含量为约14.8%。值得注意的是在进行调查测量时,n-和o-掺杂的碳材料中均未发现任何金属。
b4)h2o2生成结果
氧还原反应的电化学测量在标准三室电化学池中使用可互换的旋转环-盘电极进行,该电极与旋转控制器(松木仪器公司(pineinstruments))和生物vsp(biologicvsp)恒压器连接。为了对所形成的h2o2量进行定量,pt环电极恒压在1.2v(相对于rhe,下同),此时氧还原电流可忽略,并且h2o2氧化受扩散限制。将由乙醇、2-丙醇和全氟磺酸(nafion)溶液制备的催化剂悬浮液的等分试样沉积到抛光良好的玻璃状碳电极上,并在o2饱和pbs(磷酸盐缓冲盐水)溶液(ph=7)中进行测量。记录在0v至1.0v电压下的极化曲线,以及在脱气pbs溶液中的对应循环伏安图(cv)。通过在脱气pbs溶液中测得的cv对极化曲线的背景进行校正。为了进行比较,还在相同条件下测量了市售炭黑(c65,无定形碳)。
图3a-c显示n-和o-掺杂的碳催化剂用于在中性介质中氧还原的电催化性能。图3a显示在具有n-和o-掺杂的碳和市售炭黑c65的o2饱和的0.1mpbs溶液(ph=7)中以1600rpm运行的rred伏安图,包括对应于由环电流所获得过氧化氢的电流密度、环电流和盘电流密度。图3b显示在n-和o-掺杂的碳和炭黑c65上以氧还原反应产生h2o2的对应选择性。图3c显示用n-和o-掺杂的碳催化剂由氧还原反应产生的h2o2的浓度与psb溶液中电解时间的函数关系。电势为约0.6v(相对于rhe)。
如图3a所示,市售炭黑(c65)显示出在pbs溶液中对于orr的活性可忽略。氧还原仅在电势低于0.35v时发生(图3a)。形成鲜明对比的是,n-掺杂的催化剂在约0.7v处开始显示出orr电流(几乎为~0mv超电势),表明n-和o-掺杂的碳催化剂比炭黑更具活性。此外,我们观察到n-和o-掺杂的碳催化剂的盘和环的电流密度在0.55v至0.7v电势处重合,这表明orr在该电势范围内偏向于双电子途径,并且有利于h2o2的形成。在该电势范围内,获得了约10mamg-1的最大h2o2电流密度(图3a)。如图3b所示,在0.4v至0.65v的电势处,产生h2o2的效率高于90%,而且在市售炭黑上没有观察到orr电流。在0.6v电势下,以6.5mamg-1电流密度实现了约96%的最高效率。发现在低于0.4v的电势下,产生h2o2的电流密度和选择性都下降,意味着有利于水的形成。
此外,n-和o-掺杂的碳催化剂的稳定性通过在碳纤维纸上加载催化剂来测试。图9中显示了令人印象深刻的orr稳定性,在0.4v下,4macm-1阴极电流在20小时内没有显著退化。由于h2o2的现场生成在水消毒中特别有用,因此测试了h2o2的实际生成量。图3c显示累积的h2o2浓度相对于电解时间的曲线,其反映了h2o2的量与电解时间之间的拟线性关系。在3小时内以75mgl-1h-1的平均生成速率获得了225mgl-1的h2o2浓度。
图4a-f显示了氮物质和氧物质对orr催化性能的影响。图4a-b显示n-和o-掺杂的碳催化剂的n1s和o1s的高分辨率xps。图4c显示具有不同氮含量的n-掺杂催化剂的rrde伏安图测量值。图4d显示在具有不同氮含量的n-和o-掺杂的碳催化剂上以氧还原反应产生h2o2的对应选择性。图4e显示在700℃下进行h2(氩气中5%h2)还原1小时之前和之后,n-掺杂催化剂的rrde伏安图测量值。图4f显示在700℃下进行h2(氩气中5%h2)还原1小时之前和之后,n-和o-掺杂的碳催化剂上以氧还原反应产生h2o2的对应选择性。
为了研究掺杂剂对催化剂电化学性能的影响,对n-掺杂催化剂进行了高分辨率xps测量。如图4a-4b所示,发现了氮和氧的信号。氮以吡啶型(11.6%,398.5ev处)氮和吡咯型(88.4%,400.1ev处)氮的结构存在(图4a)。氧结构分别是cooh(羧基中的氧原子,17%,534.4ev)和-o-(酯、酸酐中的羰基氧原子和羟基中的氧原子,83%,532.9ev)(图4b)。先前讨论氧作用的研究很少,但是多个研究表明氮掺杂可以显著提高碳催化剂的orr活性。多个研究组已报告,吡啶型氮是提高orr活性的活性位点,而另一些研究组则认为,季铵型氮是n-和o-掺杂的碳催化剂的高orr活性的原因。因此,掺杂的氮的确切催化作用以及活性位点仍存在争议。此外,在大多数情况下,催化剂在碱性或酸性电解质中进行评估,并且四电子途径是有利的。文献中的理论计算表明,石墨中与季铵型n相邻形成的碳自由基位点可作为o2电还原为h2o2的活性位点。然而,在本文的情况下,除了吡啶型氮和吡咯型氮,并未观察到401.0ev处的季铵型n和402.9ev处的氧化n。因此,吡啶型氮和吡咯型氮被认为是出色催化性能的原因。
由于氮掺杂在催化剂的催化性能上扮演了重要角色,故制备具有不同n/c比值(0.026、0.043和0.050)的n-和o-掺杂的碳。在所有样品中,掺杂的氮物质是相似的,而在n-和o-掺杂的碳上仅发现了少量的季铵型n,其n/c比值为0.026和0.050(图10a-c),但季铵型n并未改进催化性能。发现n/c比值为0.043的n-掺杂和o-掺杂的碳显示出高达96%的最佳h2o2选择性(图3a-b)。然而,虽然降低氮含量(n/c=0.026)将会提高催化剂的动态电流密度和扩散限制电流密度,但是h2o2电流密度下降并且最终导致较低的h2o2选择性(图4c-d)。提高氮含量(n/c=0.050)导致较低的orr活性和较低的h2o2电流密度,类似地显示出较低的h2o2选择性。通过在制备n-和o-掺杂的碳时引入三聚氰胺作为前体而保持相同的n结构,同时进一步提高氮含量(n/c=0.087),导致甚至更低的活性和h2o2选择性(图11a-c)。因此,在我们的情况中,我们得出结论,适量的n掺杂是在h2o2的电化学生产中实现高活性和选择性的主要原因。
进一步的研究表明,氧掺杂对于实现高h2o2选择性也是必要的。一旦通过氢还原减少了氧物质,则碳催化剂变得更具活性,并且起始电势为0.8v(相对于rhe)(图4e),但是相应的h2o2选择性下降(图4f)。经还原的碳催化剂的高分辨率xps分析显示出,氮含量几乎保持不变,而氧却减少了4.6%,这表明氧物质在催化剂中对实现高h2o2选择性起关键作用。氧掺杂的具体功能可能源自氧官能团或缺陷。因此,n-和o-掺杂的碳催化剂对于h2o2电化学生成的这种史无前例的催化活性和选择性归因于氮和氧物质对催化剂的协同作用。
b5)h2o2消毒结果
图5a-b显示通过使用n-和o-掺杂的碳催化剂的电化学水消毒。图5a显示利用不同电流密度的n-和o-掺杂的碳催化剂的消毒性能。通过在电化学池中培养细菌直接进行测量,该电化学池用n-和o-掺杂的碳催化剂运行orr,用于产生h2o2。图5b显示通过使用不同浓度h2o2的水消毒,所述不同浓度h2o2利用n-和o-掺杂的碳催化剂由orr产生。n-和o-掺杂的碳催化剂以2mgcm-2的负载量负载于碳纤维纸上。
由于h2o2是用于水消毒的环境友好的强氧化剂,因此使用我们的高活性n-和o-掺杂的碳催化剂在pbs溶液(ph=7)中进行原位和非原位电化学水消毒实验。在所有实验中,革兰氏阴性细菌大肠杆菌(gram-negativebacteriume.coli)被用作模型细菌。实验各时间点的细菌浓度归一化至起始浓度,并且结果显示在图5a-b中。对于原位水消毒,细菌大肠杆菌在负位点进行培养,在该负位点处通过orr产生h2o2。负电极和正电极通过质子交换膜(全氟磺酸(nafion))分隔。如图5a所示,在未施加任何电流的情况下没有发现明显的消毒效率。一旦施加1ma电流,在120分钟内实现了99.86%的消毒效率。电流的进一步提高(2ma)导致120分钟内的消毒效率更高,为99.991%。对于非原位水消毒,细菌大肠杆菌用通过电化学orr预制的h2o2溶液进行培养。如图5b所示,当h2o2浓度大于50ppm时,在120分钟内达到99.9995%的消毒效率,此后无法检测到细菌,也未观察到恢复。基于以上的原位和非原位水消毒,h2o2现场生成用于饮用水消毒是有前景的。
总之,我们已经演示了新型氮掺杂介孔碳的合成,其显示出在中性条件下对orr的高效电催化活性以及对生成h2o2的高选择性(96%)。仔细研究了碳催化剂中掺杂剂(n和o)对催化活性的影响,碳催化剂中氮和氧物质的协同作用是通过电化学orr生成h2o2的高活性和选择性的原因。此外,通过使用我们的电化学生成的h2o2,演示了效率>99.999%的出色水消毒性能。如此出色的性能在饮用水消毒应用中显示出巨大的潜力。
b6)方法
b6a)试剂:乙二胺四乙酸(edta)、氢氧化钾(koh)、磷酸一钠(nah2po4)和磷酸二钠(nah2po4)购自西格玛奥德里奇公司(sigmaaldrich)。盐酸(hcl)和乙醇购自飞世尔化学公司(fisherchemical)。高纯度ar(99.999%)、o2(99.998%)和n2(99.99%)购自空气气体公司(airgas)。超纯水(密理博公司(millipore),≥18mωcm)。所有试剂直接使用而无需进一步纯化。
b6b)n-和o-掺杂的碳催化剂的合成:在n-和o-掺杂的碳催化剂的典型合成中,使2gedta和4gkoh混合在一起,并在研钵中研磨10分钟。将充分混合的混合物转移到燃烧舟中,然后在氩气气氛中于700℃下在管式炉中煅烧2小时。样品以10℃/分钟的升温速率从室温升至700℃。在煅烧后,用去离子水和0.5m盐酸溶液洗涤产物以除去koh,然后在真空烘箱中于60℃干燥过夜。
b6c)材料表征:tem研究是在tecnaif-20高分辨率透射电子显微镜上于200kv进行。通过将样品的乙醇分散体滴到300目碳涂覆铜栅格上并立即使溶剂蒸发来制备样品。在feixl30sirion上进行sem研究,以对碳催化剂的形态和微观结构进行表征。使用cukα辐射,在40kv和30ma下运行的panalyticalx’pertpro射线衍射仪上记录x射线衍射(xrd)图。x射线光电子能谱(xps)测量在利用alkα源(1486.6ev)的ssisprobexps光谱仪上进行。本文报道的结合能是参考284.5ev的c(1s)。电化学研究在与生物vmp3(biologicvmp3)多通道电化学工作站连接的标准三电极池中进行。对电极是超纯石墨棒(直径6毫米),参比电极是ag/agcl电极。工作电极是具有pt环和玻璃状碳盘(gc,
b6d)电化学测量:在将碳催化剂加载到电极上之前,首先通过在0.1mpbs溶液(ph=7)中在-0.5~1.1v(相对于rhe)的电势下,以500mv/s扫描速度进行循环伏安法(cv)来清洁用于检测h2o2的pt环,直到pt环干净且cv曲线稳定为止。为了将催化剂沉积到gc盘电极上,将10.0mg碳催化剂分散在0.5ml异丙醇、0.5ml乙醇和50μl5重量%全氟磺酸(nafion)溶液中,超声处理1小时,以形成均匀的催化剂油墨。然后,将3.0μl油墨滴到rrde的gc盘上,使催化剂负载量为153μgcm-2。0.1mpbs电解质用超纯氧以60ml/分钟鼓泡15分钟。以20mvs-1的扫描速率和1600rpm的旋转速率使gc盘电极经受0.25至1.1v(相对于rhe)的电势循环。补偿了85%的溶液欧姆降(即,ir降)。在相同的电势范围和扫描速率下记录背景电容电流,不同的是其在n2饱和电解质中进行。通过n2的背景电流校正o2饱和溶液中记录的电流,以获得所测催化剂的orr电流。为了检测h2o2的产率,将环电势设置为1.2v(相对于rhe),以使由gc盘电极转移的h2o2氧化。h2o2产率通过以下等式(式1)来计算:
其中,id和ir分别是盘电流和环电流,并且n0是环收集效率。在10mm铁氰化钾k3fe(cn)6+1.0mkno3溶液中测得n0为0.254。
b6e)h2o2浓度测量:通过根据所报道的文献的传统硫酸铈ce(so4)2滴定法来测量h2o2浓度。通过h2o2使ce4+的黄色溶液被还原为无色ce3+。基于该颜色变化,可以通过紫外-可见光(uv-vis)来测量反应前后的ce4+浓度。用于测量的波长为316nm。根据以下反应:
2ce4++h2o2→2ce3++2h++o2
通过下式确定h2o2浓度(n):
n=2×nce4+
其中,nce4+是经还原的ce4+摩尔数。
过程如下:制备1mmce(so4)2溶液。将33.2mgce(so4)2溶解于100ml0.5m硫酸溶液中,以形成黄色透明溶液。为了获得校准曲线,将已知浓度的h2o2加入ce(so4)2溶液中并通过紫外-可见光测量。基于信号强度与h2o2浓度(0.2~1.2mm)之间的线性关系,可以获得样品的h2o2浓度。使用市售的过氧化氢测试条(购自西格玛-奥德里奇公司)也能确定h2o2的浓度。
b6f)水消毒:将细菌(大肠杆菌)(e.coli)(jm109,普洛麦格(promega)公司和atcck-12)培养至对数期,通过900g离心来收集,用去离子水(di)洗涤两次并悬浮于去离子水中至约106c.f.u.ml–1(每毫升菌落形成单位)。使用标准涂板技术在不同的照射时间测量细菌浓度。将各样品连续稀释并将各稀释物一式三份铺在胰蛋白胨大豆琼脂上并在37℃孵育18小时。
b7)补充附图说明
图6显示了n-和o-掺杂的碳微片的横截面sem图像,显示微片的多孔结构。
图7显示n-和o-掺杂的碳催化剂的xrd分析。
图8显示在n-和o-掺杂的碳上的xps测量谱。该测量谱中列出了相应的组成,表明在样品中并未发现金属信号。样品中所含的si信号源自我们用于制备n-和o-掺杂碳的石英管。
图9显示用于orr的n-和o-掺杂的碳催化剂的稳定性测试结果。将2.0mg的n-和o-掺杂的碳催化剂加载在1cm2碳纤维纸上。电流密度为4macm-2。
图10a-c显示具有不同n/c比值的n-和o-掺杂的碳催化剂的n1s的高分辨率xps。
图11a显示由通过引入三聚氰胺作为前体获得的n-和o-掺杂的碳催化剂的n1s的高分辨率xps。图11b显示具有不同氮含量的n-掺杂催化剂的rrde伏安图测量值。n/c=0.087的n-和o-掺杂的碳催化剂通过引入三聚氰胺作为氮前体来制备。图11c显示在具有不同氮含量的n-和o-掺杂的碳催化剂上以氧还原反应产生h2o2的对应选择性。
- 还没有人留言评论。精彩留言会获得点赞!