一种木质素基固体酸催化苄基化反应方法与流程
本发明涉及一种木质素基固体酸催化苯环化合物friedel-crafts苄基化反应的方法。具体地说是采用木质素磺酸钠碳化并磺化得到的强
背景技术:
芳香族化合物苄基化是有机化学中的重要反应之一,生成的二芳基甲烷及其衍生物是关键的医药中间体或精细化学品(ioveli,mertinsk,kischelj,etal.angewandtechemieinternationaledition,2005,44(25):3913-3917.;bandinim,mellonia,umani-ronchia.angewandtechemieinternationaledition,2004,43(5):550-556.;liuzt,sunz,liuzw,etal.j.appl.polym.sci.,2008,107(3):1872-1878.)。芳香族化合物苄基化通常使用苄基氯作为试剂,以及使用均相酸如alcl3或h2so4作为催化剂,存在原子经济性差、污染、腐蚀和催化剂分离回收困难等问题(clarkjh,cullensr,barlowsj,etal.catal.commun.,2007,8(1):49-56.)。苯甲醇作为苄基化试剂可实现苄基化反应的绿色化工艺,但苯甲醇的活性较低,当催化剂酸性较弱时难以发生苄基化反应,或者反应停留在其自身脱水生成二苄醚的阶段(deshpandea,bajpaia,samants.appl.catal.a:gen.,2001,209(1-2):229-235.),且反应副产的水限制了alcl3等许多对水敏感的强酸性催化剂的使用。沸石分子筛、杂多酸和一些负载型固体酸催化剂存在制备重现性差,在水存在下活性组分易流失或失活的倾向,常见离子液体类催化剂也存在着催化活性和耐水性难以兼顾的问题(liq,jiangs,jis,etal.journalofporousmaterials,2015,22(5):1205-1214.)。
随着对绿色可持续发展理念的不断追求,木质素作为唯一含芳环的生物质可再生资源受到广泛关注。但由于其复杂的结构,现仅有不到5%的木质素资源被用于下游工业生产,大部分被废弃,因此实现木质素的高效综合利用是目前该领域的难题。木质素是酚单元组成的富碳复合网络,在热解处理后具有较高碳产率(thakur,v.k.;thakur,m.k.;raghavan,p.;kessler,m.r.acssustainablechemistry&engineering,2014,2(5):1072-1092.),其中芳香环网络倾向于形成类石墨结构,而线性分支则作为含有各种烃类的小分子而失去(tenhaeff,w.e.;rios,o.;more,k.;mcguire,m.a.adv.funct.mater.,2014,24(1):86-94.),并且木质素结构中丰富的含氧官能团及制浆过程中引入的硫元素等在催化过程中可提供有效位点,为其作为催化剂基质提供了丰富的可行性,引入的含氧官能团不仅可以协同主要的活性中心(tang,h.;li,n.;li,g.;wang,w.;wang,a.acssustainablechemistry&engineering,2018,6(4):5645-5652.),提高其催化活性,还能同时赋予催化剂对水的兼容性。
综上所述,若能采用木质素资源作为原料,经改性制备出高效催化苯环化合物与苯甲醇苄基化反应的催化剂,从而开发出二苯基甲烷及其衍生物的环境友好制备新方法,将为木质素资源的高附加值利用以及精细有机合成的绿色化工艺开发提供新途径。迄今为止,采用木质素基固体酸催化苄基化反应的方法尚未见国内外文献报道。
技术实现要素:
本发明提供了一种利用造纸工业副产木质素磺酸钠为原料,经碳化及磺化处理制备强
本发明的目的是有效利用造纸工业副产木质素磺酸钠,开发低成本生物质基催化剂,同时解决苄基化反应现有技术中,催化剂的活性、耐水性、重复使用性和环境友好性难以兼顾的问题,从而提供一种利用木质素自身结构特征引入强酸性,高效催化苯甲醇路线苄基化反应的环境友好新方法。
本发明的技术方案为:
按n苯环化合物:n苯甲醇=1.7-13.5的投料比取苯环化合物和苯甲醇于反应器中,再按2.5ml苯甲醇/g催化剂的用量投入催化剂,在回流温度(氯苯、甲苯或苯)或150℃(邻二甲苯、间二甲苯、对二甲苯、均三甲苯、硝基苯或苯甲醚)下搅拌反应0.15-3h后冷却、离心,分别回收位于下层的吸附水的催化剂相和上层有机相,催化剂经烘干除水后,即可用于循环使用。
上述技术方案中的所述催化剂为具有强
在5℃·min-1升温速率,80ml·min-1流速的n2气氛下,将干燥的木质素磺酸钠置于管式炉中400℃碳化1h,冷却至室温得到木质素碳;将木质素碳和浓硫酸按10ml浓硫酸/g木质素碳的比例,n2气氛下150℃搅拌反应10h后,加入80℃以上热水过滤,滤饼用80℃以上热水洗涤至中性,真空干燥。
本发明提供的强
(1)以造纸行业亚硫酸盐制浆工艺产生的废弃生物质衍生化产品木质素磺酸盐为前体,经碳化及磺化处理获得具有强
(2)对木质素基碳的磺化处理可提高磺酸基含量并通过π-π共轭大大提高酸强度,有利于催化活性和选择性的提高,有效抑制副产物二苄醚的生成;
(3)磺化后获得的较多磺酸基、羧基和羟基基团使木质素基固体酸催化剂具有较好的亲水和耐水性,反应中产生的水易被催化剂吸附,便于与产物的分离。
附图说明
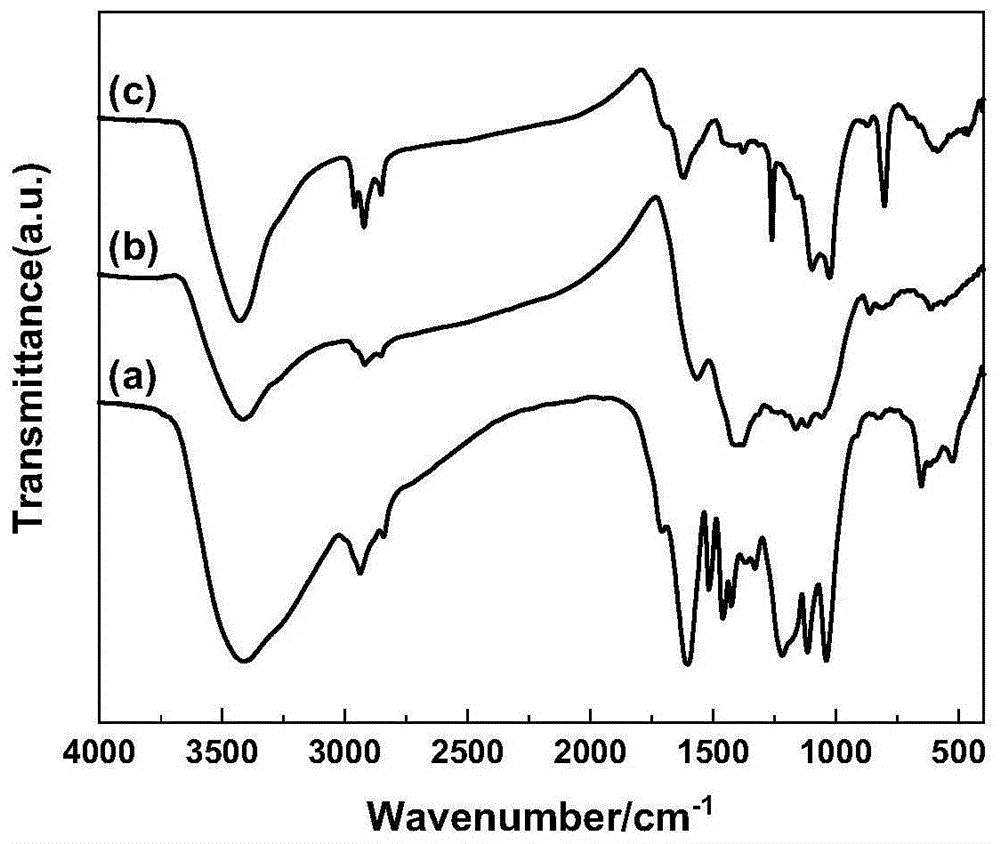
附图1为实施例1制备的强
附图2为实施例1制备的强
附图3为实施例2中强
具体实施方式
下面结合具体实施例进一步说明本发明,但不因此而限制本发明。
实施例1强
在5℃·min-1升温速率,80ml·min-1流速的n2气氛下,将干燥后的木质素磺酸钠(sls)置于管式炉中400℃碳化1h,冷却至室温,得到木质素碳slc400,1;按10ml浓硫酸/g木质素碳的比例取木质素碳slc400,1和浓硫酸于三口烧瓶中,n2气氛下400r·min-1机械搅拌,150℃反应10h后,加入50ml80℃以上热水过滤,并用80℃以上热水洗涤至中性,放入真空干燥箱50℃干燥4h,得到强
附图1所示的ft-ir(kbr,v/cm-1)谱图中,sls在3405cm-1处观察到的宽带归属为通过氢键与邻近的氧或磺酸相连的-oh基团;2939cm-1和2839cm-1属sls中-ch2-的伸缩振动;1715cm-1指示为c=o基团;1216cm-1和1036cm-1分别是o=s=o的对称伸缩振动和so3-的伸缩振动,证明sls中磺酸基的存在;1611cm-1、1513cm-1和1423cm-1为sls的苯环特征峰,1330cm-1归属于木质素中重要的c-o键的伸缩振动,低于1000cm-1的谱带归属为芳族c-h键的面内和面外振动;而slc400,1谱线中c=o、c-o等含氧基团红外振动峰均减弱,且o=s=o的对称伸缩振动和so3-的伸缩振动同样减弱,表明碳化会使sls上含氧基团分解;进一步磺化得到的木质素基固体酸a谱线1715cm-1处c=o基团的峰重新增强,1260cm-1和1021cm-1o=s=o的对称伸缩振动和so3-的伸缩振动峰同样加强,证明磺酸基被成功引入,且羧基等含氧基团含量也有所提高。
附图2所示的tg-dsc谱图中,强
实施例2
按照n苯环化合物:n苯甲醇=10的投料比取对二甲苯和苯甲醇于反应烧瓶中,再按2.5ml苯甲醇/g催化剂的用量投入实施例1中制备的强
附图3所示的是实施例2催化反应后和离心后的体系宏观状态图,催化剂a可在反应后通过离心有效分离。
实施例3
按照n苯环化合物:n苯甲醇=10的投料比取对二甲苯和苯甲醇于反应烧瓶中,再按2.5ml苯甲醇/g催化剂的用量投入实施例1中制备的强
实施例4
按照n苯环化合物:n苯甲醇=10的投料比取对二甲苯和苯甲醇于反应烧瓶中,再按2.5ml苯甲醇/g催化剂的用量投入实施例1中制备的强
实施例5
按照n苯环化合物:n苯甲醇=10的投料比取对二甲苯和苯甲醇于反应烧瓶中,再按2.5ml苯甲醇/g催化剂的用量投入实施例1中制备的强
实施例6
按照n苯环化合物:n苯甲醇=1.7的投料比取对二甲苯和苯甲醇于反应烧瓶中,再按2.5ml苯甲醇/g催化剂的用量投入实施例1中制备的强
实施例7
按照n苯环化合物:n苯甲醇=13.5的投料比取对二甲苯和苯甲醇于反应烧瓶中,再按2.5ml苯甲醇/g催化剂的用量投入实施例1中制备的强
实施例8
按照n苯环化合物:n苯甲醇=10的投料比取邻二甲苯和苯甲醇于反应烧瓶中,再按2.5ml苯甲醇/g催化剂的用量投入实施例1中制备的强
实施例9
按照n苯环化合物:n苯甲醇=10的投料比取间二甲苯和苯甲醇于反应烧瓶中,再按2.5ml苯甲醇/g催化剂的用量投入实施例1中制备的强
实施例10
按照n苯环化合物:n苯甲醇=10的投料比取均三甲苯和苯甲醇于反应烧瓶中,再按2.5ml苯甲醇/g催化剂的用量投入实施例1中制备的强
实施例11
按照n苯环化合物:n苯甲醇=10的投料比取苯和苯甲醇于反应烧瓶中,再按2.5ml苯甲醇/g催化剂的用量投入实施例1中制备的强
实施例12
按照n苯环化合物:n苯甲醇=10的投料比取甲苯和苯甲醇于反应烧瓶中,再按2.5ml苯甲醇/g催化剂的用量投入实施例1中制备的强
实施例13
按照n苯环化合物:n苯甲醇=10的投料比取氯苯和苯甲醇于反应烧瓶中,再按2.5ml苯甲醇/g催化剂的用量投入实施例1中制备的强
实施例14
按照n苯环化合物:n苯甲醇=10的投料比取硝基苯和苯甲醇于反应烧瓶中,再按2.5ml苯甲醇/g催化剂的用量投入实施例1中制备的强
实施例15
按照n苯环化合物:n苯甲醇=10的投料比取苯甲醚和苯甲醇于反应烧瓶中,再按2.5ml苯甲醇/g催化剂的用量投入实施例1中制备的强
表1强
实施例16-27
将实施例2中反应后的体系离心分离除去上层有机相,回收下层催化剂相,并置于烘箱中105℃烘干。将干燥后的回收催化剂、苯甲醚和苯甲醇按实施例2的投料比置于反应烧瓶中,于150℃磁力搅拌反应2h,反应结束后冷却离心,取上层有机相进行气相色谱分析,下层催化剂相重复上述操作,循环使用12次,所得催化结果见表2。
表2强
对比例1
按10ml浓硫酸/gsls的比例取干燥后的木质素磺酸钠(sls)和浓硫酸于三口烧瓶中,n2气氛下400r·min-1机械搅拌,150℃反应10h后,加入50ml80℃以上热水过滤,并用80℃以上热水洗涤至中性,放入真空干燥箱50℃干燥4h,得到木质素基固体酸slss150,10。
按照n苯环化合物:n苯甲醇=10的投料比取对二甲苯和苯甲醇于反应烧瓶中,再按2.5ml苯甲醇/g催化剂的用量投入上述中制备的木质素基固体酸slss150,10,于150℃磁力搅拌反应2h,反应结束后冷却离心,取上层有机相进行气相色谱分析,催化结果见表3。
对比例2
在5℃·min-1升温速率,80ml·min-1流速的n2气氛下,将干燥后的木质素磺酸钠(sls)置于管式炉中600℃碳化1h,冷却至室温,得到木质素碳slc600,1;按10ml浓硫酸/g木质素碳的比例取木质素碳slc600,1和浓硫酸于三口烧瓶中,n2气氛下400r·min-1机械搅拌,150℃反应10h后,加入50ml80℃以上热水过滤,并用80℃以上热水洗涤至中性,放入真空干燥箱50℃干燥4h,得到木质素基固体酸slc600,1s。
按照n苯环化合物:n苯甲醇=10的投料比取对二甲苯和苯甲醇于反应烧瓶中,再按2.5ml苯甲醇/g催化剂的用量投入上述中制备的木质素基固体酸slc600,1s,于150℃磁力搅拌反应2h,反应结束后冷却离心,取上层有机相进行气相色谱分析,催化结果见表3。
表3对比催化剂催化对二甲苯与苯甲醇苄基化反应结果
- 还没有人留言评论。精彩留言会获得点赞!