一种离子液体辅助的制备Pt/TiO2催化剂的新方法及用途与流程
本发明属于材料领域,涉及一种离子液体辅助的制备pt/tio2催化剂的新方法及用途。
背景技术:
二氧化钛是一种众所周知的光催化剂,可应用于不同的化学反应,如有机物降解、产氢、氮氧化物分解、醇氧化和二氧化碳还原等。然而,二氧化钛的价带宽、光生电子-空穴对复合速率相对高,使其光催化活性受限。将贵金属与二氧化钛复合,是一种提高二氧化钛光生电子-空穴分离效率和光利用能力的有效途径。贵金属和二氧化钛的复合材料通常由两步法制得:首先制得二氧化钛,随后通过光沉积或溅射等方法将贵金属与二氧化钛结合,该方法步骤复杂。另一种提高二氧化钛光催化性能的有效途径是杂原子的掺杂。例如,vaiano等人报道了使用氟化氢作为氟源,在pt/tio2催化剂中加入氟可以提高光催化产氢速率。因此,发展一种温和的、低能耗的、环境友好的方法合成具有特定组成和结构的贵金属和二氧化钛的复合材料以达到同时简化合成方法和提高光催化性能的目的,具有重要的意义。
离子液体是一类在室温下或接近室温下呈液体状态的熔融盐,由特定的有机阳离子和无机阴离子组成。相对于传统溶剂(水或有机溶剂),离子液体具有诸多特性:结构可设计性、不挥发性、良好的热稳定性、宽的液态范围和对化合物良好的溶解性等。
技术实现要素:
本发明的目的是提供一种离子液体辅助的制备pt/tio2催化剂的新方法及用途。
本发明要求保护离子液体在制备pt/tio2催化剂中的应用。
本发明提供的制备pt/tio2催化剂的方法,包括:将钛源和含铂化合物于由离子液体和水组成的混合物中进行水解还原反应,反应完毕得到所述pt/tio2催化剂。
上述方法中,所述钛源为钛酸四丁酯、异丙醇钛或四氯化钛;
所述含铂化合物为氯铂酸、氯铂酸铵、氯铂酸钾或氯铂酸钠。
所述离子液体为式i所示1-乙基-3-甲基咪唑类离子液体;具体选自1-乙基-3-甲基咪唑四氟硼酸盐(emimbf4)、1-乙基-3-甲基咪唑氯盐(emimcl)和1-乙基-3-甲基咪唑溴盐(emimbr)中至少一种;
所述式i中,x为bf4、cl或br。
所述由离子液体和水组成的混合物中,离子液体和水的质量比为1:9-0.1;具体为1:1。
所述水解还原反应步骤中,温度为50-200℃;具体为150℃;时间为8-24h;具体为12h。
上述方法中,离子液体担任多重角色:溶解前驱体的溶剂,形成金属pt的还原剂,杂原子的掺杂剂。
另外,按照上述方法制备得到的pt/tio2催化剂及该pt/tio2催化剂在光催化中的应用,也属于本发明的保护范围。
具体的,所述光催化为光催化水产氢。
所述光催化水产氢中,所述pt/tio2催化剂与水的用量比为10mg:1-10ml;具体为10mg:9ml;
所述光催化水产氢在惰性气氛和牺牲剂存在的条件下进行;
所述惰性气氛具体为氮气气氛;
所述牺牲剂具体为三乙醇胺;
所述pt/tio2催化剂与牺牲剂的用量比为10mg:1-10ml;
温度为15-35℃;具体为25℃;
所用光源的功率为150-500w;具体为300w;
所用光源为氙灯;
光照时间为4-12h。
本发明首次提出利用离子液体一步法合成杂原子掺杂的pt/tio2纳米晶体。其中,离子液体不仅作为溶解反应物的溶剂,而且作为形成pt的还原剂,不需要加入额外的还原剂。此外,离子液体还作为pt/tio2催化剂的杂原子掺杂源。由于离子液体的组成和结构具有可设计性,所以可以简单、方便地调控杂原子掺杂。本发明提供的pt/tio2催化剂,具有晶体尺寸小、表面杂原子掺杂、氧空缺丰富、光吸收能力强等优势,对模拟太阳光下光催化水产氢反应具有高催化活性和高稳定性。
附图说明
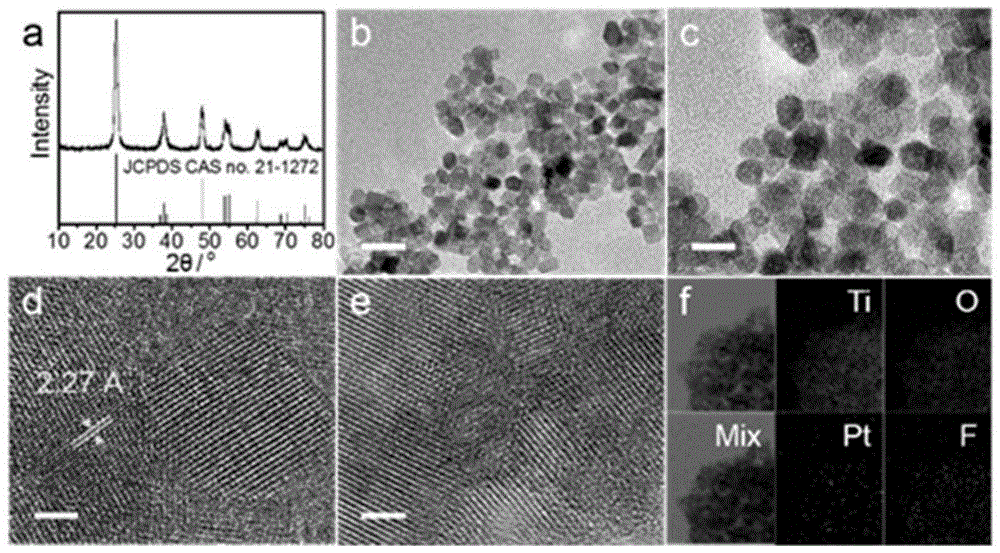
图1为emimbf4辅助合成的pt/tio2材料的x射线衍射图(a)、透射电子显微镜图(b,c)、高分辨透射电子显微镜图(d,e)、能量色散x射线元素mapping图(f)。标尺:(b)25nm、(c)15nm、(d,e)2.5nm。
图2为f-pt/tio2材料的x射线光电子能谱图:ti2p(a)、pt4f(b)、o1s(c)、f1s(d)。
图3中a.f-pt/tio2(i)、p25(ii)和emimbf4(iii)的傅里叶变换红外光谱图。b.f-pt/tio2(i)和p25(ii)的接触角。
图4为f-pt/tio2(i)和p25(ii)的紫外-可见漫反射光谱图(a)和光致发光光谱图(b)。
图5为emimcl辅助合成的pt/tio2材料的x射线衍射图。
图6为emimcl辅助合成的pt/tio2材料的透射电子显微镜图。标尺:50nm。
图7为cl-pt/tio2材料的x射线光电子能谱图:ti2p(a)、o1s(b)、cl2p(c)。
图8为emimbr辅助合成的pt/tio2材料的x射线衍射图。
图9为emimbr辅助合成的pt/tio2材料的透射电子显微镜图。标尺:50nm。
图10为br-pt/tio2材料的x射线光电子能谱图:ti2p(a)、o1s(b)、br3d(c)。
图11中a.f-pt/tio2(红色)和p25(黑色)催化时产氢总量随时间的变化。b.f-pt/tio2(红色)和p25(黑色)催化时产氢tof值随反应时间的变化。c.f-pt/tio2光催化产氢12h后回收样的x射线衍射图。d.f-pt/tio2光催化产氢12h后回收样的透射电子显微镜照片,标尺为50nm。
具体实施方式
下面结合具体实施例对本发明作进一步阐述,但本发明并不限于以下实施例。所述方法如无特别说明均为常规方法。所述原材料如无特别说明均能从公开商业途径获得。
实施例1
本实施例的pt/tio2的合成方法如下:
合成pt/tio2采用的离子液体为1-乙基-3-甲基咪唑四氟硼酸盐(emimbf4),如式(ii)所示。
将6.25mg六水合氯铂酸(h2ptcl6·6h2o)溶于1.25g1-乙基-3-甲基咪唑四氟硼酸盐与1.25g去离子水的混合物中,边剧烈搅拌边逐滴加入1ml钛酸四丁酯,将上述混合物转移入15ml高压釜中,150℃搅拌反应12h。反应结束后待反应釜自然冷却至室温,将反应悬浊液离心分离得到固体,用去离子水充分洗涤所得固体5次,80℃真空干燥过夜得到最终产物。
将所得产物分别进行x射线衍射、透射电子显微镜、高分辨透射电子显微镜和能量色散x射线元素mapping表征,结果如图1所示。x射线衍射图(图1a)表明,所得产物为锐钛矿相tio2(jcpdscardno.21-1272)。x射线衍射图无pt的结晶峰,可能是由于复合材料中pt的含量较低(电感耦合等离子体原子发射光谱法测得pt的含量为0.54wt%)。透射电子显微镜图(图1b,c)表明,制备得到的纳米晶体的平均尺寸为10nm。高分辨透射电子显微镜图(图1d,e)表明,
将所得f-pt/tio2材料进行x射线光电子能谱表征,结果如图2所示。ti2p图谱(图2a)中,位于458.9ev和464.6ev的两峰分别归属于ti2p3/2和ti2p1/2,表明ti元素的氧化态与tio2一致。pt4f图(图2b)中,70.5ev和73.7ev处的两峰分别对应pt4f7/2和pt4f5/2,说明pt以零价形式存在。然而,与传统的零价pt相比,该pt4f的峰向低结合能方向移动了至少0.3ev,这可能源于pt和tio2载体之间形成了强的金属-载体相互作用。约在76.0ev处的额外峰来源于x射线光电子能谱制样时使用的铝箔纸的alntvox峰。o1s图谱(图2c)中,529.7ev处的主峰归属于晶格氧(ti-o)。而531.4ev处的肩峰归属于非晶格氧(ti-oh),说明存在氧空缺。f1s图谱(图2d)计算得到f的含量为4.0at%,684.4ev处的主峰归属于表面吸附的f,而689.9ev处小峰归属于f原子掺入tio2晶格形成的微量的o-ti-f键。由此说明,以离子液体1-乙基-3-甲基咪唑四氟硼酸盐作为f源,可简单、环境友好地制得f掺杂的pt/tio2。
对比商用tio2(p25),将所得f-pt/tio2材料进行傅里叶变换红外光谱和润湿性表征,结果如图3所示。傅里叶变换红外光谱图(图3a)中,f-pt/tio2中无emimbf4中b-f键或咪唑环的特征峰,说明f-pt/tio2中无[bf4]-或[emim]+,f元素作为杂原子掺杂存在。400~850cm-1范围内的宽峰归属于tio2的ti-o伸缩振动和ti-o-ti桥连伸缩振动。与p25相比(665cm-1),f-pt/tio2的峰(658cm-1)向低波数移动且明显宽化,源于杂原子的掺杂和氧空缺的形成。与p25相比,f-pt/tio2在902cm-1处的新峰归属于ti-f伸缩振动。再者,与p25相比(1628cm-1),f-pt/tio2中ti-oh和物理吸附的水中羟基弯曲振动峰(1634cm-1)向高波数移动并锐化。与此同时,与p25相比(3435cm-1),f-pt/tio2中ti-oh和物理吸附的水中羟基伸缩振动峰(3420cm-1)向低波数移动并宽化。这些结果表明,与p25相比,f-pt/tio2中物理吸附的水分子和tio2表面的羟基之间存在更强的氢键作用。p25和f-pt/tio2的浸润性由其对水的静态接触角监测,结果如图3b所示。f-pt/tio2展现出超亲水性,接触角为0o,远小于p25的接触角(15o),与傅里叶变换红外光谱揭示其表面富含羟基的结果一致。
对比商用tio2(p25),将所得f-pt/tio2材料进行紫外-可见漫反射光谱和光致发光光谱表征,结果如图4所示。紫外-可见漫反射光谱图(图4a)中,f-pt/tio2的吸收峰(312nm)与p25相比(280nm),其明显的红移源于f对tio2的掺杂。此外,f-pt/tio2在可见光区有一个宽的吸收,这源于pt的等离子激元效应。f-pt/tio2在可见光区的吸光能力显著增强,有益于光催化性能。光致发光光谱图(图4b)中,f-pt/tio2的强度与p25相比显著减弱,表示其光生电子和空穴的复合效率显著降低。这说明f-pt/tio2的光生电荷的分离能力增强,有益于光催化。
实施例2
本实施例的pt/tio2的合成方法如下:
合成pt/tio2采用的离子液体为1-乙基-3-甲基咪唑氯盐(emimcl),如式(iii)所示。
将6.25mg六水合氯铂酸(h2ptcl6·6h2o)溶于1.25g1-乙基-3-甲基咪唑氯盐与1.25g去离子水的混合物中,边剧烈搅拌边逐滴加入1ml钛酸四丁酯,将上述混合物转移入15ml高压釜中,150℃搅拌反应12h。反应结束后待反应釜自然冷却至室温,将反应悬浊液离心分离得到固体,用去离子水充分洗涤所得固体5次,80℃真空干燥过夜得到最终产物。
将所得产物进行x射线衍射表征,结果如图5所示,所得产物为锐钛矿相tio2(jcpdscardno.21-1272)。
将所得产物进行透射电子显微镜表征,结果如图6所示,制备得到的纳米晶体的平均尺寸为6nm。
将所得产物进行x射线光电子能谱表征,结果如图7所示。ti2p和o1s图谱与实施例1相似(图7a,b)。cl2p图谱(图7c)中,199.7ev和198.1ev处的两峰分别对应cl2p1/2和cl2p3/2,说明催化剂表面吸附了cl。因此,将所得产物表示为cl-pt/tio2。
实施例3
本实施例的pt/tio2的合成方法如下:
合成pt/tio2采用的离子液体为1-乙基-3-甲基咪唑溴盐(emimbr),如式(iv)所示。
将6.25mg六水合氯铂酸(h2ptcl6·6h2o)溶于1.25g1-乙基-3-甲基咪唑溴盐与1.25g去离子水的混合物中,边剧烈搅拌边逐滴加入1ml钛酸四丁酯,将上述混合物转移入15ml高压釜中,150℃搅拌反应12h。反应结束后待反应釜自然冷却至室温,将反应悬浊液离心分离得到固体,用去离子水充分洗涤所得固体5次,80℃真空干燥过夜得到最终产物。
将所得产物进行x射线衍射表征,结果如图8所示,所得产物为锐钛矿相tio2(jcpdscardno.21-1272)。
将所得产物进行透射电子显微镜表征,结果如图9所示,制备得到的纳米晶体的平均尺寸为6nm。
将所得产物进行x射线光电子能谱表征,结果如图10所示。ti2p和o1s图谱与实施例1相似(图10a,b)。br3p图谱(图10c)中,68.7和67.9ev处的两峰分别对应br3d3/2和br3d5/2,说明催化剂表面吸附了br。因此,将所得产物表示为br-pt/tio2。
实施例4
对比商用tio2(p25),实施例1~3中由不同离子液体辅助合成的pt/tio2材料作为光催化剂,在水和三乙醇胺体系中,研究pt/tio2催化剂在模拟太阳光条件下的光催化水产氢活性。
具体实施步骤为:
将实施例1~3制备得到的pt/tio2催化剂用于模拟太阳光条件下光催化水产氢反应。将10mgpt/tio2催化剂加入到含有9ml水和1ml三乙醇胺的100ml单口瓶中,剧烈搅拌5min使之均匀分散,随后边搅拌边通入高纯氮气30min以除去反应器中的空气。之后将反应器置于25℃的恒温水浴锅中,用300w氙灯模拟太阳光辐照4~12h,采用气相色谱法对产生的氢气进行分析。对比实验中将pt/tio2催化剂换成商用tio2(p25),其他条件不变。
f-pt/tio2和p25为催化剂时,产生的h2随时间的变化如图11a所示。显然,f-pt/tio2的产氢速率明显高于p25。当反应12h时,f-pt/tio2的产氢总量高达1130μmol,而相同实验条件下p25只有160μmol。f-pt/tio2和p25的转化频率(tof)数值如图11b所示,f-pt/tio2的tof值高达9.26mmolg-1h-1。而且f-pt/tio2的tof值不随反应时间的延长而衰减,说明其在光催化过程中能长时间保持稳定。当反应时间延长至12h,f-pt/tio2仍然保持其原有结晶性和形貌(图11c,d)。
此外,相同条件下cl-pt/tio2和br-pt/tio2应用于光催化水产氢的tof值分别为5.14和8.10mmolg-1h-1。
上述内容仅为对本发明所作的举例说明。本发明所述技术领域的技术人员可以对所描述的实施例进行修改、补充或替换,如果不偏离本发明的构思范围,均应视为属于本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!