N-rGO-Au-Pd@Au纳米催化剂及制备方法以及大黄酚的电化学检测方法与流程
本发明涉及中药检测的技术领域,特别涉n-rgo-au-pd@au纳米催化剂及制备方法以及大黄酚的电化学检测方法。
背景技术:
大黄为蓼科植物掌叶大黄、唐古特大黄或药用大黄的干燥根及根茎,味苦、性寒,具有清热泻下、抗菌、行淤化积、消炎止血、抗肿瘤等多方面的功效。具有清热解毒、泻下等功效。其所含成分为总蒽醌衍生物,如大黄酸、芦荟大黄素、大黄酚和大黄素甲醚,其中大黄酚是产生药理作用主要有效成分。因此测定大黄药材中大黄酚的含量对大黄药材在制药领域的应用尤为重要。目前,主要采用气相色谱质谱法、高效液相色谱法、毛细管电泳分析法对大黄酚进行检测,但是这些方法涉及到的仪器昂贵、样品前处理方法复杂、仪器使用复杂等。目前,电化学分析法由于其具有设备简单、操作简单、成本低廉、分析速度快、灵敏度高等优点已经广泛应用到样品的检测领域。据查阅相关资料显示,目前采用电化学方法对大黄药材中大黄酚含量进行检测没有报道。
技术实现要素:
本发明的目的在于提供n-rgo-au-pd@au纳米催化剂及制备方法以及大黄酚的检测方法,解决上述现有技术问题中的一个或者多个。
一方面,本发明提供n-rgo-au-pd@au纳米催化剂的制备方法,包括以下步骤:
n-rgo-au-pd@au纳米催化剂的制备方法,其特征在于,包括以下步骤:
将haucl4、k2pdcl4以及氧化石墨烯加入黄嘌呤的碱溶液,之后加入抗坏血酸,加热至50至70℃,并保温30至90min;
滴加水合肼,继续保温30至90min;
清洗、分离,得到所述n-rgo-au-pd@au纳米催化剂。
在一些实施方式中,haucl4与k2pdcl4的摩尔比为0.5至2,
在一些实施方式中,haucl4与氧化石墨烯的摩尔比为0.5至2。
在一些实施方式中,黄嘌呤的碱溶液通过以下步骤制备而成:
将黄嘌呤溶于naoh溶液中,得到所述黄嘌呤的碱溶液。
在一些实施方式中,黄嘌呤与所述naoh溶液的固液比为0.5至2mg/μl。
在一些实施方式中,naoh溶液的浓度为0.5至2mol/l。
在一些实施方式中,加热前还包括超声步骤。
在一些实施方式中,超声功率为100至200w。
在一些实施方式中,超声时间为30至90min。
在一些实施方式中,抗坏血酸与所述haucl4的摩尔比为0.5至2。
在一些实施方式中,水合肼的浓度为16.7mol/l。
另一方面,本发明提供一种n-rgo-au-pd@au纳米催化剂,其通过上述制备方法制备而成。
另一方面,本发明提供一种电化学传感器,其包括上述n-rgo-au-pd@au纳米催化剂修饰的玻碳电极。
在一些实施方式中,n-rgo-au-pd@au纳米催化剂的用量为1至11μl。
在一些实施方式中,n-rgo-au-pd@au纳米催化剂的用量为7μl。
另一方面,本发明提供大黄酚的电化学检测方法,包括以下步骤:
将含有大黄药材粉碎,得到药材粉末;
将所述药材粉末溶于乙醇,并通过超声提取,得到药材提取液
通过上述电化学传感器对所述药材提取液进行检测。
在一些实施方式中,还包括使用乙醇稀释所述药材提取液的步骤。
在一些实施方式中,稀释所述药材提取液2至10倍。
在一些实施方式中,稀释所述药材提取液5倍。
在一些实施方式中,还包括加入乙酸缓冲溶液。
在一些实施方式中,乙酸缓冲溶液的ph至为2至5。
在一些实施方式中,乙酸缓冲溶液的ph为3.6。
在一些实施方式中,电极的富集时间为30s至300s。
在一些实施方式中,电极的富集时间为180s。
有益效果:
采用本发明的方法成功的制备了n-rgo-au-pd@au纳米催化剂,将制备的n-rgo-au-pd@au纳米催化剂用于构建电化学传感器检测大黄酚,结果表明n-rgo-au-pd@au纳米催化剂具有较好的电化学活性能够实现对大黄酚的检测,检测的线性范围为1.84-84.5μg·ml-1,检测限为0.58μgml-1,并且本发明提出的传感器能够成功的对大黄药材中的大黄酚进行检测。
附图说明
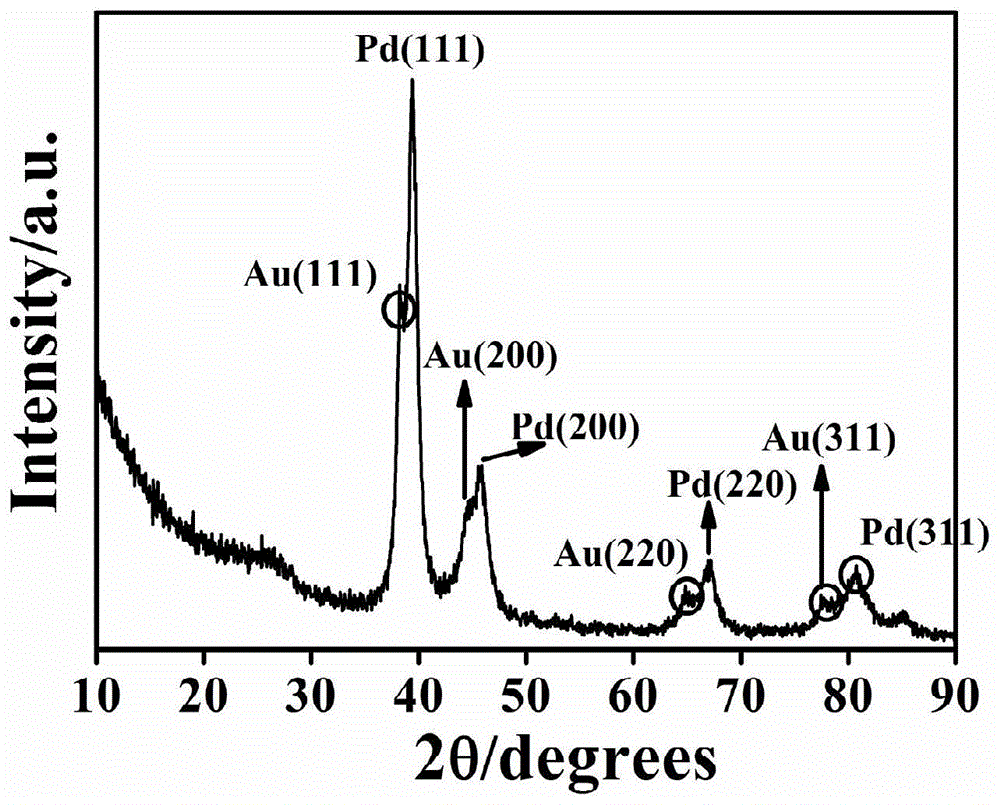
图1为实施例1制备的n-rgo-au-pd@au纳米催化剂的xrd图;
图2(a)和(b)为au-pd@au的tem图;(c)和(d)为不同放大倍数下n-rgo-au-pd@au的tem图;(e)和(f)为n-rgo-au-pd@au合金纳米催化剂的hrtem图;
图3为在7ml含有50.14μg/ml大黄酚的不同ph(3.0、3.6、4.0、4.6、5.0、5.6)的醋酸-醋酸钠缓冲液中的差分脉冲伏安图;
图4(a)为7μln-rgo-au-pd@au纳米催化剂修饰的玻碳电极在7ml含有50.14μg/ml大黄酚的ph为3.6的醋酸-醋酸钠缓冲液中,富集时间为3分钟,扫描速率分别为100、200、300、400、500、600、700、800、900、1000mv/s的循环伏安图;(b)为扫描速率的平方根与峰电流的关系曲线图;
图5(a)为n-rgo-au-pd@au纳米催化剂用量与峰电流的关系图;(b)为富集时间与峰电流的关系图;
图6(a)为n-rgo-au-pd@au/gce对大黄酚检测的差分脉冲伏安图;(b)为峰电流与浓度的关系曲线图。
具体实施方式
下面结合说明书附图,对本发明进行进一步详细的说明。
实施例1
制备n-rgo-au-pd@au纳米催化剂
取30mg黄嘌呤溶于300μl1mol/lnaoh中,转移到50ml三颈圆底烧瓶中,再加入20ml二次蒸馏水,取2mmhaucl4、2mmk2pdcl4和与haucl4相同量的氧化石墨烯连续加入到上述溶液,接着加入214μl1mol/l的抗坏血酸混合均匀,超声60min。然后将上述溶液水浴加热到60℃,反应40min后逐滴加入16.7mol/l水合肼,继续反应30至60min,得到的产物用乙醇、二次蒸馏水离心洗涤。
其中,原材料采购厂家列表如下:
对实施例1中的n-rgo-au-pd@au纳米催化剂进行tem、hrtem以及xrd。
其中,tem、hrtem采用日本jeol公司型号jem-2100的高分辨透射电镜;
xrd采用panalytical公司型号为x’pert3的粉末衍射仪。
表征结果如下:
如图1所示,2θ=26.1°为还原石墨烯(n-rgo)的衍射峰,说明氧化石墨烯已经被成功的还原为还原石墨烯。在2θ=38.19°、44.85°、65.1°、77.54°分别为au纳米粒子的(111)、(200),(220),(311)特征峰,在2θ=39.35°、45.79°、67.13°、80.86°分别为pd纳米粒子的(111)、(200),(220),(311)特征峰,并且相比于文献报道的纯的金纳米粒子和钯纳米粒子的特征吸收峰,n-rgo-au-pd@au纳米催化剂的吸收峰都较宽,这可能是由于金纳米粒子与钯纳米粒子之间的协同效应影响的,证明实施例1已经成功的制备了n-rgo-au-pd@au纳米催化剂。
如图2a和2b所示,au-pd@au合金纳米粒子是由多个很好分散的纳米枝组成的,整体尺寸约为25nm;
如图2c和2d所示,au-pd@au合金纳米枝均匀的分布在n-rgo纳米片表面,n-rgo纳米片呈一层透明的膜状结构;
如图2e和2f所示,au-pd@au合金纳米枝的分枝大约为直径4.8nm。制备的n-rgo-au-pd@au合金纳米催化剂具有很好的晶状结构,晶面晶距为0.23nm和0.19nm分别对应了au和pd纳米粒子的(111)和(200)晶面。
实施例2
先将玻碳电极(gce)用适量的a12o3粉末于麂皮上抛光成镜面,用蒸馏水将其冲洗干净,然后用氮气吹干。接着取7μl的n-rgo-au-pd@au纳米催化剂修饰玻碳电极,室温下晾干,保存备用。
实施例3
将实施例2制备的电化学传感器,在7ml含有50.14μg/ml大黄酚的不同ph(3.0、3.6、4.0、4.6、5.0、5.6)的醋酸-醋酸钠缓冲液中,开路电位富集时间为3分钟,采用差分脉冲伏安法分别考察ph对大黄酚检测的影响。
如图3所示,ph范围在3.0-5.6时,氧化峰电流随ph值的变化而变化;当ph为3.6时,氧化峰电流最大。因此,本发明选优ph=3.6的醋酸-醋酸钠缓冲溶液作为检测底液。
实施例4
将实施例2制备的电化学传感器,在7ml含有50.14μg/ml大黄酚的ph为3.6的醋酸-醋酸钠缓冲液中,开位电路富集3分钟,扫描速率分别为100、200、300、400、500、600、700、800、900、1000mv/s时的循环伏安图。
如图4所示,当扫描速率逐渐增加时,氧化峰电流和还原峰电流也随之增大。图4b为峰电流与扫描速率平方根的关系曲线图,从图中可以看出,n-rgo-au-pd@au纳米催化剂对大黄酚检测的氧化还原峰电流与扫描速率的平方根成正比,说明本实施例的电化学传感器是受扩散控制的。
实施例5
分别修饰1、3、5、7、9、11μl的n-rgo-au-pd@au纳米催化剂于玻碳电极表面,在7ml含有50.14μg/ml大黄酚的ph=3.6的醋酸-醋酸钠缓冲液中,采用差分脉冲伏安法考察n-rgo-au-pd@au纳米催化剂用量对大黄酚检测的影响。
如图5a所示,随着其用量的不断增加峰电流不断增大,当修饰7μln-rgo-au-pd@au纳米催化剂时峰电流最大,继续增加n-rgo-au-pd@au纳米催化剂的用量峰电流反而减小,故本发明最优的用量为7μl。
实施例6
将实施例2制备的电化学传感器,在7ml含有50.14μg/ml大黄酚的ph为3.6的醋酸-醋酸钠缓冲液中,采用差分脉冲伏安法分别研究富集0、60、120、180、240、300s对检测的影响,从而确定最佳富集时间。
如5b所示,随着富集时间的增加,氧化峰电流逐渐增大,当富集时间到达180s时,峰电流最大,之后便出现下降的趋势,本发明优选180s为最佳富集时间。
实施例7
将实施例2制备的电化学传感器,富集时间为3分钟,采用差分脉冲循环伏安法分别对不同浓度的大黄酚进行检测。
如图6a所示,随着大黄酚浓度的增加,峰电流依次增加;
从图6b所示出,该传感器对大黄酚检测的线性范围为1.84-84.5μgml-1,检测限为0.58μgml-1,线性方程为ipa=0.573c-0.525(r2=0.9987)。
采用标准加入法进行实际样品的分析,具体操作方法如下:采用差分脉冲伏安法测定大黄提取液中大黄酚的含量,然后加入一定量的大黄酚标准溶液,再次测定溶液中总的大黄酚的含量,按如下公式计算样品的回收率:回收率=(测得量-样品含量)/加入量,平行3次,分别计算回收率。
表1回收率实验
实验结果如表1所示,大黄药材中大黄酚的含量为5.18mgg-1,回收率在98.4-103.2%之间,表明本实施例构建的电化学传感器能够应用到大黄药材中大黄酚的检测。
采用本发明实施例的方法成功的制备了n-rgo-au-pd@au纳米催化剂,采用tem、hrtem和xrd表征制备的纳米材料,将制备的n-rgo-zno-au纳米材料用于构建电化学传感器检测大黄酚,结果表明n-rgo-zno-au具有较好的电化学活性能够实现对大黄酚的检测,检测的线性范围为1.84-84.5μg·ml-1,检测限为0.58μgml-1,并且本发明提出的传感器能够成功的对大黄药材中的大黄酚进行检测。
以上表述仅为本发明的优选方式,应当指出,对本领域的普通技术人员来说,在不脱离本发明创造构思的前提下,还可以做出若干变形和改进,这些也应视为本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!