具有自分离功能的高效净化剂及其制备方法和应用与流程
本发明涉及残留检测领域,具体涉及一种具有自分离功能的高效净化剂及其制备方法和应用。
背景技术:
随着农药的大规模使用和人们对美好生活的向往追求,农药残留问题越来越受到社会的广泛关注,世界各国制定了严格的最大残留限量法规。为了有效合理地管控农药残留量,相关的检测分析方法得到了快速发展,食品、农产品、环境样品中农药残留的检测一直是研究人员关注的焦点。在分析蔬菜、水果、肉类、粮食、茶叶、牛奶等复杂基体中农药残留时,样品前处理过程尤为重要。
传统的样品前处理方法主要有液液萃取、固相萃取、固相微萃取、基质固相分散萃取、分散液液萃取、分散固相萃取、凝胶渗透色谱等。美国农业部anastassiades教授等人借鉴这些方法的优势于2003年提出了一种快速、简便、廉价、有效、可靠、安全(quechers)方法,成为了国际上农药分析领域的标准样品制备方法之一。在quechers方法中,净化过程是一个关键步骤,而净化剂的选择和性能是最为重要的因素。传统的吸附材料有n-丙基乙二胺(psa)、c18功能化二氧化硅、石墨炭黑等。近年来,研究者们开发了新型二氧化锆、多壁碳纳米管、石墨烯等新型吸附材料。多壁碳纳米管作为一种新型纳米吸附材料,其比表面积大,具有典型的中空结构,增加了材料的附载能力,对色素、脂肪酸等杂质有较好的净化能力。
尽管如此,目前大部分前处理方法都离不开过柱子、过滤或离心操作,这需要额外的时间和操作,不利于大批量样品的高通量分析。开发更加快速、高效农药检测方法一直是研究人员的迫切需求。
技术实现要素:
本发明的目的是为了克服现有技术存在的不足,提供一种具有自分离功能的高效净化剂及其制备方法和应用。本发明提供的净化剂无需常规方法的过滤或离心操作,可自行与有机相分离,节省了额外的时间和操作,有利于样品的高通量分析,且本发明提供的净化剂具有较强的杂质净化能力。
为了实现上述目的,第一方面,本发明提供了一种净化剂ssbpcm,该净化剂包括吸附部分材料和分离剂,其中,所述吸附部分材料为羧基化吸附材料与胺类化合物的共价结合体;所述分离剂为不溶或难溶于有机溶剂的金属盐。
第二方面,本发明提供了一种净化剂ssbpcm的制备方法,该方法包括:
(1)将羧基化吸附材料与羧基活化试剂进行第一接触,以对所述羧基化吸附材料中的羧基进行活化;
(2)将步骤(1)得到的羧基活化的羧基化吸附材料与胺类化合物进行第二接触,使得羧基化吸附材料与胺类化合物形成共价结合体,得到吸附部分材料;
(3)将所述吸附部分材料与分离剂混合,得到所述净化剂;其中,所述分离剂为不溶或难溶于有机溶剂的金属盐。
第三方面,本发明提供了如上所述的方法制备的净化剂ssbpcm。
第四方面,本发明提供了如上所述的净化剂ssbpcm在作为分散固相萃取净化材料中的应用。
第五方面,本发明提供了如上所述的净化剂ssbpcm在残留检测中的应用。
与现有技术相比,本发明具有以下优点:
1、本发明提供的净化剂无需常规方法的过滤或离心操作,可自行与有机相分离,节省了额外的时间和操作,有利于样品的高通量分析。
2、本发明提供的净化剂保留并结合了传统吸附材料的有效吸附功能基团和优点,但杂质净化能力却强于传统吸附材料;
4、本发明提供的具有自分离功能的净化剂合成过程简单,成本低,易于大批量生产和使用。
本发明的其它特征和优点将在随后的具体实施方式部分予以详细说明。
附图说明
附图是用来提供对本发明的进一步理解,并且构成说明书的一部分,与下面的具体实施方式一起用于解释本发明,但并不构成对本发明的限制。在附图中:
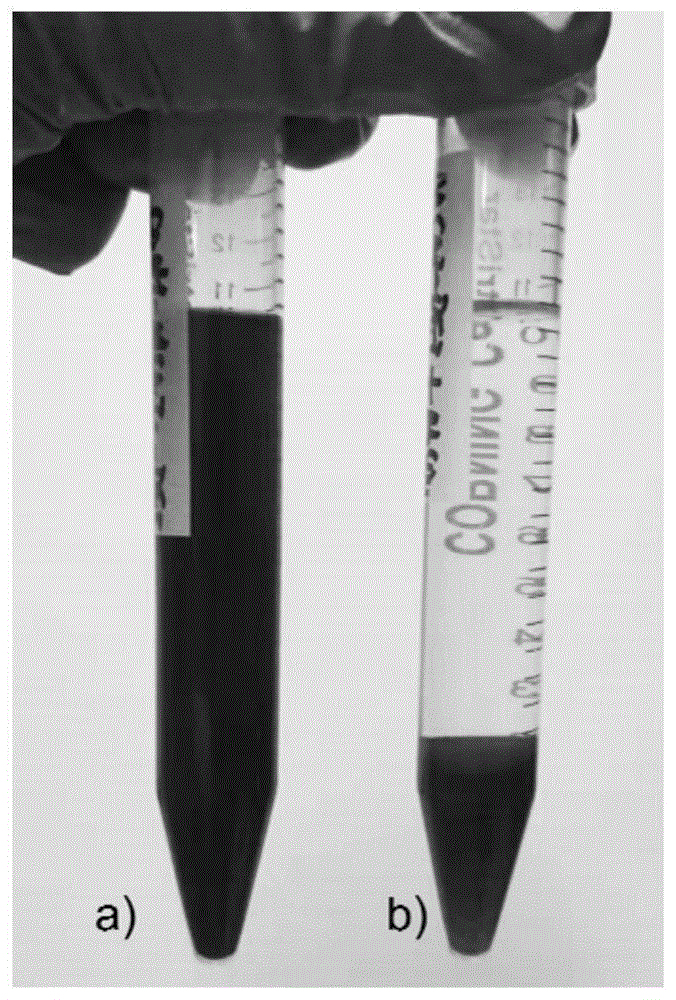
图1为制备例1制备的净化材料照片:a)bpcm,b)ssbpcm;
图2为本发明制备例1制备的bpcm和ssbpcm表征数据,a-c)扫描电镜图,d)元素分析,e)傅里叶红外光谱图;
图3为制备例2中选择不同类型分离剂对分离表现的影响;
图4为制备例3中本发明ssbpcm净化剂净化能力检验;
图5为制备例4中使用本发明ssbpcm净化剂与传统净化剂psa和多壁碳纳米管mwcnts的基质效应比较。
具体实施方式
以下对本发明的具体实施方式进行详细说明。应当理解的是,此处所描述的具体实施方式仅用于说明和解释本发明,并不用于限制本发明。
在本文中所披露的范围的端点和任何值都不限于该精确的范围或值,这些范围或值应当理解为包含接近这些范围或值的值。对于数值范围来说,各个范围的端点值之间、各个范围的端点值和单独的点值之间,以及单独的点值之间可以彼此组合而得到一个或多个新的数值范围,这些数值范围应被视为在本文中具体公开。
第一方面,本发明提供了一种净化剂,该净化剂包括吸附部分材料和分离剂,其中,所述吸附部分材料为羧基化吸附材料与胺类化合物的共价结合体;所述分离剂为不溶或难溶于有机溶剂的金属盐。
如上所述的,本发明的净化剂由两部分组成,第一部分(吸附部分材料bpcm)由含有羧基的吸附材料与胺类化合物共价交联而成,bpcm含有大量的羧基基团和氨基基团,第二部分为分离剂,含有大量的金属元素。两部分材料通过螯合作用结合在一起,能够在有机相中快速沉降。
根据本发明,所述羧基化吸附材料可以为本领域常规使用的各种羧基化吸附材料,例如,可以为但不限于羧基化碳纳米管、羧基化石墨烯、羧基化二氧化硅、羧基化psa、羧基化二氧化锆、羧基化石墨炭黑和羧基化c18中的至少一种。
根据本发明,所述羧基化吸附材料可以商购获得,也可以通过已知方法将吸附材料进行羧基化。以所述羧基化碳纳米管为例,其可以购自先锋纳米科技有限公司(中国南京),其也可以将多碳纳米管置于体积比为浓硫酸:浓硝酸=(2-4):1的混合液中,在60-70℃下回流4-6小时,冷却至室温,加入去离子水洗涤至中性,过0.45μm滤膜过滤后真空干燥获得。
根据本发明一种优选的实施方式,所述羧基化吸附材料为羧基化碳纳米管,其外径优选<8nm,长度10-30μm,羧基含量为3-4重量%。
根据本发明,所述胺类化合物可以为任意的能够提供氨基的有机化合物,优选的,所述胺类化合物选自分支状聚乙烯亚胺、甲胺、乙胺、丙胺、丁胺、四乙烯五胺和n-丙基乙二胺中的至少一种。
根据本发明一种优选的实施方式,所述胺类化合物为分支状聚乙烯亚胺,其重均分子量(mw)优选为5000-15000,其可以商购获得,例如,可以购自sigma公司(中国上海)。
根据本发明,所述金属盐可以为能够与所述吸附部分材料(bpcm)进行螯合的金属盐,优选为钙盐和/或镁盐,更优选为钙和/或镁的硫酸盐。根据本发明一种优选的实施方式,所述金属盐为硫酸钙、硫酸镁、氯化钙和氯化镁中的一种;更优选为硫酸钙。在更优选为硫酸钙的情况下,所制备得到的净化剂能够更快速的沉降,且净化效果更好。
根据本发明,所述有机溶剂可以为本领域常规的农药萃取中使用的有机溶剂,例如可以为乙腈、乙醇、乙酸乙酯和丙酮中的至少一种。
根据本发明,术语“难溶”具有公知的含义,其是指在室温20℃时溶解度在0.01克以下。
根据本发明,在所述吸附部分材料中,所述羧基化吸附材料与胺类化合物的含量使得其中的氧含量优选为0.5-12重量%,更优选为1-7.5重量%;氮的含量优选为0.5-20重量%,更优选为1-12重量%。
根据本发明,所述吸附部分材料和分离剂的用量比可以在较宽的范围内进行选择,优选的,为了进一步提高自分离效果和净化效果,以干基计的所述吸附部分材料和以干基计的分离剂的质量比为1:0.5-20;优选为1:5-15,例如,可以为1:5、1:6、1:7、1:8、1:9、1:10、1:11、1:12、1:13、1:14、1:15。
第二方面,本发明提供了一种净化剂的制备方法,该方法包括:
(1)将羧基化吸附材料与羧基活化试剂进行第一接触,以对所述羧基化吸附材料中的羧基进行活化;
(2)将步骤(1)得到的羧基活化的羧基化吸附材料与胺类化合物进行第二接触,使得羧基化吸附材料与胺类化合物形成共价结合体,得到吸附部分材料;
(3)将所述吸附部分材料与分离剂混合,得到所述净化剂;其中,所述分离剂为不溶或难溶于有机溶剂的金属盐。
步骤(1)
根据本发明,所述羧基化吸附材料可以为本领域常规使用的各种羧基化吸附材料,例如,可以为但不限于羧基化碳纳米管、羧基化石墨烯、羧基化二氧化硅、羧基化psa、羧基化二氧化锆、羧基化石墨炭黑和羧基化c18中的至少一种。
根据本发明,所述羧基化吸附材料可以商购获得,也可以通过已知方法将吸附材料进行羧基化。以所述羧基化碳纳米管为例,其可以购自先锋纳米科技有限公司(中国南京),其也可以将多碳纳米管置于体积比为浓硫酸:浓硝酸=(2-4):1的混合液中,在60-70℃下回流4-6小时,冷却至室温,加入去离子水洗涤至中性,过0.45μm滤膜过滤后真空干燥获得。
根据本发明一种优选的实施方式,所述羧基化吸附材料为羧基化碳纳米管,其外径优选<8nm,长度10-30μm,羧基含量为3-4重量%。
根据本发明,所述羧基活化试剂可以为常规的各种能够对羧基进行活化的试剂,优选的,为了进一步提高所制备的净化剂的分离效果和杂质净化效果,所述羧基活化试剂为1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐)和/或n-羟基琥珀酰亚胺,更优选为1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐)和或n-羟基琥珀酰亚胺,其质量比优选为1-3:1,例如,可以为1:1、1.2:1、1.4:1、1.6:1、1.8:1、2:1、2.2:1、2.4:1、2.6:1、2.8:1、3:1。
根据本发明,所述羧基活化试剂的用量可以在较宽的范围内进行选择,但优选的,相对于1g的羧基化吸附材料,羧基活化试剂的用量为5-10g,例如,可以为5g、5.5g、6g、6.5g、7g、7.5g、8g、8.5g、9g、9.5g、10g。
根据本发明,所述第一接触的条件可以在较宽的范围内进行选择,只要能够使得羧基化吸附材料上的羧基充分活化即可,优选的,所述第一接触在搅拌的条件下进行,所述搅拌的速度为200-1000rpm,第一接触的温度为20-50℃,时间为20-40min。
根据本发明,为了进一步提高羧基活化效果,优选的,在将羧基化吸附材料与羧基活化试剂进行第一接触前,该方法还包括将所述羧基化吸附材料在水存在的条件下进行超声分散。其中,所述超声分散的时间优选为1.5-2.5h,所述超声的频率优选为30-50khz。
步骤(2)
根据本发明,所述胺类化合物可以为任意的能够提供氨基的有机化合物,优选的,所述胺类化合物选自分支状聚乙烯亚胺、甲胺、乙胺、丙胺、丁胺、四乙烯五胺和n-丙基乙二胺中的至少一种。
根据本发明一种优选的实施方式,所述胺类化合物为分支状聚乙烯亚胺,其重均分子量(mw)优选为5000-15000,其可以商购获得,例如,可以购自sigma公司(中国上海)。
根据本发明,所述羧基化吸附材料和胺类化合物的用量可以在较宽的范围内进行选择,优选的,所述羧基化吸附材料与胺类化合物的用量使得其中的氧含量优选为0.5-12重量%,更优选为1-7.5重量%;氮的含量优选为0.5-20重量%,更优选为1-12重量%。优选的,相对于1g的羧基化吸附材料,胺类化合物的用量为0.1-1g;优选为0.3-0.8g。
根据本发明,所述第二接触的条件可以在较宽的范围内进行选择,只要能够使得羧基活化后的羧基化吸附材料和胺类化合物进行共价结合即可,优选的,所述第二接触在搅拌的条件下进行,所述搅拌的速度为200-1000rpm,第一接触的温度为20-50℃,时间为8-15h。
根据本发明,优选的,该方法还包括将得到的吸附部分材料依次进行固液分离、洗涤和干燥。
其中,所述固液分离的方法可以采用本领域常规的各种固液分离的方法,例如,过滤、离心等。优选的,通过高速(8000-15000rpm)离心的方法将反应后的物料进行固液分离。
其中,优选使用有机溶剂的水溶液对固液分离所得固相进行洗涤,所述有机溶剂可以为乙腈、乙醇、乙酸乙酯和丙酮中的至少一种,优选为乙腈的水溶液。
其中,所述干燥优选为冷冻干燥。
步骤(3)
根据本发明,所述金属盐可以为能够与所述吸附部分材料(bpcm)进行螯合的金属盐,优选为钙盐和/或镁盐,更优选为钙和/或镁的硫酸盐。根据本发明一种优选的实施方式,所述金属盐为硫酸钙、硫酸镁、氯化钙和氯化镁中的一种;更优选为硫酸钙。在更优选为硫酸钙的情况下,所制备得到的净化剂能够更快速的沉降,且净化效果更好。
根据本发明,所述有机溶剂可以为本领域常规的农药萃取中使用的有机溶剂,例如可以为乙腈、乙醇、乙酸乙酯和丙酮中的至少一种。
根据本发明,术语“难溶”具有公知的含义,其是指在室温20℃时溶解度在0.01克以下。
根据本发明,所述吸附部分材料和分离剂的用量比可以在较宽的范围内进行选择,优选的,为了进一步提高自分离效果和净化效果,以干基计的所述吸附部分材料和以干基计的分离剂的质量比为1:0.5-20;优选为1:5-15,例如,可以为1:5、1:6、1:7、1:8、1:9、1:10、1:11、1:12、1:13、1:14、1:15。
根据本发明,所述混合的方式可以为常规的将多种固相进行混合的方法,例如,可以为但不限于直接添加、碾磨、固相加热反应、液相加热反应及微波反应中的一种;优选为碾磨。在优选为碾磨的混合方式下,能够进一步提高所制备的净化剂的分离效果和杂质净化效果。
第三方面,本发明提供了如上所述的方法制备的净化剂。
第四方面,本发明提供了如上所述的净化剂在作为分散固相萃取净化材料中的应用。
第五方面,本发明提供了如上所述的净化剂在残留检测中的应用。
根据本发明,所述残留可以为农药残留,毒素残留(例如,真菌毒素残留)、添加剂残留等。
根据本发明,本发明提供的净化剂可以用在食品、农产品、环境样品中农药残留的检测,例如,蔬菜、水果、肉类、粮食、茶叶、牛奶等复杂基体中农药残留的检测。
下将通过实施例对本发明进行详细描述。
下述实施例中所使用的实验方法如无特殊说明,均为常规方法。下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
分支状聚乙烯亚胺(mw=10000),n-羟基丁二酰亚胺(98%),n-(3-二甲氨基丙基)-n'-乙基碳二亚胺盐酸盐(99%),无水baso4、caso4、mgso4、k2so4和na2so4购自sigma公司(中国上海);
羧基化碳纳米管(cm,外径<8nm,长度10–30μm,羧基含量3.86%)购自先锋纳米科技有限公司(中国南京);
去离子水(18mω/cm)通过赛默飞synergy系统(美国匹斯堡)自制;
黄瓜、卷心菜、豆角、苹果和橘子样品均购自北京当地农贸市场;
农药标准品(>98%)由中国计量科学研究院提供。重量法制备浓度为10μg/g的28种混合农药储备液,进一步稀释储备溶液制备一系列不同浓度的混合农药工作标准溶液,所有的标准溶液均溶解于乙腈并储藏于-20℃冰箱中;
所有的试剂均为hplc纯。
实施例1
本实施例用于说明ssbpcm净化剂的制备方法
1、合成吸附部分材料bpcm:将1g羧基化碳纳米管置于蒸馏水中,30khz超声分散2小时,加入5g1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐)和2.5gn-羟基琥珀酰亚胺,30-40℃下迅速搅拌(600rpm)进行羧基活化30分钟。随后加入0.5g分支状聚乙烯亚胺,30-40℃下持续搅拌(600rpm)反应12小时。10000rpm离心后使用水和乙腈反复清洗离心所得固相三次,冷冻干燥24h,得到吸附部分材料bpcm,经氧氮元素分析,在本发明范围内。
2、取步骤(1)固体产物与无水硫酸钙按1:10(m/m)碾磨混匀,制得具有自分离功能的净化剂ssbpcm。
将产物bpcm与ssbpcm置于10ml乙腈中涡流1min,观察变化情况。如图1所示,静置1min后bpcm在乙腈中依然分散良好,没有观察到沉降现象,而ssbpcm在重力作用下可自行快速沉降,上清液观察不到黑色颗粒,完全透明。
实验使用扫描电镜(sem,jeol,jsm-6330ft)对合成材料的形态进行表征,扫描电镜图如图2中a-c)所示;使用元素分析仪获得元素组成,如图2中d)所示;使用nicoletavatar330傅里叶红外光谱仪(ft-ir)获得红外谱图,如图2中e)中所示。表明成功合成了ssbpcm。
实施例2
本实施例用于说明ssbpcm净化剂的制备方法
1、合成吸附部分材料bpcm:将1g羧基化碳纳米管置于蒸馏水中,40khz超声分散1.5小时,加入2.5g1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐)和2.5gn-羟基琥珀酰亚胺,20-30℃下迅速搅拌(1000rpm)进行羧基活化20分钟。随后加入0.3g分支状聚乙烯亚胺,20-30℃下持续搅拌(1000rpm)反应10小时。8000rpm离心后使用水和乙腈反复清洗离心所得固相三次,冷冻干燥24h,得到吸附部分材料bpcm,经氧氮元素分析,在本发明范围内。
2、取步骤(1)固体产物与无水硫酸钙按1:8(m/m)碾磨混匀,制得具有自分离功能的净化剂ssbpcm。
将产物bpcm与ssbpcm置于10ml乙腈中涡流1min,观察变化情况。静置1min后bpcm在乙腈中依然分散良好,没有观察到沉降现象,而ssbpcm在重力作用下可自行快速沉降,上清液观察不到黑色颗粒,完全透明。
实验使用扫描电镜(sem,jeol,jsm-6330ft)和透射电镜(tem,jeol,jem-2010)对合成材料的形态进行表征,使用nicoletavatar330傅里叶红外光谱仪(ft-ir)获得红外谱图,表明成功合成了ssbpcm。
实施例3
本实施例用于说明ssbpcm净化剂的制备方法
1、合成吸附部分材料bpcm:将1g羧基化碳纳米管置于蒸馏水中,50khz超声分散2.5小时,加入7.5g1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐)和2.5gn-羟基琥珀酰亚胺,40-50℃下迅速搅拌(200rpm)进行羧基活化40分钟。随后加入0.8g分支状聚乙烯亚胺,40-50℃下持续搅拌(200rpm)反应15小时。15000rpm离心后使用水和乙腈反复清洗离心所得固相三次,冷冻干燥24h,得到吸附部分材料bpcm,经氧氮元素分析,在本发明范围内。
2、取步骤(1)固体产物与无水硫酸钙按1:12(m/m)碾磨混匀,制得具有自分离功能的净化剂ssbpcm。
将产物bpcm与ssbpcm置于10ml乙腈中涡流1min,观察变化情况。静置1min后bpcm在乙腈中依然分散良好,没有观察到沉降现象,而ssbpcm在重力作用下可自行快速沉降,上清液观察不到黑色颗粒,完全透明。
实验使用扫描电镜(sem,jeol,jsm-6330ft)和透射电镜(tem,jeol,jem-2010)对合成材料的形态进行表征;使用nicoletavatar330傅里叶红外光谱仪(ft-ir)获得红外谱图,表明成功合成了ssbpcm。
实施例4
本实施例用于说明ssbpcm净化剂的制备方法—分离剂的选择
按照实施例1的方法进行ssbpcm的制备,不同的是,将硫酸钙分别替换为等量的硫酸钡(实施例4-1)、硫酸镁(实施例4-2)、硫酸钾(实施例4-3)和硫酸钠(实施例4-4)。
取等量的硫酸钡、硫酸镁、硫酸钙、硫酸钾、硫酸钠置于15ml装有10ml乙腈试剂的离心管中,涡流1min后静置,观察变化情况。随后将实施例1、实施例4-1、实施例4-2、实施例4-3和实施例4-4制备的ssbpcm置于15毫升装有10ml乙腈试剂的离心管中,涡流1min后静置,观察变化情况。
图3为静置1min时数码相片,五种硫酸盐不溶或及难溶于有机溶剂乙腈,与物理化学性质手册中数据一致。其中,硫酸钡在乙腈中形成较多白色悬浮,硫酸镁次之,需要经过数小时才能完全沉降,硫酸钙、硫酸钾和硫酸钠数秒内即可完全沉降到溶液底部,上层为透明溶液。当bpcm与五种金属盐按比例碾磨后,新的净化剂在乙腈中发生不同程度的共沉降。其中使用硫酸钙、硫酸镁可以实现净化剂和乙腈的快速有效分离,优选为硫酸钙。
实施例5
本实施例用于说明ssbpcm净化剂的制备方法—bpcm与硫酸钙混合方式
按照实施例1的方法进行ssbpcm的制备,不同的是,bpcm与硫酸钙分别通过直接添加混合(实施例5-1)、固相加热反应混合(实施例5-2)、液相加热反应混合(实施例5-3)及微波反应混合(实施例5-4)。
将实施例1、实施例5-1、实施例5-2、实施例5-3和实施例5-4制备的ssbpcm置于10ml乙腈中涡流1min,观察变化情况。各净化剂在乙腈中发生不同程度的共沉降,其中,使用实施例1使用碾磨混匀方式制备的净化剂可以实现净化剂和乙腈更为快速有效的分离,微波反应混合、直接添加混合、固相加热反应混合和液相加热反应混合按效果依次递减。
实施例6
本实施例用于说明ssbpcm净化剂的制备方法—bpcm与硫酸钙混合方式
按照实施例1的方法进行ssbpcm的制备,不同的是,羧基活化试剂分别替换为等量的1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐)(实施例6-1)和等量的n-羟基琥珀酰亚胺(实施例6-1)。
将实施例1、实施例6-1和实施例6-2制备的ssbpcm置于10ml乙腈中涡流1min,观察变化情况。各净化剂在乙腈中发生不同程度的共沉降,其中,使用实施例1使用2种羧基活化试剂的方式制备的净化剂可以实现净化剂和乙腈更为快速有效的分离。
测试例1
ssbpcm净化能力检验
称量10g完全匀浆后的黄瓜样品(±0.01g)于50ml聚四氟乙烯离心管中,加入10ml乙腈并涡流1min,随后加入4gmgso4/1gnacl/1g柠檬酸钠/0.5g柠檬酸氢二钠)。8000rpm离心1min后,取2ml上清液分别加入到5ml含有200mgssbpcm(见实施例1-6)或100mgpsa/300mgmgso4,将使用ssbpcm处理的样品静置1min,将psa处理的样品在8000rpm离心2min,过0.22μm膜后取1μl进入气相色谱质谱联用仪全扫描检测。
实验仪器为赛默飞气相(trace1310)色谱三重四极杆质谱(tsq8000evo)联用质谱仪,进样器为triplusrsh自动进样器(赛默飞,austin,tx,usa)。仪器使用安捷伦j&wscientificdb-5ms(30m*0.25mm*0.25μm)毛细管柱和分流模式分离。进样器入口、传输线和离子源温度分别为250、280和280℃。升温程序为:初始80℃保持1min,以15℃/min上升到150℃,随后以5℃/min上升到210℃,最后以8℃/min上升到285℃,保持9min。载气为高纯氦气(99.999%),流速为1.0ml/min。离子源为ei源,检测模式为全扫描模式。
净化材料的色素净化效果见图4所示(a)为不经过处理的黄瓜萃取液、b)为经过psa处理的黄瓜萃取液、c)为经过ssbpcm处理的黄瓜萃取液,其余净化剂效果未示出)。根据检测结果可得出,使用本发明制备的ssbpcm,特别是实施例1-3制备的ssbpcm处理后深绿色黄瓜萃取液变为透明,色素去除效果好。进一步的气相色谱质谱全扫描谱图表明使用ssbpcm大大减少了萃取液液中杂质,且杂质去除能力优于传统净化剂psa。可见,采用1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐)和n-羟基琥珀酰亚胺共同作为羧基活化试剂,且结合碾磨的方式将bpcm与硫酸钙混合不仅能够实现有效的分析,且净化效果更佳。
测试例2
蔬菜和水果样品中农药检测表现
样品前处理:分别称量10g均桨后的黄瓜、卷心菜、豆角、苹果和橘子样品置于50ml离心管中,加入10ml乙腈,涡流1min,随后添加萃取包4gmgso4/1gnacl/1g柠檬酸钠/0.5g柠檬酸二氢钠,剧烈摇晃10min。8000rpm离心1min后,取1ml上清液到5ml含有100mg实施例1制备的ssbpcm离心管中。涡流1min,静置1min,取上清液通过0.22μm滤膜后直接进入gc–ms/ms检测。
仪器条件与测试例1不同的是检测模式为多反应监测模式(mrm)。28种杀虫剂的详细优化信息见表1。
表1.28种农药的保留时间、定量、定性离子对、最佳碰撞能量信息
检测结果如表2所示,黄瓜、卷心菜、豆角、苹果和橘子中28种农药的检测限和定量限分别为0.1~5.2μg/kg和0.33~17μg/kg,满足国家限量标准《gb2763—2019食品中农药最大残留限量》分析需求。
表2.蔬菜和水果样品中28种农药化合物的检测限和定量限
进一步对三个浓度水平(20,100和500μg/kg)的回收率进行测试,实验重复五次。如表3所示,除了20μg/kg浓度水平的三环唑之外,其他所有农药的三个浓度水平回收率都在73~119%,rsd小于17%,表明良好的精确度。
表328种农药化合物的回收率评价
测试例3
使用ssbpcm与传统psa和多壁碳纳米管mwcnts基质效应对比
样品前处理:分别称量10g均桨后的黄瓜、卷心菜、豆角、苹果和橘子样品置于50ml离心管中,加入10ml乙腈,涡流1min,随后添加萃取包4gmgso4/1gnacl/1g柠檬酸钠/0.5g柠檬酸二氢钠,剧烈摇晃10min。8000rpm离心1min后,取1ml上清液分别加入到5ml含有100mg实施例1制备的ssbpcm、50mgpsa/150mgmgso4和10mgmwcnts/150mgmgso4的离心管中,涡流1min。对于ssbpcm处理的样品静置1min,对于psa和mwcnts处理的样品置于离心机中8000rpm高速离心2min。取上清液通过0.22μm滤膜后直接进入气相色谱质谱检测。仪器条件与测试例2相同。
基质效应计算公式:me=(1-sm/ss)*100%,sm代表基质匹配校正曲线的斜率,ss代表纯溶剂校正曲线的斜率。基质效应处于-20%~+20%表明几乎没有基质效应(图5中为无),处于-50%~-20%和20%~50%之间表明中等程度基质效应(图5中为中),大于50%或小于-50%表明较大基质效应(图5中为大)。
使用ssbpcm、psa和mwcnts处理黄瓜、卷心菜、豆角、苹果和橘子样品后基质效应结果如图5所示,结果表明使用ssbpcm处理不同基体样品皆使更多的农药的基质效应处于-20%~+20%,进一步验证ssbpcm的净化能力优于psa和mwcnts。
- 还没有人留言评论。精彩留言会获得点赞!