一种由牛血清白蛋白介导合成的二氧化钌纳米粒子及其过氧化物模拟酶活性
本发明涉及一种新型的二氧化钌纳米粒子制备方法,利用牛血清白蛋白作为生物模板介导合成尺寸分布均匀、水溶性良好的二氧化钌纳米粒子,该二氧化钌纳米粒子能够高效催化过氧化氢与3,3’,5,5’-四甲基联苯胺盐酸盐发生氧化还原反应,具有类似过氧化物模拟酶的活性,在强酸强碱、高盐及高温下均能保持其过氧化物模拟酶活性,属于仿生技术和纳米技术领域。
背景技术:
2007年,四氧化三铁类过氧化物酶活性的发现催生了“纳米酶”这一新兴多学科交叉研究方向。纳米酶是具有模拟酶性质的催化纳米材料,具有成本低、稳定性高、催化活性可调、易于大规模生产等优点。纳米酶被发现以来,引起了多个领域科学家的兴趣和高度重视,越来越多的科学家开始研究和应用纳米酶,包括:生物传感、免疫分析、癌症诊断和治疗、神经保护、干细胞生长和污染物清除等,因此开发新型纳米酶具有重要的意义。
二氧化钌是一种重要的铂族贵金属氧化物,研究表明它具有很高的比表电容,高电导率和低电阻率,在超级电容器、催化剂以及电化学催化已经有很广泛的应用。众所周知,部分纳米材料的催化活性与其性质、组成、尺寸和表面修饰剂等有很大关系,纳米材料的一个特点是易于聚集的不稳定性,因此为了保护纳米材料,常常需要加入保护剂。蛋白质是肽链经过盘曲折叠形成的具有复杂空间结构的物质,近年来,越来多研究将蛋白质(如牛血清白蛋白)作为外壳或模板制备纳米材料以得到性质稳定、均匀分散或多种功能的纳米材料。而目前尚没有利用蛋白质模板制备二氧化钌纳米材料的研究,且在模拟酶领域,开发具有优秀模拟酶性质的二氧化钌也是非常值得研究和探索。
本发明以牛血清白蛋白(bsa)为模板,通过控制制备ph及温度可制备牛血清白蛋白-二氧化钌纳米粒子。牛血清白蛋白可以控制二氧化钌的形貌及尺寸(7nm),该材料能够高效催化过氧化氢与3,3’,5,5’-四甲基联苯胺盐酸盐发生氧化还原反应,具有类似过氧化物模拟酶的活性,本发明深入研究了该材料作为过氧化物模拟酶的稳态动力学参数及酶活力单位,并证明该材料在强酸强碱、高盐及高温下均能保持其过氧化物模拟酶活性。
技术实现要素:
本发明的目的是以牛血清白蛋白(bsa)为模板,通过控制制备ph及温度可制备牛血清白蛋白-二氧化钌纳米粒子。牛血清白蛋白可以控制二氧化钌的形貌及尺寸(7nm),该材料能够高效催化过氧化氢与3,3’,5,5’-四甲基联苯胺盐酸盐发生氧化还原反应,具有类似过氧化物模拟酶的活性,本发明深入研究了该材料作为过氧化物模拟酶的稳态动力学参数及酶活力单位,并证明该材料在强酸强碱、高盐及高温下均能保持其过氧化物模拟酶活性。
为了实现上述目的,本发明采用以下技术方案:
一种由牛血清白蛋白介导合成的二氧化钌纳米粒子,其特征是由下述方法制备的:将1.6ml浓度为18.75mg/ml的牛血清白蛋白与0.4ml的浓度为75mmol/l三氯化钌混合,在37℃条件下搅拌90分钟以保证混合均匀,然后用氢氧化钠调节上述体系的ph=11,在70℃条件下充分搅拌反应2.5小时,反应后溶液为黑色,所得溶液经过超滤管三次水洗,制得浓度为2mg/ml的牛血清白蛋白-二氧化钌纳米粒子,4℃保存,取部分材料冷冻干燥后用于表征。
所得的溶液在反应后,三氯化钌在310nm及500nm的紫外吸收峰在合成后发生明显消失和变化,说明钌的价态发生变化;牛血清白蛋白在280nm处有吸收,合成前后保持不变。
上述牛血清白蛋白-二氧化钌纳米粒子水溶液分散性好,纳米粒子的晶面间距为0.201nm,对应于二氧化钌晶体的210晶面,牛血清白蛋白-二氧化钌纳米粒子的平均粒径为7nm。
上述牛血清白蛋白-二氧化钌纳米粒子存在c、n、ru和o元素,且表面覆盖有牛血清白蛋白,样品中钌元素的3p轨道图谱反应3p3/2峰主要由ruo2(462.2ev),表明ruo2在牛血清白蛋白-二氧化钌纳米粒子中可能具有较高的强度比。
上述牛血清白蛋白-二氧化钌纳米粒子中的牛血清白蛋白酰胺i带1600-1700cm-1及酰胺iii带1220-1330cm-1仍然存在,说明牛血清白蛋白-二氧化钌纳米粒子仍然存在天然牛血清白蛋白的结构。
本发明所述的一种由牛血清白蛋白介导合成的二氧化钌纳米粒子的过氧化物模拟酶活性,其特征是牛血清白蛋白-二氧化钌纳米粒子的具有模拟过氧化物酶活性,通过催化过氧化氢氧化3,3’,5,5’-四甲基联苯胺盐酸盐产生有蓝色底物,在紫外分光光度仪中在652nm处有明显的吸收峰。
该反应体系的条件为:在2780μl,ph=6,浓度为20mmol/l的磷酸盐缓冲液中加入1ml浓度为10mmol/l的过氧化氢、0.2ml浓度为2mmol/l的3,3’,5,5’-四甲基联苯胺盐酸盐、最后加入2mg/ml牛血清白蛋白-二氧化钌纳米粒子,混合后在25℃室温温浴40分钟,目视观察颜色的变化或测定652nm波长处的吸光度值(a652nm)。
上述牛血清白蛋白-二氧化钌纳米粒子对3,3’,5,5’-四甲基联苯胺盐酸盐的米氏常数(km)为0.034mmol/l,最大反应速率(vmax)为5.54×10-7mmol·l-1·s-1;牛血清白蛋白-二氧化钌纳米粒子对过氧化氢的米氏常数(km)为189.42mmol/l,最大反应速率(vmax)为3.76×10-7mmol·l-1·s-1。
上述牛血清白蛋白-二氧化钌纳米粒子的过氧化物酶活力为710u/g。
上述牛血清白蛋白-二氧化钌纳米粒子在ph为2-12、盐浓度为0-2mol/l及温度为20-80℃条件下保存2小时后催化活性仍无明显变化,具有良好的稳定性。
为了实现上述目的,本发明采用具体技术方案为:
(一)牛血清白蛋白-二氧化钌纳米粒子的制备:
首先,将1.6ml浓度为18.75mg/ml的牛血清白蛋白与0.4ml的浓度为75mm三氯化钌混合,在37℃条件下搅拌90分钟以保证混合均匀,然后用氢氧化钠调节上述体系的ph=11,在70℃条件下充分搅拌反应2.5小时,反应后溶液为黑色。所得溶液经过超滤管三次水洗,为实验所需牛血清白蛋白-二氧化钌纳米粒子(2mg/ml),平均粒径为7nm,4℃保存,取部分材料冷冻干燥后用于表征。
(二)牛血清白蛋白-二氧化钌纳米粒子的过氧化物酶活性
牛血清白蛋白-二氧化钌纳米粒子的过氧化物酶活性是通过催化3,3’,5,5’-四甲基联苯胺盐酸盐产生有蓝色底物,在紫外分光光度仪中在652nm处有明显的吸收峰,步骤(一)在2780μl磷酸盐缓冲液(ph=6,20mmol/l)中加入1ml浓度为10mmol/l的过氧化氢、0.2ml浓度为2mmol/l的3,3’,5,5’-四甲基联苯胺盐酸盐、最后加入20μl的牛血清白蛋白-二氧化钌纳米粒子(2mg/ml),混合后在室温(25℃)温浴40分钟,目视观察颜色的变化或测定652nm波长处的吸光度值(a652nm)。上述液体加入2mol/l硫酸终止后,溶液由蓝色变为黄色,在450nm处由明显吸收峰。
本发明的优点:
(1)本发明所使用的制备方法简便快速。
(2)本发明所使用牛血清白蛋白作为模板制备的二氧化钌纳米材料可得到性质稳定、均匀分散、粒径较小(7nm)及多种功能的二氧化钌纳米材料。
(3)本发明中的牛血清白蛋白-二氧化钌纳米粒子具有良好的过氧化物酶活性,对3,3’,5,5’-四甲基联苯胺盐酸盐的米氏常数为0.034mmol/l,对过氧化氢的米氏常数为189.42mmol/l,酶活力单位为710u/g。
(4)本发明中的牛血清白蛋白-二氧化钌纳米粒子稳定性好,在强酸强碱、高盐及高温下均能保持其过氧化物模拟酶活性。
附图说明
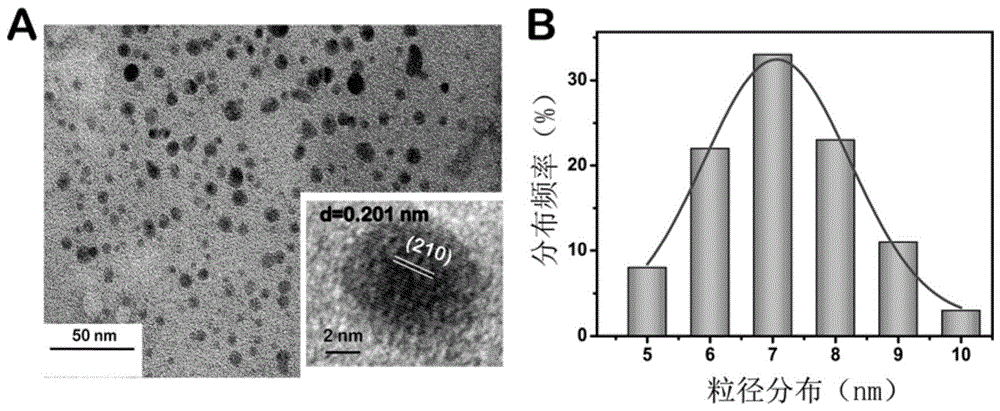
图1a为牛血清白蛋白-二氧化钌纳米粒子的透射电镜(插图:高分辨透射电镜图)。
图1b为牛血清白蛋白-二氧化钌纳米粒子的粒径分布图。
图2为牛血清白蛋白-二氧化钌纳米粒子的紫外-可见吸收光谱图(从左到右依次是牛血清白蛋白,三氯化钌和牛血清白蛋白-二氧化钌纳米粒子),插图:牛血清白蛋白-二氧化钌纳米粒子的样品照片。
图3为牛血清白蛋白-二氧化钌纳米粒子的能量色散x-射线光谱。
图4为牛血清白蛋白-二氧化钌纳米粒子的所测的各对比谱图,图中:a为xps全图谱、b为钌元素的3d轨道图谱、c为钌元素的3p轨道图谱及d为氧元素的1s轨道图谱。
图5为牛血清白蛋白及牛血清白蛋白-二氧化钌纳米粒子的红外图谱。
图6为牛血清白蛋白-二氧化钌纳米粒子催化过氧化氢氧化3,3’,5,5’-四甲基联苯胺盐酸盐显色体系的紫外吸收光谱图(从a到e依次是3,3’,5,5’-四甲基联苯胺盐酸盐,3,3’,5,5’-四甲基联苯胺盐酸盐+过氧化氢,3,3’,5,5’-四甲基联苯胺盐酸盐+牛血清白蛋白-二氧化钌纳米粒子,3,3’,5,5’-四甲基联苯胺盐酸盐+过氧化氢+牛血清白蛋白-二氧化钌纳米粒子及3,3’,5,5’-四甲基联苯胺盐酸盐+过氧化氢+牛血清白蛋白-二氧化钌纳米粒子+终止液2m硫酸)。
图7为不同ph值及不同3,3’,5,5’-四甲基联苯胺盐酸盐的浓度对于牛血清白蛋白-二氧化钌纳米粒子催化过氧化氢氧化3,3’,5,5’-四甲基联苯胺盐酸盐显色体系的影响图,图中:a为3,3’,5,5’-四甲基联苯胺盐酸盐ph值影响图,b为3,3’,5,5’-四甲基联苯胺盐酸盐浓度影响图。
图8为牛血清白蛋白-二氧化钌纳米粒子对于3,3’,5,5’-四甲基联苯胺盐酸盐及过氧化氢的稳态动力学对照图,图中:a为3,3’,5,5’-四甲基联苯胺盐酸盐稳态动力学,b为过氧化氢的稳态动力学。
图9a为不同浓度的牛血清白蛋白-二氧化钌纳米粒子催化过氧化氢氧化3,3’,5,5’-四甲基联苯胺盐酸盐显色体系,吸光值652nm在一分钟内呈线性增长图。
图9b为牛血清白蛋白-二氧化钌纳米粒子的酶活力单位图。
图10为不同ph值、不同温度、不同盐浓度各自对牛血清白蛋白-铂复合纳米材料催化活性的影响图,图中:a为ph值、b为温度、c为盐浓度。
具体实施方式
实例1:
将1.6ml浓度为18.75mg/ml的牛血清白蛋白与0.4ml的浓度为75mmmol/l三氯化钌混合,在37℃条件下搅拌90分钟以保证混合均匀,然后用氢氧化钠调节上述体系的ph=11,在70℃条件下充分搅拌反应2.5小时,反应后溶液为黑色。反应后溶液装入截止分子量为3k的超滤管,6000r/min离心超滤,并水洗3次。定容2ml体积后为实验所需牛血清白蛋白-二氧化钌纳米粒子(2mg/ml),4℃保存,取部分材料冷冻干燥后用于表征。(过程中使用的所有玻璃器皿均经过王水浸泡,并用双蒸水彻底清洗,晾干)
实例2:
将实例1中所得牛血清白蛋白-二氧化钌纳米粒子溶液滴涂在铜网上进行透射电镜检测。如图1a所示,牛血清白蛋白-二氧化钌纳米粒子水溶液分散性好,插图中的高分辨透射电镜图显示所得纳米粒子的晶面间距为0.201nm,对应于二氧化钌晶体的210晶面。图1b为从透射电镜图谱中随机选取50个纳米粒子计算其粒径,并用高斯分布拟合后的图谱,得出牛血清白蛋白-二氧化钌纳米粒子的平均粒径为7nm。
实例3:
将实例1中牛血清白蛋白、三氯化钌及牛血清白蛋白-二氧化钌纳米粒子分别用双蒸水稀释20倍后用紫外分光光度仪测其紫外吸收图谱。如图2为血清白蛋白-二氧化钌纳米粒子合成前后紫外-可见吸收光谱图,三氯化钌在310nm及500nm的紫外吸收峰在合成后发生明显消失和变化,说明钌的价态发生变化。牛血清白蛋白在280nm处有吸收,合成前后保持不变。
实例4:
将实例1中牛血清白蛋白-二氧化钌纳米粒子粉末做处理后测其能量色散x-射线光谱。如图3为牛血清白蛋白-二氧化钌纳米粒子的能量色散x-射线光谱,证明该材料中含有钌元素,其他如碳、氧、氮、硫等元素可能来自于牛血清白蛋白。
实例5:
将实例1中牛血清白蛋白-二氧化钌纳米粒子粉末做处理后测其x射线光电子能谱。如图4中的a为x射线光电子能全谱证明c、n、ru和o元素的存在,表明牛血清白蛋白-二氧化钌纳米粒子表面覆盖有牛血清白蛋白。图4中的b为钌的3d轨道图谱,表明在牛血清白蛋白-二氧化钌纳米粒子中存在多价钌(ru3+/ru4+),在281.2和285.3ev处的结合能为二氧化钌中ru4+的3d5/2和3d3/2,在283.0和287.7ev处的结合能为ru3+的3d5/2和3d3/2。图4中的c为钌的3p轨道图谱,3p3/2峰主要由ruo2(462.2ev),表明ruo2在牛血清白蛋白-二氧化钌纳米粒子中可能具有较高的强度比。图4中的d中,结合能分别为530.8、531.6和532.5ev的o1s区域可能是由羟基(oh−)、晶格氧(o2−)和吸附水三种氧元素组成的,也证明了样品中二氧化钌的存在,上述证明该材料为牛血清白蛋白-二氧化钌纳米粒子。
实例6:
将实例1中牛血清白蛋白-二氧化钌进行冷冻干燥处理得到材料的粉末。分别扫描牛血清白蛋白与牛血清白蛋白-二氧化钌纳米粒子的红外图谱,如图5,可以发现牛血清白蛋白-二氧化钌纳米粒子的部分峰值相对蛋白质减弱,证实牛血清白蛋吧与牛血清白蛋白-二氧化钌纳米粒子发生了相互作用,牛血清白蛋白-二氧化钌纳米粒子中的牛血清白蛋白在酰胺i带(1600-1700cm-1)及酰胺iii带(1220-1330cm-1)仍然存在,说明牛血清白蛋白-二氧化钌纳米粒子仍然存在天然牛血清白蛋白的结构。
实例7:
为证明实例1中所得牛血清白蛋白-二氧化钌纳米粒子的具有模拟过氧化物酶活性,通过催化过氧化氢氧化3,3’,5,5’-四甲基联苯胺盐酸盐产生有蓝色底物,在紫外分光光度仪中在652nm处有明显的吸收峰。在2780μl磷酸盐缓冲液(ph=6,20mmol/l)中加入1ml浓度为10mmol/l的过氧化氢、0.2ml浓度为2mmol/l的3,3’,5,5’-四甲基联苯胺盐酸盐、最后加入20μl的牛血清白蛋白-二氧化钌纳米粒子(2mg/ml),混合后在室温(25℃)温浴40分钟,目视观察颜色的变化或测定652nm波长处的吸光度值(a652nm)。上述液体加入2mol/l硫酸终止后,溶液由蓝色变为黄色,在450nm处由明显吸收峰。图6所示,从a到e依次是3,3’,5,5’-四甲基联苯胺盐酸盐,3,3’,5,5’-四甲基联苯胺盐酸盐+过氧化氢,3,3’,5,5’-四甲基联苯胺盐酸盐+牛血清白蛋白-二氧化钌纳米粒子,3,3’,5,5’-四甲基联苯胺盐酸盐+过氧化氢+牛血清白蛋白-二氧化钌纳米粒子及3,3’,5,5’-四甲基联苯胺盐酸盐+过氧化氢+牛血清白蛋白-二氧化钌纳米粒子+终止液2m硫酸。结果如图6中,牛血清白蛋白-二氧化钌纳米粒子能够催化3,3’,5,5’-四甲基联苯胺盐酸盐产生有蓝色底物,在紫外分光光度仪中在652nm处有明显的吸收峰,加入2mol/l硫酸终止后,溶液由蓝色变为黄色,在450nm处由明显吸收峰,证实牛血清白蛋白-二氧化钌纳米粒子的过氧化物模拟酶活性。
实例8:
在2780μl磷酸盐缓冲液(不同的ph,20mmol/l)中加入1ml浓度为10mmol/l的过氧化氢、0.2ml不同浓度的3,3’,5,5’-四甲基联苯胺盐酸盐、最后加入20μl实例1中所得的牛血清白蛋白-二氧化钌纳米粒子(2mg/ml),混合后在室温(25℃)温浴40分钟,目视观察颜色的变化或测定652nm波长处的吸光度值(a652nm)。如图7中的a和b分别所示,图7中的a为ph值及图7中的b为3,3’,5,5’-四甲基联苯胺盐酸盐的浓度对于牛血清白蛋白-二氧化钌纳米粒子催化过氧化氢氧化3,3’,5,5’-四甲基联苯胺盐酸盐显色体系的最优的条件分别为ph=6及终浓度为0.1mmol/l的3,3’,5,5’-四甲基联苯胺盐酸盐。
实例9:
为计算实例1中所得牛血清白蛋白-二氧化钌纳米粒子分别对3,3’,5,5’-四甲基联苯胺盐酸盐及过氧化氢的稳态动力学常数/米氏常数,通过催化过氧化氢氧化3,3’,5,5’-四甲基联苯胺盐酸盐产生有蓝色底物,在紫外分光光度仪中在652nm处有明显的吸收峰。具体操作为:在2780μl磷酸盐缓冲液(ph=6,20mmol/l)中加入1ml不同浓度的过氧化氢、0.2ml不同浓度的3,3’,5,5’-四甲基联苯胺盐酸盐、最后加入20μl的牛血清白蛋白-二氧化钌纳米粒子(2mg/ml),混合后在室温(25℃)温浴1分钟,目视观察颜色的变化或测定652nm波长处的吸光度值(a652nm)。通过牛血清白蛋白-二氧化钌纳米粒子和不同浓度3,3’,5,5’-四甲基联苯胺盐酸盐或过氧化氢数据结果进行米氏方程v=vmax×[s]/(km+[s])的拟合。如图8中的a,得出牛血清白蛋白-二氧化钌纳米粒子对3,3’,5,5’-四甲基联苯胺盐酸盐的米氏常数(km)为0.034mmol/l,最大反应速率(vmax)为5.54×10-7mmol·l-1·s-1。如图8中的b,牛血清白蛋白-二氧化钌纳米粒子对过氧化氢的米氏常数(km)为189.42mmol/l,最大反应速率(vmax)为3.76×10-7mmol·l-1·s-1。
实例10:
为计算实例1中所得牛血清白蛋白-二氧化钌纳米粒子的过氧化物酶酶活力单位,通过催化过氧化氢氧化底物3,3’,5,5’-四甲基联苯胺盐酸盐产生有蓝色底物,在紫外分光光度仪中在650nm处有明显的吸收峰。)在2780μl磷酸盐缓冲液(ph=6,20mmol/l)中加入1ml浓度为10mmol/l的过氧化氢、0.2ml浓度为2mmol/l的3,3’,5,5’-四甲基联苯胺盐酸盐、最后加入20μl的牛血清白蛋白-二氧化钌纳米粒子(2mg/ml),混合后在室温(25℃)温浴1分钟,每隔10秒记录652nm波长处的吸光度值(a652nm)(图9a)。利用朗伯比尔定律可计算过氧化物酶活力为710u/g(图9b)。
实例11:
将牛血清白蛋白-二氧化钌纳米粒子分别置于不同ph(2-12)、盐浓度(0-2mol/l)及温度(20-80℃)条件下保存2小时后,测定不同条件下对其相对催化活性的影响。在2780μl磷酸盐缓冲液(ph=6,20mmol/l)中加入1ml浓度为10mmol/l的过氧化氢、0.2ml浓度为2mmol/l的3,3’,5,5’-四甲基联苯胺盐酸盐、最后加入20μl在上述不同ph(2-12)、盐浓度(0-2mol/l)及温度(20-80℃)条件下保存2小时后的牛血清白蛋白-二氧化钌纳米粒子(2mg/ml),混合后在室温(25℃)温浴40分钟,目视观察颜色的变化或测定652nm波长处的吸光度值(a652nm)。由图可见,牛血清白蛋白-二氧化钌纳米粒子在图10中的a显示的不同ph(2-12)、图10中的b显示的盐浓度(0-2mol/l)及图10中的c显示的温度(20-80℃)条件下保存2小时后催化活性仍无明显变化,具有良好的稳定性。
- 还没有人留言评论。精彩留言会获得点赞!