基于三维等离激元超构材料的高通量多靶标微流生物芯片的制作方法
本发明涉及生物芯片与等离激元超构材料技术领域,具体为基于三维等离激元超构材料的高通量多靶标微流生物芯片。
背景技术:
基于光谱探测技术的生物分子传感应用对于医学检验、生物分析、药物研发、化学化工、食品安全、环境监测等诸多领域具有十分重要的现实意义。过去十年来,运用表面等离激元光学效应的生物分子传感技术展现了极高的灵敏度和分辨率,同时具备实时监测、非侵入式检测和免标记等优点,得到相关领域科学工作者和技术开发人员的普遍关注。例如,美国通用医疗旗下的biacore系列产品及生物芯片在蛋白分子互作用和动力学分析领域已成为一个行业标准。虽然基于棱镜耦合方案的商业化表面等离激元生物传感分析技术已经成熟。但是,该生物芯片存在价格昂贵、光路复杂、操作繁琐、检测分子尺寸受限、检测设备体积庞大等诸多缺点,不利于表面等离激元生物传感技术的推广和普及。
近些年来,以低成本和小型集成化为特点的三维纳米图案化贵金属结构传感设计和应用在相关领域展现出更好的应用前景。与基于棱镜配置的传感器设计相比,采用三维图案化金属纳米结构的表面等离激元传感器特征尺寸接近或小于光波长,展现出一系列的优势:(1)无需角度操控的复杂光耦合装置,可通过垂直入射直接激发表面等离激元模式,更便于结构的小型集成化;(2)检测范围更宽,传感线性度更高;(3)结构设计更自由,传感机制更灵活多样;(4)与现有的成像器件和微流控技术相兼容,为多通道、高通量的生物传感器设计提供可能性;(5)克服棱镜式表面等离激元传感器检测生物小分子灵敏度低的缺陷,有效地扩大生物传感应用范围;(6)适用光谱范围更广,可以从紫外光扩展到近红外甚至到中远红外波段。基于三维金属纳米结构电磁耦合的表面等离激元传感器具有小型化和集成化的特征,因而相比于棱镜耦合结构配置有着更巨大的商业优势。
技术实现要素:
针对现有技术的不足,本发明提供了基于三维等离激元超构材料的高通量多靶标微流生物芯片,解决了背景技术提出的部分技术问题。可以解决第一代等离激元生物芯片价格昂贵、光路复杂、操作繁琐、检测分子尺寸受限、检测设备体积庞大等诸多缺点,更利于表面等离激元生物传感技术的推广和普及。
为实现以上目的,本发明通过以下技术方案予以实现:基于三维等离激元超构材料的高通量多靶标微流生物芯片,包括:生物芯片;所述生物芯片包括:塑料盖板、三维等离激元超构材料传感器件、微流控底板及若干生物试剂;所述塑料盖板、三维等离激元超构材料传感器件、微流控底板自上而下复合而成,其中塑料盖板与微流控底板之间采用粘合剂粘连,三维等离激元超构材料传感器件嵌入在微流控底板的检测区凹坑内;所述生物试剂包括但不限于11-巯基十一烷酸溶液mua、乙基二甲基胺丙基碳化二亚胺edc、n-羟基琥珀酰亚胺nhs、牛血清白蛋白bsa、配体溶液和分析物溶液;
优选的,所述塑料盖板形状为圆形,半径为4cm,厚度为2mm,在距离圆心1cm处阵列式均匀分布着24个半径为500μm的圆形进样通孔,进样通孔与微流控底板配合;
优选的,所述三维等离激元超构材料传感器件采用纳米加工工艺制备,由柔性聚碳酸酯基底、铬膜和金膜自下而上复合形成;所述柔性聚碳酸酯基底上阵列式均匀分布三维准纳米柱,所述准纳米柱的上部四周倒圆角,顶端平齐;
优选的,所述三维等离激元超构材料传感器件其制备过程如下,首先,采用纳米压印在柔性聚碳酸酯基底上进行热压印;然后,采用电感耦合等离子刻蚀机刻蚀处理;再次,采用电子束蒸镀仪镀上铬膜和金膜;最后,将其切割成半径2mm的圆形器件。
优选的,所述柔性聚碳酸酯基底的结构为周期性阵列纳米孔洞阵列,孔洞直径为250nm,洞深200nm,周期为500nm。
优选的,所述热压印时间为8min,压力为40bar,温度为150℃。
优选的,所述刻蚀处理条件为压力8pa,射频功率40w,氧气流量50sccm,温度为20℃。
优选的,所述铬膜厚度为10nm,金膜厚度180nm。
优选的,所述微流控底板的半径为4cm,厚度为5mm,圆心处有一个卡槽,在距离圆心1cm处阵列式均匀分布24个半径为500μm圆形进样柱302;距离圆心2cm处阵列式均匀分布24个半径为2mm的圆形检测区;距离圆心3.2cm处阵列式均匀分布24个半径为4mm的圆形废液区,圆形进样柱、圆形检测区与圆形废液区之间由100μm宽的直线型微流通道连接。
基于三维等离激元超构材料的高通量多靶标微流生物芯片分子浓度、动力学测定方法,包括以下步骤:
步骤一:在生物芯片表面形成自组装膜并活化,将所述三维等离激元超构材料传感器件放在2℃-8℃的10mmol/l的11-巯基十一烷酸溶液mua中12小时,形成mua自组装膜;并采用400mmol/l的乙基二甲基胺丙基碳化二亚胺edc和100mmol/l的n-羟基琥珀酰亚胺nhs将mua在2℃-8℃下将羧基活化;
步骤二:固定配体,将步骤一中的传感器件放入配体溶液中、室温37℃、浸泡2至4个小时,使配体与表面的11-巯基十一烷酸溶液mua结合,从而固定配体;
步骤三:封闭多余羧基,将步骤二中的传感器件加入浓度为50μg/ml的牛血清白蛋白bsa,牛血清白蛋白bsa会与传感器件上没有和配体结合的11-巯基十一烷酸溶液mua相结合,从而封闭多余羧基;
步骤四:加入分析物溶液测量分子动力学过程,加入不同浓度的标准分析物溶液进行测定,可以通过光谱的实时偏移量来表征配体与分析物的结合速率;
步骤五:再生过程,可以在酸性环境下使芯片再生,从而实现重复利用,节约成本。
优选的,24个所述圆形检测区用于进行不同种类的蛋白标志物同步实时检测。如肿瘤标志物癌胚抗原(cea)、糖类抗原199(ca199)、糖类抗原125(ca125)、糖类抗原153(ca153)、甲胎蛋白(afp)、前列腺癌特异性抗原(psa);covid-19免疫球蛋白igm、covid-19免疫球蛋白igg的检测。
有益效果
本发明提供了基于三维等离激元超构材料的高通量多靶标微流生物芯片。与现有技术相比具备以下有益效果:提供基于三维等离激元超构材料的高通量多靶标微流生物芯片,可以提供24通道高通量多标志物并行实时检测,既解决了第一代等离激元生物芯片价格昂贵、光路复杂、操作繁琐、检测分子尺寸受限、检测设备体积庞大等诸多缺点,也更利于表面等离激元生物传感技术的推广和普及。
附图说明
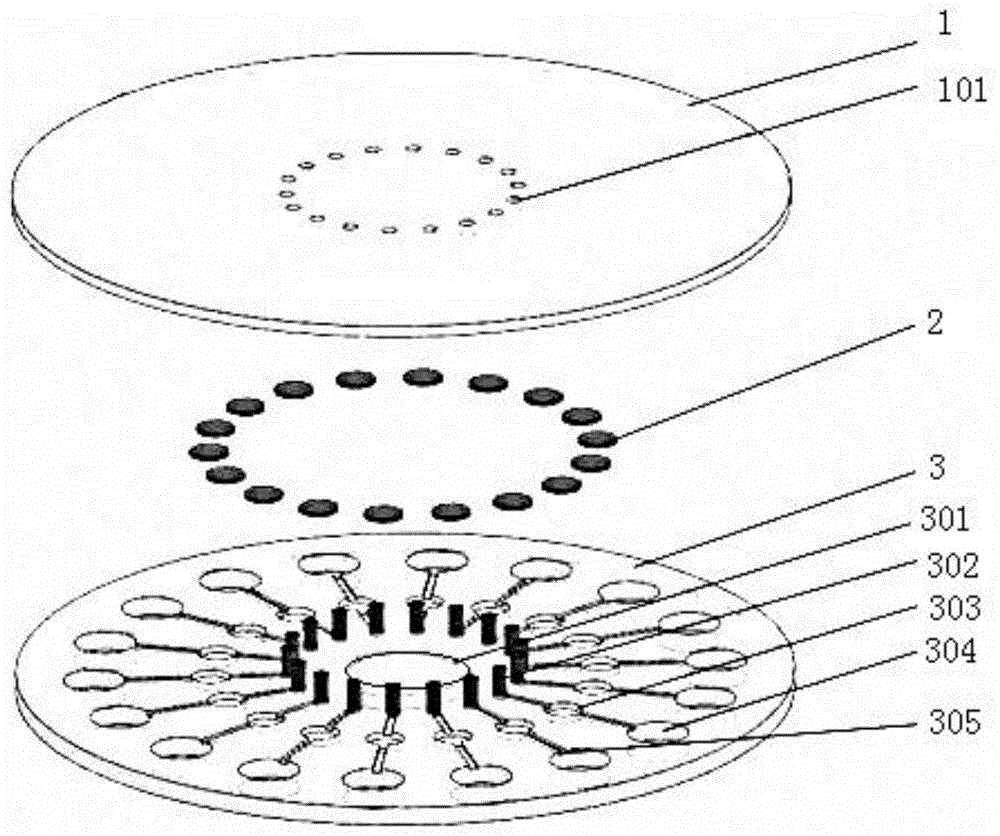
图1为本发明高通量生物芯片三维分解示意图;
图2为本发明高通量生物芯片三维结构图;
图3为本发明三维等离激元超构材料传感器件扫描电镜侧视图;
图4为本发明高通量生物芯片所配备的外部系统框架示意图;
图5为本发明等离三维激元超构材料传感器件分子动力学检测过程的横截面示意图。
图中:塑料盖板1、进样通孔101、三维等离激元超构材料传感器件2、微流控底板3、柔性聚碳酸酯基底201、铬膜202、金膜203、卡槽301、圆形检测区303、圆形废液区304、直线型微流通道305。
具体实施方式
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
请参阅图1-5,包括:生物芯片;所述生物芯片包括:塑料盖板1、三维等离激元超构材料传感器件2、微流控底板3及若干生物试剂;所述塑料盖板1、三维等离激元超构材料传感器件2、微流控底板3自上而下复合而成,其中塑料盖板1与微流控底板3之间采用粘合剂粘连,三维等离激元超构材料传感器件2嵌入在微流控底板3的检测区凹坑内;所述生物试剂包括但不限于11-巯基十一烷酸溶液mua、乙基二甲基胺丙基碳化二亚胺edc、n-羟基琥珀酰亚胺nhs、牛血清白蛋白bsa、配体溶液和分析物溶液;
进一步地,所述塑料盖板1形状为圆形,半径为4cm,厚度为2mm,在距离圆心1cm处阵列式均匀分布着24个半径为500μm的圆形进样通孔101,进样通孔101与微流控底板3配合;
进一步地,所述三维等离激元超构材料传感器件2采用纳米加工工艺制备,由柔性聚碳酸酯基底201、铬膜202和金膜203自下而上复合形成;所述柔性聚碳酸酯基底201上阵列式均匀分布三维准纳米柱,所述准纳米柱的上部四周倒圆角,顶端平齐;
进一步地,所述三维等离激元超构材料传感器件2其制备过程如下,首先,采用纳米压印在柔性聚碳酸酯基底201上进行热压印;然后,采用电感耦合等离子刻蚀机刻蚀处理;再次,采用电子束蒸镀仪镀上铬膜202和金膜203;最后,将其切割成半径2mm的圆形器件。
进一步地,所述柔性聚碳酸酯基底201的结构为周期性阵列纳米孔洞阵列,孔洞直径为250nm,洞深200nm,周期为500nm。
进一步地,所述热压印时间为8min,压力为40bar,温度为150℃。
进一步地,所述刻蚀处理条件为压力8pa,射频功率40w,氧气流量50sccm,温度为20℃。
进一步地,所述铬膜202厚度为10nm,金膜203厚度180nm。
请参阅图3,可以从三维等离激元超构材料传感器件2扫描电镜的侧视图看出,所制备的传感器件尺寸均一、形貌良好。
所述微流控底板3的半径为4cm,厚度为5mm,圆心处有一个卡槽301,在距离圆心1cm处阵列式均匀分布24个半径为500μm圆形进样柱302;距离圆心2cm处阵列式均匀分布24个半径为2mm的圆形检测区303;距离圆心3.2cm处阵列式均匀分布24个半径为4mm的圆形废液区304,圆形进样柱302、圆形检测区303与圆形废液区304之间由100μm宽的直线型微流通道305连接。
请参阅图4,所需试剂由微泵注入,微泵可以由微流管接入生物芯片圆形进样柱302形成密闭,微泵的注入速率为200μl/min-2000μl/min,便携式检测仪内部集成的光谱仪可以将光信号采集、处理上传至分析软件从而得测量结果。
基于三维等离激元超构材料的高通量多靶标微流生物芯片分子浓度、动力学测定方法,包括以下步骤:
请参阅图5,步骤一:在生物芯片表面形成自组装膜并活化,将所述三维等离激元超构材料传感器件2放在2℃-8℃的10mmol/l的11-巯基十一烷酸溶液mua中12小时,形成mua自组装膜;并采用400mmol/l的乙基二甲基胺丙基碳化二亚胺edc和100mmol/l的n-羟基琥珀酰亚胺nhs将mua在2℃-8℃下将羧基活化;
步骤二:固定配体,将步骤一中的传感器件放入配体溶液中、室温37℃、浸泡2至4个小时,使配体与表面的11-巯基十一烷酸溶液mua结合,从而固定配体;
步骤三:封闭多余羧基,将步骤二中的传感器件加入浓度为50μg/ml的牛血清白蛋白bsa,牛血清白蛋白bsa会与传感器件上没有和配体结合的11-巯基十一烷酸溶液mua相结合,从而封闭多余羧基;
步骤四:加入分析物溶液测量分子动力学过程,加入不同浓度的标准分析物溶液进行测定,可以通过光谱的实时偏移量来表征配体与分析物的结合速率;
步骤五:再生过程,可以在酸性环境下使芯片再生,从而实现重复利用,节约成本。
进一步地,24个所述圆形检测区303用于进行不同种类的蛋白标志物同步实时检测。如肿瘤标志物癌胚抗原(cea)、糖类抗原199(ca199)、糖类抗原125(ca125)、糖类抗原153(ca153)、甲胎蛋白(afp)、前列腺癌特异性抗原(psa);covid-19免疫球蛋白igm、covid-19免疫球蛋白igg的检测。
本发明提供基于三维等离激元超构材料的高通量多靶标微流生物芯片,可以提供24通道高通量多标志物并行实时检测,既解决了第一代等离激元生物芯片价格昂贵、光路复杂、操作繁琐、检测分子尺寸受限、检测设备体积庞大等诸多缺点,也更利于表面等离激元生物传感技术的推广和普及。
需要说明的是,在本文中,诸如第一和第二等之类的关系术语仅仅用来将一个实体或者操作与另一个实体或操作区分开来,而不一定要求或者暗示这些实体或操作之间存在任何这种实际的关系或者顺序。而且,术语“包括”、“包含”或者其任何其他变体意在涵盖非排他性的包含,从而使得包括一系列要素的过程、方法、物品或者设备不仅包括那些要素,而且还包括没有明确列出的其他要素,或者是还包括为这种过程、方法、物品或者设备所固有的要素。
尽管已经示出和描述了本发明的实施例,对于本领域的普通技术人员而言,可以理解在不脱离本发明的原理和精神的情况下可以对这些实施例进行多种变化、修改、替换和变型,本发明的范围由所附权利要求及其等同物限定。
- 还没有人留言评论。精彩留言会获得点赞!