一种包埋小分子亲水性成分的胶体囊及其制备方法
1.本发明属于微胶囊的制备技术领域,具体涉及一种包埋小分子亲水性成分的胶体囊及其制备方法。
背景技术:
2.胶体囊是一种新颖的以胶体粒子为壳壁结构的新型微胶囊,这是由于胶体粒子在皮克林乳浊液油
‑
水界面可自组装形成有序的球面胶体壳。与传统微胶囊相比,胶体囊在结构上更为稳定,主要表现在两个方面:(1)机械性能高,主要取决于胶体粒子经有序界面组装后所形成的壳壁的厚度及紧密度;(2)热稳定性良好,这是由于目前可用于制备胶体囊的胶体粒子大部分为无机粒子,例如二氧化硅纳米粒子、二氧化钛纳米粒子、碳酸钙纳米粒子、四氧化三铁纳米粒子等,这些无机胶体粒子通常具有更高的热稳定性和化学稳定性。基于此,在制备和应用胶体囊时,由于其结构的稳定性,使得其所包埋的芯材成分具有更好的物理化学稳定性,表现为不易发生泄漏和降解等,最终实现理想的包埋效果。因此,利用胶体囊包埋芯材成分已受到医药、化妆品、食品等领域的高度关注。
3.迄今为止,在胶体囊的制备上,多种化学或物理化学方法已被提出并得到广泛的应用。其中,基于皮克林乳浊液模板法开展胶体囊的制备还具有如下优点:(1)可通过调节胶体粒子的浓度或者乳浊液油水比,实现胶体囊的粒径从亚微米到微米级调控;(2)通过调节壳壁中无机胶体粒子的大小和固定方法,还可以调控胶体囊的渗透性,从而满足小分子成分包埋的需求。总体来说,皮克林乳浊液模板法具有简单易行、条件温和的特点,在此基础上开展胶体囊的制备也具有巨大的研究和应用潜力。
4.小分子亲水性成分是指分子量在500以下的化合物。事实上,目前已发现的大部分的功效成分均为小分子化合物,而相对分子质量小于500的分子大都是水溶性的,因此将小分子亲水性成分进行微囊化是一项具有意义的工作。所述的典型的小分子亲水性成分主要包括茶多酚、花青素、维生素b族、维生素c等。
5.小分子亲水性成分在应用过程中通常存在如下问题:(1)由于该类成分具有高运动活性,在包埋过程中易于穿过传统微胶囊表面和内部细小的孔隙或通道逃出,最终导致其包封率、负载量难以提高。(2)由于传统微胶囊在结构性能上存在不足,使得小分子亲水性成分在储存过程中物理化学稳定性较差,表现为易发生泄漏和(或)降解等。
6.因此,如何开发一种针对于小分子亲水性成分的微囊化方法,在增强传统微胶囊结构性能的同时还可解决小分子亲水性成分包埋率低,负载量低、稳定性差等问题,是本领域一个函待解决的难题。
技术实现要素:
7.本发明提供一种高包埋率,高负载量的包埋小分子亲水性成分的胶体囊及其制备方法,以增强其结构性能,并解决现有的微囊化技术中小分子亲水性成分的包埋率低,负载量低、稳定性差等缺点和不足之处。
8.本发明所述胶体囊具有核
‑
壳结构,所述胶体囊的粒径分布介于1~30μm,所述核
‑
壳结构包括胶体壳壁结构和凝胶核,所述胶体壳壁结构为一层或多层改性纳米碳酸钙壳壁结构,所述凝胶核为海藻酸/卡拉胶经交联形成的凝胶核,所述凝胶核内包埋小分子亲水性成分。改性纳米碳酸钙和疏水性表面活性剂在乳化作用下自组装排列于水(海藻酸/卡拉胶混合溶液)
‑
油(蓖麻油)两相界面处,形成由改性纳米碳酸钙为主要稳定剂而稳定的油包水皮克林乳浊液,随后加入小分子亲水性成分溶液和作为交联触发剂或交联剂的葡萄糖酸内酯/氯化钾混合溶液,从而将内水相中的海藻酸/卡拉胶凝胶固定,形成稳定的包埋小分子亲水性成分的胶体囊。由于该胶体囊壳壁由改性纳米碳酸钙排列组成,因此通过调节壳壁的厚度及紧密度,可实现小分子亲水性成分的包埋,并大大改善小分子亲水性成分的包封率、负载量以及稳定性等。
9.作为优选,所述改性碳酸钙是指以肉豆蔻酸、棕榈酸、油酸、硬脂酸为原料对纳米碳酸钙进行表面处理而得到的改性产物,其粒径分布介于40~80nm。
10.作为优选,所述小分子亲水性成分是指茶多酚、花青素、维生素b族、维生素c一种或多种。
11.作为优选,所述的小分子亲水性成分溶解于冰醋酸水溶液中,小分子亲水性成分的浓度范围为0.1~1g/ml;所述冰醋酸水溶液的ph值为4.5~6.0。
12.一种包埋小分子亲水性成分的胶体囊的制备方法,包括以下步骤:
13.(1)将海藻酸和卡拉胶加入至纯水中,于室温下搅拌,得到澄清透明的海藻酸/卡拉胶混合溶液;将小分子亲水性成分加入至冰醋酸水溶液中,于室温下避光搅拌,得到小分子亲水性成分溶液;
14.(2)将改性纳米碳酸钙和疏水性表面活性剂加入至蓖麻油中,于50~65℃恒温水浴中充分搅拌,得到含有改性纳米碳酸钙和疏水性表面活性剂的蓖麻油分散液;
15.(3)在800~2000rpm的搅拌下向所述含改性纳米碳酸钙颗粒和疏水性表面活性剂的蓖麻油分散液中逐滴加入海藻酸/卡拉胶混合溶液,于50~65℃下搅拌5~15min,随后加入小分子亲水性成分溶液,继续搅拌10~15min使其充分乳化,制备得改性纳米碳酸钙颗粒和疏水性表面活性剂稳定的油包水乳浊液;
16.(4)将葡萄糖酸内酯和氯化钾加入至纯水中,于室温下搅拌,得到澄清透明的葡萄糖酸内酯/氯化钾混合溶液;
17.(5)向所述乳浊液中逐滴加入葡萄糖酸内酯/氯化钾混合溶液,于50~65℃下连续搅拌30~60min,充分物理交联,形成包埋小分子亲水性成分的胶体囊乳浊液;
18.(6)向所述胶体囊乳浊液中,加入无水乙醇反复清洗3~4次,最终得到包埋小分子亲水性成分的胶体囊,随后将包埋小分子亲水性成分的胶体囊真空干燥后储存于4℃冰箱内得到包埋小分子亲水性成分的胶体囊。
19.进一步地,步骤(1)中所述的海藻酸的分子量为3~20kda;所述的卡拉胶的分子量为400~600kda,其型号可以是κ
‑
型、ι
‑
型、λ
‑
型中的任意类型或不同比例的混合物;所述的海藻酸/卡拉胶混合溶液中海藻酸的质量分数为0.8~3.0%;所述的海藻酸/卡拉胶混合溶液中卡拉胶的质量分数为0.3~2.5%;所述的搅拌步骤的时间为30~120min。
20.进一步地,所述的蓖麻油中改性纳米碳酸钙的质量分数为0.6~3.0%;所述的蓖麻油中含有疏水性表面活性剂;所述的疏水性表面活性剂为司盘20、司盘80、聚甘油蓖麻醇
酯;所述的蓖麻油中疏水性表面活性剂的质量分数为0.5~2.0%。
21.进一步地,步骤(3)中所述的含改性纳米碳酸钙颗粒和疏水性表面活性剂的蓖麻油分散液与海藻酸/卡拉胶混合溶液的质量比为(5~15):1;所述的小分子亲水性成分溶液与海藻酸/卡拉胶混合溶液的质量比为1:(2~5)。
22.进一步地,步骤(4)中所述的葡萄糖酸内酯/氯化钾混合溶液中葡萄糖酸内酯的质量分数为20~30%;所述的葡萄糖酸内酯/氯化钾混合溶液中氯化钾的质量分数为0.1~0.3%。
23.进一步地,步骤(5)中:所述的葡萄糖酸内酯/氯化钾混合溶液与海藻酸/卡拉胶混合溶液的质量比为1:(10~30)。
24.进一步地,步骤(6)中所述的无水乙醇与胶体囊乳浊液的质量比为(2~5):1,并通过800~1500rpm离心处理移除上层清液;所述的将包埋小分子亲水性成分的胶体囊的真空干燥温度控制为25~35℃,真空干燥时长控制为12~24h。
25.与现有技术相比,本发明具有如下有益效果:
26.(1)本发明通过在内水相中添加凝胶剂海藻酸/卡拉胶使其凝胶化,同时选用无机纳米碳酸钙粒子作为壳壁,可显著增强胶体囊核
‑
壳结构的结构性能,进而使得其所包埋的小分子亲水性成分具有较好的物理化学稳定性;
27.(2)本发明通过构建凝胶网络结构和壳壁结构,可以降低小分子亲水性成分在包埋过程中通过胶体囊表面和内部细小的孔隙或通道逃出的能力,从而大大提高该类成分的包埋率和负载量;
28.(3)本发明制备工艺简单、制备条件温和,重复性好,非常有利于小分子亲水性成分功效发挥的稳定性和工业化放大生产。
附图说明
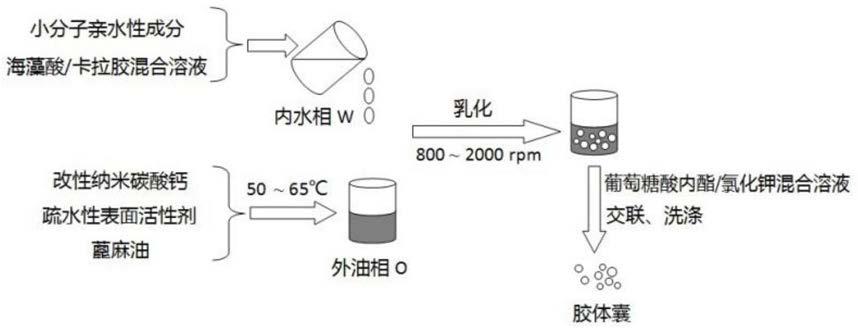
29.图1为本发明所述的一种包埋小分子亲水性成分的胶体囊的制备方法流程图;
30.图2为实施例1制备的包埋维生素c的胶体囊的扫描电镜照片;
31.(a)为包埋维生素c的胶体囊的扫描电镜图谱,
32.(b)为(a)的局部放大,
33.(c)为单独一个胶体囊的图谱,
34.(d)为单独一个胶体囊表面的局部放大图谱;
35.图3为实施例1制备的包埋维生素c的胶体囊在不同贮藏条件下活性成分的稳定性结果;
36.(a)包埋维生素c的胶体囊在4℃和30℃下的活性成分保留率结果,
37.(b)包埋维生素c的胶体囊在相对湿度85%和65%下的活性成分保留率结果,
38.(c)包埋维生素c的胶体囊在避光和自然光照下的活性成分保留率结果。
具体实施方式
39.下面根据实施例对本发明作进一步说明,本发明的方式包括但不仅限于以下实施例。
40.如图1所示,本发明包括以下步骤:
41.下面结合具体实施例对本发明作进一步描述。应理解,此处所描述的优选实施例仅用于说明和解释本发明,并不用于限定本发明。
42.实施例1
43.如图1所示,一种包埋维生素c的胶体囊的制备方法,包括如下步骤:
44.(1)分别将0.1g海藻酸和0.2gκ
‑
型卡拉胶加入至10g纯水中,于室温下搅拌,得到澄清透明的海藻酸/卡拉胶混合溶液;将2g维生素c加入至10g冰醋酸水溶液(0.2%,w/v)中,于室温下避光搅拌,得到维生素c溶液;
45.(2)分别将0.1g改性纳米碳酸钙和0.14g司盘80加入至6.8g蓖麻油中,于50℃恒温水浴中充分搅拌,得到含有改性纳米碳酸钙和司盘80的蓖麻油分散液;
46.(3)在1500rpm的搅拌下向所述含改性纳米碳酸钙颗粒和司盘80的蓖麻油分散液中逐滴加入2.2g海藻酸/卡拉胶混合溶液,于50℃下搅拌10min,随后加入0.5g维生素c溶液,继续搅拌15min使其充分乳化,制备得改性纳米碳酸钙颗粒和司盘80稳定的油包水乳浊液;
47.(4)分别将1.2g葡萄糖酸内酯和18mg氯化钾加入至6g纯水中,于室温下搅拌,得到澄清透明的葡萄糖酸内酯/氯化钾混合溶液;
48.(5)向所述乳浊液中逐滴加入0.3g葡萄糖酸内酯/氯化钾混合溶液,于50℃下连续搅拌30min,充分物理交联,形成包埋维生素c的胶体囊乳浊液;
49.(6)向所述胶体囊乳浊液中,加入无水乙醇反复清洗3次,最终得到包埋维生素c的胶体囊,随后将包埋维生素c的胶体囊真空干燥24h后储存于4℃冰箱内,至此,包埋维生素c的胶体囊制备完成。
50.性能表征:
51.(1)扫描电镜
52.将制备得到的包埋维生素c的胶体囊置于导电胶带上,利用场发射扫描电镜(s4800,日本hitachi公司)直接观察胶体囊的表面形貌结构,电镜结果如图2所示(图2为实施例1制备的包埋维生素c的胶体囊的扫描电镜照片),实施例1制备得到的包埋维生素c的胶体囊的球形度良好,并且其表面分布着较为密集的改性纳米碳酸钙胶体粒子。
53.(2)包封率和负载量
54.采用rp
‑
hplc法检测包埋维生素c的胶体囊的包封率和负载量:
55.样品处理:取适量包埋维生素c的胶体囊样品,均匀分散于50mlpbs缓冲液(20mmol/l,ph=5.8)中,超声0.5h后将维生素c从胶体囊中提取出来,过0.45μm水系膜即为待测样品溶液;
56.包封率计算公式为:包封率=胶体囊中实际活性成分含量/制备时投入的活性成分的总量
×
100%;经测定,胶体囊中维生素c的包封率为93.6%;而负载量计算公式为:包封率=胶体囊中实际活性成分含量/干燥后胶体囊样品的总质量
×
100%,经测定,胶体囊中维生素c的负载量为27.8%。
57.(3)稳定性考察
58.准确称量8~10mg包埋维生素c的胶体囊样品,分别置于不同温度(4℃、30℃)不同相对湿度(85%、65%)以及有无光照(避光、自然光照)等贮藏条件下,研究0~5周贮藏期内上述不同条件对胶体囊中维生素c保留率的影响;
59.保留率计算公式为:保留率=贮藏一定时间后胶体囊中的活性成分含量/贮藏前胶体囊中的活性成分含量
×
100%;经测定,在贮藏5周后,胶体囊中维生素c在4℃和30℃下的保留率分别为99.3%和96.0%;在贮藏5周后,胶体囊中维生素c在相对湿度85%和65%下的保留率分别为96.8%和97.6%;在贮藏5周后,胶体囊中维生素c在避光和自然光照下的保留率分别为98.3%和96.9%,测试结果如图3所示(图3为实施例1制备的包埋维生素c的胶体囊在不同贮藏条件下活性成分的稳定性结果)。
60.实施例2
61.一种包埋茶多酚的胶体囊的制备方法,包括如下步骤:
62.(1)分别将0.25g海藻酸和0.1gλ
‑
型卡拉胶加入至10g纯水中,于室温下搅拌,得到澄清透明的海藻酸/卡拉胶混合溶液;将0.5g茶多酚加入至10g冰醋酸水溶液(0.2%,w/v)中,于室温下避光搅拌,得到茶多酚溶液;
63.(2)分别将0.15g改性纳米碳酸钙和0.1g司盘20加入至6.75g蓖麻油中,于55℃恒温水浴中充分搅拌,得到含有改性纳米碳酸钙和司盘20的蓖麻油分散液;
64.(3)在1500rpm的搅拌下向所述含改性纳米碳酸钙颗粒和司盘20的蓖麻油分散液中逐滴加入2.2g海藻酸/卡拉胶混合溶液,于55℃下搅拌10min,随后加入0.5g茶多酚溶液,继续搅拌15min使其充分乳化,制备得改性纳米碳酸钙颗粒和司盘20稳定的油包水乳浊液;
65.(4)分别将2.7g葡萄糖酸内酯和10mg氯化钾加入至6g纯水中,于室温下搅拌,得到澄清透明的葡萄糖酸内酯/氯化钾混合溶液;
66.(5)向所述乳浊液中逐滴加入0.3g葡萄糖酸内酯/氯化钾混合溶液,于55℃下连续搅拌40min,充分物理交联,形成包埋茶多酚的胶体囊乳浊液;
67.(6)向所述胶体囊乳浊液中,加入无水乙醇反复清洗3次,最终得到包埋茶多酚的胶体囊,随后将包埋茶多酚的胶体囊真空干燥24h后储存于4℃冰箱内,至此,包埋茶多酚的胶体囊制备完成。
68.性能表征:
69.(1)扫描电镜,测试方法与实施例1相同,扫描电镜结果显示,实施例2制备得到的包埋茶多酚的胶体囊的球形度良好,并且其表面分布着较为密集的改性纳米碳酸钙胶体粒子。
70.(2)包封率和负载量,测试方法与实施例1相同,经测定,胶体囊中茶多酚的包封率和负载量分别为95.2%和6.0%。
71.(3)稳定性,测试方法与实施例1相同,经测定,在贮藏5周后,胶体囊中茶多酚在4℃和30℃下的保留率分别为98.5%和94.9%;在贮藏5周后,胶体囊中茶多酚在相对湿度85%和65%下的保留率分别为98.3%和98.6%;在贮藏5周后,胶体囊中茶多酚在避光和自然光照下的保留率分别为98.6%和96.7%。
72.实施例3
73.一种包埋低聚原花青素的胶体囊的制备方法,包括如下步骤:
74.(1)分别将0.15g海藻酸和0.2gκ
‑
型卡拉胶加入至10g纯水中,于室温下搅拌,得到澄清透明的海藻酸/卡拉胶混合溶液;将2.2g低聚原花青素加入至10g冰醋酸水溶液(0.1%,w/v)中,于室温下避光搅拌,得到低聚原花青素溶液;
75.(2)分别将0.12g改性纳米碳酸钙和0.08g聚甘油蓖麻醇酯加入至6.75g蓖麻油中,
于52℃恒温水浴中充分搅拌,得到含有改性纳米碳酸钙和聚甘油蓖麻醇酯的蓖麻油分散液;
76.(3)在1500rpm的搅拌下向所述含改性纳米碳酸钙颗粒和聚甘油蓖麻醇酯的蓖麻油分散液中逐滴加入2.2g海藻酸/卡拉胶混合溶液,于52℃下搅拌10min,随后加入0.5g低聚原花青素溶液,继续搅拌15min使其充分乳化,制备得改性纳米碳酸钙颗粒和聚甘油蓖麻醇酯稳定的油包水乳浊液;
77.(4)分别将1.8g葡萄糖酸内酯和18mg氯化钾加入至6g纯水中,于室温下搅拌,得到澄清透明的葡萄糖酸内酯/氯化钾混合溶液;
78.(5)向所述乳浊液中逐滴加入0.3g葡萄糖酸内酯/氯化钾混合溶液,于52℃下连续搅拌40min,充分物理交联,形成包埋低聚原花青素的胶体囊乳浊液;
79.(6)向所述胶体囊乳浊液中,加入无水乙醇反复清洗3次,最终得到包埋低聚原花青素的胶体囊,随后将包埋低聚原花青素的胶体囊真空干燥24h后储存于4℃冰箱内,至此,包埋低聚原花青素的胶体囊制备完成。
80.性能表征:
81.(1)扫描电镜,测试方法与实施例1相同,扫描电镜结果显示,实施例3制备得到的包埋低聚原花青素的胶体囊的球形度良好,并且其表面分布着较为密集的改性纳米碳酸钙胶体粒子。
82.(2)包封率和负载量,测试方法与实施例1相同,经测定,胶体囊中低聚原花青素的包封率和负载量分别为91.9%和24.7%。
83.(3)稳定性,测试方法与实施例1相同,经测定,在贮藏5周后,胶体囊中低聚原花青素在4℃和30℃下的保留率分别为98.1%和94.2%;在贮藏5周后,胶体囊中低聚原花青素在相对湿度85%和65%下的保留率分别为95.3%和97.9%;在贮藏5周后,胶体囊中低聚原花青素在避光和自然光照下的保留率分别为98.2%和93.3%。
84.申请人声明,上述实例只为说明本发明的技术构思及特点,其目的在于让本领域专业技术人员能够了解本发明的内容并据以实施,并不能以此限制本发明的保护范围。凡根据本发明精神实质所做的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
85.上述实施例仅为本发明的优选实施方式之一,不应当用于限制本发明的保护范围,但凡在本发明的主体设计思想和精神上作出的毫无实质意义的改动或润色,其所解决的技术问题仍然与本发明一致的,均应当包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1