一种用于吸附重金属离子的层状双金属氢氧化物复合体及其制备方法和应用
1.本技术涉及层状双金属氢氧化物复合体技术领域,特别是涉及一种用于吸附重金属离子的层状双金属氢氧化物复合体及其制备方法和应用。
背景技术:
2.随着现代工业的发展,环境污染问题日益严重,其中厂矿企业所排放的污水中存在大量重金属离子,对人类生存环境造成严重威胁。去除生态系统和工业用水中有毒重金属离子成为一个重要环境问题。众多材料,例如沸石、活性炭、聚合物、生物材料和吸附树脂,已经被用来去除或捕获重金属离子,但仍然不能满足重金属离子去除的需求,还需寻找新的高效去除重金属离子的材料。
技术实现要素:
3.本技术的目的在于提供一种用于吸附重金属离子的层状双金属氢氧化物复合体,以至少实现对汞离子和铜离子的高效吸附。
4.本技术第一方面提供了一种用于吸附重金属离子的层状双金属氢氧化物复合体,其包括钼硫化物和镁铝层状双金属氢氧化物,其中,所述钼硫化物mo3s
132
‑
插入镁铝层状双金属氢氧化物的层间。
5.本技术第二方面提供了本技术第一方面的层状双金属氢氧化物复合体的制备方法,其通过(nh4)2mo3s
13
·
h2o和mgal
‑
no3‑
ldh在n,n
’‑
二甲基甲酰胺或二甲亚砜中反应得到。
6.本技术第三方面提供了一种重金属吸附材料,其包括本技术第一方面的层状双金属氢氧化物复合体。
7.本技术提供的层状双金属氢氧化物复合体,层状双金属氢氧化物(ldh)层板的良好分散能力,使位于层间的mo3s
132
‑
的mo、s吸附位点充分暴露出来,提高了对hg
2+
的捕获能力,吸附量达到594mg/g,且具有很高的吸附选择性;进一步,本技术的层状双金属氢氧化物复合体对铜离子和铅离子也具有高效吸附能力,是一种优秀的重金属吸附材料。
附图说明
8.为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一种实施方式,对于本领域普通技术人员来讲,还可以根据这些附图获得其他的实施方式。
9.图1为(nh4)2mo3s
13
、mgal
‑
no3‑
ldh和mgal
‑
mo3s
13
‑
ldh的红外吸收光谱图。
10.图2为mgal
‑
mo3s
13
‑
ldh、mgal
‑
no3‑
ldh和(nh4)2mo3s
13
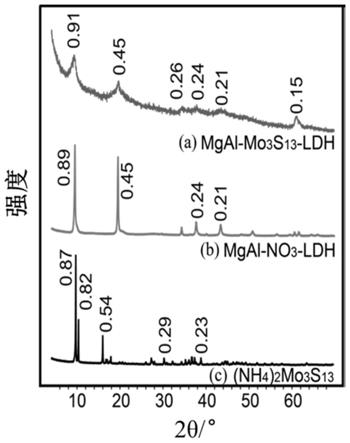
的xrd图谱。
11.图3显示了(nh4)2mo3s
13
和mgal
‑
mo3s
13
‑
ldh的拉曼光谱图。
12.图4为吸附400ppm汞离子前后mgal
‑
mo3s
13
‑
ldh固体样品的sem照片。
13.图5为mgal
‑
mo3s
13
‑
ldh对hg
2+
的吸附动力学曲线:其中(a)图为浓度
‑
时间曲线;(b)图为去除率
‑
时间曲线;(c)图为吸附量
‑
时间曲线;(d)图为拟二级动力学拟合曲线。
具体实施方式
14.为使本发明的目的、技术方案、及优点更加清楚明白,以下参照附图并举实施例,对本发明进一步详细说明。显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。本领域普通技术人员基于本技术中的实施例所获得的所有其他实施例,都属于本技术保护的范围。
15.本技术第一方面提供了一种用于吸附重金属离子的层状双金属氢氧化物复合体(mgal
‑
mo3s
13
‑
ldh),其包括钼硫化物和镁铝层状双金属氢氧化物,其中,所述钼硫化物mo3s
132
‑
插入镁铝层状双金属氢氧化物的层间。
16.在一些实施方式中,所述重金属离子选自hg
2+
、cu
2+
或pb
2+
中的至少一种。
17.在一些实施方式中,所述层状双金属氢氧化物复合体具有如下的化学组成式:mg
0.67
al
0.33
(oh)2(no3)
x
(mo3s
13
)
y
·
mh2o,其中x=0.09
‑
0.21,y=0.06
‑
0.12,m=0.7
‑
1.5。
18.在一些实施方式中,所述的层状双金属氢氧化物复合体具有六边形形貌。
19.本技术第二方面提供了本技术第一方面的层状双金属氢氧化物复合体的制备方法,其通过(nh4)2mo3s
13
·
h2o和mgal
‑
no3‑
ldh在n,n
’‑
二甲基甲酰胺或二甲亚砜中反应得到。
20.具体地,所述层状双金属氢氧化物复合体的制备方法可以包括:将(nh4)2mo3s
13
·
h2o溶解于n,n
’‑
二甲基甲酰胺(dmf)或二甲亚砜(dmso)中,将镁铝硝酸根型层状双氢氧化物(mgal
‑
no3‑
ldh)投入其中,在隔绝空气的环境下,静置反应20
‑
30小时,过滤,洗涤,得到钼硫化物层状双金属氢氧化物复合体沉淀。在此过程中,mo3s
132
‑
通过与mgal
‑
no3‑
ldh层间的no
3ˉ
发生离子交换插入镁铝层状双金属氢氧化物的层间。
21.本技术中,钼硫化物层状双金属氢氧化物复合体可在常温常压下进行,为避免空气中的二氧化碳进入反应体系,生成镁铝碳酸根型层状双氢氧化物,因此本技术的钼硫化物层状双金属氢氧化物复合体的合成过程需要在隔绝空气的环境下进行。
22.在一些实施方式中,所述(nh4)2mo3s
13
·
h2o与mgal
‑
no3‑
ldh的质量比为(1.5
‑
2):1。
23.在一些实施方式中,(nh4)2mo3s
13
·
h2o与n,n
’‑
二甲基甲酰胺或二甲亚砜的质量体积比为0.25
‑
0.5mg/ml。
24.在一些实施方式中,还包括将反应得到的产物在n,n
’‑
二甲基甲酰胺或二甲亚砜中洗涤至滤液无色,再以丙酮洗涤。
25.本技术对(nh4)2mo3s
13
·
h2o的来源不做限定,可以通过市售获得或通过现有的合成方法获得,例如可以通过采用(nh4)6mo7o
24
.4h2o、(nh4oh)
·
hcl和(nh4)2s
x
反应获得。
26.本技术对mgal
‑
no3‑
ldh的来源不做限定,可以通过市售获得或通过现有的合成方法获得,例如可以通过均匀沉淀法,通过mg(no3)2·
6h2o、al(no3)3·
9h2o通过均匀沉淀反应获得mgal
‑
co3‑
ldh;再通过离子交换法合成mgal
‑
no3‑
ldh。
27.本技术第三方面提供了一种重金属吸附材料,其包括本技术第一方面的层状双金
属氢氧化物复合体。
28.以下,基于实施例对本技术进行具体地说明,但本技术并不限于这些实施例。
29.实施例1mgal
‑
mo3s
13
‑
ldh的制备
30.1.mgal
‑
no3‑
ldh的合成
31.采用均匀沉淀法合成mgal
‑
co3‑
ldh前体:将3.21g mg(no3)2·
6h2o、3.24g al(no3)3·
9h2o、2.28g六次甲基四胺(hmt)和50ml去离子水加入反应釜中,放入干燥箱中,在140℃下反应24h,取出冷却至室温后,过滤并用蒸馏水洗涤多次,滤液为淡黄色,将固体置烘箱中40℃干燥,得到白色粉末mgal
‑
co3‑
ldh。
32.采用酸盐(nano3+hno3)离子交换法合成mgal
‑
no3‑
ldh:将1.00gmgal
‑
co3‑
ldh、100g nano3、0.36ml浓硝酸和煮沸排气的1000ml去离子水加入锥形瓶中,用塞子塞好后,再用封口膜封好,室温搅拌24h。立即过滤,用去离子水和丙酮洗涤多次,40℃真空干燥,得到白色粉末mgal
‑
no3‑
ldh。
33.2.(nh4)2mo3s
13
·
h2o的合成
34.在20ml衬聚四氟乙烯内胆的不锈钢反应釜中,放入0.4g(nh4)6mo7o
24
.4h2o、0.3g(nh4oh)
·
hcl和9ml(nh4)2s
x
,220℃反应,过滤,用水、丙酮多次洗涤,干燥,得到0.55g深红色针状晶体(nh4)2mo3s
13
·
h2o。
35.3.mgal
‑
mo3s
13
‑
ldh的合成
36.称0.078g(nh4)2mo3s
13
·
h2o于研钵中研磨成粉末状,放入烧杯中。分批次向烧杯中加入共300ml的dmf,搅拌,超声,使固体完全溶解,离心得到澄清深红色溶液。将0.05g mgal
‑
no3‑
ldh白色粉末投入上述含(nh4)2mo3s
13
的dmf溶液中,塞好塞子,封口膜密封,室温静置反应24h。反应后溶液依然为深红色,过滤,滤液澄清为浅红色,并用dmf洗涤固体至滤液基本无色(洗涤目的为去掉不溶或反应过程析出的部分(nh4)2mo3s
13
),再用少量丙酮洗涤,得到棕红色固体沉淀0.60g。
37.mgal
‑
mo3s
13
‑
ldh的表征
38.1.mgal
‑
mo3s
13
‑
ldh组成的确定
39.取实施例1获得的mgal
‑
mo3s
13
‑
ldh棕红色粉末0.01g,用硝酸溶解,定容至50ml,溶液呈淡黄色,取出6ml清液,通过电感耦合等离子体发射光谱(icp)分析和chn元素分析测试,获得各元素的质量百分含量,结果如表1所示,其中,n元素的质量含量为1.66%,说明层间还有一部分no
3 ̄
;mo元素的质量含量较高,说明mo3s
132
‑
成功进入复合体。根据表1中各元素质量含量的测量值,以及层板正电荷和层间阴离子的电荷匹配的原则,可推算复合体的组成式为mg
0.67
al
0.33
(oh)2(no3)
0.19
(mo3s
13
)
0.07
·
0.8h2o。根据该组成式,可计算得相对分子质量为134.44。然后据该组成式,计算得各元素质量分数的计算值,结果如表1所示。可见计算值与测量值基本一致,说明组成式推算合理。
40.表1.mgal
‑
mo3s
13
‑
ldh中各元素质量百分含量的测量值和计算值
[0041] mgalhnmo测量值(wt%)11.456.902.701.6614.11计算值(wt%)11.966.632.671.9814.99
[0042]
2.红外吸收光谱分析
[0043]
(nh4)2mo3s
13
·
h2o、mgal
‑
no3‑
ldh和mgal
‑
mo3s
13
‑
ldh的红外吸收光谱分析结果如
图1所示,其中,(a)中的547和505cm
‑1处的吸收峰是(nh4)2mo3s
13
的mo
‑
s振动吸收。(b)中,3540、3456cm
‑1的宽吸收峰属于结晶水的羟基(
‑
oh)振动峰和m
‑
oh的伸缩振动峰,其中m代表mg或al,1384cm
‑1处的峰为层间no3‑
的振动吸收,676和438cm
–1处的吸收归属于ldh层板的m
‑
o的振动。(c)中,1384cm
‑1处的特征吸收峰强度明显减弱,说明mo3s
132
‑
与no3‑
交换进入层间,成功得到mgal
‑
mo3s
13
‑
ldh。
[0044]
3.x
‑
射线粉末衍射分析
[0045]
mgal
‑
mo3s
13
‑
ldh、mgal
‑
no3‑
ldh和(nh4)2mo3s
13
的x
‑
射线粉末衍射(xrd)分析结果如图2所示。从(a)中可以看出,mgal
‑
mo3s
13
‑
ldh谱图基线平稳,在0.91、0.45nm出现衍射峰,层间距为0.91nm。与前体(nh4)2mo3s
13
(c)相比,mgal
‑
mo3s
13
‑
ldh(a)在0.87、0.82、0.54nm的衍射峰消失,说明复合体中不存在(nh4)2mo3s
13
前体。mgal
‑
mo3s
13
‑
ldh(a)与mgal
‑
no3‑
ldh(b)相比,层间距由原来的0.89nm增大到0.91nm,说明体积较大的mo3s
132
‑
进入层间。(a)中0.15nm处的峰对应ldh层板上(110)面的衍射,说明ldh层板得到保持,为拓扑的离子交换。
[0046]
4.拉曼光谱分析
[0047]
(nh4)2mo3s
13
和mgal
‑
mo3s
13
‑
ldh的拉曼光谱图分析结果如图3所示。从图中的(a)中可以看出,对于(nh4)2mo3s
13
,550、513、454、387~285cm
‑1处的特征峰分别为(s
‑
s)
端基
、(s
‑
s)
桥连
、mo3‑
s和mo
‑
s的伸缩振动峰;而对于mgal
‑
mo3s
13
‑
ldh(b),相应的拉伸带出现在554、517、458、388~285cm
‑1处,蓝移可能是由于mo3s
132
‑
和ldh中的mo
‑
s
··
ho氢相互作用导致的。
[0048]
5.扫描电镜分析
[0049]
mgal
‑
mo3s
13
‑
ldh扫描电镜(sem)照片如图4所示,其中(a)图为所合成的mgal
‑
mo3s
13
‑
ldh样品,可见其为明显的六边形状,样品直径约4μm,且呈现超薄的纳米片结构。(b)图为吸附400ppm汞离子后的mgal
‑
mo3s
13
‑
ldh样品sem图,可见其大小和形貌变化不大,但有少许堆叠,基本保持六边形形貌。
[0050]
mgal
‑
mo3s
13
‑
ldh对重金属离子的吸附实验
[0051]
1.mgal
‑
mo3s
13
‑
ldh对hg
2+
吸附性能
[0052]
分别称取5份0.020g mgal
‑
mo3s
13
‑
ldh于50ml离心管中,向各离心管中加入20ml具有不同浓度hg
2+
的硝酸盐溶液(浓度见表2中c0),密封离心管,振荡24h。离心,转速15000r/min,静置,取清液,进行电感耦合原子发射光谱仪(icp
‑
aes)测试,得到mgal
‑
mo3s
13
‑
ldh对hg
2+
的吸附结果如表2所示。
[0053]
表2.mgal
‑
mo3s
13
‑
ldh对hg
2+
的最大吸附量测定
[0054][0055]
从表2可以看出,在初始浓度c0在~10ppm(9.37ppm)时,吸附后hg
2+
浓度c
f
可低至0.006ppm(6ppb),hg
2+
去除率高达99.93%。在hg
2+
初始浓度为594ppm时,hg
2+
去除率仍高达99.99%,可认为实现完全吸附,此时对应的最大吸附量q
m
为594mg/g。此高的吸附量说明本材料在吸附剧毒性hg
2+
方面具有重要应用价值。此外,在10
‑
600ppm浓度范围,本技术的mgal
‑
mo3s
13
‑
ldh对汞离子吸附的分配系数k
d
在106~107ml/g,说明本技术的mgal
‑
mo3s
13
‑
ldh对高浓度、低浓度hg
2+
环境均具有非常好的选择性吸附效果。
[0056]
2.mgal
‑
mo3s
13
‑
ldh对hg
2+
的吸附动力学
[0057]
分别称量6份0.02g mgal
‑
mo3s
13
‑
ldh,加入到50ml离心管中,向各离心管加入20ml hg
2+
浓度约为10ppm的硝酸盐溶液,密封离心管,放在振荡器中分别震荡1、5、10、60、180和360min,震荡结束后,离心,然后取上清液进行icp
‑
aes测试。结果如表3所示。
[0058]
表3.mgal
‑
mo3s
13
‑
ldh对hg
2+
的动力学吸附数据
[0059][0060]
从表3的数据可以发现,mgal
‑
mo3s
13
‑
ldh对hg
2+
吸附速率非常快。在10min内,hg
2+
的去除率达到91.48%,k
d
为1.07
×
104ml/g。在60min(1h)内,hg
2+
去除率>99%(99.72%),k
d
值>105ml/g。
[0061]
为了更好地了解hg
2+
在mgal
‑
mo3s
13
‑
ldh上的吸附速率和速率控制步骤,采用拟一级(式1)和拟二级(式2)动力学方程对实验数据进行拟合。
[0062]
拟一级吸附动力学模型:
[0063]
ln(q
e
‑
q
t
)=lnq
e
‑
k1t
ꢀꢀꢀ
(式1)
[0064]
其中,q
e
(mg/g)为平衡时的吸附量,q
t
为接触时间t时的吸附量,k1(g
·
mg
‑1·
min
‑1)为拟一级动力学模型中的速率常数。
[0065]
拟二级吸附动力学模型:
[0066][0067]
其中,q
e
(mg/g)为平衡时的吸附量,q
t
为接触时间t时的吸附量,k2(g
·
mg
‑1·
min
‑1)为拟二级动力学模型中的速率常数。
[0068]
吸附hg
2+
动力学数据及拟合曲线如图5所示,其中图(a)为浓度
‑
时间曲线;(b)图为去除率
‑
时间曲线;(c)图为吸附量
‑
时间曲线;(d)图为拟二级动力学拟合曲线。采用拟二级吸附动力学模型拟合的动力学参数见表4,可见相关系数(r2)接近1(0.9999),表明该吸附过程符合拟二级模型,即该吸附过程符合形成强的金属
‑
硫键(m
‑
s)的假定。
[0069]
表4.mgal
‑
mo3s
13
‑
ldh对hg
2+
的拟二级动力学模型吸附参数
[0070][0071]
3.mgal
‑
mo3s
13
‑
ldh对hg
2+
及竞争离子的吸附选择性
[0072]
为检测竞争离子存在下mgal
‑
mo3s
13
‑
ldh对hg
2+
的吸附选择性,进行了对混合离子的吸附实验。取10mg mgal
‑
mo3s
13
‑
ldh于50ml离心管中,向离心管中加入20ml含有浓度分别为10ppm的co
2+
、ni
2+
、cu
2+
、zn
2+
、ag
+
、pb
2+
、cd
2+
、hg
2+
八种金属离子的硝酸盐溶液,密封离心管,振荡24h。离心,转速15000r/min,静置,取上清液,icp
‑
aes法检测溶液中各金属离子的含量,结果如表5所示。
[0073]
表5 mgal
‑
mo3s
13
‑
ldh对八种金属离子混合溶液的吸附数据
[0074][0075][0076]
一般,k
d
值在104‑
105ml/g的材料被视作优良吸附剂。由表5可见,mgal
‑
mo3s
13
‑
ldh对ag
+
、hg
2+
、cu
2+
有较好的选择吸附效果,分配系数k
d
分别为1.4
×
107、1.9
×
105、6.3
×
104ml/g,均大于104ml/g;此外,mgal
‑
mo3s
13
‑
ldh对pb
2+
也有一定吸附力。因此,本技术的mgal
‑
mo3s
13
‑
ldh可实现重金属离子hg
2+
、cu
2+
、和pb
2+
的共同吸附,达到一材多用的效果。发明人还意外地发现,四种过渡金属离子co
2+
,ni
2+
,cu
2+
,zn
2+
中,mgal
‑
mo3s
13
‑
ldh只对cu
2+
有很高的选择吸附性,可实现过渡金属中cu
2+
的高效分离提取。
[0077]
以上所述仅为本发明的较佳实施例而已,并非用于限定本发明的保护范围。凡在本发明的精神和原则之内所作的任何修改、等同替换、改进等,均包含在本发明的保护范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1