用于下一代测序库制备的微流控珠粒捕获装置和方法与流程
1,000,000 个之间的柱。在一些实施例中,柱从腔室的顶部或底部延伸。在一些实施例中,柱桥接腔室的顶部和底部。在一些实施例中,至少入口通道包括 1 至约 1,000,000 个之间的柱。
7.在一些实施例中,微流控芯片包括一个处理管道。在一些实施例中,微流控芯片包括 2 至 50 个之间的可独立操作的处理管道。在一些实施例中,微流控芯片包括 2 至 20 个之间的可独立操作的处理管道。
8.本公开的第二方面是包括具有两个或更多个腔室的处理管道的微流控芯片,其中两个或更多个腔室中的任意两个相邻腔室通过传递通道彼此流体地耦合,并且其中两个或更多个腔室中的至少一个包括多个珠粒;其中两个或更多个腔室中的第一个的壁的一部分包括与入口通道流体连通的第一孔口;两个或更多个腔室中的第二个的壁的一部分包括与出口通道流体连通的第二孔口;并且其中两个或更多个腔室中的至少一个包括与导管流体连通的导管开口;其中第一孔口和第二孔口小于两个或更多个腔室中的至少一个内的多个珠粒的平均直径,并且其中导管开口大于两个或更多个腔室中的至少一个内的多个珠粒的平均直径。在一些实施例中,微流控芯片不包括机械运动部分。在一些实施例中,微流控芯片包含非磁性材料。在一些实施例中,多个珠粒为非磁性珠粒。
9.在一些实施例中,传递管道包括蛇形形状。在一些实施例中,传递通道具有大于多个珠粒的平均直径的横截面高度和宽度。在一些实施例中,多个珠粒可流动通过传递管道。
10.在一些实施例中,处理管道包括两个腔室。在一些实施例中,两个腔室通过蛇形通道彼此流体地耦合。在一些实施例中,多个珠粒通过蛇形传递通道从第一腔室流动到第二腔室。
11.在一些实施例中,处理管道包括三个腔室。在一些实施例中,三个腔室中的第一个与入口通道流体地耦合,三个腔室的中间(第二)个通过两个传递通道与第一腔室和第三腔室中的每一个流体地耦合,并且第三腔室与出口通道流体地耦合。
12.在一些实施例中,两个或更多个腔室各自包括 1 至约 1,000,000 个之间的柱。在一些实施例中,柱从腔室的顶部或底部延伸。在一些实施例中,至少入口通道包括 1 至约 1,000,000 个之间的柱。在一些实施例中,两个或更多个腔室各自包括范围在约 0.1
µ
l 至约 5ml 范围内的体积。在一些实施例中,体积在约 0.1ml 至约 1ml 之间的范围内。
13.在一些实施例中,微流控芯片包括一个处理管道。在一些实施例中,微流控芯片包括 2 至 50 个之间的可独立操作的处理管道。在一些实施例中,微流控芯片包括 2 至 20 个之间的可独立操作的处理管道。
14.本公开的第三方面是获得用于测序的靶核酸序列群的方法,该方法包括:(a) 将获得的基因组样品片段化以提供核酸片段群;(b) 将寡核苷酸探针池引入核酸片段群以形成靶-探针复合物,其中寡核苷酸探针池包括能够与核酸片段群内的互补核酸序列杂交的参考核酸序列,并且其中寡核苷酸探针包括一对特异性结合实体中的第一成员;(c) 使包括形成的靶-探针复合物的溶液流过微流控芯片的处理管道,其中处理管道包括腔室,该腔室包括多个珠粒,其中该多个珠粒用特异性结合实体对中的第二成员功能化;(d) 使至少一种缓冲液流过处理管道以去除脱靶片段;以及 (e) 使至少一种试剂流过处理管道以获得靶核酸序列。在一些实施例中,第一部分为生物素。在一些实施例中,第二部分为链霉亲和素。
15.在一些实施例中,至少一种缓冲剂的流动依次重复至少两次。在一些实施例中,至少一种缓冲剂的流动依次重复至少三次。在一些实施例中,每一种依次流动的缓冲剂是相同的。在一些实施例中,每一种依次流动的缓冲剂是不同的。
16.在一些实施例中,至少一种试剂是温度在约 80℃ 至约 105℃ 范围内的缓冲剂。在一些实施例中,至少一种试剂是缓冲剂,并且其中处理管道被加热到约 90℃ 至约 100℃ 范围内的温度。在一些实施例中,试剂为酶。
17.在一些实施例中,该方法进一步包括在获得的基因组样品片段化之后,将衔接子连接至核酸片段群。在一些实施例中,该方法进一步包括对靶核酸序列群进行测序。
18.在一些实施例中,多个珠粒为非磁性珠粒。在一些实施例中,微流控芯片不包括机械运动部分。在一些实施例中,微流控芯片包含非磁性材料。
19.在本公开的第四方面是获得用于测序的靶核酸序列群的方法,该方法包括:(a) 将寡核苷酸探针池引入获得的基因组样品以形成靶-探针复合物,其中寡核苷酸探针池包括能够与获得的基因组样品内的互补核酸序列杂交的参考核酸序列,并且其中寡核苷酸探针包括一对特异性结合实体中的第一成员;(b) 使包含形成的靶-探针复合物的溶液流过微流控芯片的处理管道,其中该处理管道包括腔室,该腔室包括多个珠粒,其中该多个珠粒用特异性结合实体对中的第二成员官能化;(c) 使至少一种流体流过处理管道以去除脱靶核酸;以及 (d) 使至少一种试剂流过处理管道以获得靶核酸序列。
20.在一些实施例中,第一部分为生物素。在一些实施例中,第二部分为链霉亲和素。
21.在一些实施例中,获得的基因组样品是源自哺乳动物受试者(例如人受试者)的样品。在一些实施例中,获得的基因组样品是从哺乳动物受试者(例如人受试者)获得的血液样品或血浆样品。在一些实施例中,获得的基因组样品是无细胞核酸的形式(例如,具有约 180 bp 至约 150 bp 范围内的大小)。在一些实施例中,获得的无细胞核酸形式的基因组样品包括 dna 和/或 rna。
22.在一些实施例中,该方法进一步包括在引入寡核苷酸探针池之前将获得的基因组样品片段化。
23.在一些实施例中,至少一种流体的流动依次重复至少两次。在一些实施例中,至少一种流体的流动依次重复至少三次。在一些实施例中,每一种依次流动的流体是相同的。在一些实施例中,每一种依次流动的流体是不同的。在一些实施例中,至少一种流体为缓冲剂。
24.在一些实施例中,至少一种试剂为尿嘧啶特异性切除试剂酶。在一些实施例中,至少一种试剂是温度在约 80℃ 至约 105℃ 范围内的缓冲剂。在一些实施例中,至少一种试剂是缓冲剂,并且其中处理管道被加热到约 90℃ 至约 100℃ 范围内的温度。在一些实施例中,试剂为酶。
25.在一些实施例中,多个珠粒为非磁性珠粒。在一些实施例中,微流控芯片不包括机械运动部分。在一些实施例中,微流控芯片包含非磁性材料。
附图说明
26.有关对本公开特征的一般理解,请参考附图。在附图中,整个附图使用相同的附图标记来识别相同的元素。
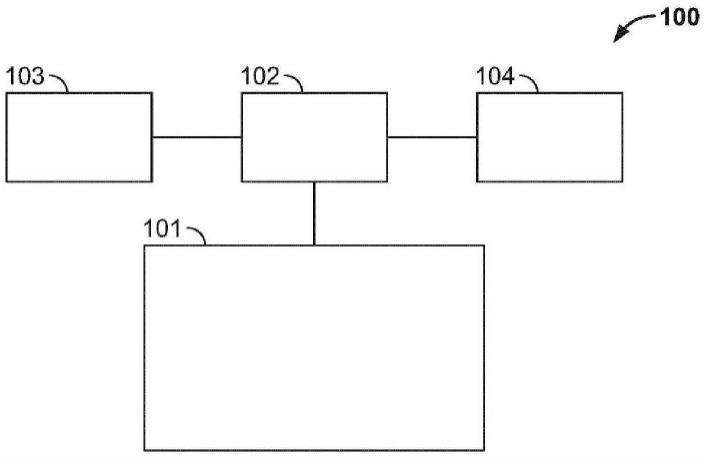
27.图 1a 描绘了根据本公开的一个实施例的包括与流控模块和控制系统连通的微流控芯片的系统。
28.图 1b 描绘了根据本公开的一个实施例的包括微流控芯片的系统,该微流控芯片包括与流控模块和控制系统连通的多个可独立操作的处理管道。
29.图 1c 描绘了根据本公开的一个实施例的包括微流控芯片的系统,该微流控芯片包括处理管道,其中该处理管道与泵、多个流体和/或试剂贮存器、废液/试剂容器、靶标收集容器和一个或多个管道连通。
30.图 1d 描绘了根据本公开的一个实施例的具有堆叠构造的多个可独立操作的处理管道的微流控芯片。
31.图 1e 描绘了根据本公开的一个实施例的包括与两个泵和多个流体和/或试剂贮存器流体连通的微流控芯片的系统。
32.图 2a 示出了根据本公开的一个实施例的具有流体地耦合到流体入口和流体出口的腔室的处理管道的俯视图。
33.图 2b 示出了根据本公开的一个实施例的具有流体地耦合到流体入口和流体出口的腔室的处理管道的俯视图,其中至少该腔室包括一个或多个柱。
34.图 2c 示出了图 2a 的处理管道的侧剖视图。
35.图 2d 提供了根据本公开的一个实施例的具有流体地耦合到流体入口和流体出口的腔室的处理管道的侧视图。
36.图 2e 提供了图 2d 的处理管道的腔室的放大图。
37.图 2f 提供了根据本公开的一个实施例的具有允许流体流动的开口的腔室壁的侧剖视图。
38.图 2g 描绘了具有包括多个珠粒的腔室的微流控芯片的侧剖视图,其中珠粒的直径大于腔室的一个或多个壁内的一个或多个孔口。
39.图 2h 描绘了根据本公开的一个实施例的处理管道的腔室的剖视图,该处理管道具有从腔室顶部和/或腔室底部之一延伸的一个或多个柱。
40.图 2i 提供了根据本公开的一个实施例的处理管道的腔室的剖视图,该处理管道具有桥接腔室顶部和腔室底部的一个或多个柱。
41.图 3a 示出了根据本公开的一个实施例的具有流体地耦合到流体入口和流体出口的腔室的处理管道。
42.图 3b 示出了根据本公开的一个实施例的具有流体地耦合到流体入口和流体出口的腔室的处理管道,其中至少该腔室包括一个或多个柱。
43.图 4a 示出了根据本公开的一个实施例的具有流体地耦合到流体入口和流体出口的腔室的处理管道。
44.图 4b 示出了根据本公开的一个实施例的具有流体地耦合到流体入口和流体出口的腔室的处理管道,其中至少该腔室包括一个或多个柱。
45.图 4c 示出了图 4a 的处理管道的侧剖视图。
46.图 5a 示出了根据本公开的一个实施例的具有通过传递通道彼此流体地耦合的两个腔室的处理管道,其中该两个腔室与流体入口和流体出口流体连通。
47.图 5b 示出了图 5a 的微流控芯片的侧剖视图。
48.图 6a 示出了根据本公开的一个实施例的具有通过蛇形传递通道彼此流体地耦合的两个腔室的处理管道,其中该两个腔室与流体入口和流体出口流体连通。
49.图 6b 示出了图 6a 的微流控芯片的侧剖视图。
50.图 7a 描绘了包括多个可独立操作的处理管道的微流控芯片,其中每一个处理管道与流体入口和流体出口流体连通。
51.图 7b 描绘了根据本公开的一个实施例的包括多个可独立操作的处理管道的微流控芯片,其中每一个处理管道与流体入口和流体出口流体连通,其中至少该处理管道的腔室被示出为包括一个或多个柱。
52.图 7c 描绘了根据本公开的一个实施例的包括多个可独立操作的处理管道的微流控芯片,其中每一个处理管道与流体入口和流体出口流体连通,其中至少该处理管道的腔室被示出为包括一个或多个柱。
53.图 7d 描绘了包括多个可独立操作的处理管道的微流控芯片,其中每一个处理管道包括两个腔室并且其中该两个腔室通过蛇形传递通道彼此流体地耦合。
54.图 8a 阐述了提供使用本公开的微流控装置纯化一种或多种类型的分子的方法的流程图。
55.图 8b 阐述了提供使用本公开的微流控装置纯化一种或多种类型的分子的方法的流程图。
56.图 9 阐述了示出根据本公开的一个实施例的富集具有靶分子的溶液的方法的流程图。
57.图 10 提供了在流过本公开的微流控装置之后收集的流体的电泳图。
58.图 11a 示出了与生物素化寡核苷酸杂交的靶分子的珠粒捕获和温度介导释放的方法。
59.图 11b 示出了当流体流过微流控装置 (ft) 时、在一种或多种洗涤溶液流过微流控装置 (w) 之后以及在收集洗脱液 (e) 之后回收的靶标的量(由定量聚合酶链反应 (qpcr) 确定)。
60.图 12a 示出了与尿嘧啶连接的生物素化寡核苷酸杂交的靶分子的珠粒捕获和酶释放的方法。
61.图 12b 示出了当流体流过微流控装置 (ft) 时、在一种或多种洗涤溶液流过微流控装置 (w) 之后以及在收集洗脱液 (e) 之后回收的靶标的量(由 qpcr 确定)。
具体实施方式
62.还应该理解的是,除非指明是相反情况,否则在本文所要求保护的包括一个以上步骤或动作的任何方法中,所述方法的所述步骤或动作的顺序不必限于表述所述方法的所述步骤或动作的所述顺序。
63.说明书中对“一个实施例”、“实施例”、“说明性实施例”等的引用表示所描述的实施例可以包括特定特征、结构或特性,但是每个实施例可以必定或可以不一定包括该特定特征、结构或特性。此外,这种短语并不必然指相同实施例。此外,当结合实施例描述具体特征、结构或特性时,需要注意的是,无论是否明确说明,本领域技术人员均知晓结合其他实施例来实现上述特征、结构或特性的效果。
64.如本文所用,除非上下文另有明确指示,否则单数形式“一 (a/an)”和“该/所述”包括复数个指代物。同样,除非上下文另有明确指示,否则词语“或”旨在包括“和”。术语“包括”定义为包容性,如“包括 a 或 b”是指包括 a、b 或 a 和 b。
65.如本文在说明书和权利要求书中所用,“或”应理解为与上文定义的“和/或”具有相同的含义。例如,在分隔列表中的项目时,“或”或“和/或”应解释为具有包容性,例如,若干元素或元素列表中的至少一个元素,但也包含一个以上元素,以及任选地包含额外的未列出的项目。只有指明与之相反的术语,如“仅其中之一”或“恰好其中之一”,或者在权利要求中使用的“由
…
组成”,将指包含若干元素或元素列表中的恰好一个元素。一般来说,本文使用的术语“或者”只有在前面有“或”、“其中之一”、“只有一个”或“恰好一个”等排他性术语时,才应解释为表示排他性的替代选择(例如,“一个或另一个,但不是两个”)。在权利要求书中使用的“基本上由...组成”应具有在专利法领域使用的普通含义。
[0066]“包括”、“包含”、“具有”等术语可互换使用,且含义相同。类似地,“包括”、“包含”、“具有”等可互换使用并且具有相同的含义。具体而言,每个术语的定义都与普通美国专利法对“包括”的定义一致,因此每个术语都可理解为一个开放性术语,其含义为“至少以下”,并且也可理释为不排除额外的特征、限制、方面等。因此,例如“具有组件 a、b 和 c 的装置”是指所述装置至少包括组件 a、b 和 c。同样,短语:“涉及步骤 a、b 和 c 的方法”是指所述方法至少包括步骤 a、b 和 c。此外,尽管本文可以特定的顺序概述步骤和过程,但是本领域技术人员将认识到,所述顺序步骤和过程可能会有所不同。
[0067]
如本文在说明书和权利要求书中所用,就一个或多个元素的列表而言,短语“至少一个”应理解为选自元素列表中任何一个或多个元素的至少一个元素,但不一定包括元素列表中具体列出的每个元素中的至少一个,也不排除元素列表中的任何元素组合。除了在短语“至少一个”所涉及的元素列表中具体确定的元素之外,该定义还允许其他元素任选地存在,无论这些元素与具体确定的元素相关与否。因此,作为一个非限制性实例,“a 和 b 中的至少一个”(或者等效地,“a 或 b 中的至少一个”,或者等效地,“a 和/或 b 中的至少一个”)在一个实施例中可以指至少一个任选地包括一个以上的 a,但没有 b(以及选择性地包括 b 以外的元素);在另一个实施例中,指至少一个选择性地包括一个以上的 b,但没有 a(以及选择性地包括 a 以外的元素);在又一个实施例中,指至少一个选择性地包括一个以上的 a,以及至少一个选择性地包括一个以上的 b(以及选择性地包括其他元素)等。
[0068]
如本文所用,术语“抗体”是指表现出所需生物学或结合活性的任何形式的抗体。因此,它以最广泛的含义使用,并且具体涵盖但不限于单克隆抗体(包括全长单克隆抗体)、多克隆抗体、多特异性抗体(例如双特异性抗体)、人源化、完全人抗体、嵌合抗体和骆驼源化单域抗体。
[0069]
如本文所用,术语“抗原”是指可以由特异性体液或细胞免疫的产物(诸如抗体分子或 t 细胞受体)特异性结合的化合物、组合物或物质。抗原可以是任何类型的分子,包括例如:半抗原、简单中间代谢物、糖(例如寡糖)、脂质和激素以及大分子(诸如复合碳水化合物(例如多糖)、磷脂和蛋白质)。
[0070]
如本文所用,术语“通道”是指流体可以流过的微流控芯片内的封闭通道。通道可以具有用于引入流体的一个或多个开口。每一个通道可以包括涂层,例如亲水涂层或疏水涂层。
[0071]
如本文所用,术语“缀合物”是指共价连接至较大构建体的两个或更多个分子(和/或诸如纳米颗粒的材料)。在一些实施例中,缀合物包括共价连接至一个或多个其他分子(诸如一个或多个其他生物分子)的一个或多个生物分子(诸如肽、蛋白质、酶、糖、多糖、脂质、糖蛋白和脂蛋白)。
[0072]
如本文所用,术语“富集”是指相对于处理之前样品中最初存在的分子的总量来增加样品中分子(例如核酸分子)群的相对丰度的过程。因此,富集步骤提供百分比或分数增加,而不是直接增加例如目标核酸序列的拷贝数作为扩增方法,诸如聚合酶链反应。
[0073]
如本文所用,术语“流体”是指任何液体或液体组合物,包括水、溶剂、缓冲剂、溶液(例如极性溶剂、非极性溶剂)和/或混合物。流体可以是含水的或非水的。流体的非限制性实例包括洗涤溶液、漂洗溶液、酸性溶液、碱性溶液、转移溶液和烃(例如烷烃、异烷烃和芳族化合物,诸如二甲苯)。
[0074]
在一些实施例中,洗涤溶液包含表面活性剂以促进洗涤液在载玻片的样本承载表面上的扩散。在一些实施例中,酸溶液包括去离子水、酸(例如乙酸)和溶剂。在一些实施例中,碱性溶液包括去离子水、碱和溶剂。在一些实施例中,转移溶液包括一种或多种二醇醚,例如一种或多种丙烯基二醇醚(例如丙二醇醚、二(丙二醇)醚和三(丙二醇)醚、乙二醇基二醇醚(例如,乙二醇醚、二(乙二醇)醚和三(乙二醇)醚)及其功能类似物。
[0075]
缓冲剂的非限制性示例包括柠檬酸、磷酸二氢钾、硼酸、二乙基巴比妥酸、哌嗪-n,n'-双(2-乙磺酸)、二甲基次胂酸、2-(n-吗啉代)乙磺酸、三(羟甲基)甲胺 (tris)、2-(n-吗啉代)乙磺酸 (taps)、n,n-双(2-羟乙基)甘氨酸 (bicine)、n-三(羟甲基)甲基甘氨酸 (tricine)、4-2-羟乙基-1-哌嗪乙磺酸 (hepes)、2-{[三(羟甲基)甲基]氨基}乙磺酸 (tes) 及其组合。在其他实施例中,缓冲剂可以包含三(羟甲基)甲胺 (tris)、2-(n-吗啉代)乙磺酸 (taps)、n,n-双(2-羟乙基)甘氨酸 (bicine)、n-三(羟甲基)甲基甘氨酸 (tricine)、4-2-羟乙基-1-哌嗪乙磺酸 (hepes)、2-{[三(羟甲基)甲基]氨基}乙磺酸 (tes) 或其组合。美国专利申请公开号 2016/0282374 中描述了额外的洗涤溶液、转移溶液、酸溶液和碱性溶液,其公开内容通过引用整体并入本文。
[0076]
如本文所用,“微流控”是指具有通常以毫米到纳米级制造的一个或多个流体通道、管道或腔室的系统或装置。因此,如本文所用,“微流控装置”是指允许精确控制和操纵流体的任何装置,其在几何上被约束为至少一个维度(宽度、长度、高度)可能小于 1 mm 的结构。在一些实施例中,微流控装置包括微流控芯片,该微流控芯片包括一个或多个通道和/或管道。
[0077]
如本文所用,短语“下一代测序 (ngs)”是指与传统的基于桑格和毛细管电泳的方法相比具有高通量测序的测序技术,其中测序过程并行执行,例如一次产生数千或数百万个相对小的序列读取。下一代测序技术的一些示例包括但不限于边合成边测序、边连接边测序以及边杂交边测序。这些技术产生较短读取(从约 25 至约 500 bp),但在相对短的时间内产生数十万或数百万次读取。术语“下一代测序”是指目前由 illumina、life technologies 和 helicos biosciences 采用的所谓的并行边合成边测序或边连接边测序平台。下一代测序方法还可以包括具有电子检测的纳米孔测序方法(oxford nanopore 和 roche diagnostics)。
[0078]
如本文所用,术语“核酸”是指由传达遗传信息的核苷酸链组成的高分子量生化大
分子。最常见的核酸是脱氧核糖核酸 (dna) 和核糖核酸 (rna)。构建核酸的单体称为核苷酸。每一个核苷酸由三种组分组成:含氮杂环碱基、嘌呤或嘧啶(也称为核碱基)以及戊糖。不同核酸类型在其核苷酸中糖的结构方面不同;dna 含有 2-脱氧核糖,而 rna 含有核糖。
[0079]
如本文所用,术语“多个”是指两个或更多个,例如 3 个或更多个、4 个或更多个、5 个或更多个等。
[0080]
如本文所用,任何两个不同反应性基团(诸如试剂和颗粒的任何两个反应性基团)之间的“反应”可以表示在两个反应性基团(或两个反应性官能团)之间形成共价键;或可以表示两个反应性基团(或两个反应性官能团)彼此缔合、彼此相互作用、彼此杂交、彼此氢键合等。在一些实施例中,“反应”包括结合事件,例如反应性官能团之间的结合事件或一对特异性结合实体中的第一成员和第二成员之间的结合事件。
[0081]
如本文所用,术语“试剂”是指包含一种或多种能够与另一实体共价或非共价反应、偶联、相互作用或杂交的一种或多种试剂的溶液或悬浮液。此类试剂的非限制性实例包括特异性结合实体、抗体(第一抗体、第二抗体或抗体缀合物)、核酸探针、寡核苷酸序列、检测探针、带有反应性官能团或受保护官能团的化学部分、酶、染料或染色剂分子的溶液或悬浮液。
[0082]
如本文所用,“测序”是指用于确定 dna 寡核苷酸中核苷酸碱基、腺嘌呤、鸟嘌呤、胞嘧啶和胸腺嘧啶的顺序的生化方法。如本文中所使用的术语,测序可以包括但不限于平行测序或本领域技术人员已知的任何其他测序方法,例如链终止法、快速 dna 测序法、游走点分析 (wandering-spot analysis)、maxam-gilbert 测序、染料终止剂测序,或使用任何其他现代的自动化 dna 测序仪器。
[0083]
如本文所用,术语“特异性结合实体”是指特异性结合对的成员。特异性结合对是特征在于彼此结合以实质性地排除与其他分子结合的分子对(例如,特异性结合对的结合常数可以比生物学样品中其他分子的结合对的两个成员中的任一者的结合常数大至少 10
3 m-1
、10
4 m-1 或 10
5 m-1
)。特异性结合部分的特定示例包括特异性结合蛋白(例如,抗体、凝集素、链霉亲和素和蛋白 a 等抗生物素蛋白)。特异性结合部分也可以包括由这种特异性结合蛋白特异性结合的分子(或其部分)。
[0084]
如本文所用,术语“基本上”意指展现出目标特征或特性的全部或接近全部范围或程度的定性条件。在一些实施例中,“基本上”意指在约 5% 以内。在一些实施例中,“基本上”意指在约 10% 以内。在一些实施例中,“基本上”意指在约 15% 以内。在一些实施例中,“基本上”意指在约 20% 以内。
[0085]
如本文所用,术语“靶”或“靶序列”是指目标核酸序列,例如与寡核苷酸探针杂交的那些。
[0086]
概述本公开涉及包括具有一个或多个可独立操作的处理管道的微流控芯片的自动化系统。在一些实施例中,自动化系统适用于样品净化和/或靶富集过程,诸如在使用下一代测序对样品进行测序之前进行的样品净化和/或靶富集过程。在一些实施例中,自动化系统还适合于纯化溶液和/或执行固相合成。如本文所述,在一些实施例中,微流控装置不依赖于磁分离过程、利用磁性珠粒和/或包括磁性部件。
[0087]
微流控装置
在本公开的一个方面是微流控装置,该微流控装置包括具有一个或多个可独立操作的处理管道的微流控芯片。参考图 1a 至图 1e,在本公开的一个方面是微流控装置 100,该微流控装置包括流体模块 102、控制系统 104 和微流控芯片 101。
[0088]
在一些实施例中,微流控装置 100 流体地耦合到一个或多个流体和/或试剂贮存器。在一些实施例中,微流控装置 100 进一步与以下项连通:一个或多个传感器、加热和/或冷却模块、和/或上游和/或下游处理系统例如测序装置、用于进行聚合酶链反应的仪器、化学分析仪、检测器等。微流控装置和构成任何微流控装置的组件(例如控制系统、泵、阀等)在本文中进一步详细描述。
[0089]
微流控芯片本公开的微流控装置 100 包括微流控芯片 101,该微流控芯片具有一个或多个可独立操作的处理管道 105。在一些实施例中,微流控芯片 101 包括 1 至 600 个之间的可独立操作的处理管道 105。在其他实施例中,微流控芯片 101 包括 1 至 500 个之间的可独立操作的处理管道 105。在又一些实施例中,微流控芯片 101 包括 1 至 400 个之间的可独立操作的处理管道 105。在进一步实施例中,微流控芯片 101 包括 1 至 300 个之间的可独立操作的处理管道 105。在一些实施例中,微流控芯片 101 包括一个可独立操作的处理管道 105。在其他实施例中,微流控芯片 101 包括两个或更多个可独立操作的处理管道 105。在又一些实施例中,微流控芯片 101 包括三个或更多个可独立操作的处理管道 105。在进一步实施例中,微流控芯片 101 包括五个或更多个可独立操作的处理管道 105。在更进一步的实施例中,微流控芯片 101 包括十个或更多个可独立操作的处理管道 105。
[0090]
在两个或更多个可独立操作的处理管道 105 包括在任何微流控芯片内的那些实施例中,处理单元可以布置在同一平面内。例如,图 1b 示出了彼此平行地布置且布置在同一平面内的三个可独立操作的处理管道 105。同样,图 7a 至图 7d 示出了彼此平行地布置且布置在同一平面中的多个可独立操作的处理管道 105。在其他实施例中,两个或更多个处理管道 105 可以布置在不同平面中。例如,在一些实施例中,两个或更多个可独立操作的处理管道 105 可以在任何微流控芯片 101 内至少部分地彼此堆叠(参见例如图 1d)。
[0091]
技术人员将理解,在一些实施例中,每一个可独立操作的处理管道可以耦合其自己的一组贮存器、管道、泵等。在其他实施例中,两个或更多个可独立操作的处理管道可以耦合到共享流体贮存器和/或共享试剂贮存器。如本文所述,可以通过控制一个或多个阀将来自共享贮存器的流体供应至每一个可独立操作的处理管道,该一个或多个阀设置在贮存器本身内或在将贮存器耦合到可独立操作的处理管道的通道或管道内。同样,可以通过与每一个可独立操作的处理管道流体连通的一个或多个泵的动作将来自共享贮存器的流体供应到可独立操作的处理管道。
[0092]
处理管道本文描述了具有不同配置的可独立操作的处理管道的示例。尽管描述了不同配置,但每一个处理管道用于允许在入口处引入的流体和/或试剂穿过入口通道并进入与入口通道流体连通的一个或多个腔室中。然后允许引入的流体和/或试剂流出一个或多个腔室并流过与其连通的出口通道。最终,流过处理管道的流体和/或试剂在穿过与出口通道流体地耦合的出口之后被收集和/或分析。
0.1
µ
m 至约 5mm 范围内的平均直径。在一些实施例中,珠粒具有约 0.1mm 至约 1mm 范围内的平均直径。在又一些实施例中,珠粒具有约 0.1mm 至约 1mm 范围内的平均直径。
[0100]
在一些实施例中,腔室可以与一个或多个导管流体连通,其有利于从腔室引入和/或去除多个珠粒。在一些实施例中,腔室与两个导管流体连通。在其他实施例中,腔室与三个或更多个导管流体连通。在又一些实施例中,腔室与四个或更多导管流体连通。
[0101]
图 2a、3a 和 4a 描绘了与两个导管 15 流体连通的腔室 14,其中两个导管 15 布置成彼此约 180 度。在一些实施例中,两个导管 15 中的一个被配置成允许引入珠粒,而两个导管 15 中的另一个被配置成允许去除珠粒。在一些实施例中,每一个导管 15 可以与珠粒传递管道、珠粒源(诸如珠粒存储容器或珠粒收集容器)、一个或多个阀和/或一个或多个泵流体连通。
[0102]
在包括两个或更多个腔室的那些实施例中,两个或更多个腔室中的每一个都可以与一个或多个导管流体连通(参见例如图 5a 和 6a)。在一些实施例中,导管包括允许导管关闭的一个或多个门或阀。在一些实施例中,一旦腔室加载有预先加载有预定数量的珠粒,可以关闭导管内的门或阀,使得珠粒密封在腔室内。稍后可以打开门或阀以回收珠粒。
[0103]
参考图 2e,导管 15 可以在腔室 14 的外部。在一些实施例中,腔室 14 的壁 20 可以包括导管开口 22,其允许珠粒从一个或多个导管 15 进入腔室 14。在一些实施例中,导管开口 22 可以具有任何尺寸和/或形状,前提条件是它允许至少一个珠粒进入或离开腔室。
[0104]
在一些实施例中,腔室适于使得任何引入的珠粒可以在腔室内移动但不会离开腔室。参考图 2d 和 2e,在一些实施例中,腔室 15 的壁 20 包括流体和/或试剂可以流过的第一孔口 21a 和第二孔口 21b,但不包括引入腔室 14 的任何珠粒。图 2e 示出了腔室 14 的剖视图,该腔室显示壁 20 和壁内的孔口 21。图 2f 和 2g 示出了处理管道 105 的剖视图并且描绘了多个珠粒 30,每一个珠粒的平均直径“w”小于壁 20 的高度“x”,但大于孔口 21 的高度“y”。以这种方式,流体和/或试剂(以及任何靶分子和/或颗粒)可以从入口通道 12 流过处理管道 105,进入腔室 14,并流出出口通道 13,但其中在流体和/或试剂的流动期间,珠粒 30 保持在腔室 14 内。
[0105]
参考图 2c,在一些实施例中,腔室的高度大于入口通道或出口通道中的至少一个的高度。例如,并且如图 2c 和 4c 所示,腔室 14 的高度“x”可以大于入口通道 12 的高度“y”或出口通道 13 的高度“y”。在一些实施例中,腔室 14 的高度“x”在 0.1
µ
m 至约 10cm 的范围内。在其他实施例中,腔室 14 的高度“x”在 0.1mm 至约 1cm 之间的范围内。在又一些实施例中,腔室 14 的高度“x”在 0.1mm 至约 1mm 之间的范围内。在一些实施例中,出口通道 13 和/或入口通道 12 的高度“x”在 0.1
µ
m 至约 10cm 之间的范围内。在其他实施例中,出口通道 13 和/或入口通道 12 的高度“x”在 0.1mm 至约 1cm 之间的范围内。在又一些实施例中,出口通道 13 和/或入口通道 12 的高度“x”在 0.1mm 至约 1mm 之间的范围内。
[0106]
在两个或更多个通道经由传递通道彼此流体地耦合的那些实施例中,可以允许引入第一腔室的任何珠粒从第一腔室流到一个或多个附加腔室。此外,一旦珠粒从第一腔室流到一个或多个附加腔室中的另一个,可以允许珠粒流回第一腔室。在这些实施例中,与传递通道连通的腔室壁包括孔口,其允许将珠粒从腔室传递到传递通道。替代地,腔室在腔室
与传递通道接合的区域中可以不包括任何壁,其再次允许将珠粒从腔室传递到传递通道。
[0107]
例如,并且参考图 5a,处理管道 105 可以包括:(i) 具有第一壁 20a 的第一腔室 14a,该第一壁包括第一孔口 21a,其中第一壁 20a 与入口通道 12 连通;(ii) 具有第二壁 20b 的第二腔室 14b,该第二壁包括与出口通道 13 连通的第二孔口 21bin;并且其中腔室 14a 和 14b 不包括在与传递通道 18 连通的腔室的那些区域中的壁或壁部分。
[0108]
在一些实施例中,入口通道 12 和出口通道 13 分别可以具有任何尺寸和/或形状。在一些实施例中,入口通道 12 包括线性侧壁,诸如图 2a、2b、3a 和 3b 所描绘的。在其他实施例中,入口通道 12 和出口通道 13 分别包括曲线或弓形侧壁,诸如图 2d、4a 和 4c 所描绘的。
[0109]
在一些实施例中,入口通道 12 和出口通道 13 分别从它们接合腔室的第一宽度到它们分别接合入口 10 和出口 11 的第二宽度逐渐变细。在一些实施例中,入口通道 12 从它接合腔室 14 的第一宽度到它连接入口 10 的第二宽度逐渐变细,其中第一宽度大于第二宽度。例如,图 2a、3a 和 4a 各自描绘了入口通道 12,其宽度从入口 10 到腔室 14 逐渐变细。
[0110]
参考图 2a 和 3a,在一些实施例中,入口通道 12 的宽度“a”在 0.1
µ
m 至约 10cm 的范围内。在其他实施例中,入口通道 12 的宽度“a”在 1mm 至约 10cm 的范围内。在其他实施例中,入口通道 12 的宽度“a”在 1mm 至约 1cm 之间的范围内。在其他实施例中,入口通道 12 的宽度“a”在 1mm 至约 5mm 之间的范围内。在一些实施例中,入口通道 12 的宽度“b”在 0.1
µ
m 至约 10cm 之间的范围内。在其他实施例中,入口通道 12 的宽度“b”在 1mm 至约 10cm 之间的范围内。在其他实施例中,入口通道 12 的宽度“b”在 1mm 至约 1cm 之间的范围内。在其他实施例中,入口通道 12 的宽度“b”在 1mm 至约 5mm 之间的范围内。据信,锥形通道基本上减轻了空气的滞留和/或有助于稳定和/或发展流体分布。
[0111]
在一些实施例中,出口通道 13 从它接合腔室 14 的第一宽度到它接合出口 11 的第二宽度逐渐变细。例如,图 2a、3a 和 4a 各自描绘了出口通道 13,其宽度从腔室 14 到出口 11 逐渐变细。在一些实施例中,出口通道 13 的宽度“a”在 0.1
µ
m 至约 10cm 之间的范围内。在其他实施例中,出口通道 13 的宽度“a”在 1mm 至约 10cm 之间的范围内。在一些实施例中,出口通道 13 的宽度“a”在 1mm 至约 50mm 之间的范围内。在其他实施例中,出口通道 13 的宽度“a”在 1mm 至约 10mm 之间的范围内。在一些实施例中,出口通道 13 的宽度“b”在 0.1um 至约 10cm 之间的范围内。在其他实施例中,出口通道 13 的宽度“b”在 1mm 至约 10cm 之间的范围内。在一些实施例中,出口通道 13 的宽度“b”在 1mm 至约 50mm 之间的范围内。在其他实施例中,出口通道 13 的宽度“b”在 1mm 至约 10mm 之间的范围内。
[0112]
在一些实施例中,处理管道的一个或多个腔室、入口通道和/或出口通道中的至少一个包括一个或多个柱。据信,一个或多个柱的包含将湍流引入穿过腔室、入口通道和出口通道的流体和/或试剂的流动,从而有利于引入的流体、试剂和/或珠粒之间的混合。据信,这种混沌微环境通过在两个或更多个不同对象之间引入平流分子输送和交换来增强混合速率。
[0113]
在一些实施例中,腔室内的柱的数量在约 1 至约 1,000,000 之间的范围内。在
其他实施例中,腔室内的柱的数量在 1 至约 1,0,000 之间的范围内。在一些实施例中,腔室内的柱的数量在约 1 至约 1,000 之间的范围内。在其他实施例中,腔室内的柱的数量在 1 至约 100 之间的范围内。在一些实施例中,入口通道和/或出口通道内的柱的数量在 1 至约 500 之间的范围内。在其他实施例中,入口通道和/或出口通道内的柱的数量在 1 至约 250 之间的范围内。在其他实施例中,入口通道和/或出口通道内的柱的数量在 1 至约 100 之间的范围内。
[0114]
例如,如图 2b 和 4b 所示,腔室 14 包括多个柱 16。再例如,并且如图 3b 所描绘的,腔室 14、入口通道 12 和出口通道 13 各自包括多个柱 16。又例如,图 5a 描绘了包括通过传递通道 18 彼此流体地耦合的第一腔室 14a 和第二腔室 14b 的处理管道 105,其中第一腔室 14a、第二腔室 14b 和传递通道 18 各自包括多个柱。
[0115]
在一些实施例中,一个或多个柱从腔室、入口通道和/或出口通道的底部或顶部延伸(参见例如图 2h)。在其他实施例中,一个或多个柱从底部延伸到腔室、入口通道和/或出口通道的顶部(参见例如图 2i)。在一些实施例中,柱可以具有任何尺寸和形状,诸如圆柱形或多边形。在一些实施例中,柱可以具有任何尺寸和/或形状。例如,柱可以是圆柱形或矩形。在一些实施例中,柱具有约 0.1
µ
m 至约 1mm 范围内的直径。在一些实施例中,柱具有约 0.5
µ
m 至约 1mm 范围内的直径。
[0116]
贮存器和容器微流控装置 100 可以流体地耦合到任何数量的试剂贮存器、珠粒存储容器、珠粒收集容器、流体贮存器、废物收集贮存器等。在一些实施例中,微流控装置包括对于每一个单独的流体和/或试剂贮存器用于引入处理管道 105 的不同流体和/或试剂。如本文所述,贮存器可以在两个或更多个可独立操作的处理管道之间共享。
[0117]
在一些实施例中,每一个贮存器可以经由如本文所述的管道与微流控装置 100 流体地耦合。例如,图 1c 示出了四个流体和/或试剂贮存器 202a 至 202d,其流体地耦合到处理管道 105 的入口。技术人员将理解,图 1c 中描绘的四个流体和/或试剂贮存器 202a 至 202d 中的一个可以是样品贮存器,待纯化或富集的样品在其引入处理管道 105 之前被存储在其中。在一些实施例中,流体和/或试剂贮存器的体积在约 10
µ
l 至约 10ml 之间的范围内。在一些实施例中,流体和/或试剂贮存器的体积在约 1ml 至约 5ml 之间的范围内。
[0118]
在一些实施例中,微流控装置 100 可以流体地耦合到一个或多个珠粒存储器 209a 或收集容器 209b。在一些实施例中,可以通过将珠粒存储容器耦合到处理管道的第一导管的管道将珠粒引入处理管道的一个或多个腔室。同样,在一些实施例中,可以通过将珠粒收集容器耦合到处理管道的第二导管的管道从处理管道的一个或多个腔室传递珠粒。在一些实施例中,珠粒存储或收集容器的体积在约 0.1
ꢀµ
l 至约 5ml 之间的范围内。在其他实施例中,珠粒存储或收集容器的体积在约 0.1ml 至约 1ml 之间的范围内。在一些实施例中,可以使用移液器或注射器通过连接到珠粒存储容器的珠粒封装入口将珠粒引入微流控装置。替代地,如果在出口侧的腔室的壁中仅有一个孔口,则可以通过流体入口引入珠粒。在该特定实施例中,这将允许消除一个或多个导管。
[0119]
流控模块本公开的微流控装置 100 还包括流控模块,该流控模块包括一个或多个管道、一
个或多个泵、一个或多个阀等。
[0120]
管道微流控装置 100 可以包括任何数量的导管,以促进将流体、试剂和/或珠粒传递到微流控装置 100 的处理管道 105 的入口 10、出口 12 和/或导管 15。在一些实施例中,用于引入处理管道 105 的每一种流体和/或试剂可以存储在单独的流体贮存器和/或试剂贮存器中,并且其中每一个流体贮存器和/或试剂储存器独立地耦合到与处理管道 105 的入口 10 流体连通的流体传递管道或试剂传递管道。以这种方式,可以经由试剂传递管道将来自单个试剂贮存器的试剂传递到处理管道 105。同样,可以经由流体传递管道将来自单个流体贮存器的流体传递到处理管道 105。在一些实施例中,每一个流体和/或试剂贮存器和/或流体和/或试剂传递管道可以包括阀,例如2 通阀,使得流体和/或试剂可以流入处理管道 105,如本文所述。
[0121]
在一些实施例中,并且参考图 1c,处理管道 105 的入口可以流体地耦合到分支管道 205a,其中分支管道 205a 中的每一个分支都流体地耦合到流体传递管道 205b。在一些实施例中,每一个流体传递管道 205b 都耦合到流体和/或试剂贮存器 202。在图 1c 中,处理管道被示为与四个流体和/或试剂贮存器 202a 至 202d 流体连通。如技术人员将理解的,图 1c 的四个流体和/或试剂贮存器 202a 至 202d 中的每一个都可以包括不同流体和/或不同试剂。
[0122]
在一些实施例中,微流控装置 100 可以包括一个或多个泵送管道 210,其中此类泵送管道用于将一个或多个泵流体地耦合到处理管道 205。在一些实施例中,微流控装置 100 可以包括与 (i) 处理管道 105 的出口、(ii) 以及废液/试剂容器 203 和/或样品收集器 204 流体连通的废物传递管道206。
[0123]
阀本公开的微流控装置 100 可以包括一个或多个阀和/或微阀。在一些实施例中,阀可以设置在微流控装置 100 的任何管道内,在微流控装置 100 的管道的任何部分,或在微流控装置 100 的任何两个管道的连接处。在一些实施例中,微流控装置 100 中的每一个阀包括一个或多个端口,例如,1 端口、2 端口或 3 端口。
[0124]
可以利用任何类型的阀,前提条件是该阀允许调节整个微流控装置 100 的流体、试剂和/或珠粒的流动,例如启动/停止流体流动、控制流体流动的量等。在一些实施例中,基于来自控制系统 104 的信号来控制阀,例如控制系统 104 可以命令阀致动到第一位置、第二位置或第三位置,使得可以调节流体、试剂和/或珠粒传递。合适的微流控阀的非限制性示例在美国专利号 10,197,188、美国专利公开号 2008/0236668 和 2006/0180779 以及 pct 公开号 wo/2018/104516 中描述,其公开内容通过引用整体并入本文。
[0125]
在一些实施例中,并且再次参考图 1c,一个或多个阀 207a、207b 和 207c 可以设置在分支管道 205a 和/或流体传递管道 205b 中,使得来自贮存器的流体和/或试剂的流动可以被独立地控制。替代地,在其他实施例中,每一个流体和/或试剂贮存器包括阀,使得来自贮存器的流体和/或试剂的流动可以被独立地控制。在一些实施例中,一个或多个阀可以设置在废物传递导管 206 内。
[0126]
泵在一些实施例中,微流控装置 100 与一个或多个泵流体连通。在一些实施例中,
微流控装置与两个泵流体连通。在其他实施例中,微流控装置与三个泵流体连通。在又一些实施例中,微流控装置与四个或更多个泵流体连通。
[0127]
在一些实施例中,一个或多个泵有利于流体、试剂和/或珠粒在微流控装置的腔室、通道和/或管道内的移动。可以在本公开的微流控装置内利用任何泵,前提条件是选择的泵允许控制加载到微流控装置中或从微流控装置排出的体积。在一些实施例中,一个或多个泵是压力泵。在其他实施例中,一个或多个泵是压电泵。在一些实施例中,一个或多个泵是蠕动泵。在一些实施例中,一个或多个泵是注射泵。在一些实施例中,一个或多个泵是容积泵。
[0128]
在一些实施例中,本公开的一个或多个泵具有约 1ml 至约 100ml 范围内的体积。在其他实施例中,本公开的一个或多个泵具有约 10ml 至约 100ml 范围内的体积。在一些实施例中,本公开的一个或多个泵可以递送约 1
µ
l/分钟至约 1000ml/分钟之间的流速。在其他实施例中,本公开的一个或多个泵可以递送约 10
µ
l/分钟至约 500ml/分钟之间的流速。在又一实施例中,本公开的一个或多个泵可以递送约 10
µ
l/分钟至约 100ml/分钟之间的流速。
[0129]
在一些实施例中,出于单一目的提供微流控装置 100 的一个或多个泵中的每一个,例如输注流体、抽取流体、将珠粒传递到一个或多个腔室中和/或传递出一个或多个腔室。在其他实施例中,任何单个泵可以用于多个目的。例如,一个泵可以有利于流体的输注和抽取。
[0130]
在一些实施例中,微流控装置与“流体注射泵”或“流体抽取泵”中的一个或多个连通。如本文所用,“流体输注泵”是指可以将流体和/或试剂引入微流控装置的任何装置,包括引入本公开的微流控装置的任何腔室、通道或管道。因此,流体输注泵可以用于将任何流体和/或试剂递送到任何腔室、通道和/或管道;和/或包括在流体内的任何珠粒可以通过流体注射泵的作用从微流控装置 100 的一个腔室移动到另一个腔室(诸如通过传递通道)。
[0131]
如本文所用,“流体抽取泵”是指可以从微流控装置去除流体的任何装置,包括从本公开的微流控装置的任何腔室、通道或管道,或从与其流体连通的任何一个或多个流体贮存器和/或试剂贮存器。因此,流体抽取泵可以用于从任何腔室、通道、管道和/或贮存器去除任何流体或试剂;并且包括在流体内的任何珠粒可以通过流体抽取泵的作用从微流控装置 100 的一个腔室移动到另一个腔室(诸如通过传递通道)。
[0132]
在一些实施例中,一个或多个泵是微泵。在一些实施例中,微泵是机械泵(例如隔膜微泵和蠕动微泵)。在一些实施例中,微泵是非机械泵(例如无阀微泵、毛细管泵和化学动力泵)。装置以通过泵送少量流体而闻名。例如,美国专利号 5,094,594、5,730,187 和 6,033,628 公开了可以泵送纳升或皮升范围内的流体体积的装置,其公开内容通过引用整体并入本文。
[0133]
适用于微流控装置的其他泵在美国专利号 10, 208,739 中公开;并且在美国公开号 2015/0050172 和 2017/0167481 中,其公开内容通过引用整体并入本文。
[0134]
控制系统和其他模块当前公开的微流控装置通信地耦合到控制系统 104。在一些实施例中,控制系统 104 用于向各种泵和/或阀发送指令,以便调节穿过微流控芯片的任何流体和/或试剂的流体流动(例如,流体和/或试剂流动的方向、流体流动的体积或流速)。在一些实施例中,控制
系统 104 被配置成发送指令以致动一个或多个阀打开或关闭,包括设置在贮存器、管道和/或通道中的一个或多个阀。在一些实施例中,控制系统被配置成发送指令以调节与微流控芯片流体连通的一个或多个泵的操作,诸如使泵从处理管道 105 或其任何部分输注或抽取流体、试剂和/或传递珠粒。
[0135]
在一些实施例中,控制模块 104 可以引导第一路径中的第一流体流过处理管道 105,例如从入口 10 到入口通道 12、腔室 14、出口通道 13 和出口 11 的流体流动路径。在其他实施例中,控制模块 104 可以引导第一流体流入处理管道中的第一路径和第二路径中,其中第一路径和第二路径彼此相对。例如,通过一个或多个泵的作用,流体、试剂和/或珠粒可以经由传输通道从第一腔室流到第二腔室;然后从第二腔室流回第一腔室。
[0136]
可以参考图 1c 示出了对通过微流控装置的流体和/或试剂流动的控制。在一些实施例中,可以首先由控制系统命令泵 201 从样品储存器 202a 抽取样品,诸如在缓冲溶液内提供的样品。在一些实施例中,表面活性剂可以包括一个或多个端口。在此,控制系统将命令阀 207a 和 207b 致动到允许样品从样品贮存器 202a 流入流体传递管道 205b、分支管道 205a 和处理管道 105 的位置。在一些实施例中,控制系统还将命令阀 208 致动到允许流体流入废物收集容器 203 的位置。如本文进一步描述的,样品内带有合适的第一反应性官能团的分子可以与处理管道 105 的腔室内提供的并具有相应的第二反应性官能团反应。未与官能化珠粒反应的分子可以在缓冲溶液中流过处理管道 105、泵送导管 210、废物传递管道 206,并进入废物收集容器 203。最后,控制系统将命令阀 207a 和 207b 致动以防止样品从贮存器 202a 流出。
[0137]
可以针对一种或多种附加流体和/或试剂重复该过程。例如,接下来可以将存储在贮存器 202b 中的洗涤缓冲剂引入处理管道 105 中。控制系统将命令阀 207a 和 207b 致动到允许洗涤缓冲剂的第一等分试样从洗涤缓冲剂贮存器 202b 流入(经由泵 201)流体传递管道 205b,分支管道 205a 和处理管道 105 中的位置。在一些实施例中,控制系统还将命令阀 208 致动到允许洗涤缓冲剂流入废物收集容器 203 的位置。在一些实施例中,并且如本文进一步描述的,洗涤缓冲剂流过处理管道的腔室,以便去除引入存储在贮存器 202a 中的样品溶液中的未结合分子和/或组分。在一些实施例中,洗涤液流过处理管道 105、泵送管道 210、废物传递管道 206,并进入废物收集容器 203。最后,控制系统可以命令阀 207a 和 207b 致动以防止附加洗涤缓冲剂从贮存器 202b 流出。在一些实施例中,附加洗涤缓冲剂的等分试样可以流过处理管道 105。例如,相同或不同洗涤缓冲剂的另外两个等分试样可以流过处理管道。
[0138]
在一些实施例中,可以重复上述过程,以便引入试剂(例如加热的缓冲剂或酶)以释放与珠粒结合的分子。例如,控制系统将命令阀 207a 和 207b 致动到允许试剂从贮存器 202d 流入流体传递管道 205b、分支管道 205a 和处理管道 105 的位置。在一些实施例中,控制系统还将命令阀 208 致动到允许流体流入样品收集容器 204 的位置。随着结合分子从珠粒中释放,将释放的分子提供给流过处理管道 105 的试剂,并且该试剂最终流入样品收集容器 204。
[0139]
在一些实施例中,系统可以进一步包括一个或多个压力传感器、温度传感器和/或流速传感器。在一些实施例中,传感器可以耦合到控制系统以允许对微流控系统进行反馈控制。在一些实施例中,控制系统被配置成接收来自传感器(例如流速传感器、温度传感器、
压力传感器、化学分析仪)的数据,处理接收的数据,并基于接收和处理的数据调节流体流量、温度、压力等。
[0140]
在一些实施例中,反馈控制涉及检测在本微流控系统中发生的一个或多个事件或过程。在一些实施例中,检测可以涉及例如确定流体的至少一个特性,流体内的组分,微流控芯片的区域内、特定处理管道 105 内的组分之间的相互作用或微流控装置的区域内或单个处理管道 105 的一部分内的状况(例如,温度、压力等)。举例来说,在一些实施例中,控制系统 104 被配置成执行一系列指令以控制或操作一个或多个系统部件以执行一个或多个操作,例如预编程的操作或例程,或从通信联接至系统的一个或多个传感器接收反馈并根据接收到的传感器反馈来命令该一个或多个系统部件运行(或停止运行)。在一些实施例中,可以由执行一个或多个计算机程序的一个或多个可编程处理器执行一个或多个预编程的操作或例程以执行动作,包括通过对接收的传感器反馈数据或成像数据进行操作并基于该接收的反馈来命令系统组件)。
[0141]
在一些实施例中,微流控装置或任何组件因此可以通信地耦合到一个或多个加热模块、冷却模块和/或混合模块。以这种方式,每一个处理管道 105 可以被独立地加热和/或冷却。在一些实施例中,微流控芯片、处理管道、试剂贮存器、流体贮存器、通道和/或任何管道各自独立地与单独的加热和/或冷却模块热连通。例如,每一个处理管道 105 可以与不同的加热和/或冷却模块热连通。在其他实施例中,加热和/或冷却模块在微流控装置的组件之间共享。
[0142]
合适的加热和/或冷却模块包括加热块、珀尔帖装置和/或热电模块。合适的珀耳帖装置包括美国专利号4,685,081、5,028,988、5,040,381 和 5,079,618 中所述的那些,其公开内容通过引用整体并入本文。在一些实施例中,控制系统可以通信地耦合到一个或多个加热和/或冷却模块并且被配置成命令加热和/或冷却模块激活以将微流控芯片、处理管道、试剂贮存器、流体贮存器和/或管道在预定时间量内加热和/或冷却到预定温度。例如,控制模块 104 可以将来自至少一个加热模块的加热引导至微流控芯片,使得在预定时间量内达到和/或维持预定温度。预定温度可以由用户输入到控制系统,或者可以在预编程指令或例程内提供。
[0143]
在一些实施例中,微流控芯片或任何单独的处理管道可以与一个或多个混合模块连通。在一些实施例中,一个或多个混合模块包括声波发生器,诸如换能器。在一些实施例中,换能器是机械换能器。在其他实施例中,换能器是压电换能器。在一些实施例中,换能器由产生机械振动的压电晶片构成。在一些实施例中,表面换能器用于在载玻片上分布或混合流体体积。用于非接触式混合的合适装置和方法在 pct 公布号 wo/2018/215844 中描述,其公开内容全文通过引用并入本文。
[0144]
在一些实施例中,控制系统 104 包括一个或多个存储器和可编程处理器。为了存储信息,控制系统 104 可以包括但不限于一个或多个存储元件,例如易失性存储器、非易失性存储器、只读存储器 (rom)、随机存取存储器 (ram) 等。在一些实施例中,控制系统 104 是系统外部的独立计算机。存储和/或存储器装置可以是用于临时或永久地存储数据或程序的一个或多个物理设备。在一些情况下,装置是易失性存储器,并且需要电源来保留存储的信息。在其他情况下,装置是非易失性存储器并且在数字处理装置未通电时保留存储的信息。在又一些情况下,非易失性存储器包括闪存。非易失性存储器可以包括动态随机
存取存储器 (dram)。非易失性存储器可以包括铁电随机存取存储器 (fram)。非易失性存储器可以包括相变随机存取存储器 (pram)。装置可以是存储装置,其包括作为非限制性示例的 cd-rom、dvd、闪存装置、磁盘驱动器、磁带驱动器、光盘驱动器和基于云计算的存储器。
[0145]
在一些实施例中,控制系统 104 是能够远程控制系统的联网计算机。术语“编程处理器”涵盖处理数据的各种设备、装置和机器,例如包括可编程微处理器、计算机、芯片上系统、或上述的多个或组合。所述设备可以包括特殊用途的逻辑电路,如 fpga(现场可编程门阵列)或 asic(特定用途集成电路)。除硬件外,所述设备还可以包括为所述有关计算机程序创建执行环境的代码,例如,构成处理器固件、协议栈、数据库管理系统、操作系统、跨平台运行时环境、虚拟机或它们的一个或多个组合的代码。所述设备和执行环境可以实现各种不同的计算模型基础架构,例如,网络服务、分布式计算和网格计算基础架构。
[0146]
在一些实施例中,系统可以进一步包括一个或多个化学分析仪和/或检测器。在一些实施例中,一个或多个化学分析仪可以用于检测收集的流体流(例如废物流)内的细胞组分、试剂、副产物等。在一些实施例中,化学分析仪选自用于核酸定量的 qubit bioanalyzer 用于 na 的大小分布、用于核酸定量的 lightcycler 480 qpcr 仪器、用于分子鉴定和/或定量的质谱仪,诸如 maldi-tof ms、lc/ms/ms、ce-ms 等。还可以利用光学显微镜(明场、荧光)、光谱(诸如 ir、nmr、拉曼)。在一些实施例中,可以通过将本公开的任何微流控装置与诸如 ce-ms 的仪器在线耦合来促进反馈控制。在其他实施例中,微流控系统 100 可以进一步耦合到荧光显微装置,诸如包括激光源和 ccd 或基于 cmos 的成像传感器和/或相机的荧光显微装置。
[0147]
在一些实施例中,微流控系统 100 可以进一步耦合到测序装置。在一些实施例中,测序装置是“下一代测序”装置。
[0148]
微流控芯片制造可以根据本领域普通技术人员已知的任何方法制造本公开的微流控芯片。合适的制造方法包括光刻、3d 打印、激光蚀刻和压花。
[0149]
微流控芯片可以由适合于形成通道和/或管道的任何材料来制造。材料的非限制性示例包括聚合物(例如,聚乙烯、聚苯乙烯、聚甲基丙烯酸甲酯、聚碳酸酯、聚(二甲基硅氧烷)、ptfe、pet 和环烯烃共聚物)、玻璃、石英和硅。形成微流控芯片和任何相关联的组件(例如,盖子)的材料可以是硬的或柔性的。本领域普通技术人员可以基于例如以下项容易选择合适的材料:其刚性、其对要穿过的流体的惰性(例如,不会被其降解)、其在要使用的特定装置的温度下的稳健性、其对光的透明度/不透明度(例如,在紫外线和可见区域)和/或用于在材料中制造特征的方法。例如,对于注塑成型或其他挤出制品,使用的材料可以包括:热塑性塑料(例如聚丙烯、聚碳酸酯、丙烯腈-丁二烯-苯乙烯、尼龙 6)、弹性体(例如聚异戊二烯、异丁烯-异戊二烯、腈、氯丁橡胶、乙烯-丙烯、海帕隆、硅树脂)、热固性材料(例如环氧树脂、不饱和聚酯、酚醛树脂)或其组合。
[0150]
本文公开的微流控芯片通常通过单层和多层软光刻 (mlsl) 技术和/或牺牲层封装方法构建。mlsl 技术在一些实施例中对于产生包括控制通道和流动通道两者的微流控装置特别有用。一般来说,mlsl 技术涉及在微加工模具上浇铸一系列弹性体层,从模具中取出这些层,然后将这些层融合在一起。在牺牲层封装方法中,光刻胶图案沉积在需要通道
的任何地方。使用这些技术制造微流控装置的元件例如由 unger et al. (2000) science 288:113
–
116 描述;由 chou, et al. (2000) "integrated elastomer fluidic lab-on-a-chip-surface patterning and dna diagnostics 描述,描述于 proceedings of the solid state actuator and sensor workshop, hilton head, s.c;描述于 pct 公开号 wo 01/01025;以及描述于 2000 年 10 月 3 日递交的美国专利申请序列号 09/679,432,其公开内容通过引用整体并入本文。
[0151]
据信,mlsl 利用了公认的光刻技术和微电子制造技术的进步。mlsl 的第一步是使用计算机绘图软件绘制设计,然后将其打印在高分辨率掩模上。覆盖有光刻胶的硅晶片暴露于紫外线光,该紫外线光在某些区域被掩模过滤掉。根据光刻胶是负性还是正性,暴露(负性)或未暴露(正性)的区域将交联并且抗蚀剂将聚合。未聚合的抗蚀剂可溶于显影剂溶液并随后被洗去。通过以不同的速度结合不同的光刻胶和旋涂,可以将晶片图案化为各种不同的形状和高度。
[0152]
在一些实施例中,然后将晶片用作模具以将图案传递到聚二甲基硅氧烷 (pdms)。在 msl 中,将不同模具浇铸的不同层 pdms 彼此堆叠,用于在重叠的“流动”层和“控制”层中创建通道。通过以互补的化学计量比混合灌封预聚物组分和硬化剂组分以实现硫化,将两个(或更多)层结合在一起。为了创建简单的微流控芯片,从包含流动层的模具中浇铸“厚”层,以及从包含控制层的模具中浇铸“薄”层。在两层部分硫化之后,将流动层从模具上剥离,并手动对准控制层。使这些层粘合,然后将该双板从控制模具中剥离,然后冲孔用于入口和出口,并将双板键合到 pdms 的空白层上。在允许更多时间粘合之后,将完成的装置安装在载玻片上。
[0153]
在一些实施例中,可以切割多个板或片(例如使用激光切割机)并且可以使用双面粘合剂组装和/或层压以创建多层微流控装置。在一些实施例中,板或片可以是塑料,诸如聚碳酸酯、丙烯醛基、聚丙烯等。
[0154]
方法本公开还涉及使用本公开的微流控装置纯化样品、用所需靶分子富集样品和/或执行固相化学反应的方法。在一些实施例中,方法采用预加载有官能化珠粒(诸如非磁性官能化珠粒)的处理管道。在一些实施例中,本文所述的方法不需要磁分离处理或技术。在一些实施例中,方法在减轻交叉污染和/或样品损失风险的封闭系统中进行。
[0155]
纯化引入微流控装置的溶液的一般方法在一些实施例中,本公开涉及使用本文所述的任何一种微流控装置 100 来纯化样品的方法。在一些实施例中,可以用本公开的微流控装置 100 来纯化样品,该微流控装置包括预先加载有具有官能化表面的珠粒的处理管道 105。在一些实施例中,处理管道可预先加载有约 10 至约 10,000 个之间的官能化珠粒。在其他实施例中,处理管道可以预先加载有约 10 至约 1000 个之间的官能化珠粒。在又一些实施例中,处理管道可以预先加载有约 10 至约 150 个之间的官能化珠粒。在一些实施例中,预加载的官能化珠粒是非磁性官能化珠粒。
[0156]
在一些实施例中,珠粒的官能化表面包括第一部分(例如第一反应性官能团),该第一部分可与待纯化样品内的分子(或包括该分子的缀合物)的第二部分(例如第二反应性官能团)反应。在一些实施例中,第一部分和第二部分之间的“反应”可以表示在两个反应性
基团或两个部分的两个反应性官能团之间形成共价键;或可以表示两个反应性基团或两个部分的两个反应性官能团彼此缔合、彼此相互作用、彼此杂交、彼此氢键合等。因此,在一些实施例中,“反应”包括结合事件,诸如半抗原与抗半抗原抗体的结合或生物素与链霉亲和素的结合。
[0157]
在一些实施例中,引入微流控装置的处理腔室的珠粒的官能化表面可以包含亲和素或链霉亲和素以结合待纯化样品内的生物素化分子(例如与生物素缀合的分子)。再例如,在一些实施例中,硫醇化分子可以结合到金表面。作为又一示例,胺封端的分子可以结合到 nhs 激活的珠粒表面。
[0158]
在一些实施例中,珠粒的官能化表面包括固定化抗体,其可以用于结合包括或缀合至特定抗原分子的分子。在又一些实施例中,珠粒的官能化表面包括酶,其可以用于结合包括或缀合至特定酶底物的分子。在进一步实施例中,珠粒的官能化表面包括受体,其可以用于结合包括或缀合至特定受体配体的分子。在更进一步的实施例中,珠粒的官能化表面包括凝集素,其可以用于结合包括或缀合至特定多糖的分子。在再进一步的实施例中,珠粒的官能化表面包括核酸,其可以用于结合包括或与缀合至互补碱基序列的分子。在一些实施例中,拴在珠粒表面上的 dna/rna 适体可以特异性结合至其靶分析物,诸如小分子、肽、蛋白质、细胞。
[0159]
在一些实施例中,并且不管珠粒的表面如何被官能化,珠粒本身可以是非磁性的。合适的非磁性珠粒描述于美国专利第 5,328,603 号中,该美国专利的公开内容通过引用整体并入本文。
[0160]
一般来说,使用本公开的微流控装置纯化样品的方法包括:(i) 将待纯化输入样品内的适当官能化分子的子集与存在于处理管道的腔室内的官能化珠粒结合;(ii) 使一种或多种洗涤溶液流过处理管道以去除输入样品内包含的未结合分子、试剂和/或杂质;以及 (iii) 使溶液流过处理管道以从官能化珠粒中释放结合的分子。在一些实施例中,可以任选地将一种或多种试剂引入处理管道中以衍生与官能化珠粒结合的分子的子集。在一些实施例中,这些方法不依赖于磁性珠粒或磁性分离来进行纯化。相反,通过使一系列流体和/或试剂流过处理管道来实现纯化。
[0161]
在一些实施例中,通过将输入样品引入预先加载有官能化珠粒的处理管道,将适当官能化分子的子集结合至官能化珠粒,其中输入样品包括适当官能化分子的子集。在一些实施例中,输入样品内的适当官能化分子的子集包括能够与官能化珠粒的第二部分反应的第一部分。在一些实施例中,适当官能化分子的子集在将输入样品引入处理管道之前生成。在一些实施例中,通过使输入样品与选择性地与输入样品内的分子的子集反应的试剂接触来生成适当官能化分子的子集。举例来说,试剂可以是具有能够与官能化珠粒反应的部分的寡核苷酸序列。在一些实施例中,反应是缀合反应,其中将能够与官能化珠粒反应的部分引入分子的子集。在一些实施例中,引入的部分是能够与官能化珠粒的第二部分反应的第一部分。
[0162]
纯化输入样品的方法在图 8a 和 8b 中示出。在一些实施例中,首先获得具有腔室的处理管道,该腔室预先加载有具有官能化表面的多个珠粒(步骤 320)。在一些实施例中,腔室预先加载有具有官能化表面的多个非磁性珠粒。在一些实施例中,官能化表面包括一对特异性结合实体的第一成员。在一些实施例中,官能化表面包括选自以下各项的第一
部分:亲和素、链霉亲和素和抗体、酶、受体、凝集素、核酸序列等。在一些实施例中,可以通过将珠粒从珠粒存储容器泵送至与腔室流体连通的一个或多个导管来引入官能化珠粒。在一些实施例中,在引入珠粒之后密封腔室。
[0163]
在一些实施例中,然后将包括待纯化分子的子集的输入样品引入具有预先加载有多个珠粒的腔室的处理管道,使得可以形成珠粒-分子复合物(步骤 310)。在一些实施例中,通过使包括待纯化分子的子集的输入样品流入并通过处理管道的腔室来形成珠粒-分子复合物(步骤 321)。例如,可以在流体或缓冲溶液中提供输入样品,并通过将流体或缓冲溶液泵送至处理管道的入口,使流体或缓冲溶液流过处理管道的入口通道并进入具有预先加载的珠粒的处理管道来引入输入样品。
[0164]
在一些实施例中,输入样品包括具有能够与官能化珠粒的第一部分反应的第二部分的分子的子集,使得第一部分和第二部分可以彼此反应。在一些实施例中,通过使输入样品与选择性地与输入样品内的分子的子集反应的试剂接触来生成具有第二部分的分子的子集。
[0165]
在一些实施例中,输入样品以允许具有第二部分的分子有时间与官能化珠粒反应的速率流过处理管道。例如,在一些实施例中,样品可以以约 0.1ml 每分钟至约 1000ml 每分钟之间的速率流过处理管道。在其他实施例中,样品可以以约 0.1ml 每分钟至约 100ml 每分钟之间的速率流过处理管道。
[0166]
在一些实施例中,允许具有第二部分且待纯化的子集分子有时间与官能化珠粒一起孵育。在一些实施例中,孵育期可以在约 15 秒至约 90 分钟之间的范围内。在一些实施例中,孵育期可以在约 1 分钟至约 60 分钟之间的范围内。在其他实施例中,孵育期可以在约 1 分钟至约 20 分钟之间的范围内。在需要孵育时间的那些实施例中,一旦输入样品流入处理管道的腔室,可以命令流体地耦合到处理管道的一个或多个泵关闭(或减慢流体流动速率)预定的孵育时间。
[0167]
在待纯化的分子的子集与珠粒结合之后(即在形成珠粒-分子复合物之后),在一些实施例中,然后使一种或多种流体流过处理管道(步骤 322)以去除未结合的分子和/或来自处理管道的腔室的杂质(步骤 311)。例如,可以通过将流体泵送入处理管道的入口、使流体流过处理管道的入口通道并进入处理管道的腔室来引入流体(例如缓冲溶液)。在一些实施例中,流体(例如第一类型的缓冲剂)流过腔室一次(例如预定体积的单一类型的缓冲剂流过腔室一次)。在其他实施例中,相同或不同流体流过腔室两次或更多次(例如,预定第一体积的第一流体流过腔室,然后预定体积的第二流体流过腔室)。在又一些实施例中,不同流体,例如不同缓冲剂依次流过腔室三次或更多次。
[0168]
在一些实施例中,流入腔室的流体(例如缓冲剂)在腔室内保持预定时间,例如约 1 分钟至约 60 分钟范围内的时间段。在其他实施例中,搅动引入处理管道的流体,诸如通过将振动引入处理管道(例如通过与处理管道连通的换能器)或通过引导一个或多个泵重复输注和抽取来自处理管道的少量流体。
[0169]
在一些实施例中,流出腔室、通过出口通道以及通过出口的流体废物流被监测,诸如使用相机,例如荧光相机,以确定是否基本上所有未结合的分子和/或杂质已经被去除。在一些实施例中,可以在出口处利用带有激光源的荧光相机以监测从未结合的分子和/或杂质发射的荧光信号,并且该信号可以反馈到控制系统以命令操作阀和/或泵。在其他实施
例中,还可以使用包括两条金属线的电导率检测器以检测由局部分子组成引起的局部 ph 变化,并且该获取的 ph 数据可以再次用于反馈控制。
[0170]
例如,当流体流过腔室、进入出口管道并流过出口时,与其连通的检测器(例如荧光检测器)可以用于检测和/或量化废物流内未结合的分子和/或杂质。与处理管道的出口连通的荧光检测器还可以用于确定靶分子是否正在丢失,如果是,则可以调整处理参数以减轻此类损失。在一些实施例中,重复和/或依次引入流体直到基本上所有未结合的分子和/或杂质已经从腔室中去除,如荧光检测器所确定的。在其他实施例中,重复和/或依次引入流体,直到废物流中未结合的分子和/或一种或多种杂质的量小于预定的杂质阈值。
[0171]
在从处理管道的腔室中去除基本上所有未结合的分子和/或杂质之后,从珠粒中释放结合到珠粒的分子的子集(步骤 312)并且随后被收集(步骤 313 和 324)。在一些实施例中,通过使流体或试剂流入适于从珠粒释放分子的处理管道中来释放分子的子集(步骤 323)。在一些实施例中,流体是被预加热或原位加热到预定温度的缓冲流体。在一些实施例中,流体被加热到约 85℃ 至约 105℃ 范围内的温度。在一些实施例中,流体被加热到约 90℃ 至约 100℃ 范围内的温度。在一些实施例中,可以通过命令与贮存器热连通的一个或多个加热模块来加热预热的流体以将流体加热至预定温度。在一些实施例中,可以命令与处理管道热连通的加热器将引入的流体加热至预定温度。在一些实施例中,引入试剂以实现分子的子集的释放。在一些实施例中,试剂是酶,例如能够在预定位置或特定键处切割分子的酶。在一些实施例中,然后释放的分子的子集可以用于一个或多个下游过程,例如进一步的化学反应、测序等。
[0172]
使用微流控装置进行靶富集本公开还涉及通过富集核酸样品中的特定核酸靶序列来降低核酸样品的复杂性的方法。在一些实施例中,本公开涉及使用寡核苷酸探针的文库富集核酸样品中的特定靶序列的方法。然后可以将富集特定靶序列的核酸样品用于下游测序操作。在一些实施例中,本文所述的靶富集的方法不利用磁珠或磁分离技术。
[0173]
在一些实施例中,本公开涉及使用本文所述的任何一种微流控装置进行靶富集的方法。本公开还涉及使用靶富集样品进行测序的方法,诸如使用本文所述的任何一种微流控装置制备的靶富集样品。在一些实施例中,靶测序通常能够检测选定基因组或基因组区域中的已知和新变体。在一些实施例中,靶富集样品使用下一代测序进行测序。例如,当包括目标核酸序列的样品溶液流过预加载有多个官能化珠粒的处理管道的腔室时,目标核酸通过各种化学物质结合到珠粒表面上。在一些实施例中,缓冲剂(例如洗涤缓冲剂)随后流过处理管道并围绕设置在其中的珠粒流动以去除未结合的非靶核酸和杂质。在一些实施例中,然后将洗脱液引入腔室以通过温度变化或酶促切割来释放靶核酸。在一些实施例中,然后通过出口来收集释放的核酸并将其传递到下游过程。
[0174]
在一些实施例中,靶富集包括获得基因组样品。在一些实施例中,获得的基因组样品是源自哺乳动物受试者(例如人受试者)的样品。在一些实施例中,获得的基因组样品是从哺乳动物受试者获得的血液样品或血浆样品,例如从人受试者获得的血液样品或血浆样品。在一些实施例中,获得的基因组样品是无细胞核酸的形式。在一些实施例中,获得的无细胞核酸形式的基因组样品包括 dna 和/或 rna。在一些实施例中,无细胞 dna 的大小通常在约 200 bp 至约 130 bp 之间的范围内。在一些实施例中,无细胞 dna 的大小通常在
约 190 bp 至约 140 bp 之间的范围内。在一些实施例中,无细胞 dna 的大小通常在约 180 bp 至约 150 bp 之间的范围内。无细胞核酸的非限制性示例包括存在于母体血液和血浆中的循环肿瘤 dna (ctdna) 和胎儿无细胞 dna。在一些实施例中,本公开还涵盖各种类型的无细胞 rna 的分离。
[0175]
替代地,并且参考图 9,在一些实施例中,靶富集包括获得基因组样品,例如从人类患者获取的基因组 dna 样品(步骤 410)。在一些实施例中,将获得的基因组样品剪切成片段以提供核酸片段群(步骤 411)。在一些实施例中,使用机械(例如雾化或超声)和/或酶促片段化(例如限制性内切核酸酶)来实现获得的基因组样品的剪切。
[0176]
在一些实施例中,生成的核酸片段是随机大小的。在一些实施例中,生成的核酸片段具有小于约 1000 个碱基对的长度。在其他实施例中,生成的核酸片段包括具有长度在约 100 至约 1000 个碱基对之间的序列大小的序列片段。在又一些实施例中,生成的核酸片段包括长度在约 500 至约 750 个碱基对之间的序列大小的序列片段。在一些实施例中,然后经由连接反应将衔接子(诸如包括特定条形码序列的那些)添加到核酸群中。
[0177]
在获得基因组样品(和/或获得的基因组样品的任选片段化)之后,在一些实施例中,将寡核苷酸探针库(诸如与一对特异性结合实体的第一成员缀合的寡核苷酸探针)引入获得的基因组样本或核酸片段群。在一些实施例中,将寡核苷酸探针库引入包括获得的基因组样品或核酸片段群的缓冲溶液中(步骤 413)。在一些实施例中,寡核苷酸探针是能够与基因组样品或核酸片段群内的互补核酸序列杂交的核酸序列参考群。在一些实施例中,寡核苷酸探针被设计为靶向基因组样品或核酸片段群体内的所需基因、外显子和/或其他目标基因组区域。在一些实施例中,选择寡核苷酸探针,使得寡核苷酸探针涉及作为非限制性示例的一组目标基因、基因组的所有外显子、特定目标遗传区域、疾病或生理状态等。
[0178]
在一些实施例中,寡核苷酸探针是 dna 捕获探针。在一些实施例中,dna 捕获探针包括 roche seqcap ez probes 库(可从 roche sequencing and life sciences, indianapolis, ind 获得)。在一些实施例中,roche seqcap ez probes 库包括溶液中不同生物素化单链 dna 寡核苷酸的混合物,每一种都有特定序列,其中单个寡核苷酸的长度可以在约 50 个核苷酸至约 100 个核苷酸的范围内,通常的大小约为 75 个核苷酸。在一些实施例中,roche seqcap ez probe pool 可以用于序列捕获实验以与 dna 测序文库的靶向互补片段杂交,从而在测序之前相对于相同 dna 测序文库的非靶向片段捕获和富集它们。dna 测序文库可以由基因组 dna 构建用于基因组分析,或由从 rna 或 mrna 制备的 cdna 构建用于转录组分析,并且它可以由任何生物体物种的 dna 或 cdna 构建,可以从该任何生物体物种中提取这些核酸。
[0179]
在一些实施例中,寡核苷酸探针与基因组样品内的互补核酸的第一子集或核酸片段群内的核酸片段杂交,该核酸片段包括所需基因、外显子和/或其他目标基因组区域以形成具有一对特异性结合实体的第一成员的靶-探针复合物。在一些实施例中,分别在不包括所需基因、外显子和/或其他目标基因组区域的获得的基因组样品或核酸片段的溶液内的核酸或核酸片段的第二子集不形成靶-探针复合物并且被称为“脱靶核酸”或“脱靶片段”。因此,在引入寡核苷酸探针之后,用于富集的任何溶液都可以包括形成的靶-探针复合物、脱靶核酸或脱靶片段和/或游离探针(假设向包括衔接子连接的 dna 片段的任何溶液提供了过量的寡核苷酸探针)。在一些实施例中,用于富集的溶液在缓冲溶液中提供。
ph 在约 5 至约 8 范围内的缓冲剂洗涤三次以上。在一些实施例中,珠粒依次用磷酸盐缓冲盐水洗涤。
[0187]
在一些实施例中,流入腔室的流体(例如缓冲剂)在腔室内保持预定时间,例如约 1 分钟至约 60 分钟范围内的时间段。在其他实施例中,搅动引入处理管道的流体,诸如通过将振动引入处理管道(例如通过与处理管道连通的换能器)或通过引导一个或多个泵重复输注和抽取来自处理管道的少量流体。
[0188]
在从处理管道的腔室中去除基本上所有脱靶核酸、脱靶片段、试剂和/或杂质之后,将靶分子从腔室中去除(步骤 416)(即从珠粒中释放)并且随后被收集(步骤 417)。在一些实施例中,通过使流体或试剂流入适于从颗粒或珠粒释放靶分子或靶分子复合物的处理管道中来释放靶分子或靶分子复合物。在一些实施例中,通过使加热流体流过处理管道来将靶分子从腔室中移除。
[0189]
例如,可以将预加热流体引入腔室以实现释放。在一些实施例中,预加热流体的温度可以在约 4℃ 至约 150℃ 之间的范围内。在其他实施例中,预加热流体的温度可以在约 20℃ 至约 95℃ 之间的范围内。在又一些实施例中,预加热流体的温度可以在约 37℃ 至约 65℃ 之间的范围内。在一些实施例中,加热流体允许靶-探针复合物变性。在一些实施例中,流体是加热缓冲剂。缓冲剂的非限制性示例包括柠檬酸、磷酸二氢钾、硼酸、二乙基巴比妥酸、哌嗪-n,n'-双(2-乙磺酸)、二甲基次胂酸、2-(n-吗啉代)乙磺酸、三(羟甲基)甲胺 (tris)、2-(n-吗啉代)乙磺酸 (taps)、n,n-双(2-羟乙基)甘氨酸 (bicine)、n-三(羟甲基)甲基甘氨酸 (tricine)、4-2-羟乙基-1-哌嗪乙磺酸 (hepes)、2-{[三(羟甲基)甲基]氨基}乙磺酸 (tes) 及其组合。在一些实施例中,去掩蔽剂是水。在其他实施例中,缓冲溶液可以包含三(羟甲基)甲胺 (tris)、2-(n-吗啉代)乙磺酸 (taps)、n,n-双(2-羟乙基)甘氨酸 (bicine)、n-三(羟甲基)甲基甘氨酸 (tricine)、4-2-羟乙基-1-哌嗪乙磺酸 (hepes)、2-{[三(羟甲基)甲基]氨基}乙磺酸 (tes) 或其组合。在一些实施例中,缓冲溶液具有约 5 至约 9 范围内的 ph。
[0190]
在一些实施例中,将流体引入腔室然后加热。在一些实施例中,流体、珠粒和/或处理管道被加热到约 85℃ 至约 105℃ 范围内的温度。在其他实施例中,流体、珠粒和/或处理管道被加热到约 90℃ 至约 100℃ 范围内的温度。在又一些实施例中,流体、珠粒和/或处理管道被加热到约 85℃ 至约 105℃ 范围内的温度。
[0191]
在其他实施例中,引入试剂(例如酶)以实现释放。合适的酶的示例包括胰蛋白酶(其在赖氨酸和精氨酸残基的羧基端部切割肽键)和梭菌蛋白酶(其在精氨酸残基的羧基侧切割)。
[0192]
在一些实施例中,使试剂有时间与珠粒结合的靶-探针复合物和/或珠粒结合的游离探针一起孵育。在一些实施例中,孵育期可以在约 1 分钟至约 60 分钟之间的范围内。在其他实施例中,孵育期可以在约 1 分钟至约 40 分钟之间的范围内。在又一些实施例中,孵育期可以在约 1 分钟至约 20 分钟之间的范围内。
[0193]
然后可以将释放的靶分子用于一个或多个下游过程,例如测序、扩增、进一步耦合等。在一些实施例中,可以根据本领域普通技术人员已知的任何方法执行测序。在一些实施例中,测序方法包括 sanger 测序和染料终止子测序,以及下一代测序技术,诸如焦磷酸测序、纳米孔测序、基于微孔的测序、纳米球测序、mpss、solid、illumina、ion torrent、
starlite、smrt、tsms、边合成边测序、边连接边测序、质谱测序、聚合酶测序、rna 聚合酶 (rnap) 测序、基于显微镜的测序、微流控 sanger 测序、基于显微镜的测序, rnap 测序等。例如,测序的仪器和方法在 pct 公开号 wo2014144478、wo2015058093、wo2014106076 和 wo2013068528 中公开,其公开内容通过引用整体并入本文。
[0194]
可以参考图 1e 示出了靶富集的方法以及流体和/或试剂通过微流控装置的流动。在一些实施例中,将包括靶-探针复合物、脱靶核酸、脱靶片段和/或游离探针的待富集的溶液存储在例如贮存器 264 中。在一些实施例中,待富集的溶液包括缓冲剂。然后,控制系统可以向阀 257 和 255 发送信号以打开以允许通过泵 250a 和 250b 中的一者或两者抽取待富集的溶液。然后控制器可以向阀 257 和 255 发送进一步的信号以致动,从而可以将抽取的用于富集的溶液输注至处理管道 105 中,其中处理管道预加载有官能化珠粒。在一些实施例中,预加载的珠粒是非磁性的。在一些实施例中,处理管道 105 不包括运动部分。如上所述,靶-探针复合物和游离探针可以与官能化珠粒结合。
[0195]
随后,控制系统可以向阀 255 和 258 发送信号以允许将第一缓冲剂从贮存器 260 中抽取并进入泵 250a 和 250b 中的一者或两者中。然后控制系统可以命令阀 255、258 和 257 致动,从而将第一缓冲剂输注至处理管道 105 中,从而从腔室中去除脱靶核酸或脱靶片段。这些步骤可以重复一次或多次,从而将相同的第一缓冲剂从贮存器 260 中抽取并输注到处理管道 105 中。
[0196]
接下来,控制系统可以向阀 255 和 256 发送信号以允许将第二缓冲剂从贮存器 263 中抽取并进入泵 250a 和 250b 中的一者或两者中。然后控制系统可以命令阀 255、256 和 257 致动,从而将第二缓冲剂注入处理管道 105 中,从而从腔室中去除脱靶核酸或脱靶片段。这些步骤可以重复一次或多次,从而将相同的第二缓冲剂从贮存器 263 中抽取并输注至处理管道 105 中。
[0197]
然后控制系统可以向阀 255 和 256 发送信号以允许将第三缓冲剂从贮存器 262 中抽取并进入泵 250a 和 250b 中的一者或两者中。然后控制系统可以命令阀 255、256 和 257 致动,从而将第三缓冲剂输注至处理管道 105 中,从而从腔室中去除脱靶核酸或脱靶片段。这些步骤可以重复一次或多次,从而将相同的第三缓冲剂从贮存器 262 中取出并输注至处理管道 105 中。
[0198]
最后,控制系统可以向阀 255 和 258 发送信号以允许将试剂从贮存器 261 中取出并进入泵 250a 和 250b 中的一者或两者中。然后控制系统可以命令阀 255、258 和 257 致动,从而将试剂输注至处理管道 105 中,从而将结合的靶-探针复合物和结合的游离探针从珠粒中释放。在试剂是缓冲剂的实施例中,控制系统可以命令与处理管道 105 热连通的加热器以加热引入的试剂。然后可以收集包括释放的靶-探针复合物和释放游离探针的洗脱液并用于下游处理,例如下一代测序。
[0199]
在微流控装置的处理管道内进行的反应/固态合成在一些实施例中,本公开提供了在微流控装置的处理管道中进行一个或多个固相反应的方法。一般来说,在本公开的微流控装置的处理管道中进行一种或多种固相反应的方法包括:(i) 将输入样品内的适当官能化分子的子集与存在于处理管道的腔室内的官能化珠粒结合;(ii) 使一种或多种洗涤溶液流过处理管道以去除包括在输入样品内的未结合分子、试剂和/或杂质;(iii) 使一种或多种试剂流入处理管道;以及 (iv) 使溶液流过
10 中的左图)。这表明可以实现用本公开的微流控装置高效捕获生物素化寡核苷酸。
[0205]
示例 2
ꢀ–
靶的捕获和温度介导释放测试了靶-探针复合物的捕获,然后是靶寡核苷酸的温度介导释放。靶寡核苷酸首先与含有互补序列的生物素化探针退火。使用 10 倍过量的探针以确保所有靶标都与生物素化探针复合。然后使包括靶-探针复合物 (500 pmol) 的 50 μl 样品输入流过装有链霉亲和素包被的珠粒的微流控装置。总共收集了流通 (ff) 的 5 个馏分(每一个 10 μl x 5 次)。然后用 pbs 缓冲剂洗涤微流控装置并且收集洗涤缓冲剂 (w)。最后,将微流控装置的装有珠粒的腔室加热至约 95℃ 以使附着在珠粒表面的探针中的靶寡核苷酸变性,并且收集洗脱液 (e)。随后使用对靶寡核苷酸特异性的引物对 1 个样品输入 (i) 和来自装置的 3 个集合 (ff、w、e) 运行 qpcr。结果在图 11 中示出,这表明靶-探针复合物被微流控装置内的珠粒捕获,捕获效率为 98%,并且洗涤损失最小 (《 1%)。温度介导释放之后的总回收率计算为约 24%。如此低的释放效率归因于流体收集效率低下,观察到流体收集受到 95℃ 下装有珠粒的腔室中生成的气泡的阻碍。
[0206]
示例 3
ꢀ–
靶的捕获和酶促释放接下来测试靶-探针复合物的捕获和酶促释放。对于特异性酶促切割,将尿嘧啶置于探针序列和生物素之间(图 12)。然后靶寡核苷酸与掺入尿嘧啶的生物素化探针退火。使用 10 倍过量的探针以确保所有靶标都与生物素化探针复合。然后使含有靶-探针复合物 (500 pmol) 的 50 μl 样品输入流过装有链霉亲和素包被的珠粒的微流控装置。总共收集了流通 (ff) 的 5 个馏分(每一个 10 μl x 5 次)。然后用 pbs 缓冲剂洗涤装置并且收集洗涤缓冲剂 (w)。最后,将装有珠粒的腔室与尿嘧啶特异性切除试剂 ("user") 酶一起孵育,以切割尿嘧啶位点并从珠粒表面释放靶-探针复合物,并且收集洗脱液 (e)。在这里,尿嘧啶位于探针序列和生物素之间。随后,使用对靶寡核苷酸特异性的引物对 1 个样品输入 (i) 和来自装置的 3 个集合 (ff、w、e) 运行 qpcr。计算出靶-探针复合物的捕获效率约为 75%,缓冲剂洗涤的损失最小 (《 1%)。酶促切割的释放效率约为 72%,导致总回收率(洗脱液/输入)为 53.6%。
[0207]
本说明书中提到的和/或应用数据表中列出的所有美国专利、美国专利申请公开、美国专利申请、国外专利、国外专利以及非专利公开均通过引用整体并入本文。如有必要,可对实施例的各个方面进行修改,从而采用各类专利、申请和公开的概念来提供其他进一步的实施例。
[0208]
尽管已经参照一些说明性实施例描述了本公开,但应当理解,本领域技术人员可以在本公开原则的精神和范围内设计出许多其他的修改和实施例。更具体地,在不违背本公开的精神的情况下,在上述公开、附图和所附权利要求的范围内,所述主题组合排列的组成部分和/或布置可以进行合理的变化和修改。除了在所述组成部分和/或布置中的变化和修改外,对于本领域技术人员来说,替代用途也将是显而易见的。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1