一种木炭基仿生催化材料的制备方法及应用
1.本发明涉及一种催化材料的制备方法及应用。
背景技术:
2.随着工业化的快速发展,大量有机污染物排放到水体中,严重威胁着人类的健康和生态系统的稳定。高级氧化工艺(aop)因其高矿化率和非选择性降解,被认为是一种非常有前途的废水处理策略。在其中,非均相芬顿反应通常比传统的均相反应具有明显优势,在一定程度上解决了均相芬顿的缺点,如ph范围的扩展和稳定性的增强。然而非均相催化剂仍存在活性位点不足、容易浸出造成二次污染等难题。当前,对非均相催化剂的调控策略,主要以调整尺寸/形貌/晶相、杂原子掺杂、异质结构建等为主。其中,异质结系统中存在不同金属之间的协同效应。一边作为电子对受体或供体,另一边作为氧化还原中心,这种微界面结构有助于实现电子的快速迁移。然而过去的研究表明,精确合成cu2o/cuo异质结构非常困难。制备的cu2o/cuo易结构混乱,异质结与污染物之间有效接触面积不足,导致其催化活性不足。同时由于cu2o/cuo结构的不确定性,催化剂与载体之间的结合强度也会减弱,使整个催化体系不稳定。因此,可控的合成兼具活性和稳定性的cu基异质结仍是一个重大挑战。
技术实现要素:
3.本发明的目的是要解决现有精确合成cu2o/cuo异质结构非常困难,制备的cu2o/cuo易结构混乱,异质结与污染物之间有效接触面积不足,导致其催化活性不足和催化剂与载体之间的结合强度弱的问题,而提供一种木炭基仿生催化材料的制备方法及应用。
4.一种木炭基仿生催化材料的制备方法,是按以下步骤完成的:
5.一、将木材制备成横切片木材;
6.二、将横切片木材进行碳化,再超声清洗并烘干,得到木炭;
7.三、将木炭置于硼氢化钠溶液中浸泡,木炭取出后再置于化学镀液中浸泡,得到cu@wc;
8.四、将cu@wc置于刻蚀溶液中刻蚀,得到cu(oh)2@wc;
9.五、将cu(oh)2@wc置于惰性气体保护的管式炉中,将管式炉升温至450℃~500℃,在450℃~500℃下煅烧,得到木炭基仿生催化材料。
10.一种木炭基仿生催化材料用于降解有机污染物。
11.本发明的原理:
12.本发明提出了在具有多孔的高比表面积结构的木炭上构建稳定的cu2o/cuo异质结,从而达到快速降解有机污染物的目的;木材具有自然形成的微/纳通道,这种独特的结构在水处理中具有广阔的应用前景;在惰性气氛下高温形成的木炭保持并丰富了天然木材的多孔结构和大比表面积,可供携带污染物的水溶液快速渗透;而且其良好的导电性促进了界面电子的快速传输;本发明中以木炭为诱导模板材料,构筑的仿生催化剂能够快速降
解污染物,且保持结构的高度稳定性。这种具有仿生结构的木炭基催化剂将为废水处理提供一种新的解决策略。
13.本发明的优点:
14.一、本发明制备的木炭基仿生催化材料做为非均相类催化剂,方块形状的固体载体,降解时使用方便;
15.二、本发明构建的类海胆仿生结构异质结催化剂cu2o/cuo@wc(木炭基仿生催化材料),异质结使反应更加活跃,极大地促进了类fenton催化反应,类fenton非选择性的降解使得该催化剂可以作用于多种污染物;
16.三、本发明是一种构建稳定异质结的简便普适方法;
17.四、本发明选用的木材(天然杨木或者泡桐木)的多孔结构和较大的比表面积有助于催化剂活性部分与溶液中污染物分子接触,且做为性质稳定的基底使催化剂能多次有效的循环利用于降解;
18.五、本发明使用的原料来自于寻常的树木,制备过程方便且廉价;
19.六、本发明制备的木炭基仿生催化材料配合h2o2可在不同ph值、温度、污染物等复杂环境下均展现出了良好降解性能,降解率可达70%~100%。
20.本发明可获得一种木炭基仿生催化材料的制备方法。
附图说明
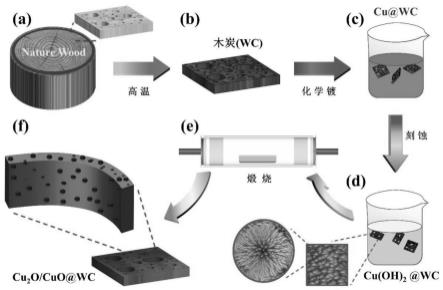
21.图1为本发明制备木炭基仿生催化材料的工艺流程图;
22.图2为天然杨木放大10000的扫描电子显微镜图;
23.图3为实施例一中步骤二得到的木炭的扫描电子显微镜图,图中(a)为木炭的孔洞形貌横切放大10000倍的扫描电子显微镜图,(b)为木炭的孔洞形貌纵切放大2000倍的扫描电子显微镜图;
24.图4为实施例一中步骤三得到的cu@wc放大10000倍的扫描电子显微镜图;
25.图5为实施例一中步骤四得到的cu(oh)2@wc放大5000倍的扫描电子显微镜图;
26.图6为实施例一中步骤五得到的cu2o/cuo@wc放大30000倍的扫描电子显微镜图;
27.图7为实施例一制备的cu@wc、cu(oh)2@wc、cu2o/cuo@wc的xrd图,图中1为cu@wc,2为cu(oh)2@wc,3为cu2o/cuo@wc;
28.图8为实施例一得到的cu2o/cuo@wc的xps图;
29.图9为实施例一得到的cu2o/cuo@wc的高分辨率透射电子显微镜图;
30.图10为降解效率图,图中
“■”
为使用h2o2降解亚甲基蓝,
“●”
为使用cu2o/cuo@wc降解亚甲基蓝,
“▼”
为使用cu2o/cuo@wc和h2o2降解亚甲基蓝,
“▲”
为使用叔丁醇、cu2o/cuo@wc和h2o2降解亚甲基蓝,c为当前时间点的浓度,c0为初始浓度;
31.图11为cu2o/cuo@wc-h2o2体系中产生的1o2的epr谱图,图中1为未加入亚甲基蓝5min时cu2o/cuo@wc-h2o2体系产生的1o2反应强度,2为加入亚甲基蓝后5min体系中1o2的反应强度;
32.图12为cu2o/cuo@wc-h2o2体系中产生的
·
oh的epr谱图,图中1为未加入亚甲基蓝5min时cu2o/cuo@wc-h2o2体系产生的
·
oh反应强度,2为加入亚甲基蓝后5min体系中
·
oh的反应强度;
33.图13为使用实施例一中步骤五得到的cu2o/cuo@wc和h2o2降解有机污染物的降解效率图,图中
“■”
为降解亚甲基蓝,
“●”
为降解双酚a,
“▲”
为降解甲基橙,
“▼”
为降解罗丹明b;
34.图14为使用实施例一中步骤五得到的cu2o/cuo@wc和h2o2降解亚甲基蓝过程中溶液颜色变化图,图中1为10min,2为30min,3为60min,4为90min,5为120min,6为180min;
35.图15为使用实施例一中步骤五得到的cu2o/cuo@wc和h2o2降解甲基橙过程中溶液颜色变化图,图中1为10min,2为30min,3为60min,4为90min,5为120min,6为180min;
36.图16为使用实施例一中步骤五得到的cu2o/cuo@wc和h2o2降解罗丹明b过程中溶液颜色变化图,图中1为10min,2为30min,3为60min,4为90min,5为120min,6为180min;
37.图17为使用实施例一中步骤五得到的cu2o/cuo@wc和h2o2降解亚甲基蓝过程中紫外吸收光谱图,图中自上而下的曲线依次为0min、10min、30min、60min、90min、120min和180min;
38.图18为使用实施例一中步骤五得到的cu2o/cuo@wc和h2o2降解甲基橙过程中紫外吸收光谱图,图中1为0min,2为60min,3为180min,其余为10min、30min、90min和120min;
39.图19为使用实施例一中步骤五得到的cu2o/cuo@wc和h2o2降解罗丹明b过程中紫外吸收光谱图,图中自上而下的曲线依次为0min、10min、30min、60min、90min、120min和180min;
40.图20为使用实施例一中步骤五得到的cu2o/cuo@wc和h2o2降解双酚a过程中紫外吸收光谱图,图中1为0min、2为10min、3为30min、4为60min、5为90min、6为120min,7为180min;
41.图21为重复使用实施例一中步骤五得到的cu2o/cuo@wc与h2o2作用降解亚甲基蓝,图中1st为第一次使用cu2o/cuo@wc,2nd为第二次使用cu2o/cuo@wc,3rd为第三次使用cu2o/cuo@wc。
具体实施方式
42.以下实施例进一步说明本发明的内容,但不应理解为对本发明的限制。在不背离本发明实质的情况下,对本发明方法、步骤或条件所作的修改和替换,均属于本发明的范围。
43.具体实施方式一:本实施方式一种木炭基仿生催化材料的制备方法是按以下步骤完成的:
44.一、将木材制备成横切片木材;
45.二、将横切片木材进行碳化,再超声清洗并烘干,得到木炭;
46.三、将木炭置于硼氢化钠溶液中浸泡,木炭取出后再置于化学镀液中浸泡,得到cu@wc;
47.四、将cu@wc置于刻蚀溶液中刻蚀,得到cu(oh)2@wc;
48.五、将cu(oh)2@wc置于惰性气体保护的管式炉中,将管式炉升温至450℃~500℃,在450℃~500℃下煅烧,得到木炭基仿生催化材料。
49.具体实施方式二:本实施方式与具体实施方式一不同点是:步骤一中所述的木材为天然杨木或者泡桐木。其它步骤与具体实施方式一相同。
50.具体实施方式三:本实施方式与具体实施方式一或二之一不同点是:步骤二中所
述的碳化工艺为:首先在220℃~250℃下碳化6h~8h,再在900℃~1000℃下碳化1.5h~2h;步骤二中所述的超声清洗的清洗剂为水,超声清洗的次数为3次~5次,每次超声清洗的时间为20min~30min,超声清洗的功率为200w~240w;步骤二中所述的烘干的温度为50℃~65℃;烘干的时间为12h~13h。其它步骤与具体实施方式一或二相同。
51.具体实施方式四:本实施方式与具体实施方式一至三之一不同点是:步骤三中所述的硼氢化钠溶液为硼氢化钠和naoh溶解到水中得到,其中,硼氢化钠溶液中硼氢化钠的浓度为5g/l~7g/l,naoh的浓度为2g/l~3g/l。其它步骤与具体实施方式一至三相同。
52.具体实施方式五:本实施方式与具体实施方式一至四之一不同点是:步骤三中将木炭置于硼氢化钠溶液中浸泡的时间为20min~30min,木炭取出后再置于化学镀液中浸泡的时间为1h~1.5h。其它步骤与具体实施方式一至四相同。
53.具体实施方式六:本实施方式与具体实施方式一至五之一不同点是:步骤三中所述的化学镀液为niso4、cuso4、nah2po2和h3bo3、na3c6h5o7·
2h2o溶解到水中得到,其中niso4的浓度为2g/l~2.5g/l,cuso4的浓度为10g/l~15g/l,nah2po2的浓度为40g/l~45g/l,h3bo3的浓度为30g/l~35g/l,na3c6h5o7·
2h2o的浓度为30g/l~32g/l。其它步骤与具体实施方式一至五相同。
54.具体实施方式七:本实施方式与具体实施方式一至六之一不同点是:步骤三中木炭取出后再置于化学镀液中浸泡的时间为1h~1.5h;步骤三中化学镀液的温度为70℃~75℃。其它步骤与具体实施方式一至六相同。
55.具体实施方式八:本实施方式与具体实施方式一至七之一不同点是:步骤四中所述的刻蚀溶液为(nh4)2s2o8、naoh和nh3·
h2o溶解到水中得到,其中(nh4)2s2o8的浓度为12.5mol/l~15mol/l,naoh的浓度为20mol/l~25mol/l,nh3·
h2o的浓度为16.7mol/l~17mol/l。其它步骤与具体实施方式一至七相同。
56.具体实施方式九:本实施方式与具体实施方式一至八之一不同点是:步骤四中所述的刻蚀时间为1h~2h;步骤五中所述的煅烧的时间为1h~2.5h;步骤五中所述的惰性气体为氮气或氩气。其它步骤与具体实施方式一至八相同。
57.具体实施方式十:本实施方式是一种木炭基仿生催化材料用于降解有机污染物。
58.下面结合附图和实施例对本发明进行详细的说明。
59.实施例一:一种木炭基仿生催化材料的制备方法,是按以下步骤完成的:
60.一、将天然杨木制备成厚度为2mm的横切片天然杨木;
61.二、将横切片天然杨木首先在240℃下碳化6h,然后在1000℃下碳化2h,超声清洗并烘干,得到木炭(wc);
62.步骤二中所述的超声清洗的清洗剂为水,超声清洗的次数为5次,每次超声清洗的时间为20min,超声清洗的功率为200w;
63.步骤二中所述的烘干的温度为60℃;烘干的时间为12h;
64.三、将木炭置于硼氢化钠溶液中浸泡20min,木炭取出后再置于温度为70℃的化学镀液中浸泡1h,得到cu@wc;
65.步骤三中所述的硼氢化钠溶液为硼氢化钠和naoh溶解到水中得到,其中,硼氢化钠溶液中硼氢化钠的浓度为5g/l,naoh的浓度为2g/l;
66.步骤三中所述的化学镀液为niso4、cuso4、nah2po2和h3bo3、na3c6h5o7·
2h2o溶解到
水中得到,其中niso4的浓度为2g/l,cuso4的浓度为10g/l,nah2po2的浓度为40g/l,h3bo3的浓度为30g/l,na3c6h5o7·
2h2o的浓度为30g/l;
67.四、将cu@wc置于刻蚀溶液中刻蚀1h,得到cu(oh)2@wc;
68.步骤四中所述的刻蚀溶液为(nh4)2s2o8、naoh和nh3·
h2o溶解到水中得到,其中(nh4)2s2o8的浓度为12.5mol/l,naoh的浓度为25mol/l,nh3·
h2o的浓度为16.7mol/l;
69.五、将cu(oh)2@wc置于惰性气体保护的管式炉中,将管式炉升温至450℃,在450℃下煅烧2h,得到木炭基仿生催化材料(cu2o/cuo@wc);
70.步骤五中所述的惰性气体为氩气。
71.图2为天然杨木放大10000的扫描电子显微镜图;
72.图3为实施例一中步骤二得到的木炭的扫描电子显微镜图,图中(a)为木炭的孔洞形貌横切放大10000倍的扫描电子显微镜图,(b)为木炭的孔洞形貌纵切放大2000倍的扫描电子显微镜图;
73.图4为实施例一中步骤三得到的cu@wc放大10000倍的扫描电子显微镜图;
74.图5为实施例一中步骤四得到的cu(oh)2@wc放大5000倍的扫描电子显微镜图;
75.图6为实施例一中步骤五得到的cu2o/cuo@wc放大30000倍的扫描电子显微镜图;
76.实施例一中通过天然杨木得到多孔结构的木片,对木材碳化,获得了优化的木炭(wc);木炭保持了与杨木木材相似的多通道结构,而且在碳表面形成更丰富的纳米孔,用作金属的选择性沉积位置;图4的cu@wc形貌表明化学镀使铜粒子均匀分散在负载木炭上;然后刻蚀将cu转换为cu(oh)2,显示了类似于海胆形状的独特纳米结构(图5);在高温处理下,形成的cu(oh)2仍呈现出海胆状的结构,最终得到了自支撑的cu2o/cuo@wc仿生催化材料(图6)。
77.图7为实施例一制备的cu@wc、cu(oh)2@wc、cu2o/cuo@wc的xrd图,图中1为cu@wc,2为cu(oh)2@wc,3为cu2o/cuo@wc;
78.图9中的hrtem图像显示了间距分别为0.243、0.255、0.250nm的晶格条纹,对应于cu2o的(111)晶面,以及cuo的(002)、(111)晶面,证明了cu2o/cuo异质结已经成功地生长在木炭上。
79.图8为实施例一得到的cu2o/cuo@wc的xps图;
80.从图8可知,图中明确证明cu
2+
与cu
+
的存在,说明煅烧后出现了cu2o与cuo。
81.图9为实施例一得到的cu2o/cuo@wc的高分辨率透射电子显微镜图;
82.从图9可知,高分辨率透射图显示出,两个不同区域的属于两种金属氧化物的晶格条纹,在平面内横向的堆叠到一起,表明了cu2o/cuo异质结的形成。
83.应用实施例:
84.应用实施例1:将160ul质量分数为30%的h2o2加入到60ml亚甲基蓝浓度为20mg/l的废水中,在室温下降解0min~180min,降解效率见图10中
“■”
所示;
85.应用实施例2:将表面积为5cm2实施例一中步骤五得到的cu2o/cuo@wc加入到60ml亚甲基蓝浓度为20mg/l的废水中,在室温下降解0min~180min,降解效率见图10中
“●”
所示;
86.应用实施例3:将表面积为5cm2实施例一中步骤五得到的cu2o/cuo@wc和160ul质量分数为30%的h2o2加入到60ml亚甲基蓝浓度为20mg/l的废水中,在室温下降解0min~
180min,降解效率见图10中
“▼”
所示;
87.应用实施例4:将表面积为5cm2实施例一中步骤五得到的cu2o/cuo@wc、160ul质量分数为30%的h2o2和8ml叔丁醇(tba)加入到60ml亚甲基蓝浓度为20mg/l,在室温下降解0min~180min,降解效率见图10中
“▲”
所示。
88.图10为降解效率图,图中
“■”
为使用h2o2降解亚甲基蓝,
“●”
为使用cu2o/cuo@wc降解亚甲基蓝,
“▼”
为使用cu2o/cuo@wc和h2o2降解亚甲基蓝,
“▲”
为使用叔丁醇、cu2o/cuo@wc和h2o2降解亚甲基蓝,c为当前时间点的浓度,c0为初始浓度;
89.从图10可知,使用cu2o/cuo@wc和h2o2对亚甲基蓝的降解效果良好。
90.图11为cu2o/cuo@wc-h2o2体系中产生的1o2的epr谱图,图中1为未加入亚甲基蓝5min时cu2o/cuo@wc-h2o2体系产生的1o2反应强度,2为加入亚甲基蓝后5min体系中1o2的反应强度;
91.从图11可知,这证明了cu2o/cuo@wc-h2o2体系了1o2,而且参与到了污染物降解的过程中。
92.图12为cu2o/cuo@wc-h2o2体系中产生的
·
oh的epr谱图,图中1为未加入亚甲基蓝5min时cu2o/cuo@wc-h2o2体系产生的
·
oh反应强度,2为加入亚甲基蓝后5min体系中
·
oh的反应强度;
93.图12证明了cu2o/cuo@wc-h2o2体系了
·
oh,而且参与到了污染物降解的过程中。
94.实施例一中步骤五得到的cu2o/cuo@wc降解双酚a、罗丹明b、亚甲基蓝和甲基橙的降解性能:
95.应用实施例5:将表面积为5cm2实施例一中步骤五得到的cu2o/cuo@wc、160ul质量分数为30%的h2o2加入到60ml亚甲基蓝浓度为20mg/l的废水中,在室温下降解0min~180min,降解效率见图13中
“■”
所示,溶液颜色变化见图14所示,紫外吸收光谱图见图17所示;
96.应用实施例6:将表面积为5cm2实施例一中步骤五得到的cu2o/cuo@wc、160ul质量分数为30%的h2o2加入到60ml双酚a浓度为10mg/l的废水中,在室温下降解0min~180min,降解效率见图13中
“●”
所示,紫外吸收光谱图见图17所示,紫外吸收光谱图见图20所示;
97.应用实施例7:将表面积为5cm2实施例一中步骤五得到的cu2o/cuo@wc、160ul质量分数为30%的h2o2加入到60ml亚甲基橙浓度为20mg/l的废水中,在室温下降解0min~180min,降解效率见图13中
“▲”
所示,溶液颜色变化见图15所示,紫外吸收光谱图见图18所示;
98.应用实施例8:将表面积为5cm2实施例一中步骤五得到的cu2o/cuo@wc、160ul质量分数为30%的h2o2加入到60ml罗丹明b浓度为20mg/l的废水中,在室温下降解0min~180min,降解效率见图13中
“▼”
所示,溶液颜色变化见图16所示,紫外吸收光谱图见图19所示;
99.图13为使用实施例一中步骤五得到的cu2o/cuo@wc和h2o2降解有机污染物的降解效率图,图中
“■”
为降解亚甲基蓝,
“●”
为降解双酚a,
“▲”
为降解甲基橙,
“▼”
为降解罗丹明b;
100.从图13可知,双酚a、罗丹明b、亚甲基蓝和甲基橙,去除率分别为85%、70%、90%、95%,正如预期,cu2o/cuo@wc均能够实现上述有机污染物有效降解。
101.图14为使用实施例一中步骤五得到的cu2o/cuo@wc和h2o2降解亚甲基蓝过程中溶液颜色变化图,图中1为10min,2为30min,3为60min,4为90min,5为120min,6为180min;
102.图15为使用实施例一中步骤五得到的cu2o/cuo@wc和h2o2降解甲基橙过程中溶液颜色变化图,图中1为10min,2为30min,3为60min,4为90min,5为120min,6为180min;
103.图16为使用实施例一中步骤五得到的cu2o/cuo@wc和h2o2降解罗丹明b过程中溶液颜色变化图,图中1为10min,2为30min,3为60min,4为90min,5为120min,6为180min;
104.从图14~图16可知,除双酚a溶液原本无色透明以外,其他溶液颜色明显变淡。
105.图17为使用实施例一中步骤五得到的cu2o/cuo@wc和h2o2降解亚甲基蓝过程中紫外吸收光谱图,图中自上而下的曲线依次为0min、10min、30min、60min、90min、120min和180min;
106.从图17可知,亚甲基蓝最大吸收峰位于664nm左右,随时间进行最大吸收峰逐渐降低,表明亚甲基蓝的逐渐去除。
107.图18为使用实施例一中步骤五得到的cu2o/cuo@wc和h2o2降解甲基橙过程中紫外吸收光谱图,图中1为0min,2为60min,3为180min,其余为10min、30min、90min和120min;
108.从图18可知,甲基橙最大吸收峰位于460nm左右,随时间进行最大吸收峰逐渐降低,表明甲基橙的逐渐去除;
109.图19为使用实施例一中步骤五得到的cu2o/cuo@wc和h2o2降解罗丹明b过程中紫外吸收光谱图,图中自上而下的曲线依次为0min、10min、30min、60min、90min、120min和180min;
110.从图19可知,罗丹明b最大吸收峰位于550nm左右,随时间进行最大吸收峰逐渐降低,表明罗丹明b的逐渐去除。
111.图20为使用实施例一中步骤五得到的cu2o/cuo@wc和h2o2降解双酚a过程中紫外吸收光谱图,图中1为0min、2为10min、3为30min、4为60min、5为90min、6为120min,7为180min;
112.从图20可知,双酚a最大吸收峰位于278nm左右,随时间进行最大吸收峰逐渐降低,表明双酚a的逐渐去除。
113.应用实施例9:将表面积为5cm2实施例一中步骤五得到的cu2o/cuo@wc和160ul质量分数为30%的h2o2加入到60ml亚甲基蓝浓度为20mg/l的废水中,在室温下降解180min,如此循环3次;
114.按照上述试验方法,以亚甲基蓝作为污染物,使用实施例一中步骤五得到的cu2o/cuo@wc重复循环降解亚甲基蓝,降解效率见图21所示;
115.图21为重复使用实施例一中步骤五得到的cu2o/cuo@wc与h2o2作用降解亚甲基蓝,图中1st为第一次使用cu2o/cuo@wc,2nd为第二次使用cu2o/cuo@wc,3rd为第三次使用cu2o/cuo@wc;
116.循环实验的结果表明cu2o/cuo@wc在第3次循环后,依旧显示出超过95.0%的降解率,表明cu2o/cuo@wc该催化剂具有稳定的催化性能。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1