一种分离氯丙烷和氯丙烯混合气体的吸附剂及其制备方法与分离方法
1.本发明属于化工分离技术领域,具体涉及一种分离氯丙烷和氯丙烯混合气体的吸附剂及其制备方法与分离方法。
背景技术:
2.氯丙烯(c3h5cl)是一种重要的有机化工原料,可用于制备环氧氯丙烷(ech),并进一步合成环氧树脂和氯醇橡胶等产品;在工业应用中对氯丙烯原料的纯度要求很高(聚合级),原料的纯度直接影响最终产物的质量。目前,氯丙烯的生产方法主要有:高温氯化法和氧化氯化法。这两种方法虽然可以获得纯度较高的氯丙烯产物,但距离聚合级纯度还有一段距离,主要原因是其生产方法不可避免的会生成一系列其他的杂质,其中最难去除的就是氯丙烷。另外,在工业产品的生产过程中,氯丙烯过量,需要回收循环使用,也存在着氯丙烷的循环积累问题。因此,需要将原料及反应中间产物中的氯丙烷杂质与氯丙烯分离。
3.对于烯烃和烷烃的分离,目前最成熟的方法是多级精馏法。cn111100683a公开了一种费托合成油中长链烷烃-烯烃的分离方法,该方法包括:先将原料通入装填有脱氧吸附剂的预吸附塔进行吸附分离脱除原料中含氧化合物,使含氧化合物质量分数降低至0.1%以下;再将得到的物料送入装填有烷烯分离吸附剂的模拟移动床吸附分离系统进行烷烯吸附分离,选择性的将α-烯烃和烷烃分离得到两股物流,一股物流为富α-烯烃组分,另一股物流为富烷烃组分;最后将富α-烯烃组分送入精馏单元,将解吸剂和α-烯烃切割得到α-烯烃和解吸剂,解吸剂循环回解吸剂储罐;将富烷烃组分送入精馏单元切割得到解吸剂和长链烷烃切割;该方法通过两段串联吸附分离工艺,可以获得具有高附加值的长链α-烯烃。
4.cn103864554a公开了一种从烃类混合物中萃取精馏分离烷烃、烯烃和芳烃的方法,涉及烃的萃取蒸馏分离方法,步骤是:在第一萃取精馏塔中,烃类混合物原料经过萃取剂萃取精馏,分离为芳烃和富含烷烃、烯烃的非芳烃混合物;在第二萃取精馏塔中,在萃取剂的作用下实现富含烷烃和烯烃的非芳烃混合物中烷烃与烯烃的分离;从第二萃取精馏塔回流泵取出烷烃产品,从一次再生塔回流泵取出烯烃产品,从第一萃取剂回收塔的塔顶得到芳烃混合物产品,萃取剂被回收循环利用;该方法克服了现有技术中经萃取精馏分离只能得到芳烃与非芳烃产品,无法实现对非芳烃中的烯烃和烷烃高附加值产品的进一步分离的缺陷。但是,低温精馏法会消耗大量能耗,例如,以精馏方式分离丙烯和丙烷往往需要精馏塔塔板数大于120,塔高高达90米,回流比大于10,还需辅助加压、制冷等工艺,因此,烯烃和烷烃的分离被列为七大能源密集型分离过程之一;相较与丙烯和丙烷,具有氯代基团的氯丙烯和氯丙烷的沸点、分子尺寸等物化性质更为相近,它们的分离更困难,耗能更高。
5.因此,亟需开发一种高效率、低能耗的氯丙烯和氯丙烷混合气体的分离方法。
技术实现要素:
6.本发明的目的在于提供一种分离氯丙烷和氯丙烯混合气体的吸附剂及其制备方
法与分离方法,所述吸附剂由过渡金属离子和有机配体构成;所述吸附剂的结构式为m(c7o5h4)
·
2h2o,其中,m为过渡金属离子;所述吸附剂的孔径为所述吸附剂为三维网状结构;本发明所述吸附剂对分子动力学尺寸较小的氯丙烯表现出了选择性吸附,分子尺寸较大的氯丙烷则排阻在孔道外,从而实现混合气体中对氯丙烯和氯丙烷的吸附分离,选择性分离效率高;且制备方法简单,原料易得,成本低,使用寿命长,易再生,可重复利用,具有显著的工业应用前景。
7.为达到此发明目的,本发明采用以下技术方案:
8.本发明的目的之一在于提供一种分离氯丙烷和氯丙烯混合气体的吸附剂,所述吸附剂由过渡金属离子和有机配体构成;所述吸附剂的结构式为m(c7o5h4)
·
2h2o,其中,m为过渡金属离子;所述吸附剂的孔径为所述吸附剂为三维网状结构。
9.本发明所述吸附剂是由有机配体与过渡金属离子通过配位键或者分子间作用力形成的三维网络结构,其孔径为从分子的动力学尺寸大小来看,氯丙烯和氯丙烷的最小分子动力学尺寸分别为和其中,氯丙烯具有更小的尺寸,能进入到吸附剂的孔道内并与孔道表面的官能团发生相互作用,而分子尺寸较大的氯丙烷则不能进入到孔道内部。本发明基于材料孔道大小对氯丙烯和氯丙烷的筛分作用,使得合成的孔径为的吸附剂对两种分子吸附量具有明显的差异,在单组分静态吸附时,超微孔金属有机框架材料对氯丙烯具有十分明显的吸附作用,在30℃条件下,其最高吸附量可达2mmol/g,但对氯丙烷几乎不吸附,最高吸附量仅为0.5mmol/g,表现出了对氯丙烯的选择性吸附,进而实现了对氯丙烯和氯丙烷的吸附分离;在混合组分的动态吸附时,因为超微孔金属有机框架材料对氯丙烷的吸附容量小,氯丙烷会最先从塔出口流出,而超微孔金属有机框架材料对氯丙烯的作用强且吸附容量大,则吸附有氯丙烯的超微孔金属有机框架材料从塔出口流出的时间更长,且本发明提供的吸附分离方法中所使用的超微孔金属有机框架材料吸附饱和后,只需在真空或者惰性气氛条件下加热至50-150℃,保持2-10h即可实现再生,从而也实现了对氯丙烯和氯丙烷的吸附分离。
10.值得说明的是,所述吸附剂的孔径为例如可以是例如可以是例如可以是等,若孔径大于则会导致氯丙烷也可扩散到吸附材料的孔道中,造成吸附材料的选择性下降;若孔径小于会导致氯丙烯的扩散阻力过大,进一步导致吸附剂的吸附量降低。
11.作为本发明优选的技术方案,所述过渡金属离子包括co
2+
、ni
2+
、fe
2+
或mg
2+
中的任意一种或至少两种的组合,所述组合典型但非限制性的实例包括co
2+
和ni
2+
的组合,co
2+
和fe
2+
的组合,co
2+
和mg
2+
的组合,ni
2+
和fe
2+
的组合,ni
2+
和mg
2+
的组合,fe
2+
和mg
2+
的组合。
12.优选地,所述有机配体为没食子酸。
13.本发明的目的之二在于提供一种目的之一所述吸附剂的制备方法,所述制备方法包括如下步骤:
14.将过渡金属盐、有机配体和碱溶液进行混合,依次经过反应和真空活化,得到吸附剂;
15.其中,所述过渡金属盐和所述有机配体的摩尔比为1:(0.5-1.5);所述过渡金属盐和所述碱溶液中碱的摩尔比为1:(0.05-10)。
16.值得说明的是,所述过渡金属盐和所述有机配体的摩尔比为1:(0.5-2),例如可以是1:0.5,1:0.7,1:0.9,1:1,1:1.2,1:1.4,1:1.5,1:1.6,1:1.8,1:2等;所述过渡金属盐和所述碱溶液中碱的摩尔比为1:(0.05-10),例如可以是1:0.05,1:0.1,1:0.5,1:1,1:2,1:3,1:4,1:5,1:6,1:7,1:8,1:9,1:10等,但并不仅限于所列举的数值,上述数值范围内其他未列举的数值同样适用。
17.作为本发明优选的技术方案,所述过渡金属盐的金属阳离子包括co
2+
、ni
2+
、fe
2+
或mg
2+
中的任意一种或至少两种的组合,所述组合典型但非限制性的实例包括co
2+
和ni
2+
的组合,co
2+
和fe
2+
的组合,co
2+
和mg
2+
的组合,ni
2+
和fe
2+
的组合,ni
2+
和mg
2+
的组合,fe
2+
和mg
2+
的组合;所述过渡金属盐的阴离子包括cl-、no
3-或so
42-中的任意一种或至少两种的组合,所述组合典型但非限制性的实例包括cl-和no
3-的组合,cl-和so
42-的组合,no
3-和so
42-的组合。
18.值得说明的是,本发明通过调控过渡金属盐的种类,将所得吸附剂的孔径控制在
19.优选地,所述有机配体为没食子酸。
20.优选地,所述碱溶液中碱的浓度为0.01-0.5mol/l;例如可以是0.01mol/l,0.05mol/l,0.1mol/l,0.15mol/l,0.2mol/l,0.25mol/l,0.3mol/l,0.35mol/l,0.4mol/l,0.45mol/l,0.5mol/l等,但并不仅限于所列举的数值,上述数值范围内其他未列举的数值同样适用。
21.优选地,所述碱溶液的溶剂包括去离子水。
22.优选地,所述碱溶液中的碱包括naoh、koh或lioh中的任意一种或至少两种的组合,所述组合典型但非限制性的实例包括naoh和koh的组合,naoh和lioh的组合,koh和lioh的组合。
23.作为本发明优选的技术方案,所述混合的方式为搅拌。
24.优选地,所述搅拌的转速为500-1000rpm,例如可以是500rpm,550rpm,600rpm,650rpm,700rpm,750rpm,800rpm,850rpm,900rpm,950rpm,1000rpm等,但并不仅限于所列举的数值,上述数值范围内其他未列举的数值同样适用。
25.作为本发明优选的技术方案,所述反应的温度为100-140℃,例如可以是100℃,105℃,110℃,115℃,120℃,125℃,130℃,135℃,140℃等,但并不仅限于所列举的数值,上述数值范围内其他未列举的数值同样适用。
26.优选地,所述反应的时间为24-72h,例如可以是24h,28h,30h,32h,35h,38h,40h,43h,45h,47h,50h,52h,56h,60h,62h,65h,67h,70h,72h等,但并不仅限于所列举的数值,上述数值范围内其他未列举的数值同样适用。
27.作为本发明优选的技术方案,所述制备方法还包括:在所述反应之后,所述真空活化之前,对所述反应的反应产物进行洗涤。
28.优选地,所述洗涤使用的洗涤剂包括乙醇。
29.作为本发明优选的技术方案,所述真空活化的温度为50-150℃,例如可以是50℃,60℃,70℃,80℃,90℃,100℃,110℃,120℃,130℃,140℃,150℃等,进一步优选为100-140℃,例如可以是100℃,105℃,110℃,115℃,120℃,125℃,130℃,135℃,140℃等,但并不仅
限于所列举的数值,上述数值范围内其他未列举的数值同样适用。
30.优选地,所述真空活化的时间为18-48h,例如可以是18h,20h,25h,30h,35h,40h,45h,48h等,进一步优选为24-32h,例如可以是24h,25h,26h,27h,28h,29h,30h,31h,32h等,但并不仅限于所列举的数值,上述数值范围内其他未列举的数值同样适用。
31.作为本发明优选的技术方案,所述制备方法包括如下步骤:
32.将过渡金属盐、没食子酸和0.01-0.5mol/l的碱溶液在500-1000rpm的转速搅拌混合,在100-140℃℃反应24-72h,并使用乙醇进行清洗;在温度50-150℃的条件下真空活化18-48h,得到吸附剂;
33.其中,过渡金属盐和没食子酸的摩尔比为1:(0.5-2);所述过渡金属盐和所述碱溶液中碱的摩尔比为1:(0.05-10);所述过渡金属盐的金属阳离子包括co
2+
、ni
2+
、fe
2+
或mg
2+
中的任意一种或至少两种的组合,所述过渡金属盐的阴离子包括cl-、no
3-或so
42-中的任意一种或至少两种的组合;所述碱溶液中的碱包括naoh、koh或lioh中的任意一种或至少两种的组合。
34.本发明的目的之三在于提供一种目的之一所述吸附剂用于氯丙烷和氯丙烯混合气体的分离方法,所述分离方法包括如下步骤:将吸附剂至于氯丙烯和氯丙烷混合气体中,在0-50℃、10-500kpa下进行吸附分离。
35.本发明所述的数值范围不仅包括上述例举的点值,还包括没有例举出的上述数值范围之间的任意的点值,限于篇幅及出于简明的考虑,本发明不再穷尽列举所述范围包括的具体点值。
36.相对于现有技术,本发明具有以下有益效果:
37.(1)本发明所述分离氯丙烷和氯丙烯混合气体的吸附剂的孔径为其对分子动力学尺寸较小的氯丙烯表现出了选择性吸附,分子尺寸较大的氯丙烷则排阻在孔道外,从而实现混合气体中对氯丙烯和氯丙烷的吸附分离,且选择性分离效率高;
38.(2)本发明所述分离氯丙烷和氯丙烯混合气体的吸附剂的制备方法简单,原料易得,成本低,使用寿命长,且易再生,可重复利用,具有显著的工业应用前景。
附图说明
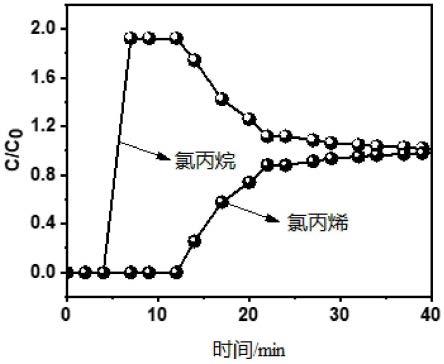
39.图1为实施例1所述吸附剂在30℃对氯丙烯和氯丙烷的穿透曲线;
40.图2为实施例1所述吸附剂在30℃对氯丙烯和氯丙烷的吸附等温线。
具体实施方式
41.下面通过具体实施方式来进一步说明本发明的技术方案。本领域技术人员应该明了,所述实施例仅仅是帮助理解本发明,不应视为对本发明的具体限制。
42.实施例1
43.本实施例提供了一种分离氯丙烷和氯丙烯混合气体的吸附剂及其制备方法,所述吸附剂的结构式为co(c7o5h4)
·
2h2o,所述吸附剂的孔径为所述吸附剂为三维网状结构;所述制备方法包括如下步骤:
44.将cocl2、没食子酸、0.05mol/l的koh水溶液在800rpm的转速搅拌混合,在120℃反应24h,并使用乙醇进行清洗;在温度120℃的条件下真空活化24h,得到吸附剂;
45.其中,cocl2和没食子酸的摩尔比为1:2;cocl2和koh的摩尔比为1:0.5。
46.实施例2
47.本实施例提供了一种分离氯丙烷和氯丙烯混合气体的吸附剂及其制备方法,所述吸附剂的结构式为mg(c7o5h4)
·
2h2o,所述吸附剂的孔径为所述吸附剂为三维网状结构;参照实施例1所述的制备方法,区别仅在于:将cocl2替换为mgcl2。
48.实施例3
49.本实施例提供了一种分离氯丙烷和氯丙烯混合气体的吸附剂及其制备方法,所述吸附剂的结构式为ni(c7o5h4)
·
2h2o,所述吸附剂的孔径为所述吸附剂为三维网状结构;参照实施例1所述的制备方法,区别仅在于:将cocl2替换为nicl2。
50.实施例4
51.本实施例提供了一种分离氯丙烷和氯丙烯混合气体的吸附剂及其制备方法,所述吸附剂的结构式为co(c7o5h4)
·
2h2o,所述吸附剂的孔径为所述吸附剂为三维网状结构;参照实施例1所述的制备方法,区别仅在于koh溶液的浓度为0.1mol/l。
52.实施例5
53.本实施例提供了一种分离氯丙烷和氯丙烯混合气体的吸附剂及其制备方法,所述吸附剂的结构式为co(c7o5h4)
·
2h2o,所述吸附剂的孔径为所述吸附剂为三维网状结构;所述制备方法包括如下步骤:
54.将cocl2、没食子酸、0.5mol/l的koh水溶液在500rpm的转速搅拌混合,在100℃反应72h,并使用乙醇进行清洗;在温度150℃条件下真空活化18h,得到吸附剂;
55.其中,cocl2和没食子酸的摩尔比为1:1;cocl2和koh的摩尔比为1:10。
56.实施例6
57.本实施例提供了一种分离氯丙烷和氯丙烯混合气体的吸附剂及其制备方法,所述吸附剂的结构式为co(c7o5h4)
·
2h2o,所述吸附剂的孔径为所述吸附剂为三维网状结构;所述制备方法包括如下步骤:
58.将cocl2、没食子酸、0.01mol/l的koh水溶液在1000rpm的转速搅拌混合,在140℃反应48h,并使用乙醇进行清洗;在温度50℃条件下真空活化48h,得到吸附剂;
59.其中,cocl2和没食子酸的摩尔比为1:0.5;cocl2和koh的摩尔比为1:0.05。
60.对比例1
61.本对比例提供了一种分离氯丙烷和氯丙烯混合气体的吸附剂及其制备方法,所述吸附剂的结构式为zn(c7o5h4)
·
2h2o,所述吸附剂的孔径为所述吸附剂为三维网状结构;所述制备方法包括如下步骤:
62.将zncl2、没食子酸、0.05mol/l的koh水溶液在在800rpm的转速搅拌混合,在120℃反应24h,并使用乙醇进行清洗;在温度120℃、条件下真空活化24h,得到吸附剂;
63.其中,zncl2和没食子酸的摩尔比为1:2;zncl2和koh的摩尔比为1:0.5。
64.对比例2
65.本对比例提供了一种分离氯丙烷和氯丙烯混合气体的吸附剂及其制备方法,所述吸附剂的结构式为mn(c7o5h4)
·
2h2o,所述吸附剂的孔径为所述吸附剂为三维网状
结构;所述制备方法包括如下步骤:
66.将mncl2、没食子酸、0.05mol/l的koh水溶液在800rpm的转速搅拌混合,在120℃反应24h,并使用乙醇进行清洗;在温度120℃条件下真空活化24h,得到吸附剂;
67.其中,mncl2和没食子酸的摩尔比为1:2;mncl2和koh的摩尔比为1:0.05。
68.将上述实施例与对比例所得吸附剂对氯丙烯、氯丙烷的吸附量和分离选择性进行测试,测试方法如下:
69.吸附量:由全自动容量法气体吸附仪(microtracbel belsorp-max)测得吸附剂对各气体的吸附等温线,从而测得吸附量;
70.分离选择性:吸附剂对氯丙烯的分离选择性计算公式为:
[0071][0072]
q1和q2是指吸附剂在p1和p2分压下的平衡吸附量,分离选择性为吸附剂在101kpa分压下的选择性;
[0073]
将上述实施例与对比例中氯丙烯、氯丙烷的吸附量和吸附选择性的测试结果列于表1。
[0074]
表1
[0075][0076][0077]
由表1可以得出以下几点:
[0078]
(1)由实施例1-6可以看出,本发明所制备的吸附剂表现出了对氯丙烯的优先吸附,对氯丙烯的吸附量均明显大于氯丙烷的吸附量,实现混合气体中对氯丙烯和氯丙烷的吸附分离,且选择性分离效率高;
[0079]
(2)由实施例1-3可以看出,吸附剂中过渡金属离子的种类实现了对吸附性能的调控,实施例1-3的孔径依次减小,其对氯丙烯和氯丙烷的吸附量依次减小;
[0080]
(3)将实施例1和实施例4进行比较,可以看出,在不同的碱含量下合成的co(c7o5h4)
·
2h2o对氯丙烯的吸附性能相差不大;
[0081]
(4)将实施例1和对比例1、2进行比较,可以看出,由于对比例1中吸附剂的孔径为低于本发明优选的会导致氯丙烯的扩散阻力过大,进而导致吸附剂的吸附量降低;由于对比例2中吸附剂的孔径为超出本发明优选的会导致氯丙烷也可扩散到吸附材料的孔道中,造成吸附材料的选择性下降。
[0082]
应用例1
[0083]
将实施例1所得吸附剂co(c7o5h4)
·
2h2o装入内径为5mm的吸附柱中,30℃条件下,以氮气作为载气,将质量比为1:1的氯丙烯和氯丙烷的混合气体以3ml/min的速度通入吸附柱与吸附剂接触、在压力350kpa的条件下吸附混合气体中的氯丙烯,对流出的气体采用气相色谱仪进行气相检测,测试得到氯丙烷的浓度突然增加时,即为氯丙烷穿透,当氯丙烯穿透时完成氯丙烯和氯丙烷混合气体的吸附分离。
[0084]
本应用例得到的对氯丙烯和氯丙烷的穿透曲线如图1所示,从图1可以看出,氯丙烷在5分钟左右率先突破,并保持了一段时间;氯丙烯在13分钟左右突破,并最终达到平衡。
[0085]
本应用例在30℃时对氯丙烯和氯丙烷的吸附等温线如图2所示,从图2可以看出随着压力的升高,吸附剂对氯丙烯的吸附量明显增加,但对氯丙烷的吸附量很低。
[0086]
通过对本应用例中流出的气体进行气相色谱仪检测分析,在100℃抽真空将吸附氯丙烯后吸附剂进行解吸,得到氯丙烯气体,测试得到本应用例获得的氯丙烯的纯度大于99.99%,吸附柱可以循环使用。
[0087]
应用例2
[0088]
将实施例2所得吸附剂mg(c7o5h4)
·
2h2o装入内径为5mm的吸附柱中,45℃条件下,以氦气作为载气,将质量比为1:1的氯丙烯和氯丙烷的混合气体以3ml/min的速度通入吸附柱与吸附剂接触、在压力100kpa的条件下吸附混合气体中的氯丙烯,对流出的气体采用气相色谱仪进行气相检测,测试得到氯丙烷的浓度突然增加时,即为氯丙烷穿透,当氯丙烯穿透时完成氯丙烯和氯丙烷混合气体的吸附分离。
[0089]
通过对本应用例中流出的气体进行气相色谱仪检测分析,在100℃抽真空将吸附氯丙烯后吸附剂进行解吸,得到氯丙烯气体,测试得到本应用例获得的氯丙烯的纯度大于99.99%,吸附柱可以循环使用。
[0090]
应用例3
[0091]
将实施例3所得吸附剂ni(c7o5h4)
·
2h2o装入内径为5mm的吸附柱中,20℃条件下,以氦气作为载气,将质量比为1:1的氯丙烯和氯丙烷的混合气体以3ml/min的速度通入吸附柱与吸附剂接触、在压力200kpa的条件下吸附混合气体中的氯丙烯,对流出的气体采用气相色谱仪进行气相检测,测试得到氯丙烷的浓度突然增加时,即为氯丙烷穿透,当氯丙烯穿透时完成氯丙烯和氯丙烷混合气体的吸附分离。
[0092]
通过对本应用例中流出的气体进行气相色谱仪检测分析,在100℃抽真空将吸附氯丙烯后吸附剂进行解吸,得到氯丙烯气体,测试得到本应用例获得的氯丙烯的纯度大于99.99%,吸附柱可以循环使用。
[0093]
应用例4
[0094]
参照应用例1所述的方法将实施例1所得吸附剂co(c7o5h4)
·
2h2o用于分离氯丙烯和氯丙烷的混合气体,区别仅在于:氯丙烯和氯丙烷的混合气体以1ml/min的速度通入吸附柱与吸附剂接触。
[0095]
通过对本应用例中流出的气体进行气相色谱仪检测分析,在100℃抽真空将吸附氯丙烯后吸附剂进行解吸,得到氯丙烯气体,测试得到本应用例获得的氯丙烯的纯度大于99.99%,吸附柱可以循环使用。
[0096]
应用例5
[0097]
参照应用例1所述的方法将实施例1所得吸附剂co(c7o5h4)
·
2h2o用于分离氯丙烯和氯丙烷的混合气体,区别仅在于:氯丙烯和氯丙烷的混合气体以2ml/min的速度通入吸附柱与吸附剂接触。
[0098]
通过对本应用例中流出的气体进行气相色谱仪检测分析,在100℃抽真空将吸附氯丙烯后吸附剂进行解吸,得到氯丙烯气体,测试得到本应用例获得的氯丙烯的纯度大于99.99%,吸附柱可以循环使用。
[0099]
应用例6
[0100]
参照应用例1所述的方法将实施例1所得吸附剂co(c7o5h4)
·
2h2o用于分离氯丙烯和氯丙烷的混合气体,区别仅在于:氯丙烯和氯丙烷的混合气体中氯丙烯和氯丙烷的质量比为9:1。
[0101]
通过对本应用例中流出的气体进行气相色谱仪检测分析,在100℃抽真空将吸附氯丙烯后吸附剂进行解吸,得到氯丙烯气体,测试得到本应用例获得的氯丙烯的纯度大于99.99%,吸附柱可以循环使用。
[0102]
应用例7
[0103]
参照应用例1所述的方法将实施例1所得吸附剂co(c7o5h4)
·
2h2o用于分离氯丙烯和氯丙烷的混合气体,区别仅在于:吸附分离氯丙烯和氯丙烷的混合气体的温度由30℃替换为40℃。
[0104]
通过对本应用例中流出的气体进行气相色谱仪检测分析,在100℃抽真空将吸附氯丙烯后吸附剂进行解吸,得到氯丙烯气体,测试得到本应用例获得的氯丙烯的纯度大于99.99%,吸附柱可以循环使用。
[0105]
应用例8
[0106]
参照应用例1所述的方法将实施例1所得吸附剂co(c7o5h4)
·
2h2o用于分离氯丙烯和氯丙烷的混合气体,区别仅在于:吸附柱的内径由5mm替换为10mm。
[0107]
通过对本应用例中流出的气体进行气相色谱仪检测分析,在100℃抽真空将吸附氯丙烯后吸附剂进行解吸,得到氯丙烯气体,测试得到本应用例获得的氯丙烯的纯度大于99.99%,吸附柱可以循环使用。
[0108]
对比应用例1
[0109]
参照应用例1所述的方法将对比例1所得吸附剂zn(c7o5h4)
·
2h2o用于分离氯丙烯和氯丙烷的混合气体。
[0110]
通过对本应用例中流出的气体进行气相色谱仪检测分析,在100℃抽真空将吸附氯丙烯后吸附剂进行解吸,得到氯丙烯气体,测试得到本应用例获得的氯丙烯的纯度为
99.8%,吸附柱可以循环使用。
[0111]
对比应用例2
[0112]
参照应用例1所述的方法将对比例2所得吸附剂mn(c7o5h4)
·
2h2o用于分离氯丙烯和氯丙烷的混合气体。
[0113]
通过对本应用例中流出的气体进行气相色谱仪检测分析,在100℃抽真空将吸附氯丙烯后吸附剂进行解吸,得到氯丙烯气体,测试得到本应用例获得的氯丙烯的纯度为98%,吸附柱可以循环使用。
[0114]
申请人声明,以上所述仅为本发明的具体实施方式,但本发明的保护范围并不局限于此,所属技术领域的技术人员应该明了,任何属于本技术领域的技术人员在本发明揭露的技术范围内,可轻易想到的变化或替换,均落在本发明的保护范围和公开范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1