一种水相Hg(Ⅱ)同位素的原位富集方法及分析方法
一种水相hg(ⅱ)同位素的原位富集方法及分析方法
技术领域
1.本发明涉及水相hg(ⅱ)同位素测定技术领域,尤其提供了一种水相hg(ⅱ)同位素的原位富集方法及分析方法。
背景技术:
2.汞是一种全球性的污染物,因其具有累积性和持久性而备受关注。它可以在全球范围内通过大气进行传输,随后在陆地和水生生态系统中沉积下来。一旦沉积到陆地和水生系统中,汞会被某些厌氧微生物转化为毒性更强的甲基汞(mehg),随后在食物链中积累,对人类和环境健康构成威胁。游离的水相hg
2+
及其不稳定态hg(ⅱ)(统称hg(ⅱ)),是甲基化的主要物种,由于其高度活性和生物有效性,在水生生态系统中发挥着至关重要的作用。汞同位素是一种强大的溯源工具,有助于更好地了解水生生态系统中汞物种之间发生的生物地球化学循环过程。
3.目前使用汞同位素技术精确示踪汞在水生生态系统中的来源和迁移过程仍存在较大挑战,主要体现在:传统的采样方法步骤复杂繁琐,采样和储存要求苛刻,并且在样品的收集、储存和运输过程中,可能会导致样品的污染,另外,样品的物理化学性质(例如ph值、氧化还原条件)容易发生变化,这也对后期样品的浓度和同位素组成的测定造成了较大的不确定性,使得检测结果存在较大误差。
技术实现要素:
4.有鉴于此,本发明的目的在于提供一种水相hg(ⅱ)同位素的原位富集方法及分析方法。本发明提供的原位富集方法减小了待测水体样品转移过程中的污染可能性,用于后续水相中hg(ⅱ)同位素的检测时,准确度高。
5.为了实现上述发明目的,本发明提供以下技术方案:
6.本发明提供了一种水相中hg(ⅱ)同位素的原位富集方法,包括以下步骤:
7.(1)采用dgt装置对待测水体进行吸附,得到吸附了hg(ⅱ)的dgt装置;所述dgt装置的吸附膜为nsba吸附膜;
8.(2)对步骤(1)中所述吸附了hg(ⅱ)的dgt装置中的nsba吸附膜进行洗脱,得到hg(ⅱ)洗脱液,所述hg(ⅱ)洗脱液中汞浓度≥0.5ng/ml;
9.所述洗脱的洗脱剂为反王水;
10.所述nsba吸附膜为聚丙烯酰胺水凝胶薄膜,所述聚丙烯酰胺水凝胶薄膜内分布有巯基氨基双修饰的sba-15型介孔硅材料;所述巯基和氨基的摩尔数比为(4~6):1。
11.优选地,所述吸附的时间≥24h。
12.优选地,当所述洗脱得到的溶液中汞浓度《0.5ng/ml时,还包括进行富集;所述富集包括第一富集方法或第二富集方法;所述第一富集方法包括:向所述洗脱得到的溶液中加入还原剂,将hg(ⅱ)进行还原,得到还原体系;向所述还原体系中鼓吹氮气,将还原出的hg(0)反富集至体积百分含量为40%的稀释反王水中,得到满足上机要求的hg(ⅱ)洗脱液;
所述还原剂为浓度为0.2g/ml的sncl2水溶液;所述氮气的鼓吹流速≤200ml/min,所述氮气的鼓吹时间为2h。
13.优选地,所述第二富集方法包括:所述第二富集方法包括:将多个所述吸附了hg(ⅱ)的dgt装置中的nsba吸附膜进行洗脱,将所述洗脱得到的溶液合并,得到满足上机要求的hg(ⅱ)洗脱液。
14.优选地,所述hg(ⅱ)洗脱液的酸度≥40%。
15.本发明提供了一种水相hg(ⅱ)同位素的分析方法,包括以下步骤:
16.按照上述技术方案所述的方法对待测水体进行原位富集,得到hg(ⅱ)洗脱液;
17.通过mc-icp-ms对所述hg(ⅱ)洗脱液进行检测,得到δ
202
hg,δ
199
hg和δ
201
hg的测定值;
18.对所述δ
202
hg的测定值进行校正,得到所述待测水体的δ
202
hg的实际值;
19.所述校正的校正值为-0.18
‰
。
20.优选地,所述mc-icp-ms以gbw07405、bcr-482固体标准物质,以nist srm 3133汞同位素标准溶液和nist srm 8610汞同位素标准溶液作为外标物,以nist 997 tl标溶液为内标物来对样品进行质量控制。
21.本发明提供了一种水相中hg(ⅱ)同位素的原位富集方法,包括以下步骤:(1)采用dgt装置对待测水体进行吸附,得到吸附了hg(ⅱ)的dgt装置;所述dgt装置的吸附膜为nsba吸附膜;(2)对步骤(1)中所述吸附了hg(ⅱ)的dgt装置中的nsba吸附膜进行洗脱,得到hg(ⅱ)洗脱液,所述hg(ⅱ)洗脱液中汞浓度≥0.5ng/ml;所述洗脱的洗脱剂为反王水;所述nsba吸附膜为聚丙烯酰胺水凝胶薄膜,所述聚丙烯酰胺水凝胶薄膜内分布有巯基氨基双修饰的sba-15型介孔硅材料;所述巯基和氨基的摩尔数比为(4~6):1。本发明提供的原位富集方法只需将装有nsba吸附膜的dgt装置置于待测水体中对待测水体中的hg(ⅱ)进行原位吸附即可,不用进行直接的抓取采样,减小了待测水体样品转移过程中的污染可能性,用于后续水相hg(ⅱ)同位素的检测时,提高了检测准确度。
22.本发明还提供了一种水相hg(ⅱ)同位素的分析方法,包括以下步骤:按照上述技术方案所述的原位富集方法对待测水体进行原位富集,得到hg(ⅱ)洗脱液;通过mc-icp-ms对所述hg(ⅱ)洗脱液进行检测,得到δ
202
hg、δ
199
hg和δ
201
hg的测定值;对所述δ
202
hg的测定值进行校正,得到所述待测水体的δ
202
hg的实际值;所述校正的校正值为-0.18
‰
。由于本发明的分析方法,将装有nsba吸附膜的dgt装置置于待测水相中对待测水体中的hg(ⅱ)进行原位富集,与传统的方法相比,减小了待测水体样品转移过程中的污染可能性,提高了检测准确度。
附图说明
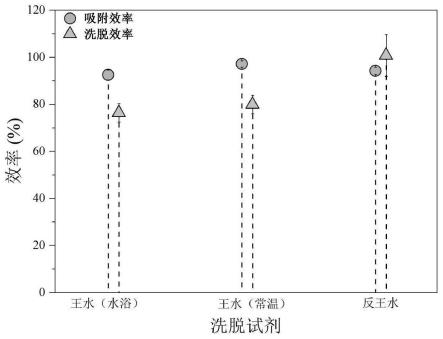
23.图1为利用王水和反王水对nsba吸附膜进行洗脱的效果图。
具体实施方式
24.本发明提供了一种水相中hg(ⅱ)同位素的原位富集方法,包括以下步骤:
25.(1)采用dgt装置对待测水体进行吸附,得到吸附了hg(ⅱ)的dgt装置;所述dgt装置的吸附膜为nsba吸附膜;
26.(2)对步骤(1)中所述吸附了hg(ⅱ)的dgt装置中的nsba吸附膜进行洗脱,得到hg(ⅱ)洗脱液,所述hg(ⅱ)洗脱液中汞浓度≥0.5ng/ml;
27.所述洗脱的洗脱剂为反王水;
28.所述nsba吸附膜为聚丙烯酰胺水凝胶薄膜,所述聚丙烯酰胺水凝胶薄膜内分布有巯基氨基双修饰的sba-15型介孔硅材料;所述巯基和氨基的摩尔数比为(4~6):1。
29.在本发明中,如无特殊说明,本发明所用原料均优选为市售产品。
30.本发明采用dgt装置对待测水体进行吸附,得到吸附了hg(ⅱ)的dgt装置;所述dgt装置的吸附膜为nsba吸附膜。
31.在本发明中,所述nsba吸附膜为聚丙烯酰胺水凝胶薄膜,所述聚丙烯酰胺水凝胶薄膜内分布有巯基氨基双修饰的sba-15型介孔硅材料;所述巯基和氨基的摩尔数比为(4~6):1。
32.在本发明中,所述nsba吸附膜的制备方法优选包括以下步骤:
33.步骤一、制备巯基氨基双修饰sba-15介孔硅材料:
34.(1)在锥形瓶中,用1.9mol/l盐酸溶解聚环氧乙烷-聚环氧丙烷-聚环氧乙烷三嵌段共聚物(p123),待p123充分溶解后将反应温度升高至40℃,滴加正硅酸乙酯(teos),添加量为所含硅占p123摩尔数的5%,搅拌60min后,再滴加巯基丙基三甲氧基硅烷(mptms),二者的滴加摩尔比为x=mptms/((teos+mptms)),x=0.2,搅拌20h后,将混合溶液转移到高压反应釜中,100℃陈化24h,将所得产物冷却抽滤、洗涤、干燥;
35.(2)将步骤(1)中所得的材料真空脱水后,移入圆底烧瓶,并加入甲苯和3-氨基丙基三甲氧基硅烷(aptms),110℃条件下搅拌24h,将所得产物依次用甲苯、无水乙醇、去离子水清洗2~3次,真空干燥;
36.(3)将步骤(2)所得的材料与95%乙醇加入到圆底烧瓶中,加热搅拌回流24h,冷却抽滤、洗涤、真空干燥,制得巯基氨基双修饰的sba-15介孔硅重金属吸附剂。
37.步骤二、利用购买自英国dgt研究有限公司的浓度为2%的交联剂dgtgel cross-linker、mq水和通用电气医疗集团(ge healthcare)生产的丙烯酰胺溶液按体积比15:47.5:37.5的比例混合得到制胶溶液,其中丙烯酰胺溶液的质量百分比浓度为40%,在4℃冰箱中保存备用。
38.步骤三、将步骤一制备得到的巯基氨基双修饰sba-15介孔硅材料充分研磨后与步骤二制备得到的制胶溶液按质量体积比1:30混匀得到制胶溶液,超声3分钟制得混合溶液。
39.步骤四、向步骤三制备得到的混合溶液中按聚丙烯酰胺溶液体积的1/150加入质量百分比浓度为10%的过硫酸铵溶液,按聚丙烯酰胺溶液体积的1/800加入四甲基二乙胺溶液,混和均匀得到混合溶液。
40.步骤五、将步骤四制备得到的混合溶液以5ml/min的速率注入夹有0.25mm厚的u型特氟龙材质薄片的两片玻璃板孔隙中,赶尽气泡,水平转移至42℃的烘箱中放置40min,待玻璃板中的溶液凝胶成膜,在纯水中浸泡24h,期间用纯水换洗4次,即制得所述nsba吸附膜。
41.在本发明中,所述吸附的时间优选≥24h。
42.在本发明中,所述dgt装置的外壳、滤膜和扩散层均购自南京维申环保科技有限公司。在本发明中,所述dgt装置的滤膜的材质优选为聚醚砜(pes);所述滤膜的孔径优选为
0.45μm,所述滤膜的厚度优选为0.14mm。在本发明中,所述dgt装置的扩散层的材质优选为琼脂糖凝胶;所述扩散层的厚度优选为0.8mm。在本发明中,所述dgt装置的其他结构与现有技术一致。
43.得到吸附了hg(ⅱ)的dgt装置后,本发明对所述吸附了hg(ⅱ)的dgt装置中的nsba吸附膜进行洗脱,得到hg(ⅱ)洗脱液,所述hg(ⅱ)洗脱液中汞浓度≥0.5ng/ml。
44.所述洗脱之前,本发明优选还包括对所述吸附了hg(ⅱ)的dgt装置中的nsba吸附膜进行冲洗。在本发明中,所述冲洗的试剂优选包括去离子水。本发明对所述冲洗的时间和次数不做具体限定,只要能够将吸附了hg(ⅱ)的dgt装置中的nsba吸附膜上的杂质去除干净即可。
45.在本发明中,所述洗脱的洗脱剂为反王水。在本发明中,所述洗脱的洗脱剂的体积和nsba吸附膜的面积的比优选为5ml:3.14cm2。在本发明中,所述洗脱的方式优选为振荡洗脱;所述振荡洗脱的时间优选为8~12h。
46.在本发明中,所述hg(ⅱ)洗脱液的酸度优选≥40%,进一步优选为40%。
47.在本发明中,所述hg(ⅱ)洗脱液中汞浓度≥0.5ng/ml。在本发明中,当所述洗脱得到的溶液中汞浓度《0.5ng/ml时,优选还包括进行富集;所述富集优选包括第一富集方法或第二富集方法。
48.在本发明中,所述第一富集方法优选包括:向所述洗脱得到的溶液中加入还原剂,将hg(ⅱ)进行还原,得到还原体系;向所述还原体系中鼓吹氮气,将还原出的hg(0)反富集至体积百分含量为40%的稀释反王水中,得到满足上机要求的hg(ⅱ)洗脱液。在本发明中,所述体积百分含量为40%的稀释反王水为反王水和水按照体积比4:6混合而成的溶液。在本发明中,所述还原剂优选为浓度为0.2g/ml的sncl2水溶液;本发明对所述还原剂的用量不做具体限定,只要能够将hg(ⅱ)全部转化为hg(0)即可。在本发明中,所述氮气的鼓吹流速优选≤200ml/min,进一步优选为100~200ml/min;所述氮气的鼓吹时间优选为2h。
49.在本发明中,所述第二富集方法优选包括:将多个所述吸附了hg(ⅱ)的dgt装置中的nsba吸附膜进行洗脱,将所述洗脱得到的溶液合并,得到满足上机要求的hg(ⅱ)洗脱液。
50.本发明还提供了一种水相中hg(ⅱ)同位素的分析方法,包括以下步骤:
51.按照上述技术方案所述的原位富集方法对待测水体进行原位富集,得到hg(ⅱ)洗脱液;
52.通过mc-icp-ms对所述hg(ⅱ)洗脱液进行检测,得到δ
202
hg,δ
199
hg和δ
201
hg的测定值;
53.对所述δ
202
hg的测定值进行校正,得到所述待测水体的δ
202
hg的实际值;
54.所述校正的校正值为-0.18
‰
。
55.本发明按照上述技术方案所述的原位富集方法对待测水体进行原位富集,得到hg(ⅱ)洗脱液。在本发明中,所述原位富集的参数优选与上述技术方案一致,在此不再赘述。
56.得到hg(ⅱ)洗脱液后,本发明通过mc-icp-ms对所述hg(ⅱ)洗脱液进行检测,得到δ
202
hg,δ
199
hg和δ
201
hg的测定值。
57.在本发明中,所述mc-icp-ms优选以gbw07405、bcr-482固体标准物质,以nist srm 3133汞同位素标准溶液和nist srm 8610汞同位素标准溶液作为外标物,以nist 997 tl标溶液为内标物来对样品进行质量控制。
58.本发明对所述mc-icp-ms的检测参数不做具体限定,采用本领域技术人员熟知的检测参数即可。
59.得到δ
202
hg的测定值后,本发明对所述δ
202
hg的测定值进行校正,得到所述待测水体的δ
202
hg的实际值。
60.在本发明中,所述校正的校正值优选为-0.18
‰
。
61.在本发明中,所述校正值优选通过以下步骤得到:
62.(a)将dgt装置(吸附膜为nsba吸附膜)放入不同温度(15℃、25℃和35℃)下100ml含有0.01mol/l nacl和~60ng/ml的nist srm 3133同位素汞标准溶液中,恒温振荡器的振荡速度为120rpm,在0至24h不同的时间点,从溶液中取出dgt装置,取出dgt装置的吸附膜,利用5ml反王水对吸附膜进行洗脱8~12h,得到不同时间点的洗脱液。另外,向残留液(不同时间点取出dgt装置后的剩余溶液)中加入1%brcl使其他形态的汞均转化为hg(ⅱ),而后将其放入4℃冰箱冷藏保存,以便于后续hg(ⅱ)浓度和同位素分析。
63.如若不同时间点的洗脱液中汞浓度达不到上机测定同位素的标准(≥0.5ng/ml),可利用cvafs的汞富集系统对不同时间点的洗脱液进行反富集;具体为:将10~12ml待富集洗脱液装入气泡瓶中,向气泡瓶中加入5ml浓度为0.2g/ml的sncl2水溶液还原hg(ⅱ),使待富集洗脱液中的hg(ⅱ)转化为hg(0),然后向气泡瓶中通入流速为100~200ml/min的氮气,持续鼓吹2h,使还原出的hg(0)反富集在5ml体积百分含量为40%的稀释反王水里。
64.(b)准备gbw07405和bcr-482固体标准物质待测溶液,准确配置0.5ng/ml的nist srm 3133汞同位素标准溶液和nist srm 8610汞同位素标准溶液,20ng/ml tl(nist 997)的标溶液以控制样品质量标准。
65.(c)通过在线汞发生系统与多接收电感耦合等离子体质谱仪(mc-icp-ms)对不同时间点的洗脱液进行检测,可得到样品中δ
202
hg,δ
199
hg和δ
201
hg值。
66.不同温度下dgt装置吸附汞的比例及其同位素值,如表1所示。
67.表1不同温度下dgt吸附汞的比例及其同位素值
[0068][0069]
从表1可以看出:在15、25和35℃的条件下,与初始溶液的nist srm 3133中δ
202
hg和δ
199
hg参考值(~0
‰
)相比,dgt在吸附汞分子的过程中hg-mdf产生了大约0.1~0.2
‰
的偏差,三个温度下的偏差值无显著差异(p》0.05),因此取三个不同温度下δ
202
hg的均值(-0.18
‰
)作为校正值;另外,在整个实验过程中未检测到明显的同位素非质量分馏(hg-mif~0
‰
)。由此,本发明可利用hg-mdf偏差值(-0.18
‰
)对野外样品进行校正,无需对mif进行校正。
[0070]
下面结合实施例对本发明提供的水相中hg(ⅱ)同位素的原位富集方法及分析方法进行详细的说明,但是不能把它们理解为对本发明保护范围的限定。
[0071]
实施例1
[0072]
洗脱剂的选择
[0073]
(i)将nsba吸附膜(面积为3.14cm2,按照具体实施部分描述的nsba吸附膜的方法进行制备)浸入30ml含有0.01mol/lnacl和1ng/ml的hg(ⅱ)待测溶液中吸附24h,得到吸附了hg(ⅱ)的nsba吸附膜。
[0074]
(ii)用超纯水冲洗步骤(i)得到的吸附了hg(ⅱ)的nsba吸附膜的表面杂质,用擦镜纸将吸附了hg(ⅱ)的nsba吸附膜表面的水吸干,然后将冲洗后的吸附了hg(ⅱ)的nsba吸附膜分别置于装有5ml王水和5ml反王水的特氟龙瓶中连续振荡洗脱,其中王水的洗脱方式有两种,水浴加热洗脱3h,常温洗脱8h,反王水洗脱为常温下洗脱8~12h即可,所述得到三种洗脱液。
[0075]
(iii)在步骤(ii)得到的三种洗脱液中分别加入5ml超纯水进行稀释,得到三种hg(ⅱ)洗脱液。
[0076]
(iv)采用cvafs(tekran 2500)测定步骤(iii)得到的三种hg(ⅱ)洗脱液的浓度、nsba吸附膜吸附前后待测溶液的浓度。
[0077]
(v)由步骤(iv)的数据计算出nsba吸附膜对hg(ⅱ)的吸附效率及王水和反王水对hg(ⅱ)的洗脱效率,结果如图1所示。
[0078]
从图1可以看出:5ml反王水对hg(ⅱ)的洗脱效率为100.75
±
8.91%,而5ml王水(水浴和常温两种方式)对hg(ⅱ)的洗脱效率为76.36~79.87%,最终确定反王水为nsba吸附膜的洗脱试剂。
[0079]
实施例2
[0080]
室内实验验证
[0081]
(1)将dgt装置(吸附膜为nsba吸附膜;滤膜为聚醚砜膜(pes),孔径为0.45μm,厚度为0.14mm;扩散层为琼脂糖凝胶膜,厚度为0.8mm)放入不同温度(15℃、25℃和35℃)下100ml含有0.01mol/lnacl和~60ng/ml的nist srm 3133同位素汞标准溶液中,恒温振荡器的振荡速度为120rpm,在0至24h不同的时间点,从溶液中取出dgt装置,取出dgt装置的吸附膜,利用5ml反王水对吸附膜进行洗脱12h,得到不同时间点的洗脱液。另外,向残留液(不同时间点取出dgt装置后的剩余溶液)中加入1%brcl使其他形态的汞均转化为为hg(ⅱ),而后将其放入4℃冰箱冷藏保存,重复实施例1的步骤(iii)和(iv)。
[0082]
如若不同时间点的洗脱液中汞浓度达不到上机测定同位素的标准(≥0.5ng/ml),可利用cvafs的汞富集系统对不同时间点的洗脱液进行反富集;具体为:将10ml待富集洗脱液装入气泡瓶中,向气泡瓶中加入5ml浓度为0.2g/ml的sncl2水溶液还原hg(ⅱ),使待富集洗脱液中的hg(ⅱ)转化为hg(0),然后向气泡瓶中通入流速为100~200ml/min的氮气,持续鼓吹2h,使还原出hg(0)反富集在5ml体积百分含量为40%的稀释反王水里。
[0083]
(2)准备gbw07405和bcr-482固体标准物质待测溶液,准确配置0.5ng/ml的nist srm 3133汞同位素标准溶液和nist srm 8610汞同位素标准溶液,20ng/ml tl(nist 997)的标溶液以控制样品质量标准。
[0084]
(3)通过在线汞发生系统与多接收电感耦合等离子体质谱仪(mc-icp-ms)对不同时间点的洗脱液进行检测,可得到样品中δ
202
hg,δ
199
hg和δ
201
hg值。
[0085]
首先,通过nist srm 3133及三种标准物质(内标和外标)来确定mc-icp-ms仪器的
稳定性,具体结果如表2所示。
[0086]
表2mc-icp-ms仪器的稳定性实验数据
[0087][0088][0089]
从表2可以看出:其测定结果与参考值一致,说明在所有样品的测定过程中,mc-icp-ms仪器运行过程中较为稳定。
[0090]
不同温度下dgt装置吸附汞的比例及其同位素值,如表1所示。从表1可以看出:dgt在吸附汞分子的过程中hg-mdf产生了0.18
‰
的偏差,基于此,对于后续的野外研究可以以此为校正值对野外dgt样品进行校正;并且,在整个实验过程中未检测到明显的同位素非质量分馏(hg-mif~0
‰
),说明dgt后续检测到的mif值可以反映自然样品的真实mif信号,进一步证实了该方法的可靠性。
[0091]
实施例3
[0092]
野外应用
[0093]
将nsba-dgt装置放入稻田土壤溶液中,14天后取出,利用超纯水将其表面的杂质冲洗干净,带回实验室进行洗脱和检测,洗脱和检测同实施例1和2,结果如表3所示。
[0094]
表3环境样品中dgt的同位素组成(校正值)
[0095][0096]
由表3可以看出,dgt与mc-icp-ms联用可用于捕捉稻田土壤溶液中水相hg(ⅱ)的汞同位素组成,如表3所示,测定的δ
202
hg值为-2.10~-1.99
‰
,监测到微小的非质量分馏(mif),δ
199
hg值为0.11~0.22
‰
。
[0097]
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1