一种二氧化碳电化学还原用金属催化剂及其制备和应用的制作方法
本发明涉及一种二氧化碳电化学还原领域,特别涉及二氧化碳电化学还原用催化剂技术。
背景技术:
化石能源的逐渐枯竭和全球气候变暖,是人类面临的两个难题,与人类未来的可持续发展息息相关。当今化石燃料的消耗,使大气中的co2含量不断升高。co2作为一种温室气体,可导致全球气候变暖,引起“温室效应”。但是,co2也是一种潜在的碳资源,如果能够加以回收,转化成有用的化学原料,既能降低大气中co2的含量,变害为利,减缓“温室效应”,又能补充化石燃料的替代品。在众多的co2转化方法中,电化学还原co2能够利用可再生能源发电和水,将co2转化为有价值的化合物,如甲酸,co,ch4和c2h2等。电化学还原co2能够可在常温常压下实现co2的高效转化,设备简单,环境友好,具有良好的发展前景和应用价值,吸引了众多国内外研究者的高度关注。
co2是一种化学结构非常稳定的分子,将co2还原成中间产物需要很高的过电位;且co2还原成产物的过程涉及到多步骤电子转移,导致产物的选择性差。因此选择合适的催化剂来降低co2还原的过电位,提高产物的选择性至关重要。催化剂的种类不同,得到的co2还原的产物也不同。目前,高产甲酸的催化剂多为重金属,如pb、hg等,对环境有污染,且难以同时满足高选择性和高电流密度;高产co的催化剂主要为贵金属,如au、ag等,价格昂贵,难以满足市场化应用;高产ch4和c2h2等催化剂主要为金属cu,单一产物选择性差。
甲酸是一种重要的化工原料,可以用来合成其他化学产品,也可用作金属表面处理剂、橡胶助剂和工业溶剂,广泛用于农药、皮革、染料、医药和橡胶等工业。因此,开发廉价高效的催化剂,将co2电化学还原为甲酸具有重要的意义。
zn是一种地壳中含量丰富,环境友好且廉价的金属,是一种有潜力将co2电化学还原为co的催化剂,但是过电位较高。bi是一种比zn稍微昂贵一些的金属,但是价格相对贵金属来说要廉价得多,且安全无毒,能将co2电化学还原为甲酸和co,但是选择性有待提高。通过改变材料的组成和微观结构,可以提高其催化性能。因此,以zn和bi金属为基础材料,开发简单高效的制备方法来合成低成本、高性能的erc催化剂,提高co2电化学还原为甲酸的选择性,降低其过电位,具有重要的研究价值,是未来erc转变为实际应用的重要一步。
技术实现要素:
本发明提供了一种二氧化碳电化学还原用金属催化剂的制备方法,这种制备方法简单高效,条件可控,易于操作。该催化剂表面为纳米片状或颗粒状多晶结构,由zn、bi两种元素,为催化剂提供催化性能;催化剂内部为金属zn,为催化剂提供强度支撑和导电性。该催化剂用于二氧化碳电化学还原,对目标产物甲酸具有优良的选择性和催化活性。该催化剂成本低廉,可以满足大规模商业应用的需求。
二氧化碳电化学还原用金属催化剂的制备方法,包括如下6个步骤:1)先后用微米级和纳米级al2o3粉末对锌片进行打磨,用超纯水和乙醇对锌片进行超声清洗,在惰性气体保护下进行干燥;2)将洗好的锌片置于内有聚四氟乙烯套的反应釜中,并加浓度为0.01~2mm的bi(no3)3水溶液,溶液体积占高压釜容积的20~80%,室温下静置0.1~5h;3)将反应釜放入控温烘箱中,在160~200℃下反应2~24h后自然降温至室温;4)将锌片取出,用超纯水清洗后放入控温烘箱中,在60~150℃下干燥1~12h;5)将干燥后的锌片置于co2或惰性气氛中的一种或两种以上的饱和盐溶液中,在-1.2~-2vvssce电压下还原0.5~4h;(优选co2气氛饱和的盐溶液中,co2可在催化剂表面被还原形成气泡,从而调控催化剂的表面形貌,提高其比表面积);6)将还原后的锌片行超声清洗,并在在惰性气体保护下进行干燥。
步骤:1)所述的锌片厚度为0.01~2mm,最佳厚度为0.1~0.2mm;
步骤:2)所述锌片完全淹没在溶液中。在静置过程中,bi(no3)3与zn反应,置换出部分zn2+溶于水溶液中,在zn片表面金属bi。
步骤:3)所述最佳反应时间为6~12个小时,期间,反应釜内的氧气将zn片表面的zn金属和bi金属氧化。
步骤:4)所述干燥过程中,zn片表面的zn终以zno形式存在,bi最终以bi2o3或bi2o2co3形式存在。
步骤:5)所述盐溶液由阳离子na+或k+和阴离子cl-或so42-或co32-或hco3-或po43-或no3-组成。在电还原过程中,zno被还原为金属zn,bi2o3或bi2o2co3被还原为金属bi,从而形成znbi双金属多晶结构的催化剂。
所述的惰性气氛为氮气、氩气或氦气气体中的一种或二种以上混合。
所述金属催化剂表面为纳米片状或颗粒状多晶结构,为催化剂提供催化性能,其元素组成为zn、bi两种元素,纳米片的直径为10~800nm,厚度为3~100nm,纳米颗粒的粒径为5nm~1.5μm;催化剂内部未发生氧化还原,为金属zn,为催化剂提供强度支撑和导电性。
所述金属催化剂可用于催化二氧化碳的电化学还原反应。
本发明的优点和有益效果如下:
1)制备过程成本低、操作简单、重复性高,适合大规模生产。而催化剂本身所含bi和zn元素的价格低廉,环境友好,可满足大规模使用。
2)制备好的催化剂即为电极,可以直接使用,无需担载在其他电极上,简单方便。
3)金属催化剂表面为纳米片状或颗粒状多晶结构,而且这些结构的尺寸可调,比表面积高。
4)高的比表面积增加了电极与电解液和co2气体的接触面积,有效地增加了反应活性面积,从而提高co2的转化效率;
5)多晶结构具有更多的晶界,能够稳定中间产物。具有双金属界面产生协同效应,对co2电化学还原具有更高的催化活性,对目标产物具有优良的选择性。
6)少量bi金属的存在,就可以大大提高zn对甲酸的选择性,显著降低其过电位,也降低了成本。可通过改变制备条件调节bi含量,从而调节产物的选择性。
应用
将所制的催化剂,用作二氧化碳还原制甲酸的催化剂。通过三电极体系进行电化学测试:工作电极为制得的催化剂;对电极为pt片,参比电极为hg/hg2cl2/饱和kcl(sce)。采用盐桥以降低液接电势。电解液为0.5mnahco3aq.sol,阴阳极电解液用nafion115膜隔开。co2流量用流量计控制,流速为60ml/min;。
附图说明
图1.实施例1制备的电极sem图;
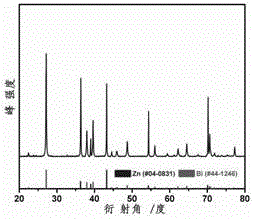
图2.实施例1制备的电极xrd图;
图3.实施例2制备的电极sem照片;
图4.实施例1制备的电极与对比例1制备的电极在不同电位下,对甲酸选择性的对比图。
具体实施方式
下面通过实施例对本发明作详细描述,但是本发明不仅限于实施例。
实施例1
1.金属催化剂的制备:
1)取一块厚度为0.1mm,面积为10cm2,质量纯度为99.99%的锌片,先后用30μm级和30nm级al2o3粉末对锌片进行打磨,再超纯水和乙醇对锌片进行超声清洗,并在在氩气气体保护下进行干燥;
2)将洗好的锌片置于内有聚四氟乙烯套的反应釜中,并加60ml浓度为0.8mm的bi(no3)3水溶液,室温下静置3h;
3)将反应釜放入控温烘箱中,在180℃下反应12h后自然降温至室温;
4)将锌片取出,用超纯水清洗后放入控温烘箱中,在80℃下干燥4h;
5)将干燥后的锌片置于co2气体饱和的0.5mnahco3盐溶液中,在-1.5vvssce电压下还原3h;
6)将还原后的锌片进行超声清洗,并在在氩气气体保护下进行干燥。2.金属催化剂对co2电化学还原反应的性能评价:
在h型电解池中,阴阳极腔中分别加入180ml和100ml0.5mnahco3水溶液,使用dupont公司生产的nf115作为阴阳极腔的隔膜。其中,阴极腔的co2气体从电解池下端进入,在工作电极表面发生co2电化学还原反应后,从阴极腔的上端出口排出。测试前,首先向阴极腔中通入纯度为99.995%的co2气体,co2的流速控制为20sccm。1h后,以金属催化剂为工作电极,pt片为对电极,饱和甘汞电极为参比电极。co2电化学还原反应15min后,反应尾气通入气相色谱进行气体产物的定量检测,液体产物采用离子色谱进行定量分析。在-1.47vvssce的电位下,甲酸的选择性最高,可达到为94%;通过图1sem图可看出,制备的电极表面为纳米颗粒,粒径为100nm-1.5μm,bi元素的摩尔含量为20%。xrd表明电极的成分为金属bi和金属zn。
实施例2
1.金属催化剂的制备:
1)取一块厚度为0.1mm,面积为8cm2,纯度为99.99%的锌片,先后用100μm级和500nm级al2o3粉末对锌片进行打磨,再超纯水和乙醇对锌片进行超声清洗,并在在氩气气体保护下进行干燥;
2)将洗好的锌片置于内有聚四氟乙烯套的反应釜中,并加80ml浓度为0.1mm的bi(no3)3水溶液,室温下静置1h;
3)将反应釜放入控温烘箱中,在170℃下反应10h后自然降温至室温;
4)将锌片取出,用超纯水清洗后放入控温烘箱中,在70℃下干燥4h;
5)将干燥后的锌片置于氮气气体饱和的0.5mkhco3盐溶液中,在-1.4vvssce电压下还原3h;
6)将还原后的锌片进行超声清洗,并在在氩气气体保护下进行干燥。2.金属催化剂对co2电化学还原反应的性能评价:
在h型电解池中,阴阳极腔中分别加入180ml和100ml0.5mnahco3水溶液,使用dupont公司生产的nf115作为阴阳极腔的隔膜。其中,阴极腔的气体从电解池下端进入,在工作电极表面发生co2电化学还原反应后,从阴极腔的上端出口排出。测试前,首先向阴极腔中通入纯度为99.995%的co2气体,co2的流速控制为20sccm。1h后,以金属催化剂为工作电极,pt片为对电极,饱和甘汞电极为参比电极。co2电化学还原反应15min后,反应尾气通入气相色谱进行气体产物的定量检测,液体产物采用离子色谱进行定量分析。在-1.67vvssce的电位下,甲酸的选择性最高,可达到为72%。通过sem图可看出,制备的电极表面为纳米片,纳米片的直径为30~110nm,厚度为10~30nm,bi元素的摩尔含量为3%。
实施例3
1.金属催化剂的制备:
1)取一块厚度为0.1mm,面积为5cm2,纯度为99.99%的锌片,先后用50μm级和100nm级al2o3粉末对锌片进行打磨,再超纯水和乙醇对锌片进行超声清洗,并在在氩气气体保护下进行干燥;
2)将洗好的锌片置于内有聚四氟乙烯套的反应釜中,并加70ml浓度为0.01mm的bi(no3)3水溶液,室温下静置5h;
3)将反应釜放入控温烘箱中,在180℃下反应15h后自然降温至室温;
4)将锌片取出,用超纯水清洗后放入控温烘箱中,在70℃下干燥5h;
5)将干燥后的锌片置于氩气气体饱和的0.2mna2so4盐溶液中,在-1.5vvssce电压下还原3h;
6)将还原后的锌片进行超声清洗,并在在氩气气体保护下进行干燥。
制备的电极表面为纳米片,纳米片的直径为500~700nm,厚度为60~80nm,bi元素的摩尔含量为1%。
2.金属催化剂对co2电化学还原反应的性能评价:
在h型电解池中,阴阳极腔中分别加入180ml和100ml0.5mnahco3水溶液,使用dupont公司生产的nf115作为阴阳极腔的隔膜。其中,阴极腔的气体从电解池下端进入,在工作电极表面发生co2电化学还原反应后,从阴极腔的上端出口排出。测试前,首先向阴极腔中通入纯度为99.995%的co2气体,co2的流速控制为20sccm。1h后,以金属催化剂为工作电极,pt片为对电极,饱和甘汞电极为参比电极。co2电化学还原反应15min后,反应尾气通入气相色谱进行气体产物的定量检测,液体产物采用离子色谱进行定量分析。在-1.77vvssce的电位下,甲酸的选择性最高,可达到为61%。
实施例4
1.金属催化剂的制备:
1)取一块厚度为0.2mm,面积为25cm2,纯度为99.99%的锌片,先后用50μm级和50nm级al2o3粉末对锌片进行打磨,再超纯水和乙醇对锌片进行超声清洗,并在在氩气气体保护下进行干燥;
2)将洗好的锌片置于内有聚四氟乙烯套的反应釜中,并加50ml浓度为2mm的bi(no3)3水溶液,室温下静置2h;
3)将反应釜放入控温烘箱中,在190℃下反应10h后自然降温至室温;
4)将锌片取出,用超纯水清洗后放入控温烘箱中,在90℃下干燥4h;
5)将干燥后的锌片置于氮气气体饱和的0.5mkno3盐溶液中,在-1.5vvssce电压下还原2h;
6)将还原后的锌片进行超声清洗,并在在氩气气体保护下进行干燥。
制备的电极表面为纳米颗粒,纳米颗粒的粒径为1~1.4μm,bi元素的摩尔含量为8%。
2.金属催化剂对co2电化学还原反应的性能评价:
在h型电解池中,阴阳极腔中分别加入180ml和100ml0.5mnahco3水溶液,使用dupont公司生产的nf115作为阴阳极腔的隔膜。其中,阴极腔的气体从电解池下端进入,在工作电极表面发生co2电化学还原反应后,从阴极腔的上端出口排出。测试前,首先向阴极腔中通入纯度为99.995%的co2气体,co2的流速控制为20sccm。1h后,以金属催化剂为工作电极,pt片为对电极,饱和甘汞电极为参比电极。co2电化学还原反应15min后,反应尾气通入气相色谱进行气体产物的定量检测,液体产物采用离子色谱进行定量分析。甲酸的选择性为69%。在-1.87vvssce的电位下,甲酸的选择性最高,可达到为69%。
对比例1
用相同方法,但是不加bi(no3)3所制备得到的zn催化剂:
1.金属催化剂的制备:
1)取一块厚度为0.1mm,面积为10cm2,纯度为99.99%的锌片,先后用30μm级和30nm级al2o3粉末对锌片进行打磨,再超纯水和乙醇对锌片进行超声清洗,并在在氩气气体保护下进行干燥;
2)将洗好的锌片置于内有聚四氟乙烯套的反应釜中,并加60ml超纯水室温下静置3h;
3)将反应釜放入控温烘箱中,在180℃下反应12h后自然降温至室温;
4)将锌片取出,用超纯水清洗后放入控温烘箱中,在80℃下干燥4h;
5)将干燥后的锌片置于co2气体饱和的0.5mnahco3盐溶液中,在-1.5vvssce电压下还原3h;
6)将还原后的锌片进行超声清洗,并在在氩气气体保护下进行干燥。
2.金属催化剂对co2电化学还原反应的性能评价:
在h型电解池中,阴阳极腔中分别加入180ml和100ml0.5mnahco3水溶液,使用dupont公司生产的nf115作为阴阳极腔的隔膜。其中,阴极腔的气体从电解池下端进入,在工作电极表面发生co2电化学还原反应后,从阴极腔的上端出口排出。测试前,首先向阴极腔中通入纯度为99.995%的co2气体,co2的流速控制为20sccm。1h后,以金属催化剂为工作电极,pt片为对电极,饱和甘汞电极为参比电极。co2电化学还原反应15min后,反应尾气通入气相色谱进行气体产物的定量检测,液体产物采用离子色谱进行定量分析。在-1.47vvssce的电位下,甲酸的选择性仅为1%,在-1.67vvssce的电位下,甲酸的选择性仅为5%,。
可见,在-1.47vvssce的电位下,本发明实施例1制备的电极甲酸选择性(法拉第效率)最高,可达到94%;而对比例1制备的电极甲酸选择性仅为1%。
对比例2
用水热法,以bi(no3)3为原料制备得到的bi催化剂:
1.金属催化剂的制备:
1)向水热釜中加60ml浓度为0.8mm的bi(no3)3水溶液;
3)将反应釜放入控温烘箱中,在180℃下反应12h后自然降温至室温;
4)反应釜中的沉淀和溶液进行离心,得到的固体用超纯水清洗后放入烘箱中,在80℃下干燥4h;
5)将干燥后的固体担载到玻碳电极上,置于co2气体饱和的0.5mnahco3盐溶液中,在-1.5vvssce电压下还原3h;
2.金属催化剂对co2电化学还原反应的性能评价:
在h型电解池中,阴阳极腔中分别加入180ml和100ml0.5mnahco3水溶液,使用dupont公司生产的nf115作为阴阳极腔的隔膜。其中,阴极腔的气体从电解池下端进入,在工作电极表面发生co2电化学还原反应后,从阴极腔的上端出口排出。测试前,首先向阴极腔中通入纯度为99.995%的co2气体,co2的流速控制为20sccm。1h后,以金属催化剂为工作电极,pt片为对电极,饱和甘汞电极为参比电极。co2电化学还原反应15min后,反应尾气通入气相色谱进行气体产物的定量检测,液体产物采用离子色谱进行定量分析。-1.47vvssce的电位下,甲酸的选择性仅为17%,在-1.67vvssce的电位下,甲酸的选择性最高,可达到为34%。
对比例3
结合对比例1和对比例2中的催化剂:
1.金属催化剂的制备:
1)将对比例2中制备步骤4)所得到的固体担载到对比例1中制备步骤4)所得到的锌片表面,置于co2气体饱和的0.5mnahco3盐溶液中,在-1.5vvssce电压下还原3h;
2)将还原后的锌片进行行超声清洗,并在在氩气气体保护下进行干燥。2.金属催化剂对co2电化学还原反应的性能评价:
在h型电解池中,阴阳极腔中分别加入180ml和100ml0.5mnahco3水溶液,使用dupont公司生产的nf115作为阴阳极腔的隔膜。其中,阴极腔的气体从电解池下端进入,在工作电极表面发生co2电化学还原反应后,从阴极腔的上端出口排出。测试前,首先向阴极腔中通入纯度为99.995%的co2气体,co2的流速控制为20sccm。1h后,以金属催化剂为工作电极,pt片为对电极,饱和甘汞电极为参比电极。co2电化学还原反应15min后,反应尾气通入气相色谱进行气体产物的定量检测,液体产物采用离子色谱进行定量分析。-1.47vvssce的电位下,甲酸的选择性仅为8%,在-1.67vvssce的电位下,甲酸的选择性最高,可达到为25%。
本发明和对比例制备的催化剂性能对比可知,本发明制备的催化剂应用于二氧化碳电化学还原中甲酸的选择性具有明显提高。
- 还没有人留言评论。精彩留言会获得点赞!