高价态金属离子掺杂富含氧空位的氧化钴纳米复合材料及其制备与应用
1.本发明属于纳米结构功能材料和电催化析氧技术领域,具体涉及一种高价态金属离子掺杂富含氧空位的氧化钴(记作:m/coo
x
,金属阳离子m为mo,w)纳米复合材料及其制备方法,以及在电催化析氧反应中的应用。
背景技术:
2.为了克服对传统化石燃料的依赖以及缓解环境污染问题,开发可再生清洁能源势在必行。氢能因极高的能量密度、高效的热转换效率以及燃烧产物零污染等优势被视为最具潜力的清洁能源。在各种制氢技术中,电催化裂解水是工业制氢的重要手段,具有零排放、制氢纯度高且可耦合太阳能、风能、核能等可再生能源的特点,也是通向氢经济的最佳途径。
3.电解水制氢主要包括阴极析氢反应(her)和阳极析氧反应(oer)两个半反应,相对于her 的双电子转移过程,oer涉及四电子参与的、多种中间产物的复杂反应过程,是一个动力学迟滞过程,需要更高的过电势,使得整个电解水的过程效率很低;而高效oer催化剂的引入能够显著降低动力学势垒,提高电解水析出氧气的速率。通常,贵金属氧化物(例如ruo2和iro2)在酸性和碱性环境里都有着高的催化活性和稳定性,被认为是oer的基准电催化剂。然而,它们的稀缺性和高成本是制约实际应用的主要障碍。鉴于此,迫切需要开发高效的低成本非贵金属oer电催化剂以降低反应过电位,提高能量转换效率。
4.近年来,过渡金属氧化物因其低廉的成本和出色的催化活性而备受关注。其中钴的氧化物由于其出色的氧化还原活性和环境友好性,在电化学领域应用广泛,但受限于其低的本征电导率和有限的反应活性位,其电化学性能有待进一步提高。掺杂是调节材料载流子浓度及导电性的常用方法,材料化学组成的改变能够有效调控其电子结构,进而起到优化本征电导率的作用。大量研究表明适当的过渡金属的掺杂可以从导电性、反应能垒、电化学活性面积、活性位等多方面实现对催化剂的性能改善,尤其是高价态非3d过渡金属离子(mo
6+
,w
6+
)的掺杂可以显著提升材料的电催化稳定性。另一方面,空位缺陷的存在使得电催化剂暴露出更多的配位不饱和位点和悬空键,可以有效调节费米能级附近的电子密度,进而优化电催化性能。
5.然而,掺杂和空位两种缺陷结构相结合的策略在电催化剂材料的制备中还较少。鉴于此,本发明提供了一种高价态金属离子掺杂富氧空位的氧化钴复合纳米材料(m/coo
x
,m=mo或w),该材料的微观形貌具有可调节性,能提供较大的比表面积和丰富的氧化还原反应位点;第二种金属的掺杂和氧空位的引入有效调控了氧化钴的电子结构,提高材料的本征电导率。在碱性体系下,该材料具有优异的电催化性能,有效缩短离子传输路径。
技术实现要素:
6.本发明目的在于提供一种高价态金属离子掺杂富含氧空位的氧化钴复合纳米材
料(记作: m/coo
x
,金属阳离子m为mo或w),并将其作为电极应用于电解水的半反应析氧反应中。
7.本发明采用金属阳离子掺杂和引入氧空位的方式,有效调控材料电子结构和载流子浓度,提高材料的本征电导率和氧化还原反应的多样性;还进一步调节了复合纳米材料的微观形貌,增加其比表面积,有效的缩短离子的传输路径。
8.本发明复合纳米材料的制备方法具有工艺简单、耗时短、成本低廉等优点。采用该类材料作为析氧反应电极,在碱性体系中表现出优异的析氧催化性能和稳定性,有望成为一种新的电催化材料。
9.本发明的技术方案如下:
10.一种高价态金属离子掺杂富含氧空位的氧化钴纳米复合材料,按如下方法制备得到:
11.(1)将钴盐与金属m盐的混合水溶液与尿素水溶液混合,得到前驱体溶液,加入经预处理的泡沫镍基底,于90~160℃反应1~12h,之后取出泡沫镍,洗涤干燥,即在泡沫镍基底上得到前驱体材料;
12.所述钴盐为硝酸钴、氯化钴或乙酸钴;
13.所述金属m盐为钼(mo)盐或钨(w)盐;所述钼盐为钼酸钠或钼酸铵;所述钨盐为钨酸钠或氯化钨;
14.所述钴盐与金属m盐的混合水溶液中,钴盐浓度为50~150mmol/l,金属m盐溶液浓度为5~40 mmol/l;
15.所述尿素水溶液的浓度为500~600mmol/l;
16.所述钴盐与金属m盐的混合水溶液与尿素水溶液的体积比为1:1;
17.所述泡沫镍基底的预处理方法为:将泡沫镍基底依次用丙酮、去离子水(di)、3m盐酸、去离子水、无水乙醇在超声条件下清洗15min,真空干燥后备用;
18.(2)将步骤(1)所得负载有前驱体材料的泡沫镍基底和nabh4放入管式炉中,在惰性气体保护下升温至300~350℃煅烧2~9h,得到所述高价态金属离子掺杂富含氧空位的氧化钴纳米复合材料;
19.所述nabh4与前驱体材料的质量比为20~200:1;
20.所述惰性气体为氮气、氩气或氦气,优选氮气;
21.所述煅烧的升温速率为2℃/min。
22.本发明以钼或钨的金属盐掺杂剂、钴盐及尿素为反应原料,去离子水为溶剂,泡沫镍为基底,采用恒温水热法将金属阳离子替代部分钴直接掺杂到含钴盐材料中,并对纳米材料的形貌进行调节;然后在惰性气体保护下的硼氢化钠(nabh4)还原气氛中进行煅烧得到最终产物m/coo
x
。
23.本发明通过调节金属阳离子m(钼或钨)替换部分co来优化材料的形貌和电子结构,从而提高电极材料的活性位点和导电率。
24.本发明制得的高价态金属离子掺杂富含氧空位的氧化钴纳米复合材料可作为电极材料应用于电解水的半反应析氧反应中。
25.与现有技术比较,本发明的有益效果是:
26.本发明采用水热法,将高价态金属阳离子m取代部分钴原子直接掺杂在原位生长
在泡沫镍上的 co前驱体中,调节了材料的微观形貌,使得催化材料的比表面积和孔隙率大幅提高;引入第二种金属并还原煅烧制造氧空位,增加了氧化还原反应的多样性,优化了电子结构,最终使材料的析氧性能得到大幅提升。
27.本发明所述复合纳米材料具有二维超薄纳米片堆积的多级结构,其比表面积不少于120m
2 g
‑1,有利于提供更多的氧化还原反应位点,有效缩短离子传输路径。本发明中掺杂剂为钼源或钨源,以最高价金属离子的形式(+6)存在,掺杂原子百分比为3.5~20%,同时钴基复合材料富含氧空位,可以有效调控氧化钴材料的电子结构,提高本征电导率。
28.本发明所述复合纳米材料的制备方法具有工艺简单、重现性好、成本低廉、环境友好等优点。将所制备的m/coo
x
复合纳米材料用于电催化析氧反应,在碱性溶液中表现出较低的过电位,具有较为广阔的应用前景。值得注意的是,这也是m/coo
x
在电催化析氧领域的首次应用。
附图说明
29.图1为实施例1中所得到的coo
x
电极材料在不同放大倍率下的电镜扫描图。
30.图2为实施例1中所得到的coo
x
电极材料的x射线衍射图。
31.图3为实施例2中所得到的w/coo
x
‑
1电极材料在不同放大倍率下的电镜扫描图。
32.图4为实施例3中所得到的mo/coo
x
‑
2电极材料在不同放大倍率下的电镜扫描图。
33.图5是实施例3所得到的mo/coo
x
‑
2材料的afm图像。
34.图6为实施例3中所得到的mo/coo
x
‑
2电极材料的x射线衍射图。
35.图7为实施例3所得到的mo/coo
x
‑
2材料mo 3d的xps图。
36.图8为实施例3中所得到的mo/coo
x
‑
2电极材料在不同放大倍率下的透射电镜图。
37.图9为实施例1和3所得到的coo
x
和mo/coo
x
‑
2材料的o1s xps图和epr图。
38.图10为实施例4中所得到的mo/coo
x
‑
3电极材料在不同放大倍率下的扫描电镜图。
39.图11为coo
x
,w/coo
x
‑
1,mo/coo
x
‑
2和mo/coo
x
‑
3的bet和bjh图。
40.图12为实施例1,2,3和4中所得到的coo
x
,w/coo
x
‑
1,mo/coo
x
‑
2和mo/coo
x
‑
3电极材料的电化学性能图。
具体实施方式
41.下面通过具体实施例进一步描述本发明,但本发明的保护范围并不仅限于此。
42.实施例1:coo
x
的制备及其析氧性能(未掺杂高价态金属离子)
43.取硝酸钴(0.582g,2mmol)溶于20mldi中,取尿素(0.6g,10mmol)溶于20ml di,两者混合均匀后将溶液转移至50ml水热釜中;加入预处理过的4
×
1cm泡沫镍基体,于120℃下反应6小时。反应完成后自然冷却至室温,取出泡沫镍基体,用去离子水以及无水乙醇冲洗数次,60℃真空干燥12小时,即得到前驱体材料。
44.将制备得到的泡沫镍(负载有前驱体材料0.01g)放置在瓷舟内,称取1.0g nabh4置于另一瓷舟内。装有nabh4的瓷舟置于上游,装有泡沫镍的瓷舟置于管式炉中间段。在氮气氛围下,以2℃/min 的速率升温至350℃并保温2小时,即得coo
x
样品。
45.图1是实施例1所得到的coo
x
材料在不同放大倍率下的扫描电镜图像。图1a清晰地看到我们所得到的样品是由一维纳米线和二维纳米片共同组成的形貌,纳米片与纳米线交
叉连接(图1b
‑
c)。
46.图2为实施例1中所得到的coo
x
材料的x射线衍射图。从图中可以看出,coo
x
样品的图谱可以分为co3o4(jcpds no.43
‑
1003),coo(jcpds no.70
‑
2855)和co(jcpds no.05
‑
0727)。在2θ值分别为36.8
°
,42.8
°
和62.2
°
处的三个强峰与coo的(111),(200)和(220)晶面相对应,而2θ值分别为47.5
°
和75.9
°
处的峰与co的(101)和(110)晶面相对应。
47.实施例2:w/coo
x
‑
1的制备及其析氧性能
48.取氯化钴(0.582g,2.45mmol)、钨酸钠(0.04g,0.12mmol)溶于20ml di中,取尿素(0.6 g,10mmol)溶于20ml di,两者混合均匀后将溶液转移至50ml水热釜中;加入预处理过的4
×
1 cm泡沫镍基体,于120℃下反应6小时。反应完成后自然冷却至室温,取出泡沫镍基体,用去离子水以及无水乙醇冲洗数次,60℃真空干燥12小时,即得到前驱体材料。
49.将制备得到的泡沫镍(负载有前驱体材料0.007g)放置在瓷舟内,称取1.0g nabh4置于另一瓷舟内。装有nabh4的瓷舟置于上游,装有泡沫镍的瓷舟置于管式炉中间段。在氮气氛围下,以2℃/min的速率升温至350℃并保温2小时,即得w/coo
x
‑
1样品。
50.图3是实施例2所得到的w/coo
x
‑
1材料在不同放大倍率下的扫描电镜图像。与图1对比,我们可以清晰地看到,随着少量钨酸钠的加入,纳米材料的形貌发生了明显变化。纳米片的含量大大增加,而纳米线的数量有所减少,这证明钨源的加入对改变纳米材料的形貌有明显效果。
51.实施例3:mo/coo
x
‑
2的制备及其析氧性能
52.取乙酸钴(0.582g,2.3mmol)、钼酸钠(0.12g,0.5mmol)溶于20ml di中,取尿素(0.6g, 10mmol)溶于20ml di,两者混合均匀后将溶液转移至50ml水热釜中;加入预处理过的4
×
1cm 泡沫镍基体,于120℃下反应6小时。反应完成后自然冷却至室温,取出泡沫镍基体,用去离子水以及无水乙醇冲洗数次,60℃真空干燥12小时,即得到前驱体材料。
53.将制备得到的泡沫镍(负载有前驱体材料0.008g)放置在瓷舟内,称取1.0g nabh4置于另一瓷舟内。装有nabh4的瓷舟置于上游,装有泡沫镍的瓷舟置于管式炉中间段。在氮气氛围下,以 2℃/min的速率升温至350℃并保温2小时,即得mo/coo
x
‑
2样品。
54.图4是实施例3所得到的mo/coo
x
‑
2材料在不同放大倍率下的扫描电镜图像。与图1、图3对比,我们可以清晰地看到,材料的微观形貌由纳米线、纳米片共存完全转变为由超薄的二维纳米片组成的三维纳米片网络结构。超薄纳米片具有非常光滑的表面和较大的比表面积,这将有利于电解质的渗透和离子传输,提高其电化学性能。
55.图5是实施例3所得到的mo/coo
x
‑
2材料的afm图像,可以看到mo/coo
x
‑
2纳米片厚度不到 2nm,确实具有超薄特性。
56.图6是实施例3所得到的mo/coo
x
‑
2材料的x射线衍射图。从图中可以看出,mo/coo
x
‑
2样品的图谱可以分为coo(jcpds no.42
‑
1300)和coo(jcpds no.70
‑
2855)。在xrd结果中并未发现钼化合物的衍射峰,表明在掺杂过程中未形成钼的化合物相。
57.图7是实施例3所得到的mo/coo
x
‑
2材料mo的xps图,从图可以分析出,mo/coo
x
‑
2的反卷积mo 3d光谱显示mo 3d
3/2
(235.5ev)和mo 3d
5/2
(232.2ev)的两个峰,表明mo(+6)的高价态。
58.图8a
‑
d为实施例3所得到的mo/coo
x
‑
2材料在不同放大倍率下的透射电镜图像。可以清晰的看到超薄纳米片结构,且纳米片上具有很多穿透的开放型小孔,这将非常有利于
离子的传输,透射电镜的结果与扫描电镜的结果很好的吻合。此外,通过晶格条纹我们也判断出纳米材料由两种不同晶相的coo共同组成。图8e为样品的能量弥散x射线光谱(eds),结果显示co、mo、c、n、 o元素均匀分布。
59.图9是实施例1和3所得到的coo
x
和mo/coo
x
‑
2材料的o1s xps图和epr图。o 1s图由在 530.1ev时晶格氧(o1)、532.7ev时表面吸附水分子(o3)和531.6ev时缺陷氧(o2)三个氧峰组成。丰富氧气空位来源于nabh4的强还原作用。令人印象深刻的是,mo/coo
x
‑
2具有比coo
x
高的氧空位,峰值强度更强(o2)。此外,epr可以检查与缺陷相关的物种和空位中未配对的电子。 co3o4,coo
x
和mo/coo
x
‑
2复合材料在g=2.002时显示对称的epr信号。与co3o4相比,很容易观察到coo
x
和mo/coo
x
‑
2的峰强度更高,这与o1s xps结果一致。coo
x
和mo/coo
x
‑
2复合材料在epr吸收光谱中顺磁性相的突出共振线表明,nabh4的强烈还原和氧空位的存在。
60.实施例4:mo/coo
x
‑
3的制备及其析氧性能
61.取乙酸钴(0.582g,2mmol)、钼酸铵(0.24g,0.2mmol)溶于20ml di中,取尿素(0.6g, 10mmol)溶于20ml di,两者混合均匀后将溶液转移至50ml水热釜中;加入预处理过的4
×
1cm 泡沫镍基体,于120℃下反应6小时。反应完成后自然冷却至室温,取出泡沫镍基体,用去离子水以及无水乙醇冲洗数次,60℃真空干燥12小时,即得到前驱体材料。
62.将制备得到的泡沫镍(负载有前驱体材料0.008g)放置在瓷舟内,称取1.0g nabh4置于另一瓷舟内。装有nabh4的瓷舟置于上游,装有泡沫镍的瓷舟置于管式炉中间段。在氮气氛围下,以 2℃/min的速率升温至350℃并保温2小时,即得mo/coo
x
‑
3样品。
63.图10是实施例4所得到的mo/coo
x
‑
3材料在不同放大倍率下的扫描电镜图像。与图1、图3 和图4对比,我们可以清晰地看到,随着钼盐浓度的进一步增加,mo/coo
x
的微观形貌由3d纳米花与2d纳米片阵列一起形成。
64.图11是coo
x
,w/coo
x
‑
1,mo/coo
x
‑
2和mo/coo
x
‑
3的bet和bjh图,可以看到当没有mo 或w掺杂时,coo
x
的比表面积和孔的数量最小。随着mo或w掺杂量的增加,比表面积先增加后减小,这也可以从sem图像推测出来。材料的形貌先从一维向二维转变,比表面积增加。最后从二维变化为三维,比表面积对应减小。
65.图12a为coo
x
,w/coo
x
‑
1,mo/coo
x
‑
2和mo/coo
x
‑
3电极材料在1m koh溶液中的lsv曲线。可以看出,在电流密度为10ma/cm2时,mo/coo
x
‑
2电极的过电势为260mv,高于coo
x
,w/coo
x
‑
1和mo/coo
x
‑
3的性能。这是由于超薄二维片层结构暴露了更多的活性位点,更有利于离子的传输;同时第二金属的加入也使得氧化还原反应的多样性增加。
66.图12b为coo
x
,w/coo
x
‑
1,mo/coo
x
‑
2和mo/coo
x
‑
3电极在1m koh溶液中的tafel曲线。其tafel曲线斜率分别为102mf
·
dec
‑1,150mf
·
dec
‑1,63mf
·
dec
‑1和118mf
·
dec
‑1这进一步表明超薄片层结构能够加快电子的传输速率。
67.图12c为coo
x
,w/coo
x
‑
1,mo/coo
x
‑
2和mo/coo
x
‑
3电极在1m koh溶液的电化学比表面积柱状图。可以看出4个电极的电化学比表面积分别为26.4mf
·
dec
‑1,34.5mf
·
dec
‑1,68.3mf
·
dec
‑1, 64.8mf
·
dec
‑1,进一步说明二维结构具有更大的电化学有效面积。
68.图12d为coo
x
,w/coo
x
‑
1,mo/coo
x
‑
2和mo/coo
x
‑
3电极在1m koh溶液中的电化学阻抗谱。从图中也可以看出mo/coo
x
‑
2具有较小的阻抗,说明该电催化剂与电解液界面上的电荷转移动力学更快,最终使得催化性能大大提升。
69.表1是coo
x
,w/coo
x
‑
1,mo/coo
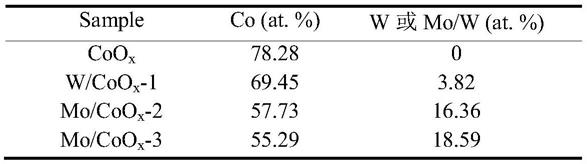
x
‑
2和mo/coo
x
‑
3的icp含量分析。coo
x
,w/coo
x
‑
1,mo/coo
x
‑
2 和mo/coo
x
‑
3中w或mo的含量分别为0,3.82%,16.36%,18.59%。
70.表1
[0071][0072]
从上述实施例可以看出,本发明中所述的制备方法是一种比较普适性的方法,通过调控掺杂金属盐的量来调控纳米材料的微观形貌并得到前驱体,再经过惰性气体保护下硼氢化钠中煅烧,最终获得了coo
x
,w/coo
x
‑
1,mo/coo
x
‑
2和mo/coo
x
‑
3样品,这些样品在碱性溶液中都表现出较好的析氧性能。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1