一种1,2,4-三唑并六元氮杂环-3-胺的合成方法
1.本发明涉及有机合成技术领域,具体涉及一种1,2,4-三唑并六元氮杂环-3-胺的合成方法。
背景技术:
2.三氮唑类化合物在医药、农药、化学化工等领域中有着广泛的应用。三唑环自身是一个含六电子的五原子体系,可构成富电子π共轭体系,同时包含咪唑和吡啶的配位特点。三唑环作为生物电子等排体,可代替咪唑、噁唑、吡唑、噻唑等基团用于设计开发新型药物,在改善化合物的生物活性方面有重要作用。1,2,4-三唑并六元氮杂环-3-胺是三唑衍生物中具有代表性的一类,该类衍生物因其独特的生理活性得到了广泛关注。
3.目前,1,2,4-三唑并六元氮杂环-3-胺的合成方法主要有三种,阴离子介导的脱硫关环反应生成1,2,4-三唑并[3,4-a]吡啶,碘催化的脱硫关环反应构建1,2,4-三唑并六元氮杂环,以及聚合物负载的mukaiyama试剂辅助的脱硫关环反应。这些合成方法为该类母核的合成提供了一些思路,然而它们仍然存在一定的限制,例如底物范围窄、收率低、反应温度较高以及需要使用大量金属催化剂等。
[0004]
因此开发一种环境友好、底物范围广,收率高的1,2,4-三唑并六元氮杂环类化合物的新方法具有重要的意义。
技术实现要素:
[0005]
本发明旨在至少解决现有技术中存在的技术问题之一。为此,本发明提出一种1,2,4-三唑并六元氮杂环-3-胺的方法的合成方法,在电催化的条件下,无需加入金属催化剂和氧化剂,反应产率高,底物范围广,且后处理简单。
[0006]
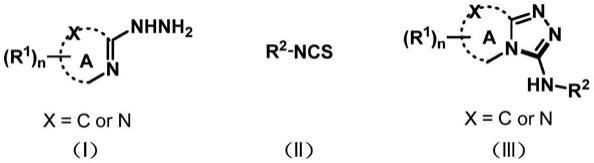
1.一种1,2,4-三唑并六元氮杂环-3-胺的合成方法,包括以下步骤:在电解体系中,电催化式(i)所示的杂环肼类化合物和式(ii)所示的异硫氰酸酯类化合物反应,得到式(iii)所示的1,2,4-三唑并六元氮杂环-3-胺类化合物;
[0007][0008]
式中,a环为氮杂芳环;
[0009]
x为氮原子或碳原子;
[0010]
r1和r2均独立选自氢、烷基、烷氧基、酯基、卤素原子、卤代烷基、取代或未取代芳基、取代或未取代杂芳基;
[0011]
n为1~2的整数;
[0012]
所述电解体系中包括碱性添加剂;
[0013]
所述电催化的电解质中包括含碘化合物。
[0014]
本发明的1,2,4-三唑并六元氮杂环-3-胺的合成方法,至少具有如下有益效果:
[0015]
1.该反应适用底物主要为杂环肼类化合物与异硫氰酸酯类化合物,电催化氧化将碘离子原位转化为碘阳离子,在经历反应循环后,这些碘阳离子还原为碘负离子,实现催化循环;通过电催化脱硫关环一步合成1,2,4-三唑并六元氮杂环-3-胺衍生物。因此相比于碘介导反应,本发明的电催化脱硫关环反应只需使用少量的碘盐,同时,该反应适用的底物类型丰富,说明其反应官能团耐受性好,反应条件温和,反应产率高,部分的反应产率高达90%以上;反应中使用的原料和溶剂等廉价易得,反应过程快且操作简单安全,适合工业化生产。
[0016]
在本发明的一些实施方式中,式(i)中,a环为c1~c
20
的氮杂芳环。
[0017]
在本发明的一些优选地实施方式中,式(i)中,a环为c1~c
10
以下的氮杂芳环。
[0018]
在本发明的一些优选地实施方式中,式(i)中,a环为吡啶、异喹啉、嘧啶、吡嗪和哒嗪中的至少一种。
[0019]
在本发明的一些实施方式中,所述取代或未取代芳基中,所述芳基为c1~c
20
的芳基。
[0020]
在本发明的一些优选地实施方式中,所述取代或未取代芳基中,所述芳基为c1~c
10
的芳基。
[0021]
在本发明的一些更优选地实施方式中,所述c1~c
10
的芳基中,所述芳基为苯基或萘基。
[0022]
在本发明的一些优选地实施方式中,所述取代芳基包括取代苯基,所述取代苯基包括一取代苯基、二取代苯基和三取代苯基中的一种。
[0023]
在本发明的一些实施方式中,所述取代芳基包括烷基苯基、烷氧基苯基、苯甲氧基苯基、硝基苯基、氰基苯基、三氟甲基苯基、三氟甲氧基苯基、甲氧基羟基苯基和卤代苯基中的至少一种。
[0024]
在本发明的一些优选地实施方式中,所述卤代苯基为一取代卤代苯基或二取代卤代苯基。
[0025]
在本发明的一些更优选地实施方式中,所述卤代苯基中的卤素原子选自氟、氯或溴原子中的至少一种。
[0026]
在本发明的一些更优选地实施方式中,所述二取代卤代苯基中的卤素原子可以相同或不同。
[0027]
在本发明的一些实施方式中,所述烷基为c1~c
20
的烷基。
[0028]
在本发明的一些优选地实施方式中,所述烷基为c
1~4
烷基。
[0029]
在本发明的一些优选地实施方式中,所述c
1~
c4烷基包括甲基。
[0030]
在本发明的一些优选地实施方式中,所述烷基包括取代烷基和未取代烷基中的至少一种。
[0031]
在本发明的一些优选地实施方式中,所述取代烷基包括一取代烷基或二取代烷基。
[0032]
在本发明的一些优选地实施方式中,所述烷氧基包括一取代烷氧基或三取代烷氧基。
[0033]
在本发明的一些实施方式中,所述烷氧基包括甲氧基。
[0034]
在本发明的一些实施方式中,所述酯基包括甲酸乙酯基。
[0035]
在本发明的一些实施方式中,所述卤素包括氟、氯或溴中的至少一种。
[0036]
在本发明的一些实施方式中,所述取代或未取代杂芳基中,所述杂芳基包括c1~c
20
的含氮杂环。
[0037]
在本发明的一些优选地实施方式中,所述取代或未取代杂芳基中,所述杂环为c1~c
10
的含氮杂环。
[0038]
在本发明的一些更优选地实施方式中,所述杂环包括吲哚和吡啶中的至少一种。
[0039]
在本发明的一些优选地实施方式中,所述取代杂芳基为n-苯磺酰基吲哚基。
[0040]
在本发明的一些优选地实施方式中,所述含碘化合物包括含碘有机化合物和含碘无机化合物中的至少一种。
[0041]
在本发明的一些优选地实施方式中,所述含碘有机化合物包括含碘季铵盐。
[0042]
在本发明的一些优选地实施方式中,所述含碘季铵盐包括含碘烷基季铵盐。
[0043]
在本发明的一些优选地实施方式中,所述含碘烷基季铵盐包括四丁基碘化铵。
[0044]
在本发明的一些实施方式中,所述碱性添加剂为无机碱性添加剂和有机碱性添加剂中的至少一种。
[0045]
在本发明的一些优选地实施方式中,所述无机碱添加剂包括碳酸钾和碳酸铯中的至少一种。
[0046]
在本发明的一些更优选地实施方式中,所述无机碱添加剂为碳酸钾。
[0047]
在本发明的一些实施方式中,所述溶剂包括乙腈和甲醇中的至少一种。
[0048]
在本发明的一些更优选地实施方式中,所述溶剂为乙腈。
[0049]
在本发明的一些实施方式中,所述电解体系中选用直流电流;
[0050]
所述直流电流大小为5~60ma。
[0051]
在本发明的一些实施方式中,所述式(i)所示的杂环肼类化合物与式(ii)所示的异硫氰酸酯类化合物的摩尔比为1:1.0~1.5。
[0052]
在本发明的一些优选地实施方式中,所述式(i)所示的杂环肼类化合物与式(ii)所示的异硫氰酸酯类化合物的摩尔比为1:1.2。
[0053]
在本发明的一些实施方式中,所述式(i)所示的杂环肼类化合物与电解质的摩尔比为1:0.05~0.2。
[0054]
在本发明的一些实施方式中,所述杂环肼类化合物与碱性添加剂的摩尔比为1:0.5~1.0。
[0055]
在本发明的一些优选地实施方式中,所述式(i)所示的杂环肼类化合物与碱性添加剂的摩尔比为1:0.5。
[0056]
在本发明的一些实施方式中,所述溶剂体积用量与杂环肼类化合物摩尔比为10~15ml/mmol。
[0057]
在本发明的一些实施方式中,所述电催化的反应时间为5~10h,所述电催化的反应温度为20~30℃。
[0058]
在本发明的一些实施方式中,所述式(i)所示的杂环肼类化合物选自2-肼基吡啶、2-氯-6-肼基吡啶、5-氯-2-肼基吡啶、3-氯-2-肼基吡啶、2-溴-6-肼基吡啶、5-溴-2-肼基吡啶、5-三氟甲基-2-肼基吡啶、3-三氟甲基-2-肼基吡啶、2-甲基-6-肼基吡啶、5-甲基-2-肼
基吡啶、3-氟-5-溴-2-肼基吡啶、3-氯-5-三氟甲基-2-肼基吡啶、3-氟-5-(3,4,5-三甲氧基苯基)-2-肼基吡啶、3-肼基喹啉、5-(1-(苯基磺酰基)-1h-吲哚-5-基)-2-肼基吡啶、3-氟-5-(1-(苯基磺酰基)-1h-吲哚-5-基)-2-肼基吡啶、2-肼基吡啶、2-肼基嘧啶、4,6-二甲基-2-肼基嘧啶、6-氯-4-肼基嘧啶、2-甲氧基-5-氟-4-肼基嘧啶、2-肼基吡嗪、3-氯-2-肼基吡嗪、6-甲基-3-肼基哒嗪、6-氯-3-肼基哒、5-溴-2-肼基吡啶、6-溴-2-肼基吡啶、3-氟-5-溴-2-肼基吡啶、5-(1-(苯基磺酰基)-1h-吲哚-5-基)-2-肼基吡啶和3-氟-5-(1-(苯基磺酰基)-1h-吲哚-5-基)-2-肼基吡啶中的一种。
[0059]
在本发明的一些实施方式中,所述式(ii)所示的异硫氰酸酯类化合物选自异硫氰酸苯酯、2-氟苯基异硫氰酸酯、2-溴苯基异硫氰酸酯、2-甲基苯基异硫氰酸酯、3-溴苯基异硫氰酸酯、3-硝基苯基异硫氰酸酯、4-氟苯基异硫氰酸酯、4-氯苯基异硫氰酸酯、4-溴苯基异硫氰酸酯、4-硝基苯基异硫氰酸酯、4-氰基苯基异硫氰酸酯、4-甲基苯基异硫氰酸酯、4-三氟甲基苯基异硫氰酸酯、3,4,5-三甲氧基苯基异硫氰酸酯、3-苯甲氧基苯基异硫氰酸酯、1-萘基异硫氰酸酯、2,6-二甲基苯基异硫氰酸酯、3,5-双三氟甲基苯基异硫氰酸酯、4-叔丁基苯基异硫氰酸酯、2,4-二氟苯基异硫氰酸酯、异丙基异硫氰酸酯、异丙基异硫氰酸酯、甲酸乙酯基异硫氰酸酯、3-吡啶基异硫氰酸酯、异硫氰酸苯酯、4-甲基苯基异硫氰酸酯、3,4,5-三甲氧基苯基异硫氰酸酯、(1h-吲哚-4-基)异硫氰酸酯、(1h-吲哚-6-基)异硫氰酸酯中的一种。
[0060]
在本发明的一些实施方式中,所述点解体系还包括阳极和阴极。
[0061]
在本发明的一些实施方式中,所述阳极包括碳棒(ф=6~18mm)。
[0062]
在本发明的一些实施方式中,所述阴极包括铂片(10~20mm
×
10~20mm)。
[0063]
在本发明的一些实施方式中,式(i)所示的杂环肼类化合物和式(ii)所示的异硫氰酸酯类化合物反应结束后,后处理包括抽滤、水洗、干燥、浓缩、柱层析或浓缩、柱层析得到1,2,4-三唑并六元氮杂环-3-胺类化合物。
具体实施方式
[0064]
以下将结合实施例对本发明的构思及产生的技术效果进行清楚、完整地描述,以充分地理解本发明的目的、特征和效果。显然,所描述的实施例只是本发明的一部分实施例,而不是全部实施例,基于本发明的实施例,本领域的技术人员在不付出创造性劳动的前提下所获得的其他实施例,均属于本发明保护的范围。
[0065]
实施例1:n-苯基-[1,2,4]三唑并[4,3-a]吡啶-3-胺(1a)的合成
[0066][0067]
取40ml反应管,加入2-肼基吡啶(54.6mg,0.50mmol)、异硫氰酸苯酯(81.1mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(94.6mg,0.45mmol),收率为90%(94.6/(210.24
×
0.5)=90%)。
[0068]
2-肼基吡啶cas号:4930-98-7,异硫氰酸苯酯cas:103-72-0。
[0069]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.23(s,1h),8.34(d,j=7.1hz,1h),7.62(d,j=9.3hz,1h),7.56(d,j=8.0hz,2h),7.31(t,j=7.7hz,2h),7.24(dd,j=9.3,6.4hz,1h),6.95
–
6.86(m,2h);
13
c nmr(125mhz,dmso-d6)δ146.3,144.4,141.5,129.0,126.6,122.7,120.5,116.3,115.6,112.3;hr-esi-msfor c
12h10
n4([m+h]
+
)calcd:211.0978;found:211.0973。
[0070]
实施例2:5-氯-n-苯基-[1,2,4]三唑并[4,3-a]吡啶-3-胺(1b)的合成
[0071][0072]
取40ml反应管,加入2-氯-6-肼基吡啶(71.8mg,0.50mmol)、异硫氰酸苯酯(81.1mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(99.1mg,0.41mmol),收率为81%(99.1/(244.68
×
0.5)=81%)。
[0073]
2-氯-6-肼基吡啶cas号:5193-03-3,异硫氰酸苯酯cas:103-72-0。
[0074]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ8.56(s,1h),7.72(dd,j=9.2,0.8hz,1h),7.29(dd,j=9.2,7.0hz,1h),7.22
–
7.17(m,2h),7.06(dd,j=7.0,0.8hz,1h),6.84
–
6.79(m,3h);
13
c nmr(125mhz,dmso-d6)δ150.1,144.9,143.6,129.1,128.2,124.2,119.6,115.1,115.0,114.9;hr-esi-ms for c
12
h9cln4([m+h]
+
)calcd:245.0589;found:245.0586。
[0075]
实施例3:6-氯-n-苯基-[1,2,4]三唑并[4,3-a]吡啶-3-胺(1c)的合成
[0076][0077]
取40ml反应管,加入5-氯-2-肼基吡啶(71.8mg,0.50mmol)、异硫氰酸苯酯(81.1mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经抽滤固液分离,滤饼水洗干燥得产品(61.7mg,0.25mmol)。母液减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(44.7mg,0.18mmol),合并产品(106.4mg,0.44mmol),收率为87%((61.7+44.7)/(244.68
×
0.5)=87%)。
[0078]
5-氯-2-肼基吡啶cas号:27032-63-9,异硫氰酸苯酯cas:103-72-0。
[0079]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.26(s,1h),8.69(s,1h),7.67(d,j=9.8hz,1h),7.65(d,j=7.3hz,2h),7.35
–
7.31(m,2h),7.26(dd,j=9.8,1.8hz,1h),6.94(t,j=7.3hz,1h);
13
c nmr(125mhz,dmso-d6)δ144.7,144.6,140.8,129.0,127.4,120.8,120.7,119.2,116.5,116.5;hr-esi-ms for c
12
h9cln4([m+h]
+
)calcd:245.0589;found:245.0587。
[0080]
实施例4:8-氯-n-苯基-[1,2,4]三唑并[4,3-a]吡啶-3-胺(1d)的合成
[0081][0082]
取40ml反应管,加入3-氯-2-肼基吡啶(71.8mg,0.50mmol)、异硫氰酸苯酯(81.1mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(91.8mg,0.38mmol),收率为75%(91.8/(244.68
×
0.5)=75%)。
[0083]
3-氯-2-肼基吡啶cas号:22841-92-5,异硫氰酸苯酯cas:103-72-0。
[0084]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.37(s,1h),8.37(d,j=7.0hz,1h),7.60(d,j=7.3hz,2h),7.46(d,j=7.0hz,1h),7.35
–
7.31(m,2h),6.94(t,j=7.3hz,1h),6.90(t,j=7.0hz,1h);
13
c nmr(125mhz,dmso-d6)δ145.8,143.9,141.0,129.1,125.6,122.1,120.9,120.2,116.5,112.1;hr-esi-ms for c
12
h9cln4([m+h]
+
)calcd:245.0589;found:245.0587。
[0085]
实施例5:5-溴-n-苯基-[1,2,4]三唑并[4,3-a]吡啶-3-胺(1e)的合成
[0086][0087]
取40ml反应管,加入2-溴-6-肼基吡啶(94.0mg,0.50mmol)、异硫氰酸苯酯(81.1mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经抽滤固液分离,滤饼水洗干燥得产品(40.2mg,0.14mmol)。母液减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(85.5mg,0.30mmol),合并产品(125.8mg,0.44mmol),收率为87%((40.2+85.5)/(289.14
×
0.5)=87%)。
[0088]
2-溴-6-肼基吡啶cas号:26944-71-8,异硫氰酸苯酯cas:103-72-0。
[0089]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ8.50(s,1h),7.75(dd,j=7.5,2.3hz,1h),7.24
–
7.15(m,4h),6.79(t,j=7.3hz,1h),6.74(d,j=7.9hz,2h);
13
c nmr(125mhz,dmso-d6)δ150.1,145.3,143.8,129.1,128.4,119.6,119.4,115.5,114.6,111.6;hr-esi-ms for c
12
h9brn4([m+h]
+
)calcd:289.0083;found:289.0079。
[0090]
实施例6:6-溴-n-苯基-[1,2,4]三唑并[4,3-a]吡啶-3-胺(1f)的合成
[0091][0092]
取40ml反应管,加入5-溴-2-肼基吡啶(94.0mg,0.50mmol)、异硫氰酸苯酯(81.1mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈
5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经抽滤固液分离,滤饼水洗干燥得产品(72.1mg,0.25mmol)。母液减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(56.6mg,0.20mmol),合并产品(128.7mg,0.45mmol),收率为89%((72.1+56.6)/(289.14
×
0.5)=89%)。
[0093]
5-溴-2-肼基吡啶cas号:77992-44-0,异硫氰酸苯酯cas:103-72-0。
[0094]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.28(s,1h),8.77(s,1h),7.65(d,j=7.3hz,2h),7.61(d,j=9.7hz,1h),7.35
–
7.30(m,3h),6.94(t,j=7.3hz,1h);
13
c nmr(125mhz,dmso-d6)δ144.6,144.4,140.8,129.3,129.0,122.8,120.8,116.7,116.5,106.2;hr-esi-ms for c
12
h9brn4([m+h]
+
)calcd:289.0083;found:289.0082。
[0095]
实施例7:6-三氟甲基-n-苯基-[1,2,4]三唑并[4,3-a]吡啶-3-胺(1g)的合成
[0096][0097]
取40ml反应管,加入5-三氟甲基-2-肼基吡啶(88.6mg,0.50mmol)、异硫氰酸苯酯(81.1mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经减压蒸馏除去溶剂,再经柱层析(石油醚:乙酸乙酯=4:1)得到产品(102.9mg,0.37mmol),收率为74%(102.9/(278.24
×
0.5)=74%)。
[0098]
5-三氟甲基-2-肼基吡啶cas号:89570-85-4,异硫氰酸苯酯cas:103-72-0。
[0099]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.50(s,1h),9.11(s,1h),7.78(d,j=9.8hz,1h),7.73(d,j=7.9hz,2h),7.40(d,j=9.8hz,1h),7.36(t,j=7.9hz,2h),6.97(t,j=7.3hz,1h);
13
c nmr(125mhz,dmso-d6)δ145.7,145.2,140.5,129.0,123.8(c-f,3j
c-f
=6.1hz),123.7(c-f,1j
c-f
=268.9hz),121.4,121.0,117.0,116.7,114.4(c-f,2j
c-f
=33.3hz);hr-esi-ms for c
13
h9f3n4([m+h]
+
)calcd:279.0852;found:279.0848。
[0100]
实施例8:8-三氟甲基-n-苯基-[1,2,4]三唑并[4,3-a]吡啶-3-胺(1h)的合成
[0101][0102]
取40ml反应管,加入3-三氟甲基-2-肼基吡啶(88.6mg,0.50mmol)、异硫氰酸苯酯(81.1mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经减压蒸馏除去溶剂,再经柱层析(石油醚:乙酸乙酯=4:1)得到产品(98.8mg,0.36mmol),收率为71%(98.8/(278.24
×
0.5)=71%)。
[0103]
3-三氟甲基-2-肼基吡啶:89570-83-2,异硫氰酸苯酯cas:103-72-0。
[0104]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.44(s,1h),8.61(d,j=7.1hz,1h),7.75(d,j=6.8hz,1h),7.62(dd,j=8.6,1.0hz,2h),7.35
–
7.31(m,2h),7.02(t,j=6.9hz,1h),6.95(t,j=7.3hz,1h);
13
c nmr(125mhz,dmso-d6)δ145.4,141.4,140.9,129.1,
127.2,126.6(c-f,3j
c-f
=5.3hz),122.5(c-f,1j
c-f
=269.9hz),120.9,116.6,115.9(c-f,2j
c-f
=34.3hz),110.8;hr-esi-ms for c
13
h9f3n4([m+h]
+
)calcd:279.0852;found:279.0849。
[0105]
实施例9:5-甲基-n-苯基-[1,2,4]三唑并[4,3-a]吡啶-3-胺(1i)的合成
[0106][0107]
取40ml反应管,加入2-甲基-6-肼基吡啶(61.6mg,0.50mmol)、异硫氰酸苯酯(81.1mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经抽滤固液分离,滤饼水洗干燥得产品(19.4mg,0.09mmol)。母液减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(52.4mg,0.23mmol),合并产品(71.8mg,0.32mmol),收率为64%((19.4+52.4)/(224.27
×
0.5)=64%)。
[0108]
2-溴-6-肼基吡啶cas号:26944-71-8,异硫氰酸苯酯cas:103-72-0。
[0109]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ8.42(s,1h),7.55(d,j=8.8hz,1h),7.24
–
7.16(m,3h),6.79(t,j=6.5hz,1h),6.66(d,j=6.5hz,3h),2.66(s,3h);
13
c nmr(125mhz,dmso-d6)δ149.9,146.1,143.8,135.0,129.3,127.9,119.3,114.2,113.8,17.6;hr-esi-ms for c
13h12
n4([m+h]
+
)calcd:225.1135;found:225.1133。
[0110]
实施例10:6-甲基-n-苯基-[1,2,4]三唑并[4,3-a]吡啶-3-胺(1j)的合成
[0111][0112]
取40ml反应管,加入5-甲基-2-肼基吡啶(61.6mg,0.50mmol)、异硫氰酸苯酯(81.1mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经抽滤固液分离,滤饼水洗干燥得产品(43.9mg,0.20mmol)。母液减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(58.1mg,0.26mmol),合并产品(102.0mg,0.46mmol),收率为91%((43.9+58.1)/(224.27
×
0.5)=91%)。
[0113]
5-甲基-2-肼基吡啶cas号:4931-01-5,异硫氰酸苯酯cas:103-72-0。
[0114]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.12(s,1h),8.13(s,1h),7.56
–
7.50(m,3h),7.29(t,j=7.7hz,2h),7.10(d,j=9.4hz,1h),6.90(t,j=7.2hz,1h),2.25(s,3h);
13
c nmr(125mhz,dmso-d6)δ145.8,143.9,141.6,129.8,129.0,121.7,120.3,119.3,116.0,114.9,17.6;hr-esi-ms for c
13h12
n4([m+h]
+
)calcd:225.1135;found:225.1132。
[0115]
实施例11:6-溴-8-氟-n-苯基-[1,2,4]三唑并[4,3-a]吡啶-3-胺(1k)的合成
[0116][0117]
取40ml反应管,加入3-氟-5-溴-2-肼基吡啶(103.0mg,0.50mmol)、异硫氰酸苯酯(81.1mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经抽滤固液分离,滤饼水洗干燥得产品(64.1mg,0.21mmol)。母液减压蒸馏除去溶剂,再经柱层析(石油醚:乙酸乙酯=6:1)得到产品(69.5mg,0.23mmol),合并产品(133.6mg,0.44mmol),收率为87%((64.1+69.5)/(307.13
×
0.5)=87%)。
[0118]
3-氟-5-溴-2-肼基吡啶cas号:1289084-83-8,异硫氰酸苯酯cas:103-72-0。
[0119]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.39(s,1h),8.67(s,1h),7.67(d,j=7.9hz,2h),7.46(d,j=10.5hz,1h),7.34(t,j=7.9hz,2h),6.96(t,j=7.3hz,1h);
13
c nmr(125mhz,dmso-d6)δ148.5(c-f,1j
c-f
=257.3hz),145.7,140.4,138.5(c-f,2j
c-f
=30.7hz),129.1,121.1,120.0(c-f,4j
c-f
=5.1hz),116.7,112.2(c-f,3j
c-f
=19.0hz),104.1(c-f,4j
c-f
=7.2hz);hr-esi-ms for c
12
h8brfn4([m+h]
+
)calcd:306.9989;found:306.9987。
[0120]
实施例12:6-氯-8-氟-n-苯基-[1,2,4]三唑并[4,3-a]吡啶-3-胺(1l)的合成
[0121][0122]
取40ml反应管,加入3-氟-5-氯-2-肼基吡啶(80.8mg,0.50mmol)、异硫氰酸苯酯(81.1mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经抽滤固液分离,滤饼水洗干燥得产品(86.7mg,0.33mmol)。母液减压蒸馏除去溶剂,再经柱层析(石油醚:乙酸乙酯=6:1)得到产品(35.4mg,0.14mmol),合并产品(122.1mg,0.47mmol),收率为93%((86.7+35.4)/(262.67
×
0.5)=93%)。
[0123]
3-氟-5-氯-2-肼基吡啶cas号:248255-70-1,异硫氰酸苯酯cas:103-72-0。
[0124]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.38(s,1h),8.60(d,j=1.1hz,1h),7.67(d,j=7.9hz,2h),7.40(dd,j=10.8,1.1hz,1h),7.34(t,j=7.9hz,2h),6.96(t,j=7.3hz,1h);
13
c nmr(125mhz,dmso-d6)δ148.5(c-f,1j
c-f
=256.2hz),145.9,140.4,138.4(c-f,2j
c-f
=31.5hz),129.0,121.1,118.0(c-f,4j
c-f
=5.7hz),117.7(c-f,4j
c-f
=8.7hz),116.7,110.4(c-f,3j
c-f
=19.4hz);hr-esi-ms for c
12
h8clfn4([m+h]
+
)calcd:263.0494;found:263.0492。
[0125]
实施例13:6-三氟甲基-8-氯-n-苯基-[1,2,4]三唑并[4,3-a]吡啶-3-胺(1m)的合成
[0126][0127]
取40ml反应管,加入3-氯-5-三氟甲基-2-肼基吡啶(105.8mg,0.50mmol)、异硫氰酸苯酯(81.1mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经抽滤固液分离,滤饼水洗干燥得产品(40.0mg,0.13mmol)。母液减压蒸馏除去溶剂,再经柱层析(石油醚:乙酸乙酯=6:1)得到产品(71.0mg,0.23mmol),合并产品(111.0mg,0.36mmol),收率为71%((40.0+71.0)/(312.68
×
0.5)=71%)。
[0128]
3-氯-5-三氟甲基-2-肼基吡啶cas号:89570-82-1,异硫氰酸苯酯cas:103-72-0。
[0129]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.60(s,1h),9.12(t,j=1.2hz,1h),7.77(d,j=1.2hz,1h),7.75
–
7.72(m,2h),7.39
–
7c.34(m,2h),7.01
–
6.96(m,1h);
13
c nmr(125mhz,dmso-d6)δ147.1,143.0,140.1,129.1,123.2(c-f,3j
c-f
=6.2hz),123.1(c-f,1j
c-f
=269.5hz),121.8,121.3,120.5,116.9,114.3(c-f,2j
c-f
=34.3hz);hr-esi-ms for c
13
h8clf3n4([m+h]
+
)calcd:313.0462;found:313.0458。
[0130]
实施例14:8-氟-n-苯基-6-(3,4,5-三甲氧基苯基)-[1,2,4]三唑并[4,3-a]吡啶-3-胺(1n)的合成
[0131][0132]
取40ml反应管,加入3-氟-5-(3,4,5-三甲氧基苯基)-2-肼基吡啶(146.7mg,0.50mmol)、异硫氰酸苯酯(81.1mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经减压蒸馏除去溶剂,再经柱层析(石油醚:乙酸乙酯=4:1)得到产品(122.3mg,0.31mmol),收率为62%(122.3/(394.41
×
0.5)=62%)。
[0133]
3-氟-5-(3,4,5-三甲氧基苯基)-2-肼基吡啶cas号:2671809-56-4,异硫氰酸苯酯cas:103-72-0。
[0134]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.41(s,1h),8.59(s,1h),7.71
–
7.66(m,3h),7.36(t,j=7.7hz,2h),7.02(s,2h),6.97(t,j=7.2hz,1h),3.89(s,6h),3.71(s,3h);
13
c nmr(125mhz,dmso-d6)δ153.4,148.9(c-f,1j
c-f
=251.7hz),146.2,140.7,138.9(c-f,2j
c-f
=32.0hz),137.9,131.0,129.1,125.1(c-f,4j
c-f
=5.8hz),121.1,116.8,116.3(c-f,4j
c-f
=4.3hz),109.4(c-f,3j
c-f
=16.2hz),104.5,60.2,56.3;hr-esi-ms for c
21h19
fn4o3([m+h]
+
)calcd:395.1514;found:395.1511。
[0135]
实施例15:n-苯基-[1,2,4]三唑并[4,3-b]异喹啉-3-胺(1o)的合成
[0136][0137]
取40ml反应管,加入3-肼基喹啉(79.6mg,0.50mmol)、异硫氰酸苯酯(81.1mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经抽滤固液分离,滤饼水洗干燥得产品(75.0mg,0.29mmol)。母液减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(18.7mg,0.07mmol),合并产品(93.7mg,0.36mmol),收率为72%((75.0+18.7)/(260.30
×
0.5)=72%)。
[0138]
3-肼基喹啉cas号:15793-78-9,异硫氰酸苯酯cas:103-72-0。
[0139]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.09(s,1h),8.50(d,j=8.5hz,1h),7.96(d,j=7.4hz,1h),7.74(d,j=9.6hz,1h),7.64
–
7.59(m,2h),7.53(t,j=7.4hz,1h),7.21(t,j=7.9hz,2h),6.88
–
6.83(m,3h);
13
c nmr(125mhz,dmso-d6)δ147.9,146.8,144.0,131.4,129.4,129.3,129.3,129.0,126.1,124.2,120.3,116.3,115.5,115.0;hr-esi-ms for c
16h12
n4([m+h]
+
)calcd:261.1135;found:261.1132。
[0140]
实施例16:n-苯基-6-(1-(苯基磺酰基)-1h-吲哚-5-基)-[1,2,4]三唑并[4,3-a]吡啶-3-胺(1p)的合成
[0141][0142]
取40ml反应管,加入5-(1-(苯基磺酰基)-1h-吲哚-5-基)-2-肼基吡啶(182.2mg,0.50mmol)、异硫氰酸苯酯(81.1mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(195.5mg,0.42mmol),收率为84%(195.5/(465.53
×
0.5)=84%)。
[0143]
5-(1-(苯基磺酰基)-1h-吲哚-5-基)-2-肼基吡啶cas号:15793-78-9,异硫氰酸苯酯cas:103-72-0。
[0144]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.30(s,1h),8.72(s,1h),8.08(d,j=8.7hz,1h),8.04
–
8.00(m,2h),7.96(d,j=1.6hz,1h),7.91(d,j=3.7hz,1h),7.72
–
7.67(m,5h),7.63
–
7.58(m,3h),7.36
–
7.31(m,2h),6.96
–
6.91(m,2h);
13
c nmr(125mhz,dmso-d6)δ145.4,144.8,141.1,137.0,134.8,133.9,131.8,131.3,130.0,129.1,128.1,127.1,126.8,125.2,123.6,120.6,119.8,119.6,116.4,115.6,113.8,109.8;hr-esi-ms for c
26h19
n5o2s([m+h]
+
)calcd:466.1332;found:466.1330。
[0145]
实施例17:8-氟-n-苯基-6-(1-(苯基磺酰基)-1h-吲哚-5-基)-[1,2,4]三唑并[4,3-a]吡啶-3-胺(1q)的合成c12
h9fn4([m+h]
+
)calcd:229.0884;found:229.0879。
[0155]
实施例19:n-(2-溴苯基)-[1,2,4]三唑并[4,3-a]吡啶-3-胺(2b)的合成
[0156][0157]
取40ml反应管,加入2-肼基吡啶(54.6mg,0.50mmol)、2-溴苯基异硫氰酸酯(128.4mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(104.1mg,0.36mmol),收率为72%(104.1/(289.14
×
0.5)=72%)。
[0158]
2-肼基吡啶cas号:4930-98-7,2-氟苯基异硫氰酸酯cas:13037-60-0。
[0159]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ8.34(s,1h),8.13(d,j=7.0hz,1h),7.70(d,j=9.3hz,1h),7.61(dd,j=8.0,1.1hz,1h),7.35
–
7.31(m,1h),7.26
–
7.22(m,1h),7.10(dd,j=8.1,1.2hz,1h),6.93(t,j=6.7hz,1h),6.90
–
6.86(m,1h);
13
c nmr(125mhz,dmso-d6)δ147.8,143.7,140.8,133.0,128.6,127.3,123.0,122.5,118.0,115.5,112.9,111.4;hr-esi-ms for c
12
h9brn4([m+h]
+
)calcd:289.0083;found:289.0078。
[0160]
实施例20:n-(邻甲苯基)-[1,2,4]三唑并[4,3-a]吡啶-3-胺(2c)的合成
[0161][0162]
取40ml反应管,加入2-肼基吡啶(54.6mg,0.50mmol)、2-甲基苯基异硫氰酸酯(89.5mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经抽滤固液分离,滤饼水洗干燥得产品(17.2mg,0.08mmol)。母液减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(64.7mg,0.29mmol),合并产品(81.9mg,0.37mmol),收率为73%((17.2+64.7)/(224.27
×
0.5)=73%)。
[0163]
2-肼基吡啶cas号:4930-98-7,2-甲基苯基异硫氰酸酯cas:13037-60-0。
[0164]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ8.17(s,1h),8.10(d,j=7.0hz,1h),7.65(d,j=9.4hz,1h),7.31
–
7.25(m,1h),7.19(d,j=7.3hz,1h),7.10
–
7.05(m,1h),7.02
–
6.97(m,1h),6.92
–
6.85(m,2h),2.29(s,3h);
13
c nmr(125mhz,dmso-d6)δ147.3,144.7,140.5,130.7,126.8,126.6,126.6,123.0,121.5,117.1,115.5,112.5,17.9;hr-esi-ms for c
13h12
n4([m+h]
+
)calcd:225.1135;found:225.1131。
[0165]
实施例21:n-(3-溴苯基)-[1,2,4]三唑并[4,3-a]吡啶-3-胺(2d)的合成
[0166]
[0167]
取40ml反应管,加入2-肼基吡啶(54.6mg,0.50mmol)、3-溴苯基异硫氰酸酯(128.4mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经抽滤固液分离,滤饼水洗干燥得产品(102.0mg,0.35mmol)。母液减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(19.4mg,0.07mmol),合并产品(121.4mg,0.42mmol),收率为84%((102.0+19.4)/(289.14
×
0.5)=84%)。
[0168]
2-肼基吡啶cas号:4930-98-7,3-溴苯基异硫氰酸酯cas:2131-59-1。
[0169]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.51(s,1h),8.36(d,j=6.9hz,1h),7.96(s,1h),7.63(d,j=9.3hz,1h),7.49(d,j=7.9hz,1h),7.30
–
7.22(m,2h),7.09(d,j=7.7hz,1h),6.92(t,j=6.6hz,1h);
13
c nmr(125mhz,dmso-d6)δ146.3,143.8,142.9,131.0,126.8,123.0,122.7,122.0,118.4,115.6,115.2,112.5;hr-esi-ms for c
12
h9brn4([m+h]
+
)calcd:289.0083;found:289.0079。
[0170]
实施例22:n-(3-硝基苯基)-[1,2,4]三唑并[4,3-a]吡啶-3-胺(2e)的合成
[0171][0172]
取40ml反应管,加入2-肼基吡啶(54.6mg,0.50mmol)、3-硝基苯基异硫氰酸酯(108.1mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经抽滤固液分离,滤饼水洗干燥得产品(99.9mg,0.39mmol)。母液减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(11.1mg,0.05mmol),合并产品(111.0mg,0.44mmol),收率为87%((99.9+11.1)/(255.24
×
0.5)=87%)。
[0173]
2-肼基吡啶cas号:4930-98-7,3-硝基苯基异硫氰酸酯cas:3529-82-6。
[0174]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.90(s,1h),8.65(t,j=2.0hz,1h),8.40(d,j=7.0hz,1h),7.98(dd,j=8.0,1.6hz,1h),7.77(dd,j=8.0,1.6hz,1h),7.66(d,j=9.4hz,1h),7.61(t,j=8.0hz,1h),7.28(dd,j=9.0,6.5hz,1h),6.96(t,j=6.7hz,1h);
13
c nmr(125mhz,dmso-d6)δ148.4,146.4,143.7,142.4,130.4,127.0,122.7,122.5,115.6,115.0,112.7,110.2;hr-esi-ms for c
12
h9n5o2([m+h]
+
)calcd:256.0829;found:256.0823。
[0175]
实施例23:n-(4-氟苯基)-[1,2,4]三唑并[4,3-a]吡啶-3-胺(2f)的合成
[0176][0177]
取40ml反应管,加入2-肼基吡啶(54.6mg,0.50mmol)、4-氟苯基异硫氰酸酯(91.9mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经抽滤固液分离,滤饼水洗干燥得产品(60.0mg,0.27mmol)。母液减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(32.4mg,0.14mmol),合并产品
(92.4mg,0.41mmol),收率为81%((60.0+32.4)/(228.23
×
0.5)=81%)。
[0178]
2-肼基吡啶cas号:4930-98-7,4-氟苯基异硫氰酸酯cas:1544-68-9。
[0179]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.29(s,1h),8.34(d,j=7.1hz,1h),7.65
–
7.58(m,3h),7.25
–
7.21(m,1h),7.19
–
7.14(m,2h),6.92
–
6.88(m,1h);
13
c nmr(125mhz,dmso-d6)δ156.6(c-f,1j
c-f
=236.5hz),146.2,144.6,137.8(c-f,4j
c-f
=1.6hz),126.6,122.6,117.8(c-f,3j
c-f
=7.6hz),115.6,115.5(c-f,2j
c-f
=15.5hz),112.3;hr-esi-ms for c
12
h9fn4([m+h]
+
)calcd:229.0884;found:229.0879。
[0180]
实施例24:n-(4-氯苯基)-[1,2,4]三唑并[4,3-a]吡啶-3-胺(2g)的合成
[0181][0182]
取40ml反应管,加入2-肼基吡啶(54.6mg,0.50mmol)、4-氯苯基异硫氰酸酯(101.8mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经抽滤固液分离,滤饼水洗干燥得产品(83.3mg,0.34mmol)。母液减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(19.5mg,0.08mmol),合并产品(102.8mg,0.42mmol),收率为84%((83.3+19.5)/(244.68
×
0.5)=84%)。
[0183]
2-肼基吡啶cas号:4930-98-7,4-氯苯基异硫氰酸酯cas:2131-55-7。
[0184]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.44(s,1h),8.35(d,j=7.0hz,1h),7.65
–
7.59(m,3h),7.36(d,j=8.8hz,2h),7.25(dd,j=9.2,6.5hz,1h),6.91(t,j=6.7hz,1h);
13
c nmr(125mhz,dmso-d6)δ146.3,144.1,140.3,128.8,126.7,123.9,122.7,117.8,115.6,112.4;hr-esi-ms for c
12
h9cln4([m+h]
+
)calcd:245.0589;found:245.0583。
[0185]
实施例25:n-(4-溴苯基)-[1,2,4]三唑并[4,3-a]吡啶-3-胺(2h)的合成
[0186][0187]
取40ml反应管,加入2-肼基吡啶(54.6mg,0.50mmol)、4-溴苯基异硫氰酸酯(128.4mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经抽滤固液分离,滤饼水洗干燥得产品(90.2mg,0.31mmol)。母液减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(25.5mg,0.09mmol),合并产品(115.7mg,0.40mmol),收率为80%((90.2+25.5)/(289.14
×
0.5)=80%)。
[0188]
2-肼基吡啶cas号:4930-98-7,4-溴苯基异硫氰酸酯cas:1985-12-2。
[0189]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.45(s,1h),8.35(d,j=7.0hz,1h),7.62(d,j=9.4hz,1h),7.60
–
7.52(m,2h),7.53
–
7.39(m,2h),7.25(dd,j=9.1,6.5hz,1h),6.91(t,j=6.7hz,1h);
13
c nmr(125mhz,dmso-d6)δ146.3,144.0,140.7,131.7,126.7,122.7,118.3,115.6,112.5,111.6;hr-esi-ms for c
12
h9brn4([m+h]
+
)calcd:289.0083;found:289.0081。
[0190]
实施例26:n-(4-硝基苯基)-[1,2,4]三唑并[4,3-a]吡啶-3-胺(2i)的合成
[0191][0192]
取40ml反应管,加入2-肼基吡啶(54.6mg,0.50mmol)、4-硝基苯基异硫氰酸酯(90.1mg,0.50mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经抽滤固液分离,滤饼水洗干燥得产品(95.3mg,0.38mmol)。母液减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(10.6mg,0.04mmol),合并产品(105.9mg,0.42mmol),收率为83%((95.3+10.6)/(255.24
×
0.5)=83%)。
[0193]
2-肼基吡啶cas号:4930-98-7,4-硝基苯基异硫氰酸酯cas:2131-61-5。
[0194]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ10.20(s,1h),8.40(d,j=7.1hz,1h),8.24(d,j=9.3hz,2h),7.76
–
7.68(m,3h),7.34
–
7.30(m,1h),7.00
–
6.96(m,1h);
13
c nmr(125mhz,dmso-d6)δ147.8,146.9,142.9,139.9,127.3,125.7,122.9,115.6,113.0;hr-esi-ms for c
12
h9n5o2([m+h]
+
)calcd:256.0829;found:256.0824。
[0195]
实施例27:n-(4-氰基苯基)-[1,2,4]三唑并[4,3-a]吡啶-3-胺(2j)的合成
[0196][0197]
取40ml反应管,加入2-肼基吡啶(54.6mg,0.50mmol)、4-氰基苯基异硫氰酸酯(96.1mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经抽滤固液分离,滤饼水洗干燥得产品(79.9mg,0.34mmol)。母液减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(13.0mg,0.06mmol),合并产品(92.9mg,0.40mmol),收率为79%((79.9+13.0)/(235.25
×
0.5)=79%)。
[0198]
2-肼基吡啶cas号:4930-98-7,4-硝基苯基异硫氰酸酯cas:2719-32-6。
[0199]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.88(s,1h),8.36(d,j=7.1hz,1h),7.78
–
7.72(m,2h),7.71
–
7.62(m,3h),7.33
–
7.26(m,1h),6.98
–
6.92(m,1h);
13
c nmr(125mhz,dmso-d6)δ146.7,145.6,143.1,133.6,127.1,122.7,119.6,116.2,115.6,112.8,101.6;hr-esi-ms for c
13
h9n5([m+h]
+
)calcd:236.0931;found:236.0926。
[0200]
实施例28:n-(对甲苯基)-[1,2,4]三唑并[4,3-a]吡啶-3-胺(2k)的合成
[0201][0202]
取40ml反应管,加入2-肼基吡啶(54.6mg,0.50mmol)、4-甲基苯基异硫氰酸酯(89.5mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。
反应结束后经抽滤固液分离,滤饼水洗干燥得产品(72.6mg,0.32mmol)。母液减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(14.9mg,0.07mmol),合并产品(87.5mg,0.39mmol),收率为78%((72.6+14.9)/(224.27
×
0.5)=78%)。
[0203]
2-肼基吡啶cas号:4930-98-7,4-甲基苯基异硫氰酸酯cas:2719-32-6。
[0204]
产品的表征数据为:1h nmr(500mhz,dmso-)δ9.11(s,1h),8.32(d,j=7.1hz,1h),7.59(d,j=9.3hz,1h),7.47(d,j=8.3hz,2h),7.22(dd,j=9.3,6.4hz,1h),7.12(d,j=8.3hz,2h),6.88(t,j=6.8hz,1h),2.25(s,3h);
13
c nmr(125mhz,dmso-d6)δ146.1,d6144.6,138.9,129.4,129.2,126.4,122.6,116.4,115.5,112.2,20.3;hr-esi-ms for c
13h12
n4([m+h]
+
)calcd:225.1135;found:225.1130。
[0205]
实施例29:n-(4-三氟甲基苯基)-[1,2,4]三唑并[4,3-a]吡啶-3-胺(2l)的合成
[0206][0207]
取40ml反应管,加入2-肼基吡啶(54.6mg,0.50mmol)、4-三氟甲基苯基异硫氰酸酯(121.9mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(98.8mg,0.36mmol),收率为71%(98.8/(278.24
×
0.5)=71%)。
[0208]
2-肼基吡啶cas号:4930-98-7,4-三氟甲基苯基异硫氰酸酯cas:1645-65-4。
[0209]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.75(s,1h),8.37(d,j=7.0hz,1h),7.76
–
7.69(m,2h),7.70
–
7.60(m,3h),7.33
–
7.24(m,1h),6.98
–
6.91(m,1h);
13
c nmr(125mhz,dmso-d6)δ146.6,145.0,143.5,126.9,126.4(c-f,3j
c-f
=3.8hz),124.8(c-f,1j
c-f
=269.5hz),122.7,120.3(c-f,2j
c-f
=32.0hz),115.9,115.6,112.7;hr-esi-ms for c
13
h9f3n4([m+h]
+
)calcd:279.0852;found:279.0847。
[0210]
实施例30:n-(4-三氟甲氧基苯基)-[1,2,4]三唑并[4,3-a]吡啶-3-胺(2m)的合成
[0211][0212]
取40ml反应管,加入2-肼基吡啶(54.6mg,0.50mmol)、4-三氟甲氧基苯基异硫氰酸酯(131.5mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经抽滤固液分离,滤饼水洗干燥得产品(125.8mg,0.43mmol)。母液减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(14.0mg,0.05mmol),合并产品(139.8mg,0.48mmol),收率为95%((125.8+14.0)/(294.24
×
0.5)=95%)。
[0213]
2-肼基吡啶cas号:4930-98-7,4-三氟甲氧基苯基异硫氰酸酯cas:1645-65-4。
[0214]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.50(s,1h),8.36(d,j=7.1hz,1h),7.72
–
7.65(m,2h),7.63(d,j=9.3hz,1h),7.32(d,j=8.8hz,2h),7.25(dd,j=9.3,6.4hz,1h),6.92(t,j=6.7hz,1h);
13
c nmr(125mhz,dmso-d6)δ146.3,144.1,141.6,140.7,
126.7,122.7,122.1,120.3(c-f,1j
c-f
=253.5hz),117.3,115.6,112.5;hr-esi-ms for c
13
h9f3n4o([m+h]
+
)calcd:295.0801;found:295.0797。
[0215]
实施例31:n-(3,4,5-三甲氧基苯基)-[1,2,4]三唑并[4,3-a]吡啶-3-胺(2n)的合成
[0216][0217]
取40ml反应管,加入2-肼基吡啶(54.6mg,0.50mmol)、3,4,5-三甲氧基苯基异硫氰酸酯(135.2mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经抽滤固液分离,滤饼水洗干燥得产品(71.4mg,0.24mmol)。母液减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=30:1)得到产品(27.7mg,0.09mmol),合并产品(99.1mg,0.33mmol),收率为66%((71.4+27.7)/(300.32
×
0.5)=66%)。
[0218]
2-肼基吡啶cas号:4930-98-7,3,4,5-三甲氧基苯基异硫氰酸酯cas:35967-24-9。
[0219]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.19(s,1h),8.34(d,j=7.1hz,1h),7.60(d,j=9.4hz,1h),7.25
–
7.21(m,1h),6.99(s,2h),6.92
–
6.88(m,1h),3.77(s,6h),3.61(s,3h);
13
c nmr(125mhz,dmso-d6)δ153.1,146.0,144.5,137.5,131.5,126.5,122.5,115.5,112.3,94.2,60.2,55.7;hr-esi-ms for c
15h16
n4o3([m+h]
+
)calcd:301.1295;found:301.1290。
[0220]
实施例32:n-(3-(苄氧基)苯基)-[1,2,4]三唑并[4,3-a]吡啶-3-胺(2o)的合成
[0221][0222]
取40ml反应管,加入2-肼基吡啶(54.6mg,0.50mmol)、3-苯甲氧基苯基异硫氰酸酯(144.8mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经抽滤固液分离,滤饼水洗干燥得产品(119.2mg,0.38mmol)。母液减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(27.9mg,0.09mmol),合并产品(147.1mg,0.47mmol),收率为93%((119.2+27.9)/(316.36
×
0.5)=93%)。
[0223]
2-肼基吡啶cas号:4930-98-7,3-苯甲氧基苯基异硫氰酸酯cas:35967-24-9。
[0224]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.24(s,1h),8.33(d,j=7.1hz,1h),7.62(d,j=9.4hz,1h),7.49
–
7.43(m,2h),7.39(t,j=7.5hz,2h),7.35
–
7.30(m,2h),7.27
–
7.23(m,1h),7.21(t,j=8.1hz,1h),7.07(dd,j=8.1,1.9hz,1h),6.94
–
6.86(m,1h),6.59(dd,j=8.1,2.3hz,1h),5.09(s,2h);
13
c nmr(125mhz,dmso-d6)δ159.1,146.3,144.2,142.7,137.2,129.8,128.4,127.8,127.7,126.6,122.6,115.5,112.4,109.1,106.6,103.1,69.1;hr-esi-ms for c
19h16
n4o([m+h]
+
)calcd:317.1397;found:317.1394。
[0225]
实施例33:n-(1-萘基)-[1,2,4]三唑并[4,3-a]吡啶-3-胺(2p)的合成
[0226][0227]
取40ml反应管,加入2-肼基吡啶(54.6mg,0.50mmol)、1-萘基异硫氰酸酯(111.1mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经抽滤固液分离,滤饼水洗干燥得产品(40.1mg,0.16mmol)。母液减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(60.1mg,0.23mmol),合并产品(100.2mg,0.39mmol),收率为77%((40.1+60.1)/(260.30
×
0.5)=77%)。
[0228]
2-肼基吡啶cas号:4930-98-7,1-萘基异硫氰酸酯cas:551-06-4。
[0229]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.15(s,1h),8.39
–
8.31(m,1h),8.17(d,j=6.1hz,1h),7.96
–
7.89(m,1h),7.71(d,j=8.9hz,1h),7.61
–
7.50(m,3h),7.36(t,j=7.4hz,1h),7.32(t,j=7.4hz,1h),7.11(d,j=6.9hz,1h),6.90(t,j=6.0hz,1h);
13
c nmr(125mhz,dmso-d6)δ147.6,144.7,138.0,134.2,128.3,127.1,126.2,126.2,125.4,125.0,123.1,122.4,121.4,115.7,112.8,112.0;hr-esi-ms for c
16h12
n4([m+h]
+
)calcd:261.1135;found:261.1129。
[0230]
实施例34:n-(2,6-二甲基苯基)-[1,2,4]三唑并[4,3-a]吡啶-3-胺(2q)的合成
[0231][0232]
取40ml反应管,加入2-肼基吡啶(54.6mg,0.50mmol)、2,6-二甲基苯基异硫氰酸酯(122.4mg,0.75mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(54.8mg,0.23mmol),收率为46%(54.8/(238.29
×
0.5)=46%)。
[0233]
2-肼基吡啶cas号:4930-98-7,2,6-二甲基苯基异硫氰酸酯cas:19241-16-8。
[0234]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ8.26(d,j=7.0hz,1h),8.12(s,1h),7.52(d,j=9.4hz,1h),7.17(dd,j=9.2,6.5hz,1h),7.13
–
7.08(m,2h),7.08
–
7.03(m,1h),6.85(t,j=6.7hz,1h),2.10(s,6h);
13
c nmr(125mhz,dmso-d6)δ146.4,146.3,137.4,134.0,128.3,125.8,125.3,122.5,115.5,111.9,18.0;hr-esi-ms for c
14h14
n4([m+h]
+
)calcd:239.1291;found:239.1288。
[0235]
实施例35:n-(3,5-双(三氟甲基)苯基)-[1,2,4]三唑并[4,3-a]吡啶-3-胺(2r)的合成
[0236][0237]
取40ml反应管,加入2-肼基吡啶(54.6mg,0.50mmol)、3,5-双三氟甲基苯基异硫氰酸酯(162.7mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经抽滤固液分离,滤饼水洗干燥得产品(73.7mg,0.22mmol)。母液减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(49.2mg,0.14mmol),合并产品(122.9mg,0.36mmol),收率为71%((73.7+49.2)/(346.24
×
0.5)=71%)。
[0238]
2-肼基吡啶cas号:4930-98-7,3,5-双三氟甲基苯基异硫氰酸酯cas:23165-29-9。
[0239]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ10.12(s,1h),8.38(d,j=7.0hz,1h),8.31(s,2h),7.67(d,j=9.4hz,1h),7.58(s,1h),7.30(dd,j=9.3,6.5hz,1h),6.98(t,j=6.7hz,1h);
13
c nmr(125mhz,dmso-d6)δ146.4,143.4,142.9,131.0(c-f,2j
c-f
=32.6hz),127.1,123.5(c-f,1j
c-f
=272.8hz),122.5,115.9(c-f,3j
c-f
=3.2hz),115.6,112.9,112.8;hr-esi-ms for c
14
h8f6n4([m+h]
+
)calcd:347.0726;found:347.0721。
[0240]
实施例36:n-(4-叔丁基苯基)-[1,2,4]三唑并[4,3-a]吡啶-3-胺(2s)的合成
[0241][0242]
取40ml反应管,加入2-肼基吡啶(54.6mg,0.50mmol)、4-叔丁基苯基异硫氰酸酯(114.8mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经抽滤固液分离,滤饼水洗干燥得产品(54.3mg,0.21mmol)。母液减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(48.2mg,0.18mmol),合并产品(102.5mg,0.39mmol),收率为77%((54.3+48.2)/(266.35
×
0.5)=77%)。
[0243]
2-肼基吡啶cas号:4930-98-7,4-叔丁基苯基异硫氰酸酯cas:19241-24-8。
[0244]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.12(s,1h),8.33(d,j=7.1hz,1h),7.60(d,j=9.4hz,1h),7.50
–
7.46(m,2h),7.34
–
7.31(m,2h),7.24
–
7.20(m,1h),6.91
–
6.86(m,1h),1.27(s,9h);
13
c nmr(125mhz,dmso-d6)δ146.2,144.6,142.8,138.9,126.4,125.6,122.6,116.1,115.5,112.2,33.8,31.3;hr-esi-ms for c
16h18
n4([m+h]
+
)calcd:267.1604;found:267.1600。
[0245]
实施例37:n-(2,4-二氟苯基)-[1,2,4]三唑并[4,3-a]吡啶-3-胺(2t)的合成
[0246]
[0247]
取40ml反应管,加入2-肼基吡啶(54.6mg,0.50mmol)、2,4-二氟苯基异硫氰酸酯(102.7mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经抽滤固液分离,滤饼水洗干燥得产品(27.1mg,0.11mmol)。母液减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(66.5mg,0.27mmol),合并产品(93.6mg,0.38mmol),收率为76%((27.1+66.5)/(246.22
×
0.5)=76%)。
[0248]
2-肼基吡啶cas号:4930-98-7,2,4-二氟苯基异硫氰酸酯cas:141106-52-7。
[0249]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ8.89(s,1h),8.30(d,j=7.0hz,1h),7.73
–
7.66(m,1h),7.63(d,j=9.4hz,1h),7.37
–
7.29(m,1h),7.29
–
7.25(m,1h),7.06
–
7.01(m,1h),6.90(t,j=6.7hz,1h);
13
c nmr(125mhz,dmso-d6)δ156.3(dd,1j
c-f
=240.1,3j
c-f
=11.1hz),152.0(dd,1j
c-f
=246.0,3j
c-f
=12.3hz),147.0,144.2,126.8,126.4(dd,3j
c-f
=11.3,4j
c-f
=3.3hz),123.0,120.1(dd,3j
c-f
=9.1,4j
c-f
=3.4hz),115.4,112.4,111.2(dd,2j
c-f
=21.9,4j
c-f
=3.5hz),104.2(dd,2j
c-f
=26.8,2j
c-f
=23.1hz);hr-esi-ms for c
12
h8f2n4([m+h]
+
)calcd:247.0790;found:247.0786。
[0250]
实施例38:n-异丙基-[1,2,4]三唑并[4,3-a]吡啶-3-胺(3a)的合成
[0251][0252]
取40ml反应管,加入2-肼基吡啶(54.6mg,0.50mmol)、异丙基异硫氰酸酯(60.7mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和5ma恒流反应5h。反应结束后经减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=30:1)得到产品(37.0mg,0.21mmol),收率为42%(37.0/(176.22
×
0.5)=42%)。
[0253]
2-肼基吡啶cas号:4930-98-7,2,4-二氟苯基异硫氰酸酯cas:2253-73-8。
[0254]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ8.09(d,j=7.0hz,1h),7.42(d,j=9.4hz,1h),7.09
–
7.02(m,1h),6.71(t,j=6.6hz,1h),6.40(d,j=6.8hz,1h),3.98
–
3.90(m,1h),1.26(d,j=6.4hz,6h);
13
c nmr(125mhz,dmso-d6)δ148.1,145.8,125.3,122.3,115.4,111.2,44.7,22.7;hr-esi-ms for c9h
12
n4([m+h]
+
)calcd:177.1135;found:177.1133。
[0255]
实施例39:乙基[1,2,4]三唑并[4,3-a]吡啶-3-氨基甲酸酯(3b)的合成
[0256][0257]
取40ml反应管,加入2-肼基吡啶(54.6mg,0.50mmol)、甲酸乙酯基异硫氰酸酯(78.7mg,0.60mmol)、四丁基碘化铵(36.9mg,0.1mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和5ma恒流反应5h。反应结束后经减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=30:1)得到产品(20.6mg,
0.10mmol),收率为20%(20.6/(206.21
×
0.5)=20%)。
[0258]
2-肼基吡啶cas号:4930-98-7,甲酸乙酯基异硫氰酸酯cas:16182-04-0。
[0259]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ10.34(s,1h),8.17(d,j=6.8hz,1h),7.73(d,j=9.3hz,1h),7.42
–
7.35(m,2h),6.99(t,j=6.7hz,1h),4.17(q,j=7.0hz,2h),1.27
–
1.20(m,3h);
13
c nmr(125mhz,dmso-d6)δ154.0,148.7,139.8,127.8,123.6,115.5,113.6,61.6,14.4;hr-esi-ms for c9h
10
n4o2([m+h]
+
)calcd:207.0877;found:207.0875。
[0260]
实施例40:n-(3-吡啶基)-[1,2,4]三唑并[4,3-a]吡啶-3-胺(3c)的合成
[0261][0262]
取40ml反应管,加入2-肼基吡啶(54.6mg,0.50mmol)、3-吡啶基异硫氰酸酯(81.7mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(69.1mg,0.50mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经抽滤固液分离,滤饼水洗干燥得产品(58.9mg,0.28mmol)。母液减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=30:1)得到产品(27.7mg,0.13mmol),合并产品(86.6mg,0.41mmol),收率为82%((58.9+27.7)/(211.23
×
0.5)=82%)。
[0263]
2-肼基吡啶cas号:4930-98-7,3-吡啶基异硫氰酸酯cas:17452-27-6。
[0264]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.52(s,1h),8.78(d,j=2.5hz,1h),8.37(d,j=7.0hz,1h),8.18
–
8.12(m,1h),8.12
–
8.07(m,1h),7.63(d,j=9.4hz,1h),7.34(dd,j=8.3,4.6hz,1h),7.26(dd,j=9.0,6.5hz,1h),6.93(t,j=6.7hz,1h);
13
c nmr(125mhz,dmso-d6)δ146.4,143.9,141.5,138.5,138.0,126.7,123.7,122.7,122.6,115.6,112.5;hr-esi-ms for c
11
h9n5([m+h]
+
)calcd:212.0931;found:212.0929。
[0265]
实施例41:n-苯基-[1,2,4]三唑并[4,3-a]嘧啶-3-胺(3d)的合成
[0266][0267]
取40ml反应管,加入2-肼基嘧啶(55.1mg,0.50mmol)、异硫氰酸苯酯(81.1mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经抽滤固液分离,滤饼水洗干燥得产品(59.2mg,0.28mmol)。母液减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=30:1)得到产品(25.3mg,0.12mmol),合并产品(84.5mg,0.40mmol),收率为80%((59.2+25.3)/(211.23
×
0.5)=80%)。
[0268]
2-肼基嘧啶cas号:7504-94-1,异硫氰酸苯酯cas:103-72-0。
[0269]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.39(s,1h),8.78(dd,j=7.0,1.8hz,1h),8.58(dd,j=3.8,1.8hz,1h),7.61(d,j=7.8hz,2h),7.32(t,j=7.8hz,2h),7.01(dd,j=7.0,3.8hz,1h),6.94(t,j=7.3hz,1h);
13
c nmr(125mhz,dmso-d6)δ154.1,149.9,143.3,140.9,131.5,129.1,120.8,116.4,108.4;hr-esi-ms for c
11
h9n5([m+h]
+
)
calcd:212.0931;found:212.0927。
[0270]
实施例42:5,7-二甲基-n-苯基-[1,2,4]三唑并[4,3-a]嘧啶-3-胺(3e)的合成
[0271][0272]
取40ml反应管,加入4,6-二甲基-2-肼基嘧啶(69.1mg,0.50mmol)、异硫氰酸苯酯(81.1mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=30:1)得到产品(93.3mg,0.39mmol),收率为78%(93.3/(239.28
×
0.5)=78%)。
[0273]
4,6-二甲基-2-肼基嘧啶cas号:23906-13-0,异硫氰酸苯酯cas:103-72-0。
[0274]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ8.47(s,1h),7.22
–
7.16(m,2h),6.80(t,j=7.3hz,1h),6.78
–
6.72(m,3h),2.64(s,3h),2.48(s,3h);
13
c nmr(125mhz,dmso-d6)δ164.3,153.1,145.5,144.0,142.4,129.3,119.6,114.6,111.2,24.5,17.1;hr-esi-ms for c
13h13
n5([m+h]
+
)calcd:240.1244;found:240.1239。
[0275]
实施例43:7-氯-n-苯基-[1,2,4]三唑并[4,3-c]嘧啶-3-胺(3f)的合成
[0276][0277]
取40ml反应管,加入6-氯-4-肼基嘧啶(72.3mg,0.50mmol)、异硫氰酸苯酯(81.1mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经抽滤固液分离,滤饼水洗干燥得产品(32.7mg,0.13mmol)。母液减压蒸馏除去溶剂,再经柱层析(石油醚:乙酸乙酯=10:1)得到产品(53.3mg,0.22mmol),合并产品(86.0mg,0.35mmol),收率为70%((32.7+53.3)/(245.67
×
0.5)=70%)。
[0278]
6-氯-4-肼基嘧啶cas号:5767-35-1,异硫氰酸苯酯cas:103-72-0。
[0279]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.69(s,1h),9.27(d,j=1.3hz,1h),7.82(d,j=1.3hz,1h),7.72(d,j=7.3hz,2h),7.38
–
7.35(m,2h),6.98(t,j=7.3hz,1h);
13
c nmr(125mhz,dmso-d6)δ144.9,143.9,142.0,140.1,138.9,129.1,121.3,116.9,108.3;hr-esi-ms for c
11
h8cln5([m+h]
+
)calcd:246.0541;found:246.0541。
[0280]
实施例44:8-氟-5-甲氧基-n-苯基-[1,2,4]三唑并[4,3-c]嘧啶-3-胺(3g)的合成
[0281][0282]
取40ml反应管,加入2-甲氧基-5-氟-4-肼基嘧啶(79.1mg,0.50mmol)、异硫氰酸苯酯(81.1mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙
腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经减压蒸馏除去溶剂,再经柱层析(石油醚:乙酸乙酯=6:1)得到产品(77.8mg,0.30mmol),收率为60%(77.8/(259.24
×
0.5)=60%)。
[0283]
2-甲氧基-5-氟-4-肼基嘧啶cas号:166524-64-7,异硫氰酸苯酯cas:103-72-0。
[0284]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ8.56(s,1h),7.76(d,j=7.9hz,2h),7.54(d,j=3.1hz,1h),7.34(t,j=7.9hz,2h),7.00(t,j=7.3hz,1h),4.13(s,3h);
13
c nmr(125mhz,dmso-d6)δ145.6,145.2,143.2,141.1(d,j=32.0hz),140.3,129.2,122.9(d,j=23.0hz),122.2,118.5,57.1;hr-esi-ms for c
12h10
fn5o([m+h]
+
)calcd:260.0942;found:260.0939。
[0285]
实施例45:n-苯基-[1,2,4]三唑并[4,3-a]吡嗪-3-胺(3h)的合成
[0286][0287]
取40ml反应管,加入2-肼基吡嗪(55.1mg,0.50mmol)、异硫氰酸苯酯(81.1mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经抽滤固液分离,滤饼水洗干燥得产品(45.9mg,0.22mmol)。母液减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(20.6mg,0.10mmol),合并产品(66.5mg,0.32mmol),收率为63%((45.9+20.6)/(211.23
×
0.5)=63%)。
[0288]
2-肼基吡嗪cas号:54608-52-5,异硫氰酸苯酯cas:103-72-0。
[0289]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.55(s,1h),9.21(d,j=1.6hz,1h),8.39(dd,j=4.9,1.6hz,1h),7.80(d,j=4.9hz,1h),7.68(d,j=7.8hz,2h),7.35(t,j=7.8hz,2h),6.97(t,j=7.3hz,1h);
13
c nmr(125mhz,dmso-d6)δ145.3,144.2,142.0,140.5,129.1,127.6,121.1,116.7,115.5;hr-esi-ms for c
11
h9n5([m+h]
+
)calcd:212.0931;found:212.0929。
[0290]
实施例46:8-氯-n-苯基-[1,2,4]三唑并[4,3-a]吡嗪-3-胺(3i)的合成
[0291][0292]
取40ml反应管,加入3-氯-2-肼基吡嗪(72.3mg,0.50mmol)、异硫氰酸苯酯(81.1mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经减压蒸馏除去溶剂,再经柱层析(石油醚:乙酸乙酯=4:1)得到产品(88.4mg,0.36mmol),收率为72%(88.4/(245.67
×
0.5)=72%)。
[0293]
3-氯-2-肼基吡嗪cas号:63286-28-2,异硫氰酸苯酯cas:103-72-0。
[0294]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.66(s,1h),8.44(d,j=4.8hz,1h),7.69(d,j=7.9hz,2h),7.65(d,j=4.8hz,1h),7.36(t,j=7.9hz,2h),6.99(t,j=
7.3hz,1h);
13
c nmr(125mhz,dmso-d6)δ146.9,141.8,140.1,139.7,129.1,126.2,121.4,116.9,116.2;hr-esi-ms for c
11
h8cln5([m+h]
+
)calcd:246.0541;found:246.0539。
[0295]
实施例47:6-甲基-n-苯基-[1,2,4]三唑并[4,3-b]哒嗪-3-胺(3j)的合成
[0296][0297]
取40ml反应管,加入6-甲基-3-肼基哒嗪(62.1mg,0.50mmol)、异硫氰酸苯酯(81.1mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(61.9mg,0.28mmol),收率为55%(61.9/(225.26
×
0.5)=55%)。
[0298]
6-甲基-3-肼基哒嗪cas号:175135-44-1,异硫氰酸苯酯cas:103-72-0。
[0299]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.44(s,1h),8.07(d,j=9.5hz,1h),7.85(d,j=7.8hz,2h),7.30(t,j=7.8hz,2h),7.10(d,j=9.5hz,1h),6.92(t,j=7.2hz,1h),2.55(s,3h);
13
c nmr(125mhz,dmso-d6)δ153.9,146.2,140.7,140.1,128.8,124.2,121.8,120.7,116.9,21.2;hr-esi-ms for c
12h11
n5([m+h]
+
)calcd:226.1087;found:226.1083。
[0300]
实施例48:6-氯-n-苯基-[1,2,4]三唑并[4,3-b]哒嗪-3-胺(3k)的合成
[0301][0302]
取40ml反应管,加入6-氯-3-肼基哒嗪(72.3mg,0.50mmol)、异硫氰酸苯酯(81.1mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经抽滤固液分离,滤饼水洗干燥得产品(32.2mg,0.13mmol)。母液减压蒸馏除去溶剂,再经柱层析(石油醚:乙酸乙酯=4:1)得到产品(62.4mg,0.26mmol),合并产品(94.6mg,0.39mmol),收率为77%((32.2+62.4)/(245.67
×
0.5)=77%)。
[0303]
6-氯-3-肼基哒嗪cas号:17284-97-8,异硫氰酸苯酯cas:103-72-0。
[0304]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.69(s,1h),8.28(d,j=9.7hz,1h),7.85(d,j=7.8hz,2h),7.34
–
7.28(m,3h),6.95(t,j=7.3hz,1h);
13
c nmr(125mhz,dmso-d6)δ147.8,146.4,140.3,139.7,128.8,127.1,121.3,121.0,117.2;hr-esi-ms for c
11
h8cln5([m+h]
+
)calcd:246.0541;found:246.0540。
[0305]
实施例49:6-溴-n-(对甲苯基)-[1,2,4]三唑并[4,3-a]吡啶-3-胺(3l)的合成
[0306][0307]
取40ml反应管,加入5-溴-2-肼基吡啶(94.0mg,0.50mmol)、4-甲基苯基异硫氰酸
酯(89.5mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经抽滤固液分离,滤饼水洗干燥得产品(75.8mg,0.25mmol)。母液减压蒸馏除去溶剂,再经柱层析(石油醚:乙酸乙酯=4:1)得到产品(48.5mg,0.16mmol),合并产品(124.3mg,0.41mmol),收率为82%((75.8+48.5)/(303.16
×
0.5)=82%)。
[0308]
5-溴-2-肼基吡啶cas号:77992-44-0,4-甲基苯基异硫氰酸酯cas:622-59-3。
[0309]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.16(s,1h),8.74(s,1h),7.60
–
7.53(m,3h),7.28(d,j=9.6hz,1h),7.13(d,j=7.8hz,2h),2.25(s,3h);
13
c nmr(125mhz,dmso-d6)δ145.1,144.3,138.9,129.3,129.0,129.0,122.9,116.8,116.6,105.8,20.4;hr-esi-ms for c
13h11
brn4([m+h]
+
)calcd:303.0240;found:303.0238。
[0310]
实施例50:6-溴-n-(3,4,5-三甲氧基苯基)-[1,2,4]三唑并[4,3-a]吡啶-3-胺(3m)的合成
[0311][0312]
取40ml反应管,加入5-溴-2-肼基吡啶(94.0mg,0.50mmol)、3,4,5-三甲氧基苯基异硫氰酸酯(135.2mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(144.1mg,0.38mmol),收率为76%(144.1/(379.21
×
0.5)=76%)。
[0313]
5-溴-2-肼基吡啶cas号:77992-44-0,3,4,5-三甲氧基苯基异硫氰酸酯cas:35967-24-9。
[0314]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.36(s,1h),8.84(s,1h),7.62(d,j=9.7hz,1h),7.36(dd,j=9.7,1.2hz,1h),7.07(s,2h),3.79(s,6h),3.62(s,3h);
13
c nmr(125mhz,dmso-d6)δ153.1,144.5,144.1,136.7,131.8,130.0,122.9,116.3,106.4,94.5,60.2,55.7;hr-esi-ms for c
15h15
brn4o3([m+h]
+
)calcd:379.0400;found:379.0398。
[0315]
实施例51:5-溴-n-(3,4,5-三甲氧基苯基)-[1,2,4]三唑并[4,3-a]吡啶-3-胺(3n)的合成
[0316][0317]
取40ml反应管,加入6-溴-2-肼基吡啶(94.00mg,0.50mmol)、3,4,5-三甲氧基苯基异硫氰酸酯(135.2mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经抽滤固液分离,滤饼水洗干燥得产品(91.2mg,0.24mmol)。
母液减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(49.1mg,0.13mmol),合并产品(140.3mg,0.37mmol),收率为74%((91.2+49.1)/(379.21
×
0.5)=74%)。
[0318]
6-溴-2-肼基吡啶cas号:26944-71-8,3,4,5-三甲氧基苯基异硫氰酸酯cas:35967-24-9。
[0319]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ8.33(s,1h),7.73(d,j=8.4hz,1h),7.24
–
7.18(m,2h),6.14(s,2h),3.66(s,6h),3.58(s,3h);
13
c nmr(125mhz,dmso-d6)δ153.4,149.8,144.0,141.2,131.0,128.3,119.5,115.5,111.7,92.8,60.2,55.7;hr-esi-ms for c
15h15
brn4o3([m+h]
+
)calcd:379.0400;found:379.0396。
[0320]
实施例52:6-溴-8-氟-n-(3,4,5-三甲氧基苯基)-[1,2,4]三唑并[4,3-a]吡啶-3-胺(3o)的合成
[0321][0322]
取40ml反应管,加入3-氟-5-溴-2-肼基吡啶(103.0mg,0.50mmol)、3,4,5-三甲氧基苯基异硫氰酸酯(135.2mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经抽滤固液分离,滤饼水洗干燥得产品(78.4mg,0.20mmol)。母液减压蒸馏除去溶剂,再经柱层析(石油醚:乙酸乙酯=4:1)得到产品(88.4mg,0.22mmol),合并产品(166.8mg,0.42mmol),收率为84%((78.4+88.4)/(397.20
×
0.5)=84%)。
[0323]
3-氟-5-溴-2-肼基吡啶cas号:26944-71-8,3,4,5-三甲氧基苯基异硫氰酸酯cas:35967-24-9。
[0324]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.33(s,1h),8.65(s,1h),7.44(d,j=10.5hz,1h),7.06(s,2h),3.79(s,6h),3.63(s,3h);
13
c nmr(125mhz,dmso-d6)δ153.1,148.5(c-f,1j
c-f
=257.0hz),145.7,138.3(c-f,2j
c-f
=31.4hz),136.5,131.9,119.9(c-f,4j
c-f
=5.6hz),112.2(c-f,3j
c-f
=19.1hz),104.1(c-f,4j
c-f
=7.8hz),94.6,60.2,55.7;hr-esi-ms for c
15h14
brfn4o3([m+h]
+
)calcd:397.0306;found:397.0298。
[0325]
实施例53:6-(1-(苯基磺酰基)-1h-吲哚-5-基)-n-(3,4,5-三甲氧基苯基)-[1,2,4]三唑并[4,3-a]吡啶-3-胺(3p)的合成
[0326][0327]
取40ml反应管,加入5-(1-(苯基磺酰基)-1h-吲哚-5-基)-2-肼基吡啶(182.2mg,0.50mmol)、3,4,5-三甲氧基苯基异硫氰酸酯(135.2mg,0.60mmol)、四丁基碘化铵(9.2mg,
0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈7.5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经抽滤固液分离,滤饼水洗干燥得产品(62.0mg,0.11mmol)。母液减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(110.2mg,0.20mmol),合并产品(172.2mg,0.31mmol),收率为62%((62.0+110.2)/(555.61
×
0.5)=62%)。
[0328]
5-(1-(苯基磺酰基)-1h-吲哚-5-基)-2-肼基吡啶cas号:26944-71-8,3,4,5-三甲氧基苯基异硫氰酸酯cas:35967-24-9。
[0329]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.27(s,1h),8.73(s,1h),8.09(d,j=8.7hz,1h),8.05
–
8.00(m,2h),7.97(d,j=1.4hz,1h),7.91(d,j=3.7hz,1h),7.73
–
7.66(m,3h),7.64
–
7.58(m,3h),7.11(s,2h),6.94(d,j=3.6hz,1h),3.80(s,6h),3.63(s,3h);
13
c nmr(125mhz,dmso-d6)δ153.2,145.1,144.9,137.2,137.0,134.8,133.9,131.8,131.6,131.3,130.0,128.1,127.0,126.7,125.2,123.6,119.8,119.4,115.6,113.8,109.8,94.4,60.2,55.8;hr-esi-ms for c
29h25
n5o5s([m+h]
+
)calcd:556.1649;found:556.1646。
[0330]
实施例54:8-氟-6-(1-(苯基磺酰基)-1h-吲哚-5-基)-n-(3,4,5-三甲氧基苯基)-[1,2,4]三唑并[4,3-a]吡啶-3-胺(3q)的合成
[0331][0332]
取40ml反应管,加入3-氟-5-(1-(苯基磺酰基)-1h-吲哚-5-基)-2-肼基吡啶(191.2mg,0.50mmol)、3,4,5-三甲氧基苯基异硫氰酸酯(135.2mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈7.5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经抽滤固液分离,滤饼水洗干燥得产品(192.1mg,0.34mmol)。母液减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=100:1)得到产品(28.7mg,0.05mmol),合并产品(220.8mg,0.39mmol),收率为77%((192.1+28.7)/(573.60
×
0.5)=77%)。
[0333]
3-氟-5-(1-(苯基磺酰基)-1h-吲哚-5-基)-2-肼基吡啶cas号:2671809-43-9,3,4,5-三甲氧基苯基异硫氰酸酯cas:35967-24-9。
[0334]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.38(s,1h),8.64(s,1h),8.08(d,j=8.7hz,1h),8.02(d,j=7.7hz,2h),7.97(s,1h),7.92(d,j=3.6hz,1h),7.74
–
7.68(m,2h),7.63
–
7.57(m,3h),7.11(s,2h),6.93(d,j=3.6hz,1h),3.79(s,6h),3.63(s,3h);
13
c nmr(125mhz,dmso-d6)δ153.1,149.0(c-f,1j
c-f
=251.9hz),146.2,138.6(c-f,2j
c-f
=32.1hz),136.9,136.7,134.9,134.0,131.8,131.2,131.0,130.0,128.2,126.7,124.9(c-f,4j
c-f
=5.6hz),123.6,119.9,116.3(c-f,4j
c-f
=4.6hz),113.7,109.8,109.1(c-f,3j
c-f
=16.2hz),94.6,60.2,55.7;hr-esi-ms for c
29h24
fn5o5s([m+h]
+
)calcd:574.1555;found:574.1553。
[0335]
实施例55:n-(1h-吲哚-4-基)-[1,2,4]三唑并[4,3-a]吡啶-3-胺(3r)的合成
[0336][0337]
取40ml反应管,加入2-肼基吡啶(54.6mg,0.50mmol)、(1h-吲哚-4-基)异硫氰酸酯(104.5mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=30:1)得到产品(64.8mg,0.26mmol),收率为52%(64.8/(249.28
×
0.5)=52%)。
[0338]
2-肼基吡啶cas号:4930-98-7,(1h-吲哚-4-基)异硫氰酸酯cas:208511-10-8。
[0339]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ11.11(s,1h),8.81(s,1h),8.19(d,j=7.0hz,1h),7.67(d,j=9.3hz,1h),7.31
–
7.25(m,2h),7.00(d,j=8.0hz,1h),6.95(t,j=7.8hz,1h),6.89(t,j=6.7hz,1h),6.84(d,j=7.4hz,1h),6.65(s,1h);
13
c nmr(125mhz,dmso-d6)δ147.2,144.5,137.0,134.5,126.9,123.6,123.2,121.7,118.3,115.6,112.5,104.8,104.3,99.0;hr-esi-ms for c
14h11
n5([m+h]
+
)calcd:250.1087;found:250.1082。
[0340]
实施例56:n-(1h-吲哚-6-基)-[1,2,4]三唑并[4,3-a]吡啶-3-胺(3s)的合成
[0341][0342]
取40ml反应管,加入2-肼基吡啶(54.6mg,0.50mmol)、(1h-吲哚-6-基)异硫氰酸酯(104.5mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=30:1)得到产品(69.8mg,0.28mmol),收率为56%(69.8/(249.28
×
0.5)=56%)。
[0343]
2-肼基吡啶cas号:4930-98-7,(1h-吲哚-6-基)异硫氰酸酯cas:471938-43-9。
[0344]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ10.94(s,1h),9.12(s,1h),8.40(d,j=7.0hz,1h),7.98(s,1h),7.60(d,j=9.3hz,1h),7.46(d,j=8.4hz,1h),7.23
–
7.19(m,2h),7.14
–
7.08(m,1h),6.87(t,j=6.6hz,1h),6.34(s,1h);
13
c nmr(125mhz,dmso-d6)δ146.0,145.1,136.6,135.8,126.3,123.9,122.8,122.2,120.2,115.6,112.0,110.8,101.0,98.9;hr-esi-ms for c
14h11
n5([m+h]
+
)calcd:250.1087;found:250.1082。
[0345]
实施例57:6-溴-n-苯基-[1,2,4]三唑并[4,3-a]吡啶-3-胺(1f)的合成
[0346][0347]
取200ml三颈烧瓶,加入5-溴-2-肼基吡啶(1128.2mg,6.0mmol)、异硫氰酸苯酯(973.4mg,7.2mmol)、四丁基碘化铵(110.8mg,0.30mmol)、碳酸钾(414.6mg,3.0mmol)、乙腈60ml,以碳棒(ф=18mm)作为阳极,铂片(20mm
×
20mm)作为阴极,在室温和60ma恒流反应
10h。反应结束后经抽滤固液分离,滤饼水洗干燥得产品(728.6mg,2.5mmol)。母液减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(572.5mg,2.0mmol),合并产品(1301.1mg,4.5mmol),收率为75%((728.6+572.5)/(289.14
×
6)=75%)。
[0348]
5-溴-2-肼基吡啶cas号:77992-44-0,异硫氰酸苯酯cas:103-72-0。
[0349]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.28(s,1h),8.77(s,1h),7.65(d,j=7.3hz,2h),7.61(d,j=9.7hz,1h),7.35
–
7.30(m,3h),6.94(t,j=7.3hz,1h);
13
c nmr(125mhz,dmso-d6)δ144.6,144.4,140.8,129.3,129.0,122.8,120.8,116.7,116.5,106.2;hr-esi-ms for c
12
h9brn4([m+h]
+
)calcd:289.0083;found:289.0082。
[0350]
对比例1:n-苯基-[1,2,4]三唑并[4,3-a]吡啶-3-胺(1a)的合成
[0351][0352]
取40ml反应管,加入2-肼基吡啶(54.6mg,0.50mmol)、异硫氰酸苯酯(81.1mg,0.60mmol)、四丁基六氟磷酸铵(9.7mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(31.5mg,0.15mmol),收率为30%(31.5/(210.24
×
0.5)=30%)。
[0353]
2-肼基吡啶cas号:4930-98-7,异硫氰酸苯酯cas:103-72-0。
[0354]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.23(s,1h),8.34(d,j=7.1hz,1h),7.62(d,j=9.3hz,1h),7.56(d,j=8.0hz,2h),7.31(t,j=7.7hz,2h),7.24(dd,j=9.3,6.4hz,1h),6.95
–
6.86(m,2h);
13
c nmr(125mhz,dmso-d6)δ146.3,144.4,141.5,129.0,126.6,122.7,120.5,116.3,115.6,112.3;hr-esi-msfor c
12h10
n4([m+h]
+
)calcd:211.0978;found:211.0973。
[0355]
对比例2:n-苯基-[1,2,4]三唑并[4,3-a]吡啶-3-胺(1a)的合成
[0356][0357]
取40ml反应管,加入2-肼基吡啶(54.6mg,0.50mmol)、异硫氰酸苯酯(81.1mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钠(26.5mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(25.2mg,0.12mmol),收率为24%(25.2/(210.24
×
0.5)=24%)。
[0358]
2-肼基吡啶cas号:4930-98-7,异硫氰酸苯酯cas:103-72-0。
[0359]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.23(s,1h),8.34(d,j=7.1hz,1h),7.62(d,j=9.3hz,1h),7.56(d,j=8.0hz,2h),7.31(t,j=7.7hz,2h),7.24(dd,j=9.3,6.4hz,1h),6.95
–
6.86(m,2h);
13
c nmr(125mhz,dmso-d6)δ146.3,144.4,141.5,129.0,126.6,122.7,120.5,116.3,115.6,112.3;hr-esi-msfor c
12h10
n4([m+h]
+
)calcd:
211.0978;found:211.0973。
[0360]
对比例3:n-苯基-[1,2,4]三唑并[4,3-a]吡啶-3-胺(1a)的合成
[0361][0362]
取40ml反应管,加入2-肼基吡啶(54.6mg,0.50mmol)、异硫氰酸苯酯(81.1mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、甲醇5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在室温和10ma恒流反应5h。反应结束后经减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(47.3mg,0.23mmol),收率为45%(47.3/(210.24
×
0.5)=45%)。
[0363]
2-肼基吡啶cas号:4930-98-7,异硫氰酸苯酯cas:103-72-0。
[0364]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.23(s,1h),8.34(d,j=7.1hz,1h),7.62(d,j=9.3hz,1h),7.56(d,j=8.0hz,2h),7.31(t,j=7.7hz,2h),7.24(dd,j=9.3,6.4hz,1h),6.95
–
6.86(m,2h);
13
c nmr(125mhz,dmso-d6)δ146.3,144.4,141.5,129.0,126.6,122.7,120.5,116.3,115.6,112.3;hr-esi-msfor c
12h10
n4([m+h]
+
)calcd:211.0978;found:211.0973。
[0365]
对比例4:n-苯基-[1,2,4]三唑并[4,3-a]吡啶-3-胺(1a)的合成
[0366][0367]
取40ml反应管,加入2-肼基吡啶(54.6mg,0.50mmol)、异硫氰酸苯酯(81.1mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在0℃下10ma恒流反应5h。反应结束后经减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(46.3mg,0.22mmol),收率为44%(46.3/(210.24
×
0.5)=44%)。
[0368]
2-肼基吡啶cas号:4930-98-7,异硫氰酸苯酯cas:103-72-0。
[0369]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.23(s,1h),8.34(d,j=7.1hz,1h),7.62(d,j=9.3hz,1h),7.56(d,j=8.0hz,2h),7.31(t,j=7.7hz,2h),7.24(dd,j=9.3,6.4hz,1h),6.95
–
6.86(m,2h);
13
c nmr(125mhz,dmso-d6)δ146.3,144.4,141.5,129.0,126.6,122.7,120.5,116.3,115.6,112.3;hr-esi-msfor c
12h10
n4([m+h]
+
)calcd:211.0978;found:211.0973。
[0370]
对比例5:n-苯基-[1,2,4]三唑并[4,3-a]吡啶-3-胺(1a)的合成
[0371][0372]
取40ml反应管,加入2-肼基吡啶(54.6mg,0.50mmol)、异硫氰酸苯酯(81.1mg,0.60mmol)、四丁基碘化铵(9.2mg,0.025mmol)、碳酸钾(34.6mg,0.25mmol)、乙腈5ml,以碳
棒(ф=6mm)作为阳极,铂片(10mm
×
10mm)作为阴极,在常温和15ma恒流反应5h。反应结束后经减压蒸馏除去溶剂,再经柱层析(二氯甲烷:甲醇=50:1)得到产品(84.1mg,0.40mmol),收率为80%(84.1/(210.24
×
0.5)=80%)。
[0373]
2-肼基吡啶cas号:4930-98-7,异硫氰酸苯酯cas:103-72-0。
[0374]
产品的表征数据为:1h nmr(500mhz,dmso-d6)δ9.23(s,1h),8.34(d,j=7.1hz,1h),7.62(d,j=9.3hz,1h),7.56(d,j=8.0hz,2h),7.31(t,j=7.7hz,2h),7.24(dd,j=9.3,6.4hz,1h),6.95
–
6.86(m,2h);
13
c nmr(125mhz,dmso-d6)δ146.3,144.4,141.5,129.0,126.6,122.7,120.5,116.3,115.6,112.3;hr-esi-msfor c
12h10
n4([m+h]
+
)calcd:211.0978;found:211.0973。
[0375]
上面对本发明实施例作了详细说明,但是本发明不限于上述实施例,在所属技术领域普通技术人员所具备的知识范围内,还可以在不脱离本发明宗旨的前提下作出各种变化。此外,在不冲突的情况下,本发明的实施例及实施例中的特征可以相互组合。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1