一种质子导体型固体氧化物电化学池氧电极材料及其制备方法
1.本发明属于电化学池技术领域,涉及一种质子导体型固体氧化物电化学池氧电极材料及其制备方法。
背景技术:
2.质子导体型固体氧化物电化学池是一种绿色环保的能源转换装置,由于其较低的工作温度被逐渐应用于氢分离膜、sofc电解质、氨合成等方面。与氧离子导体型固体氧化物电化学池不同的是,h2o是在氧电极侧生成,这有效地避免h2o对燃料气体的稀释,一定程度上提高了燃料利用率。当然,这使得阴极的反应更加复杂,同时对h-sofc阴极材料的选择提出了更高要求。
3.随着工作温度降低,电池阻抗主要来源为氧电极。因此,氧电极材料的选择对电池性能有重要的影响。氧电极反应可以分为氧气在氧电极表面吸附、解离,同时与电子反应生成氧离子,最后与质子反应生成水等过程。根据质子导体氧电极的反应原理可知氧电极材料需要具有以下几点要求:(1)良好的质子、氧离子和电子导电性,单相三重导电材料能将整个氧电极都能作为电化学反应界面,提高反应速率;(2)良好的稳定性。氧电极直接与电解质接触,要保证电极在工作条件不与电解质发生反应。氧电极在工作状态会产生水,如果空气中的氧气全部燃烧,会产生34%左右的水分压。因此,材料在水蒸气气氛中需要保持稳定的相结构;(3)热膨胀系数匹配,为了保证电池能长期工作,氧电极材料需要与电解质保持相近的热膨胀系数,避免氧电极从电解质上脱落,导致性能降低。
4.在质子导体氧化物的诸多结构类型中,钙钛矿型质子导体因其独特的性质而最受关注。目前,质子导体氧电极材料的获得途径是通过对单钙钛矿(abo3)、双钙钛矿(aa
′
b2o6)和ruddlesden
–
popper(rp)结构(a
n+1bn
o3
n+1
)进行掺杂。掺杂后,材料的orr活性及结构稳定性都会得到改善。单钙钛矿结构简单,易于掺杂而不形成杂相的特点使其成为优异的候选材料。baco
1-x
fe
x
o3材料由于b位是co,fe变价元素,能提供较高的氧还原能力。但a、b位离子半径差距较大,导致结构呈现低对称性的六方相结构,不利于氧离子的传输。
技术实现要素:
5.针对现有技术的缺点和不足,本发明的目的在于提供一种质子导体型固体氧化物电化学池氧电极材料及其制备方法。本发明通过在baco
1-x
fe
xo3-δ
的b位上进行zn和y的共掺杂,制备了钙钛矿结构的baco
x
feyzn
zy1-x-y-zo3-δ
系列质子导体型氧化物,通过一系列的表征(xrd、tem、xps、tg、epr等)证明,baco
x
feyzn
zy1-x-y-zo3-δ
在质子导体型固体氧化物电化学池的工作环境下具有稳定的相结构及丰富的氧空位。以baco
x
feyzn
zy1-x-y-zo3-δ
为氧电极材料的电化学测试结果表明,600-700℃温度范围内,质子导体型固体氧化物电化学池(nio-bzcyyb/bzcyyb/baco
x
feyzn
zy1-x-y-zo3-δ
)获得了优异的电化学性能。此外,长达100h的恒流放电结果表明,baco
x
feyzn
zy1-x-y-zo3-δ
在水蒸气气氛中具有较好的稳定性。
6.本发明的目的通过以下技术方案实现:
7.一种质子导体型固体氧化物电解池氧电极材料,其组成分子式为baco
x
feyzn
zy1-x-y-zo3-δ
,其中0<x<1,0<y<1,0<z≤0.3,δ表示氧空位的数量。
8.优选的,x=0.3~0.5,y=0.3~0.5,z=0.05~0.15;更优选x=0.4,y=0.4,z=0.1。
9.所述的质子导体型固体氧化物电化学池氧电极材料的制备方法,包括以下步骤:
10.1)根据分子式baco
x
feyzn
zy1-x-y-zo3-δ
,按照化学计量比,将硝酸钡、硝酸钴、硝酸铁、硝酸锌和硝酸钇溶于水中,获得混合溶液ⅰ;混合溶液ⅰ中硝酸钡、硝酸钴、硝酸铁、硝酸锌和硝酸钇的总浓度为0.25mol/l-0.5mol/l;
11.2)将乙二胺四乙酸溶于氨水中,获得混合溶液ⅱ;
12.3)将混合溶液ⅰ、混合溶液ⅱ以及柠檬酸混匀,调节ph至8-10,获得溶胶;
13.4)将溶胶进行加热搅拌,获得凝胶;将凝胶干燥,在1000℃下煅烧10-20h,获得质子导体型固体氧化物电化学池氧电极材料baco
x
feyzn
zy1-x-y-zo3-δ
。
14.步骤2)中氨水的浓度为11~15mol/l;乙二胺四乙酸与氨水的摩尔体积比为0.05mol:(45~70)ml。
15.乙二胺四乙酸与混合溶液ⅰ中金属离子总的摩尔比为1:1。金属离子包括钡、钴、铁、锌和钇离子。
16.步骤3)的具体步骤:将混合溶液ⅰ和混合溶液ⅱ混匀,随后加入柠檬酸,混匀后,加入氨水调节ph为8-10,得到溶胶。
17.柠檬酸与与混合溶液ⅰ中金属离子总的摩尔比为(1.5~2):1;金属离子包括钡、钴、铁、锌和钇离子。
18.步骤4)中加热搅拌的温度为80-90℃。所述干燥的条件为250~300℃干燥5-10h。
19.煅烧前进行研磨。
20.所述本发明还提供了一种质子导体型固体氧化物电化学池的制备方法,包括以下步骤:将所述质子导体型固体氧化物电化学池氧电极材料的粉体与乙基纤维素-松油醇粘结剂均匀混合制成浆料,将浆料均匀地涂在致密的bzcyyb电解质(钡锆铈钇镱,钙钛矿结构)的表面,经1000~1100℃温度下煅烧2~4小时,制成多孔的质子导体型固体氧化物电化学池氧电极,质子导体型固体氧化物电化学池的燃料电极则采用nio-bzcyyb电极材料。
21.所述电池的结构依次为燃料电极||功能层||电解质||氧电极;
22.所述电解质的材料为bazr
0.1
ce
0.7y0.1
yb
0.1o3-δ
;
23.所述燃料电极的材料为nio和bazr
0.1
ce
0.7y0.1
yb
0.1o3-δ
构成的复合燃料极;所述燃料电极中nio和bzcyyb的质量比为5.5-6.5:3.5-4.5。
24.与现有技术相比,本发明具有以下优点及有益效果:
25.1)本发明所制备的baco
x
feyzn
zy1-x-y-zo3-δ
颗粒小,活性高,在质子导体电化学池的测试范围内可以保持结构稳定,在长期的电池工作过程中仍然保持稳定,具有很好的电催化性能,适合作为中低温质子导体型固体氧化物电化学池的氧电极材料。
26.2)以本发明的氧电极材料baco
x
feyzn
zy1-x-y-zo3-δ
作为电极,bzcyyb作为电解质,nio-bzcyyb复合电极材料装配的电池在以氢气为燃料发电及电解水方面性能优异。
附图说明
27.图1为bcfz(即baco
0.4
fe
0.4
zn
0.2o3-δ
)和bcfzy(实施例1制备的baco
0.4
fe
0.4
zn
0.1y0.1o3-δ
)的xrd图和晶体结构示意图;bcfz(a)和bcfzy(b)的xrd精修结果;(c)bcfzy晶体结构示意图;bcfz(d)、bcfzy(e)与bzcyyb电解质的化学相容性的xrd图;(f)bcfzy样品在不同温度(室温至800℃)下的xrd图谱;
28.图2为实施例1制备的bcfzy粉末(baco
0.4
fe
0.4
zn
0.1y0.1o3-δ
)的高分辨率tem图像和元素分布图像;其中(a)bcfzy的hr-tem图像的晶体结构特征;(b)沿区轴的相应样品saed图谱;(c)bcfzy晶粒的sem图像和ba、co、fe、zn和y的相关eds图谱;
29.图3中(a)和(b)分别为bcfz(即baco
0.4
fe
0.4
zn
0.2o3-δ
)和bcfzy(实施例1制备的baco
0.4
fe
0.4
zn
0.1y0.1o3-δ
)的o1s xps数据曲线;
30.图4为bcfz(即baco
0.4
fe
0.4
zn
0.2o3-δ
)和bcfzy(实施例1制备的baco
0.4
fe
0.4
zn
0.1y0.1o3-δ
)氧空位浓度的评估图:(a)空气中30~900℃的tg曲线和(b)室温下的epr光谱;
31.图5为以bcfz作为空气电极的单电池(cell-1)以及以bcfzy作为电极的电池(cell-2)在600~700℃下的电化学性能:(a)和(b)cell-1和cell-2在燃料电池模式下的峰值功率密度;(c)和(d)电池1和电池2的电化学阻抗;(e)和(f)cell-1和cell-2之间的峰值功率密度和rp比较结果;
32.图6为燃料电池和电解模式下长期稳定性的电化学性能;(a)燃料电池模式下电池1和电池2在0.5a cm-2
和650℃下的长期稳定性试验;(b)50小时循环运行:在
±
0.5a cm-2
电流密度下,在燃料电池和电解模式之间切换运行模式(每种模式0.5小时)时,电池2的电压随时间的变化。
具体实施方式
33.下面结合实施例对本发明作进一步详细地描述,但本发明的实施方式不限于此。
34.实施例1:baco
0.4
fe
0.4
zn
0.1y0.1o3-δ
的合成、电化学性能的测试。
35.1)根据化学式baco
0.4
fe
0.4
zn
0.1y0.1o3-δ
,按照化学计量比称取硝酸钡、硝酸钴、硝酸铁、硝酸锌和硝酸钇溶于200ml的去离子水中,搅拌均匀,获得混合溶液i;溶液中硝酸钡、硝酸钴、硝酸铁、硝酸锌和硝酸钇的总浓度为0.25mol/l;
36.2)按照乙二胺四乙酸与金属离子(钡、钴、铁、锌和钇离子)摩尔比为1:1称取乙二胺四乙酸溶于50ml的氨水(浓度为13mol/l)中,搅拌均匀,获得溶液ii;
37.3)将混合溶液i与溶液ii搅拌均匀后,按照柠檬酸与金属离子总摩尔比为1.5:1加入柠檬酸并继续搅拌,并用氨水调ph值为8-9,制得溶胶;
38.4)将溶胶置于油浴锅中,90℃搅拌(水分挥发完毕为止),使其变为凝胶;
39.5)将凝胶在300℃干燥10小时,可以得到蓬松的前驱体粉末,将前驱体粉末置于研钵中研磨;
40.6)将所述研磨产物置于1000℃空气中煅烧10小时,即得质子导体型固体氧化物电化学池氧电极材料baco
0.4
fe
0.4
zn
0.1y0.1o3-δ
。
41.另外,本实例还提供了一种质子导体型固体氧化物电化学池的制备方法,将所述质子导体型固体氧化物电化学池氧电极材料的粉体与乙基纤维素-松油醇粘结剂以1∶1均
匀混合制成浆料,将浆料均匀地涂在致密的bzcyyb电解质的表面(浆料的涂覆量为厚度约为10微米),经1000℃温度下煅烧2个小时,制成多孔的质子导体型固体氧化物电化学池氧电极。质子导体型固体氧化物电化学池的燃料电极则采用nio-bzcyyb电极材料。
42.实施例2:baco
0.4
fe
0.3
zn
0.2y0.1o3-δ
的合成、电化学性能的测试。
43.1)根据化学式baco
0.4
fe
0.3
zn
0.2y0.1o3-δ
,按照化学计量比称取硝酸钡、硝酸钴、硝酸铁、硝酸锌和硝酸钇溶于200ml的去离子水中,搅拌均匀,获得混合溶液i;溶液中硝酸钡、硝酸钴、硝酸铁、硝酸锌和硝酸钇的总浓度为0.3mol/l;
44.2)按照乙二胺四乙酸与金属离子总摩尔比为1.5:1称取乙二胺四乙酸溶于60ml的氨水中,搅拌均匀,获得溶液ii;
45.3)将混合溶液i与溶液ii搅拌均匀后,搅拌均匀后,按照柠檬酸与金属离子总摩尔比1.7:1加入柠檬酸并继续搅拌,并用氨水调ph值9,制得溶胶;
46.4)将溶胶置于油浴锅中,90℃搅拌(水分挥发完毕为止),使其变为凝胶;
47.5)将凝胶在300℃干燥10小时,可以得到蓬松的前驱体粉末,将前驱体粉末置于研钵中研磨;
48.6)将所述研磨产物进行1000℃空气中煅烧15小时,即得质子导体型固体氧化物电化学池氧电极材料baco
0.4
fe
0.3
zn
0.2y0.1o3-δ
。
49.另外,本实施例还提供了一种质子导体型固体氧化物电化学池的制备方法,将所述质子导体型固体氧化物电化学池氧电极材料的粉体与乙基纤维素-松油醇粘结剂以6∶4均匀混合制成浆料,将浆料均匀地涂在致密的bzcyyb电解质的表面,经1050℃温度下煅烧2小时,制成多孔的baco
0.4
fe
0.3
zn
0.2y0.1o3-δ
质子导体型固体氧化物电化学池氧电极,质子导体型固体氧化物电化学池的燃料电极则采用nio-bzcyyb电极材料。
50.实施例3:baco
0.3
fe
0.3
zn
0.2y0.2o3-δ
的合成、电化学性能的测试。
51.1)根据化学式baco
0.3
fe
0.3
zn
0.2y0.2o3-δ
,按照化学计量比称取硝酸钡、硝酸钴、硝酸铁、硝酸锌和硝酸钇溶于300ml的去离子水中,搅拌均匀,获得混合溶液i;溶液中硝酸钡、硝酸钴、硝酸铁、硝酸锌和硝酸钇的总浓度为0.5mol/l;
52.2)按照乙二胺四乙酸与金属离子摩尔比为2:1称取乙二胺四乙酸溶于70ml的氨水中,搅拌均匀,获得溶液ii;
53.3)将混合溶液i与溶液ii搅拌均匀后,按照柠檬酸与金属离子摩尔比为2:1加入柠檬酸并继续搅拌,并用氨水调ph值10,制得溶胶;
54.4)将溶胶置于油浴锅中,100℃搅拌(水分挥发完毕为止),使其变为凝胶;
55.5)将凝胶在300℃干燥10小时,可以得到蓬松的前驱体粉末,将前驱体粉末置于研钵中研磨;
56.6)将所述研磨产物进行1000℃空气中煅烧20小时,即得质子导体型固体氧化物电化学池氧电极材料baco
0.3
fe
0.3
zn
0.2y0.2o3-δ
。
57.另外,本实施例还提供了一种质子导体型固体氧化物电化学池的制备方法,将所述质子导体型固体氧化物电化学池氧电极材料的粉体与乙基纤维素-松油醇粘结剂以7:3均匀混合制成浆料,将浆料均匀地涂在致密的钇稳定氧化锆电解质的表面,经温度1050℃下煅烧4个小时,制成多孔的baco
0.3
fe
0.3
zn
0.2y0.2o3-δ
质子导体型固体氧化物电化学池氧电极,质子导体型固体氧化物电化学池的燃料电极则采用nio-bzcyyb电极材料。
58.结构和性能分析:
59.图1为bcfz(即baco
0.4
fe
0.4
zn
0.2o3-δ
)和bcfzy(实施例1制备的baco
0.4
fe
0.4
zn
0.1y0.1o3-δ
)的xrd图和晶体结构示意图;bcfz(a)和bcfzy(b)的xrd精修结果;(c)bcfzy晶体结构示意图;bcfz(d)、bcfzy(e)与bzcyyb电解质的化学相容性的xrd图;(f)bcfzy样品在不同温度(室温至800℃)下的xrd图谱。
60.图1(a)和(b)显示了bcfzy和bcfz粉末的rietveld精修结果和相关晶格参数,其中所有可靠性系数都在合理范围内。两个样品出现了类似的衍射峰,没有观察到不希望出现的杂质峰。两个样品显示出良好的立方钙钛矿结构,其空间群为pm-3m,与bacoo
2.23
(jcpdf-75-0227)和yba2co3o
9-x
(jcpdf-46-0642)的晶体结构一致。对于bcfzy样品,b位掺杂后的立方钙钛矿结构得到了很好的保持,表明y
3+
成功地进入了bcfz晶格。bcfzy属于典型的立方钙钛矿结构,ba离子位于立方晶胞的顶点,co/fe/zn/y离子占据晶胞的体心位置,氧位于面中心。晶体结构示意图如图1(c)所示。此外,bcfzy的主峰(~30.73
°
)相对于bcfz的主峰(~31.45
°
)移动到较低的角度,这主要是是晶格体积变化的结果。根据rietveld精修结果,在bcfz的b位引入较大的y
3+
(0.09nm),并取代zn,导致晶格膨胀,体积从变为
61.相结构的稳定性对单电池的长期运行至关重要。图1(d)和(e)所示为bcfzy和bcfz与bzcyyb(质量比1:1)的化学相容性结果。结果表明,bcfz-bzcyyb样品经1000℃煅烧10h后,混合物中可观察到baco3相等杂质。相反,在bcfzy-bzcyyb模式中未观察到baco3峰。这一现象表明bcfz容易与空气中的co2发生反应,放置6个月的两个样品xrd也证实了这一结果。这一结果表明bcfzy在相同条件下具有更好的co2耐受性。用ht-xrd研究了bcfzy在较宽温度范围内的相结构稳定性。图1(f)为bcfzy粉末在室温-800℃-室温下每隔200℃检测到的ht-xrd结果,bcfzy粉末在不同温度下的衍射峰与室温一致。在此过程中没有观察到其他杂质峰,表明bcfzy在质子陶瓷燃料电池工况下具有良好的结构稳定性。
62.图2为实施例1制备的bcfzy粉末(baco
0.4
fe
0.4
zn
0.1y0.1o3-δ
)的高分辨率tem图像和元素分布图像。图2中(a)bcfzy的hr-tem图像的晶体结构特征;(b)沿区轴的相应样品saed图谱;(c)bcfzy晶粒的sem图像和ba、co、fe、zn和y的相关eds图谱。
63.如图2(a)所示,(100)和(110)平面的面间距分别为0.35nm和0.25nm。它们之间的晶面角与理论值基本吻合。图2(b)显示了bcfzy样品的选区电子衍射图(saed)。(101)和(201)的晶面夹角为68
°
,与理论值71
°
非常接近。同时,利用矢量算法可以确定(300)晶面对应的衍射光斑,(300)晶面与(101)、(201)晶面夹角分别为40
°
和28
°
。图2(b)中样品的晶带轴为bcfzy粉末的eds谱图显示ba、co、fe、zn、y和o元素分布均匀,这进一步表明y元素已经掺杂到bcfz晶格中。
64.图3中(a)bcfz(即baco
0.4
fe
0.4
zn
0.2o3-δ
)和(b)bcfzy(实施例1制备的baco
0.4
fe
0.4
zn
0.1y0.1o3-δ
)的o1s xps数据。
65.材料的表面化学性质(缺陷、电子结构等)是pcecs空气电极氧反应的关键。bcfz和bcfzy的o1s拟合xps谱如图3(a)和(b)所示。位于528~529ev处的结合能峰值对应于晶格氧(o
l
),~529ev、~531ev和~532ev处的峰值分别对应于o
2-、o-、o
2-的化学吸附氧。在~533ev位置的oh可以归属于被吸附的分子水(h2o)或碳酸盐(co
32-)。co
32-主要来源于ba基钙钛矿中
的碳酸钡(baco3)。oh、oc、o
l
和oc/o
l
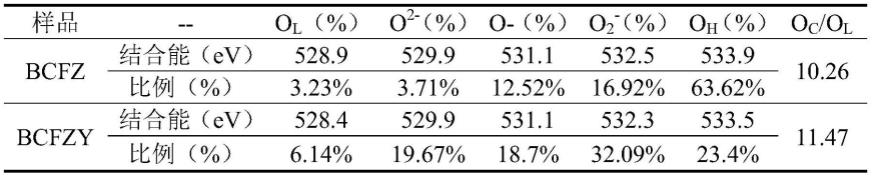
的结合能和比面积见表1。
66.表1两个样品的结合能位置(ev)、含量百分比(%)和oc/o
l
值。
[0067][0068]y3+
掺杂后oc的峰面积明显增加,oc含量越高,氧还原过程中的氧传输速率越快。oc/o
l
的值可以反映材料表面氧缺陷的数量。表面氧缺陷通常表现出较高的能量状态,是orr的重要活性中心。y
3+
掺杂使电池的oc/o
l
值从10.26提高到11.47,表明bcfzy阴极的单电池具有更好的电化学性能。此外,bcfz表面的oh峰面积比bcfzy高出一倍,这可能是由于bcfz表面形成了大量的碳酸盐,同时也表明bcfzy在空气中具有较好的相稳定性。值得注意的是,co2p和ba 3d的峰值由于重叠需要同步分析。
[0069]
图4为bcfz(即baco
0.4
fe
0.4
zn
0.2o3-δ
)和bcfzy(实施例1制备的baco
0.4
fe
0.4
zn
0.1y0.1o3-δ
)氧空位浓度的评估图:(a)空气中30~900℃的tg曲线和(b)室温下的epr光谱。
[0070]
众所周知,钙钛矿氧化物的orr/oer活性很大程度上取决于氧空位浓度。图4(a)所示为bcfz和bcfzy样品在空气中的tga(热重)曲线,通过tga曲线可以了解材料从室温加热到900℃期间的晶格氧损失状况。两个样品在初始阶段的重量损失主要是由于吸附h2o的损失。在这一阶段,bcfzy的失重值在273℃时为1.65%,高于bcfz。当温度升高到900℃时,bcfzy的失重达到1.15%,这与co/fe的热还原有关。这一结果得到了epr测试的支持。如图4(b)所示,bcfzy在g=2.003时表现出氧缺陷密度的增强信号,表明y
3+
掺杂产生更多的氧空位。tg和epr结果表明bcfzy具有较高的氧空位浓度。
[0071]
电化学性能
[0072]
电化学性能(eis、i-v-p和长期稳定性)通过对ni-bzcyyb/bzcyyb/bcfzy燃料电池进行测试获得,测试温度为600-700℃。以bcfz(即baco
0.4
fe
0.4
zn
0.2o3-δ
)作为空气电极的单电池表示为cell-1,以bcfzy(实施例1制备的baco
0.4
fe
0.4
zn
0.1y0.1o3-δ
)作为电极的电池被称为cell-2。以湿氢气(3%h2o)作为燃料,静态空气作为氧化剂分别引入至电池的燃料电极和空气电极。
[0073]
图5为以bcfz作为空气电极的单电池(cell-1)以及以bcfzy作为电极的电池(cell-2)在600~700℃下的电化学性能:(a)和(b)cell-1和cell-2在燃料电池模式下的峰值功率密度;(c)和(d)电池1(cell-1)和电池2(cell-2)的电化学阻抗;(e)和(f)cell-1和cell-2之间的峰值功率密度和rp比较结果。
[0074]
图5(a)和5(b)所示为cell-1和cell-2的典型i-v-p曲线。如图所示,在600、650和700℃时,cell-1的峰值功率密度分别为357、517和700mw cm-2
。与cell-1相比,cell-2的峰值功率密度在600~700℃时可以达到510、690和870mw cm-2
。我们进一步评估了cell-2的电解性能,在电压为1.4v时,在600~700℃时可获得1.71、2.46和3.45a cm-2
的电解电流密度。通过测量电化学阻抗进一步评估两个电池的电化学性能,如图5(c)和(d)所示。对于cell-1,600~700℃时的欧姆电阻(ro)值为0.24、0.18、0.12ωcm2,极化电阻(rp)值为0.76、
0.28、0.14ωcm2,如图5(c)所示。这些结果表明,cell-1的rp在总阻力中占主导地位。但是,对于cell-2,在600~700℃下rp分别降低到0.2ω、0.1和0.04ωcm2,结果表明,y掺杂bcfzy阴极显著提高了电池2的性能。
[0075]
图6为燃料电池和电解模式下长期稳定性的电化学性能;(a)燃料电池模式下电池1(cell-1)和电池2(cell-2)在0.5a cm-2
和650℃下的长期稳定性试验;(b)50小时循环运行:在
±
0.5a cm-2
电流密度下,在燃料电池和电解模式之间切换运行模式(每种模式0.5小时)时,电池2的电压随时间的变化。
[0076]
当使用湿氢气(3%h2o)作为燃料时,在650℃下,在0.5a cm-2
的恒定电流密度下对比两个电池的长期稳定性。cell-2(电池2)表现出更好的长期稳定性,如图6(a)所示。cell-2的性能衰减率约为4.2%/100h,远低于cell-1的55%/100h。随后,可逆pcec的测试结果进一步证明了cell-2优异的长期电化学。当电池以0.5h的间隔动态由电解模式(-0.5acm-2
)切换到燃料电池模式(0.5acm-2
)时,电池表现出显著的耐用性(图6(b))。良好的长期稳定性数据表明,bcfzy作为质子陶瓷电化学电池中的空气电极比bcfz具有更好的相稳定性。
[0077]
本发明的中低温是指600-700℃。本发明的电极材料适合中低温质子导体型固体氧化物电化学池的氧电极材料,在600-700℃取得较好的电化学性能,且材料性能稳定。
[0078]
本领域的技术人员容易理解,以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1