一种基于固定化MnO2的流动注射化学发光分析方法与流程
本发明涉及一种基于固定化MnO2流动注射化学发光的分析方法,属于化学发光分析领域。
背景技术:
化学发光(chemiluminescence,CL)是在化学反应过程中产生的光发射现象,由于其具有高灵敏度、线性范围宽、设备简单、操作方便、易于实现自动化和分析快速的特点,已成为当前痕量分析领域的一个十分重要的研究方法[1]。在众多的发光体系中,酸性高锰酸钾氧化有机物产生化学发光得到了广泛的应用。1975年Stauff和Jaeschke[2]利用KMnO4作为氧化剂应用于SO2的分析测定。1986年Townshend[3]通过KMnO4氧化吗啡产生CL应用于血液和尿样中吗啡的测定,随后KMnO4体系在各领域的分析与应用均得到了迅速的发展。高锰酸钾作为液相化学发光反应中应用最广泛的氧化剂之一,在其还原过程中常常伴随着各种低价态锰的生成。研究表明,锰的这些中间价态可以作为化学发光反应的氧化剂[4]。Mn(Ⅳ)常以难溶的二氧化锰形式存在,这限制了其在液相化学发光分析中的应用。Barnett[5]等发现新制备的MnO2沉淀可经超声分散于3mol/L的H3PO4后得到可溶性的Mn(Ⅳ)。但这种Mn(Ⅳ)溶液需在强酸溶液中才可以稳定存在。随后有学者报道了在中性条件下用Na2S2O3还原KMnO4可制备出在水溶液中均匀分散且性质稳定的MnO2纳米溶胶,并且建立了MnO2-甲醛、MnO2-抗坏血酸等发光体系[6-8]。由于目前对于MnO2化学发光的研究大部分都是局限在液相反应的条件下,因此在检测装置的设计中至少要存在两条以上的流路。这势必会导致操作繁琐,并增加分析成本。因此,本发明所要解决的问题就是寻找一种MnO2的固定化方法,直接采用固液两相反应方法,以实现简化装置,节约成本的目的。采用电沉积的方法在碳电极上制备纳米MnO2,然后配合使用PDMS和固化剂组装流通池。采用流动注射分析方法,选取水作为载液,当待测溶液通过注射流入流通池内与MnO2接触时产生化学发光。通过采集光信号对待测物质的含量进行定量分析。
技术实现要素:
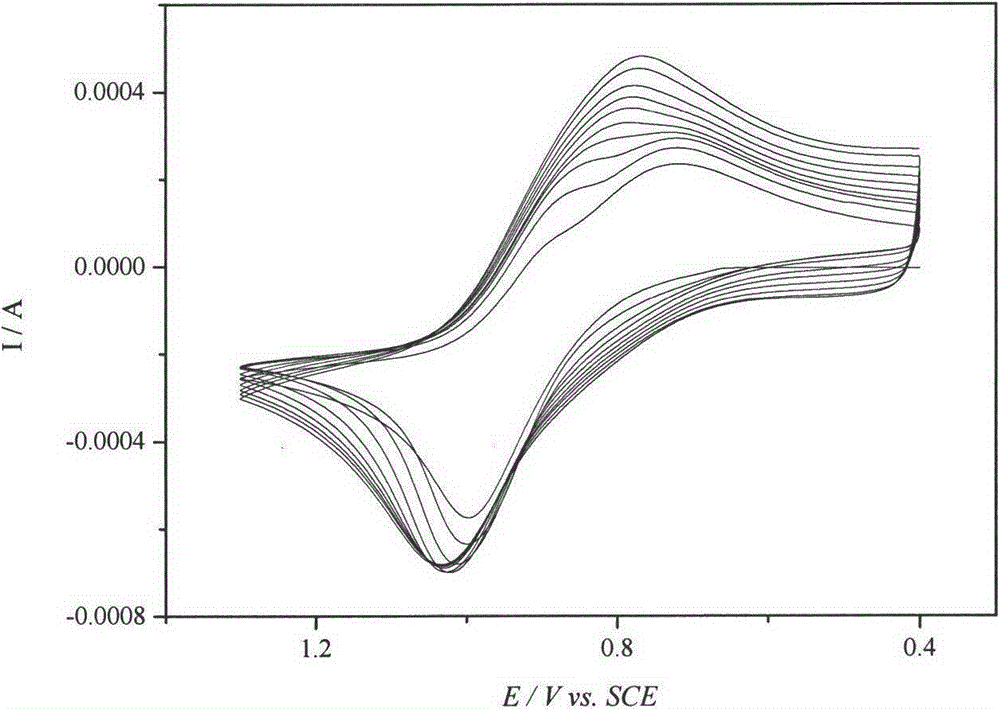
本发明提出一种基于固定化MnO2流动注射化学发光分析方法,该方法大大降低了测量成本、简化了操作步骤,经济实用且环境友好,能够快速准确地测量水溶液中多种待测物质含量(如甲醛,葡萄糖等)。本发明的技术方案如下:1)MnO2的固定化:有文献报道,可以直接在ITO电极表面电沉积制备纳米MnO2[9]。但这种方法制备的纳米MnO2在空气中极容易风干脱落,不利于MnO2的固定化及在流动体系中的应用。因此我们尝试先在ITO玻璃表面涂覆一层碳浆,经过烘干后再电沉积制备MnO2。具体操作如下:将大小适当的ITO玻璃(如5.5×2.5cm)分别在乙醇、超纯水中超声清洗10min。然后在其表面涂覆碳浆并放入烘箱中80℃~100℃干燥20~40min后作为工作电极。结构如图1所示。铂电极和饱和甘汞电极分别作为对电极和参比电极。采用循环伏安法电沉积制备纳米MnO2,电压范围0.4~1.3V,扫描速度10mV/s,扫描圈数30圈。电解液为含1.0×10-3~8.0×10-3mol/LMnSO4的0.05~0.5mol/LNa2SO4溶液。循环伏安图如图2所示。实验表明在碳层表面制备的MnO2层牢固可靠,成功地实现了MnO2的固定化。利用超景深三维显微镜对电极表面进行初步观察,结果如图3所示。从图中可以看出沉积前后电极表面形貌截然不同。沉积前,碳电极表面均匀,粗糙,无裂纹。沉积后表面有裂纹,且有颗粒状物质生成。图4和图5分别是沉积前后电极表面的三维显示图。图3显示碳电极表面凹凸不平,这说明相对于ITO电极其具有更大的表面积。因此,推测与面积相同的ITO玻璃相比,涂碳有利于生成更多的纳米MnO2。从图5可以看出在碳表面的峰顶和谷底都布满了颗粒状物质,证明了以上推测的成立。从图6的电镜图片可以看出所制备的纳米MnO2表面结构致密、紧凑且呈棒状结构。以上结果表明在ITO玻璃表面涂覆碳浆后电沉积制备MnO2层可以解决固体MnO2的固定化问题。2)流通反应池的制作:图7是流通池的示意图。从图中可以看出流通池分为两个部分。(a)图是一块附着MnO2的玻璃片;(b)图是流通池的主体部分,包括一个进口、一个凹槽(流路)和一个出口。左右两个部分结合在一起,组成一个完整的流通池。(a)部分制作:如1)所述,在ITO玻璃上涂覆碳层,制备固定化纳米MnO2。(b)部分制作:将PDMS和固化剂按10:1的量混合均匀,后在真空度0.1Mpa的真空干燥箱中放置10~20min。选取6.0×4.0×1.5cm的无盖硬质纸盒作为模具。同时在其底部中间部分用双面胶固定大小为5.0×2.5cm的玻璃。玻璃上层用双面胶固定相同面积的厚度约为0.1cm塑料板。塑料板的四个角应为圆弧状,以避免池内出现死体积。另外,在纸盒两端各开一个孔,插入外径为0.2cm的聚四氟乙烯管,并将管一端固定在塑料板上,用于制作进出口。至此,反应池制作完成。将PDMS和固化剂的混合物转移至模具内。将模具在0.1Mpa的真空干燥箱中放置10~20min,后移至烘箱中80℃干燥20~40min进行固化。固化完成后将纸盒、塑料板、玻璃和聚四氟乙烯管剥落(管内充满PDMS造成阻塞),并放入新的聚四氟乙烯管作为进出管。此时,池体部分制作完成,包括进口、流路、出口。最后,将(a)部分嵌入(b)部分,并用PDMS和固化剂进行封装,80℃干燥20~40min。至此,流通池已制作完成。其中(b)部分可以循环使用,只需更换(a)部分碳层即可。3)化学发光实验:实验装置如图8所示。按照步骤1)和2)制作流通池。将流通池紧挨着光电倍增管(PMT),由光电倍增管收集光信号。实验数据由光子计数单元采集,由计数卡处理系统记录数据并显示对应的发光强度。本发明可用于测定水溶液中多种还原性物质,以甲醛和葡萄糖含量的测定为例:首先使用硫酸溶液配制一系列酸度相同、分析物含量不同的溶液作为标准溶液。并将其分别通过上述的流通池与固体MnO2混合记录发光强度。得到线性拟合方程为:甲醛y=2.9+807.7x,R2=0.992式中x,y分别代表甲醛含量(mol/L)和发光强度;葡萄糖y=100.5+2204.3x,R2=0.995式中x,y分别代表葡萄糖含量(mol/L)和发光强度。本发明的特点在于采用简单快速的电沉积方法在碳表面制备固定化的MnO2,利用PDMS和固化剂自制流通池,作为化学发光场所,检测水中还原性物质。附图说明图1电沉积制备MnO2的工作电极结构图。在ITO玻璃上涂覆一层碳浆(留出一定面积用于引出导线),将导线连接在ITO上进行电沉积。所制备的MnO2附着在碳层上表面。图2电沉积制备MnO2的循环伏安图。图3电极表面超景深三维显微镜图片:(a)碳表面;(b)电沉积制备的MnO2表面。图4碳层的三维显示图。图5电沉积MnO2层的三维显示图。图6电沉积MnO2层的扫描电镜图图7自制流通池示意图:(a)附着MnO2的普通玻璃;(b)流通池主体部分,包括进口、流路、出口。图8实验装置图:C-载液;S-样品;V-六通阀;P-蠕动泵;FC-流通池;PMT-光电倍增管;HV-高压电源;W-废液;PC-显示器。具体实施方式把管道分别插入超纯水、硫酸溶液中,开启蠕动泵冲洗整个流路15min,使得流通池处于稳定状态。选择超纯水作为载液,样品通过六通阀注入流路。在流通池中与MnO2接触产生化学发光。检测和记录发光强度对样品进行定量。应用实例1设定体积流量为2.5~4.5mL/min,硫酸浓度为2.5mol/L。选取五种已知浓度的甲醛溶液采用本法测量其含量,结果如表1所示:表1.甲醛溶液的测量值和真实值的比较应用实例2设定体积流量为2.5~4.5mL/min,硫酸浓度为2.8mol/L。选取五种已知浓度的葡萄糖溶液采用本法测量其含量,结果如表2所示:表2.葡萄糖溶液的测量值和真实值的比较从测量结果可以看出,该法的准确度较高。因此,本发明所提出的MnO2化学发光法简单快速、经济实用,且环境友好,可以作为一种检测手段用于多种还原性物质的检测和分析。参考文献[1]ShoiiMotomizu,Z.H.Li.Traceandultratraceanalysismethodsforthedeterminationofphosphorusbyflow-injectiontechniques.Talanta,2005,66(2):332-340[2]StauffJ,JaeschkeW.Achemiluminescencetechniqueformeasuringatmospherictraceconcentrationsofsulfurdioxide.Atmos.Environ.,1975,9(11):1038[3]AbbottRW,TownshendA,GillR.Determinationofmorphinebyflowinjectionanalysiswithchemiluminescencedetection.Analyst,1986,111(6):635-640[4]BarnettN.W.,HindsonB.J.,JonesP.,SmithT.A.ChemicallyInducedPhosphorescencefromManganese(Ⅱ)duringtheOxidationofVariousCompoundsbyMnaganese(Ⅲ),(Ⅳ)breakand(Ⅶ)inacidicaqueousSolutions[J].Anal.Chim.Acta,2002,451(2):181-188[5]JakyM,SimandiLI,ShafiovichVY.InorgChimActa,1984,90(3):L39[6]Perez-BenitoJF.Identificationofasolubleformofcolloidalmanganese(IV)InorgChem,1989,28(3):390[7]Perez-BenitoJF,AriasC,AmatE.Akineticstudyofthereductionofcolloidalmanganesedioxidebyoxalicacid.JColloidInterfSci,1996,177(2):288[8]王虹,杜建修.MnO2纳米溶胶-抗坏血酸化学发光反应的研究[J].分析实验室,2010,29(12):43-46[9]Nakayama,etal.Anodicdepositionoflayeredmanganeseoxideintoacolloidalcrystalremplateforelectrochemicalsupercapacitors.Electrochemistrycommunications,2007,9:1154-1158
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1
- 一种用于micro RNA检测的电化学发光活性DNA纳米探针的制备方法与制造工艺
- 一种中枢神经特异蛋白的化学发光酶联免疫检测试剂盒的制造方法与工艺
- 一种人附睾蛋白的化学发光酶联免疫检测试剂盒的制造方法与工艺
- 一种抗RA33抗体IgG化学发光免疫检测试剂盒及其制备方法与制造工艺
- 一种醛固酮化学发光免疫检测试剂盒及其制备方法与制造工艺
- 抗环瓜氨酸多肽抗体化学发光免疫检测试剂盒及其制备方法与制造工艺
- 一种抗Sm抗体IgG测定试剂盒(化学发光法)及其制备方法与制造工艺
- 抗透明带抗体化学发光免疫检测试剂盒及其制备方法与制造工艺
- 一种基于化学发光法的septin9检测试剂盒的制造方法与工艺
- 一种基于纸电化学发光芯片的POCT装置的制造方法