本发明涉及用于诊断或预测诸如冠状动脉疾病等闭塞性动脉病的标记物。
背景技术:
闭塞性动脉病由一组以动脉狭窄为特征的病理现象组成。该狭窄可影响各类动脉,尤其是冠状动脉、脑动脉、下肢动脉。闭塞性动脉病的最常见类型是冠状动脉疾病。
冠状动脉疾病(cad)是心脏病的主要类型,并且是心脏病的主要原因。cad还是世界上主要的死因之一。cad是由沿着心脏动脉内壁积累的斑块所引起的,积累的斑块使动脉变窄并使流向心脏的血液减少。患有cad的大多数个体在首次出现症状(大部分情况是心脏病)之前,几十年没有出现任何疾病的迹象,但随着疾病的发展最终会发病。
腺苷是一种内源性嘌呤核苷,其由三磷酸腺苷(atp)水解产生并在缺血期间释放到细胞外间隙中(sollevietal.,1986;paganellietal.,2000)。它通过四类g蛋白偶联受体,即a1、a2a、a2b和a3受体发挥各种生理作用。腺苷通过激活腺苷a2a受体(a2ar),是增加冠状动脉血流量的冠状血管扩张剂(olsson,1990;shryocketal.,1997)。
a2ar和较小程度的a2br参与缺血诱导的冠状动脉血管舒张(eckleetal.,2007,berwicketal.,2012,sanjanietal.,2011)。在实验性冠状动脉反应性充血期间,腺苷以剂量依赖性方式将冠状动脉血流量增加高达3倍(berwicketal.,2012)。这种血管舒张经由a2ar发生,并涉及kv和katp通道(berwicketal.,2012)。
因此,这样的冠状动脉血管舒张构成了对血氧不足或缺血期间发生o2供应下降的适应性反应(grenzetal.,2011;hedegaardetal.,2014)。在运动压力测试期间,心肌o2需求增加,这可能导致cad患者缺血。
deharoetal.(2012)报道了低a2ar表达与低腺苷血浆浓度(apc)相关,而高a2ar表达与高apc相关。因此,通过调节核苷转运蛋白的表达,a2ar表达自身部分控制细胞外apc(pinto-duarteetal.,2005)。还示出a2ar的多态性与缺血性心肌病患者的梗死面积相关(tangetal.,2007)。该a2ar的多态性与a2ar表达水平的变化相关(saadjianetal.,2009)。
跑步机(treadmill)是诊断和评估冠状动脉疾病的最常用的测试。然而,其预测价值有限(nymanetal.,1993)。特别地,尽管一些患者存在缺血负荷,但可能缺乏心电图(ecg)变化和胸痛。因此,提出使用额外的研究,如应力回波、磁共振成像(mri)和闪烁扫描,以克服这些局限。然而,它们的可用性有限且成本很高。
在闭塞性动脉病,例如冠状动脉疾病的诊断或预测中提供新的生物学标记物是有临床价值的。该标记物可进一步增加平板运动测试的预测价值。
技术实现要素:
发明人发现,特别与确定是否存在保留的a2ar(储备a2ar)和/或与确定个体在运动压力测试(est)期间apc变化相结合时,个体中在外周血单核细胞(pbmc)的细胞表面上表达的a2ar的表达水平,构成冠状动脉疾病的新型生物学标记物。此外,由于a2ar还在冠状动脉区外,包括脑部(murphyetal.,2003)和主动脉(iwamototetal.,1994),的动脉中表达,所以可能在闭塞性动脉病中发现a2ar的表达异常。
因此,本发明涉及一种诊断或预测个体中的闭塞性动脉病,尤其是冠状动脉疾病或外周闭塞性动脉病,优选冠状动脉疾病的体外方法,所述体外方法包括以下步骤:
a)确定在获自所述个体的外周血单核细胞(pbmc)的细胞表面上表达的腺苷a2a受体(a2ar)的表达水平,以及
b)将步骤a)中确定的表达水平与在先前获自所述个体的pbmc细胞表面上表达的a2ar的表达水平,或与在pbmc细胞表面上表达的a2ar的标准表达水平进行比较;
低于先前获自所述个体的a2ar的表达水平,或者低于所述a2ar的标准表达水平的步骤a)中确定的表达水平,构成闭塞性动脉病,尤其是冠状动脉疾病或外周闭塞性动脉病的标记物,或构成易患闭塞性动脉病,尤其是冠状动脉疾病或外周闭塞性动脉病的标记物。
“个体”是指哺乳动物,优选人。
闭塞性动脉病是指以导致动脉阻塞的狭窄为特征的动脉病理现象。所述阻塞可能是由于动脉粥样硬化或血栓形成。闭塞性动脉病可影响任何种类的动脉,如脑动脉(导致中风)、冠状动脉、下肢动脉。闭塞性动脉病特别是冠状动脉疾病或外周闭塞性动脉病,优选冠状动脉疾病。
冠状动脉疾病(cad)是指冠状(心脏)动脉的病理学现象,如阻塞性冠状动脉疾病。
外周闭塞性动脉病包括除冠状动脉外的血管床中的狭窄,如下肢缺血和中风。
优选地,外周血单核细胞(pbmc)是淋巴细胞。
在本发明方法的优选实施方式中,pbmc获自从个体的肱静脉收集的血液样品。该血液样品可以被收集在含有柠檬酸钠、聚酯凝胶和密度梯度液体的管中。
用于确定在pbmc细胞表面上表达的a2ar的表达水平的方法是本领域已知的(franceschietal.,2013;jacquinetal.,2013)。
在本发明方法的一个有利的实施方式中,通过蛋白质印迹法(westernblotting)确定a2ar的表达水平。
在本发明方法的另一个有利的实施方式中,可以通过使用完整(未裂解)的pbmc样品和a2arab进行流式细胞术测定(参见例如koshibaetal.,1999)来确定a2ar的表达水平。
制备和裂解pbmc的方法是本领域公知的。在裂解前,可用商业试剂盒制备pbmc。举例来说,可以使用用于蛋白质印迹法应用的缓冲液样品,直接制备pbmc:含有2%sds、10%甘油、0.01%溴酚蓝和5%巯基乙醇的62.5mmtris-hcl缓冲液,ph8.3。可以通过在47khz下施加10分钟的超声处理来裂解pbmc。
可以通过使用a2ar抗体(a2arab)的蛋白质印迹法,来确定裂解物中的a2ar的表达水平。
超声后,样品可以进行标准电泳。可将分离的蛋白质电转到膜上,然后将膜置于蛋白质检测装置的印迹架中,并与a2arab孵育。
印迹可以通过经标记的抗a2arab种类进行可视化。可对条带(人a2ar为45kda)进行密度测量。结果可以以定义成a2ar条带对印迹背景的像素的任意单位来表示。
如本文所使用的,术语“抗体”包括多克隆或单克隆抗体,天然、合成或重组的抗体,嵌合抗体如人源化抗体,及其保留了结合a2ar能力的片段(例如,fab'2、fab、fv、scfv)。全长抗体可以是五种主要类型之一:iga、igd、ige、igg和igm。将这些全长抗体中的几种进一步分为亚类或同种型,例如igg1、igg2、igg3、igg4等。不同类型的免疫球蛋白的亚基结构和三维构型是本领域公知的。本发明所使用的抗体的优选类型是igg和/或igm,因为它们是在生理状况下最常见的抗体,并且因为它们最容易在实验室环境中制备。抗体还包括免疫粘附素、双抗体、纳米抗体、janusins、微型抗体。保留了结合a2ar能力的片段抗体包括fab、fab'2、fv、scfv片段。
术语“重组(的)抗体”旨在表示通过遗传工程,例如通过克隆和基因扩增产生的抗体。
术语“合成(的)抗体”旨在表示通过酶法合成和/或化学合成产生的抗体。
术语“嵌合抗体”旨在表示来自特定动物物种或特定抗体种类的抗体,其包括来自另一物种或另一抗体种类的抗体的全部或部分重链和/或轻链。
术语“嵌合抗体”还可以表示多特异性抗体,即对至少两种不同表位具有特异性的抗体。可以从如上定义的所述抗体片段获得多特异性抗体。
术语“人源化抗体”是指如下的人免疫球蛋白,在该人免疫球蛋白中,形成抗原结合位点的cdr(互补决定区)的残基被替代成具有期望特异性、亲和力和/或活性的非人单克隆抗体中的cdr。
抗体和抗体片段可以通过本领域技术人员熟知的常规技术来制备。
a2ar抗体是本领域已知的。举例来说,可以使用抗a2ar的细胞内结构域的单克隆ab(koshibaetal.1999)或市售的多克隆a2arab,例如refssab1408884和sab1410228(sigma-aldrich)。
在一个优选的实施方式中,a2arab可使用对应于人a2ar的第二胞外环的、序列seqidno:1的30个氨基酸残基的肽免疫哺乳动物,优选小鼠来获得。由于该肽在不同物种(小鼠、大鼠、狗和人)间的保守氨基酸序列,因此具有低免疫原性。有利地,a2arab结合序列seqidno:2的线性表位。包含在序列seqidno:2中的氨基酸残基,苯丙氨酸和谷氨酸对于抗体结合是重要的(jaakolaetal.,2010)。
在另一个优选实施方式中,a2arab是根据布达佩斯条约于2014年11月7日保藏于巴黎15区75724,鲁博士路25街(25ruedudocteurroux,75724pariscedex15)的cncm,保藏编号为i-4908的杂交瘤产生的单克隆抗体。该命名为阿多尼斯(adonis)的单克隆抗体的性质描述于byetal.,2009中。
如byetal.,2009中所述,by等人用seqidno:1的肽免疫小鼠来生产阿多尼斯。by等人不得不进行了许多细胞融合和杂交瘤筛选实验,最终只得到一种可行的杂交瘤。因此,不可能使用相同的免疫方案来重新生产出该杂交瘤(和相应的阿多尼斯)。
通常,健康人(即未患有冠状动脉疾病或外周闭塞性动脉病变的人)中pbmc细胞表面上a2ar的标准表达水平(以任意单位表示)比cad患者中的a2ar表达水平高1.5至2倍。
在本发明方法的一个优选实施方式中,进一步包括确定在获自个体的pbmc,优选淋巴细胞,上是否存在储备a2ar的步骤,储备a2ar的存在构成闭塞性动脉病变,尤其是冠状动脉疾病或外周闭塞性动脉病变,优选冠状动脉疾病的另一标记物,或构成易患闭塞性动脉病变,尤其是冠状动脉疾病或外周闭塞性动脉病,优选冠状动脉疾病的另一标记物。
从药理学角度来看,在仅占用少量的可用受体时,给定的配体能发挥最大的生物学效应。这种受体保留,也称为储备受体,可以对与几种t细胞性质兼容的低、瞬时配体浓度和低亲和力的相互作用作出反应,因此支持了用于t细胞受体活化的保留受体的存在(mcneiletal.,2002)。以实用的方式,当半数最大有效浓度(ec50)低于解离常数(kd)时,确定储备受体的存在,其中半数最大有效浓度是指达到最大生物学效应(在当前情况中为pbmc产生的camp)的50%所需的配体浓度,而解离常数是指达到最大结合的50%所需的配体浓度。
用于确定是否存在储备a2ar的方法是本领域中已知的(例如,参见shryocketal.,1998)。
有利地,可以使用a2ar不可逆激动剂作为camp产生的特异性效应剂,来确定是否存在储备a2ar,并确定a2ar的ec50和kd。
不可逆激动剂是指a2ar激动剂,该a2ar激动剂至少在确定kd和ec50值所需的孵育期间稳定地结合a2ar胞外部分(jacquinetal.,2013;franceschietal.,2013)。
举例来说,可以使用pbmc与六种浓度的a2ar激动剂孵育,来建立a2ar激动剂结合曲线。可以使用适当的软件,用一个位点特异性结合方程y=bmax×x/(kd+x)进行非线性回归分析。可以估计与每一pbmc制备物结合的a2ar激动剂的bmax和kd,其中bmax以与y值相同的单位来表示,且kd以与x值相同的单位来表示。可以对与a2ar激动剂(优选用a2ar的激动剂样抗体,如市售的elisa试剂盒中的单克隆抗体阿多尼斯[见下文])孵育的pbmc,进行细胞camp的测量。可以通过加入适当的化合物,如十二烷基三甲基溴化铵乙酸盐缓冲液来终止刺激。结果可以表示为最大camp产量的百分比。使用六种浓度的a2ar激动剂获得的结果可以用合适的软件和s型剂量-反应曲线进行检查:y=底部+(顶部-底部)/(1+10[(logec50-x)×希尔斜率])。顶部(此处的emax)和底部是以y为单位的平台值,ec50是给出顶部值和底部值之间一半处的反应的a2ar激动剂的浓度。希尔斜率描述了一系列曲线的倾斜度。
a2ar激动剂可以是抗a2ar的激动剂样抗体,例如保藏于cncm,保藏编码为i-4908的杂交瘤所生产的单克隆抗体阿多尼斯。根据本发明的(见下文),名为阿多尼斯的单克隆a2arab至少在估计kd和ec50值所需的孵育期间被同化为不可逆激动剂。
术语“激动剂样抗体”是指像常规有机激动剂那样、具有活化a2ar的性质的抗体,其中有机激动剂被定义为与a2ar结合并导致靶细胞产生camp的分子。
可以通过使用a2ar的有机拮抗剂(例如fsptp)使受体失活并降低对激动剂(尤其是不可逆激动剂)的反应,以确定平衡解离常数和ec50,来确定是否存在储备a2ar(shryocketal.,1998)。
在本发明方法的另一个优选实施方式中,进一步包括由血液样品确定运动压力测试(est)期间,所述个体中的腺苷血浆浓度(apc)变化的步骤,apc在est期间的增加构成闭塞性动脉病变,尤其是冠状动脉疾病或外周闭塞性动脉病变,优选冠状动脉疾病的另一标记物,或构成易患闭塞性动脉病变,尤其是冠状动脉疾病或外周闭塞性动脉病,优选冠状动脉疾病的另一标记物。
在一个具体的实施方式中,apc的增加与阳性est相关。
阳性est指的是存在显著的st段波变化(>2mm)和st段水平或向下循环下移和/或典型的胸痛)。
该步骤可以与或不与上述确定在pbmc上是否存在储备a2ar的步骤组合进行。
如果进行该步骤,则从处于基础水平(即,在运动压力测试之前)的所述个体获得用于确定a2ar的表达水平及可选地用于确定是否存在储备a2ar的pbmc。
用于由血液样品确定个体中的apc的方法是本领域公知的(guieuetal.,1999;saadjianetal.,2002和2009;jacquinetal.,2013)。
举例来说,血液样品收集后,离心,然后脱蛋白。然后使用高压液相色谱定量腺苷。
est是本领域众所周知的,因为它是广泛使用的cad筛选方法(banerjeeetal.,2012)。est包括跑步运动,自行车运动,或下肢瘫痪患者使用手臂的自行车运动。
有利地,est是可以根据bruce方案进行的平板运动测试(bruce,1974)。在此过程中,在自行车上,从20瓦特起每分钟逐渐增加工作负荷,直至达到最大心率(220次/分钟-年龄)。还可以使用空气面罩估计o2消耗,来估计运动压力测试期间的vo2最大值。
通过在基础水平(t0)和est结束(t1)时测量apc,有利地确定apc变化。
本发明还涉及产生抗人a2ar的激动剂样单克隆抗体(称为阿多尼斯)的杂交瘤,所述杂交瘤于2014年11月7日保藏于cncm,保藏编号为i-4908。
本发明还涉及由2014年11月7日保藏于cncm、保藏编号为i-4908的杂交瘤细胞系产生的,抗人a2ar的激动剂样单克隆抗体或其片段。
本发明还涉及由保藏于cncm、保藏编号为i-4908的杂交瘤细胞所产生的激动剂样单克隆抗体的分离片段,该分离片段由所述激动剂样单克隆抗体的一个互补决定区(cdr)组成,或包括所述激动剂样单克隆抗体的一个、两个或三个cdr,优选三个cdr或六个cdr。
测定抗体中cdr的方法是本领域技术人员所熟知的(kurodaetal.,2012)。
所述分离片段可以是fab或fab'2片段。
本发明还涉及一种多肽,该多肽包括由保藏于cncm、保藏编号为i-4908的杂交瘤细胞所产生的激动剂样单克隆抗体的一个、两个、三个cdr,或六个cdr,优选三个或六个cdr。
有利地,所述分离片段或多肽能结合a2ar。
本发明还涉及一种抗人a2ar的激动剂样单克隆抗体或其片段,包括由保藏于cncm、保藏编号为i-4908的杂交瘤所产生的激动剂样单克隆抗体的三个cdr。
本发明还涉及根据本发明的抗人a2ar的激动剂样单克隆抗体或能结合a2ar的分离片段或多肽,用于在体外诊断或预测个体中的闭塞性动脉病,尤其是冠状动脉疾病或外周闭塞性动脉病,优选冠状动脉疾病中的用途。
有利地,所述抗人a2ar的激动剂样单克隆抗体由保藏于cncm,保藏编号为i-4908的杂交瘤产生。
本发明还涉及一种用于在体外诊断或预测个体中的闭塞性动脉病,尤其是冠状动脉疾病或外周闭塞性动脉病,优选冠状动脉疾病的试剂盒,包括:
-抗人a2ar的激动剂样单克隆抗体,例如由保藏于cncm、保藏编号为i-4908的杂交瘤产生的单克隆抗体,或根据本发明的能结合a2ar的分离片段或多肽,
-至少一种阳性对照,例如患有闭塞性动脉病,尤其是冠状动脉疾病或外周闭塞性动脉病,优选冠状动脉疾病的个体的pbmc裂解物,以及
-至少一种阴性对照,例如健康个体的pbmc裂解物。
除上述特征之外,本发明进一步包括从下文对本发明实施例及附图的描述中所逐渐显现出来的其它特征。
附图说明
图1显示了30例患者在基础水平(t0)、运动压力测试结束时(t1)和10分钟恢复后(t2)的腺苷血浆浓度(apc)。a:与t0相比,p<0.01。
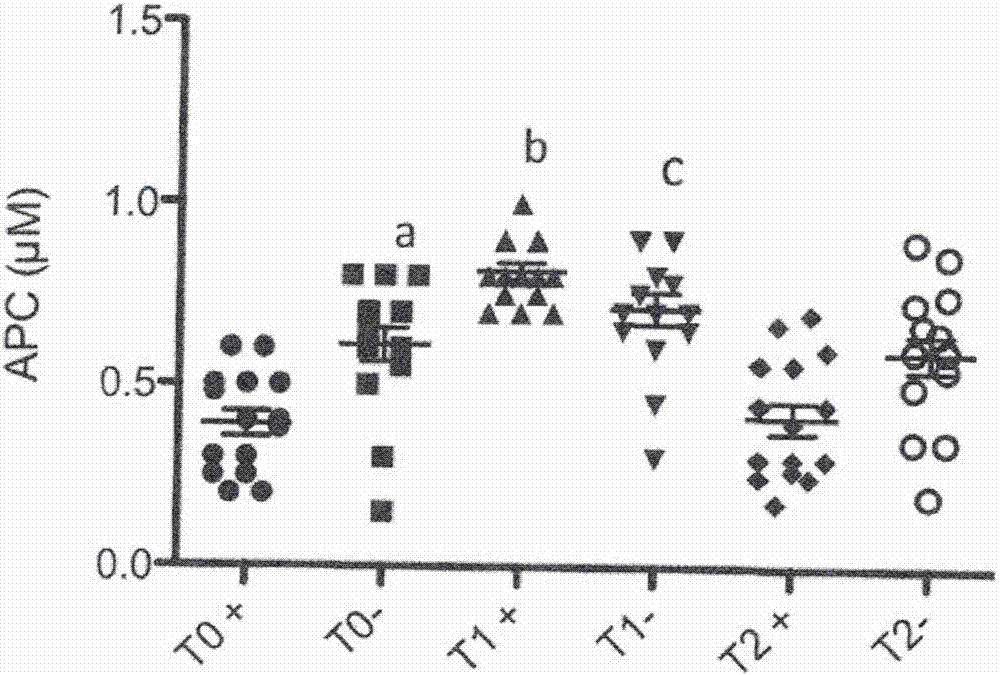
图2显示了具有阳性(+,n=15)est或阴性(-,n=15)est的患者及作为对照的15名健康个体中,在基础水平(t0)、est结束时(t1)和10分钟恢复后(t2)的apc。a:与t0+相比,p<0.01;b:与t0-相比,p=0.12。
图3显示了(a)通过蛋白质印迹法,估计了按照临床随访计划进行了est的患者(全组患者n=30),及作为对照的15名健康个体中的a2a腺苷受体表达(a2ar)。15例患者est为阳性,而15例患者est为阴性。还给出了作为阳性或阴性est及对照的函数的a2ar表达。(b):对获自阳性est(est+)、阴性est(est-)的患者及对照个体的a2ar进行的蛋白质印迹的实施例。
具体实施方式
实施例:冠状动脉疾病的诊断
1)患者及方法
患者
进行了一项包括连续发病的33例患者的单中心观察性研究(monocenterobservationalstudy):25男8女,平均年龄为62.6±13.5岁,年龄范围为33~89岁。在患者中,16例已确定为冠状动脉疾病并且作为临床随访计划的一部分进行了est,而17例作为其临床随访计划的一部分首次进行了est。15名健康个体(9名男性和6名女性,平均年龄为60±15.6岁,年龄范围为27~81岁)作为基础生物学参数的对照。
est方案
所有患者根据bruce方案进行平板运动测试(brucera1974)。当患者发生显著的st段波变化(>2mm)和st段水平或向下循环下移和/或典型的胸痛时,则认为est是阳性的。
apc测量
在真空下,使用含有2ml冷终止液的实验室制管子收集血液样品(3ml)并如前所述(saadjianetal.,2002;deharoetal.,2012)进行处理。终止液由以下物质构成:含有0.2mm双嘧达莫的盐酸;乙二胺四乙酸二钠(na2edta4mm);赤-9-(2-羟基-3-壬基腺嘌呤(ehna,5mm);α,β-亚甲基腺苷5'二磷酸(aopcp,79mm);2'脱氧柯福霉素10μg/ml;和硫酸肝素1iu/ml。
这种方法允许全血与终止液快速混合,从而防止红细胞摄取和腺苷降解(guieuetal.,1999,saadjianetal.,2002,deharoetal.,2012,bonelloetal.,2013)。对于患者,在基础水平、est结束时及10分钟恢复期后收集样品。
已描述了apc剂量(guieuetal.,1999;saadjianetal.,2002)。简言之,收集后,将样品快速离心(4℃,1500g),然后脱蛋白(高氯酸,70%1/10v)。再次离心(2500g,10分钟)后,移出上清液,将其与1ml磷酸盐缓冲液混合,并用hplc进行分析。使用具有二极管阵列检测器(chromsystem,德国)的模块化系统。在mercklichrospherc18柱(nottingham,uk)上用甲醇梯度(60分钟内从0%至35%)洗脱样品。用洗脱时间和光谱来鉴定腺苷,并通过与已知量腺苷的峰面积进行比较,来定量。灵敏度阈值为2nm血浆基质。分析内和分析间变化系数范围为1%至3%。
外周血单核细胞上的a2ar表达
选择pbmc是因为,在外周血单核细胞(pbmc)表面上表达a2ar的行为反映了这些受体在心血管系统的细胞上的行为(varanietal.,2003)。已经描述了该方法(franceschietal.,2013;jacquinetal.,2013)。简言之,在基础水平将来自患者肱静脉的血液样品收集到含有柠檬酸钠、聚酯凝胶和密度梯度液体的管中(bdvacutainercpt,becktondickinson,富兰克林湖,nj)。根据制造商的说明书制备pbmc,之后使用含有2%sds、10%甘油、0.01%溴酚蓝和5%巯基乙醇的62.5mmtris-hcl缓冲液ph8.3裂解,接着在47khz下超声处理10分钟。通过蛋白质印迹法,使用命名为阿多尼斯的抗a2ar的单克隆抗体确定裂解物中的a2ar表达(byetal.,2009)。超声处理后,样品在miniproteanii系统(biorad,hercules,ca)中进行标准电泳。将12%丙烯酰胺微型凝胶中的分离的蛋白质电转到pvdf膜上,然后将其置于snapi.d.蛋白质检测系统(millipore,billerica,ma)的印迹架中,用脱脂奶粉饱和,并与阿多尼斯(1μg/ml)孵育20分钟。使用柯达系统,通过辣根过氧化物酶标记的抗小鼠抗体和增强的化学发光底物(supersignalwestfemto,piercebiotechnology,rockford,il)使印迹可视化。使用美国国立卫生研究院开发的imagej1.42q软件,对条带(a2ar为45kda)进行密度测量。结果以定义成a2ar条带对印迹背景的像素的任意单位来表示。
统计分析
使用中位数和四分位数或平均值和标准偏差(sd),表示定量的变量。方差分析(双因素方差分析)用于比较apc和a2ar表达。威尔科克森检验(wilcoxontest)通过邦费罗尼校正(bonferronicorrection)用于配对比较,以解释i型误差的膨胀。所有统计检验均为双侧的,p值小于0.05被认为具有统计学意义。使用软件进行分析。
2)结果
患者的临床特征在下表1中给出。运动压力测试的结果在下表2中给出。表i:患者基线特征n=30。cabg:冠状动脉旁路移植;cad:冠状动脉疾病;pci:经皮冠状动脉介入治疗
表2:压力测试结果。数据以中位数和四分位数范围表示。
十五例est为阳性,十五例为阴性,一例可疑病例并在进一步调查中被排除在外。一名患者无法达到最大心率。
在基础水平上,全组患者(n=30)的apc(μm)(中位数[25%~75%])为0.6[0.5~0.7],其与对照:0.6[0.5~0.7]无显著差异;p=0.7。参见图2,基础的est-或est+患者的apc与对照无显著差异:est-:0.65[0.55~0.7]比对照;p=0.7,est+:0.6[0.5~0.6]比对照;p=0.7。在est期间,apc在全组患者中显著增加,0.6[0.5~0.7]比0.8[0.7~0.9],p=0.0002。然而,该增加限于est+患者,0.6[0.5~0.6]比0.80[0.75~0.9];p<0.01。参见图2,apc在est-组中未显著增加,0.65[0.55~0.7]比0.70[0.65~0.9];p=0.12。参见图1,在10分钟恢复后,apc回到基础值,0.52[0.31~0.63]。
全组患者中,a2ar表达量(任意单位,au)低于对照,22.5[19~29]比30[26.75~32.25];p=0.005(参见图3)。然而,低a2ar表达限于est+患者,19[16~21.25];与对照相比p<0.0001。参见图3,est-患者的a2ar表达与对照无显著差异,29[26~32.25];p=0.75。
3)结论
这些结果表明,阳性平板运动测试患者具有比阴性平板运动测试患者低的a2ar表达,且与阴性平板运动测试患者相比,在峰值运动处apc显著增加。这种增加可能与阻塞性冠状动脉疾病患者在est期间发生的心肌缺血过程有关。
本研究表明低基础的a2ar表达和平板运动期间apc的增加,与阳性est和冠状动脉疾病相关。
由于100%的cad患者也具有低基础的a2ar表达,因此本研究表明单核细胞的低a2ar表达水平与cad有关。因此,对单核细胞的基础a2ar表达的测量对筛选cad患者是有用的。
参考文献
banerjeea,etal.,intjclinpract.2012;66:477-92.
berwickzc,etal.,jmolcellcardiol.2012;52:912-9.
bonellol,etal.,jamcollcardiol.2014;63:872-7.
brucera.listingrescardiovascularfield.1964;10:283-6.review.
brucera.methodsofexercisetesting.steptest,bicycle,treadmill,isometrics.amjcardiol.1974may20;33(6):715-20.
byy,etal.,molimmunol.2009;46:400-5.
deharojc,etal.,heart.2012;98:855-9.
ecklet,etal.,circulation.2007;115:1581-90.
franceschif,etal.,europace.2013;15:1328-32.
grenza,etal.,antioxidredoxsignal.2011;15:2221-34.
guieur,etal.,jliqchromatogr.1999;22:1829-1841.
hedegaarder,etal.,eurjpharmacol.2014;723:216-26.
iwamototetal.biochembiophysrescommun.1994;199:905-10.
jaakolavpetal.,jbc.2010;285:13032-44.
jacquinl,etal.,febsopenbio.2013;3:1-5.
koshibametal.,molpharmacol.1999;55:614-24.
kurodad,etal.,proteinengdessel.2012;25:507-21
mcneillk,etal.,proc.natl.acad.sci.usa.2002;99:4520–4525.
murphyketal.molpharmacol.2003;64:640-9.
nymani,internationaljournalofcardiology.1993;39:131-42.
olssonra,etal.,physiolrev.1990;70:761-845.
paganellif,etal.,eurjclininvest.2000;30:105-10.
pinto-duartea,etal.,jneurochem.2005;93:595-604.
saadjianay,etal.,circulation.2002;106:569-74.
saadjianay,etal.,eurheartj.2009;30:1510-5.
sanjanims,etal.,amjphysiolheartcircphysiol.2011;301:h2322-33.
shryockjc,etal.,amjcardiol.1997;79:2-10.review.
shryockjc,etal.,circulation.1998;98:711-8.
sollevia.etal.,progneurobiol.1986;27:319-49.review.
tangz,etal.,clinpharmacolther.2007;82:435-40.
varanik,etal.,fasebj.2003;17:280-2.
序列表
<110>艾克斯-马赛大学
马赛公立援助医院
国立健康与医学研究所
吉恩·拉夫
瑞吉斯·归尤
弗兰克·帕加内利
劳伦特·博内洛
乔瓦那·莫托拉
娜塔丽·克普森
<120>闭塞性动脉病的诊断
<130>xrnclgf2245-12pct
<150>ep14306885.6
<151>2014-11-26
<160>2
<170>patentinversion3.5
<210>1
<211>30
<212>prt
<213>人类
<400>1
asnasncysglyglnprolysgluglylysasnhisserglnglycys
151015
glygluglyglnvalalacysleuphegluaspvalvalpro
202530
<210>2
<211>7
<212>prt
<213>人类
<400>2
leuphegluaspvalvalpro
15
pct/ro/134表