铁氰化钾在检测头孢氨苄中的应用的制作方法
本发明涉及头孢氨苄检测技术,具体涉及铁氰化钾在检测头孢氨苄中的应用。
背景技术:
头孢氨苄(cefalexin,CEX)是一种β-内酰胺类抗生素,具有抗菌谱广、无交叉耐药性、低残留、毒副作用小等特点,广泛用于临床医学、兽医界。因此,对头孢氨苄的测定研究具有重要的意义。目前,已报道的头孢氨苄的测定方法有:高效液相色谱法、光化学荧光分析法、旋光法、限度检测方法等。
技术实现要素:
本申请建立了以铁氰化钾为探针利用分光光度法测定头孢氨苄的新方法,通过正交实验优化了测定条件。研究表明:Fe(III)被头孢氨苄还原,生成的Fe(II)与K3[Fe(CN)6]反应生成可溶性的普鲁士蓝,通过测定普鲁士蓝KFeⅢ[FeⅡ(CN)6]的吸光度可以得到头孢氨苄的含量。与其他方法相比,该方法具有操作简便、快速、分析成本低等优点。
附图说明
图1是以蒸馏水为基线测得混合物抽滤后的清液的吸收光谱。
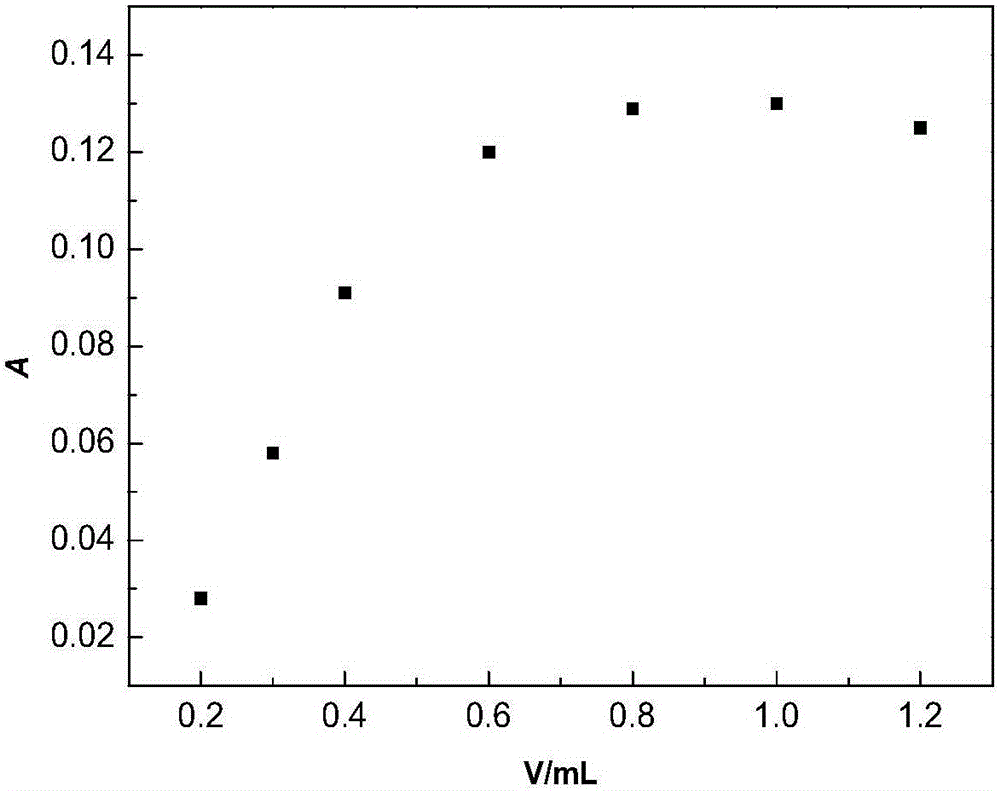
图2是三氯化铁的量对吸光度的影响。
图3是铁氰化钾的量对吸光度的影响。
图4是温度对吸光度的影响。
图5是时间对吸光度的影响。
图6是标准曲线。
具体实施方式
下面结合附图对本发明做详细说明。
1实验部分
1.1仪器与试剂
表1主要仪器
表2主要试剂
1.2主要药品和试剂
取整瓶头孢氨苄药片研磨,用分析天平称量0.5481g药品在烧杯中溶解,并在500mL容量瓶中定容,配制成1.096g/L的标准储备液,在遮光,密封,凉暗处(不超过20℃)保存;准确称量2.4695g的K3[Fe(CN)6],溶解于小烧杯中,用蒸馏水定容于500mL容量瓶中,其浓度为1.5×10-2mol/L;准确称量2.0275g的FeCl3,溶解于小烧杯中,用蒸馏水定容于500mL容量瓶中,其浓度为1.5×10-2mol/L;pH=4.6的醋酸—醋酸钠缓冲溶液;所用水均为蒸馏水;其他试剂均为分析纯。
1.3实验方法
分别移取1.00mL、1.5×10-2mol/L的K3[Fe(CN)6]和3.00mL、1.5×10-2mol/L的FeCl3及3.00mL1.096g/L的头孢氨苄于50mL比色管中,用新煮沸冷却的蒸馏水稀释至刻度,摇匀于50℃下反应40min,以试剂空白为参比,于700nm处测定吸光度。
1.4实验原理
根据查阅文献(刘礼涛.多种还原性药物的测定与分析研究[D].河南师范大学硕士学位论文,2011:25~43.),噻嗪基团中的S原子易失去电子而被氧化成亚砜,与其结构相似的头孢氨苄中噻嗪环上的S原子也应具有还原性。根据一定量的头孢氨苄加入到Fe(III)与K3[Fe(CN)6]混合体系中,溶液由浅黄色Fe(III)转变为深蓝色这一实验现象,表明头孢氨苄可将Fe(III)还原为Fe(II),还原生成的Fe(II)可与K3[Fe(CN)6]反应生成可溶性的普鲁士蓝KFeⅢ[FeⅡ(CN)6]。因此,反应机理推断如下:
Fe(III)将头孢氨苄结构中的噻嗪环上的S原子氧化为亚砜,根据电子得失关系可推测头孢氨苄与Fe(III)反应化学计量之比为1:2。被头孢氨苄噻嗪环上的S原子还原生成的Fe(II)与K3[Fe(CN)6]生成可溶性普鲁士蓝。
Fe(II)+K3[Fe(CN)6]→KFeⅢ[FeⅡ(CN)6]
通过测定溶液中可溶性普鲁士蓝KFeⅢ[FeⅡ(CN)6]的吸光度,可以测定头孢氨苄的含量。
1.5吸收光谱
以蒸馏水为参比,按照方法1.3分别测得空白试剂FeCl3—K3[Fe(CN)6]、头孢氨苄的吸收光谱。再以FeCl3—K3[Fe(CN)6为参比,分别测得头孢氨苄与FeCl3—K3[Fe(CN)6]的反应产物(可溶性普鲁士蓝KFeⅢ[FeⅡ(CN)6])、抽滤过的牛奶清液及其显色剂、头孢氨苄与牛奶混合物抽滤后的清液的吸收光谱。从图1中可以看出以蒸馏水为基线测得:曲线1是FeCl3—K3[Fe(CN)6]的吸收光谱,曲线2是头孢氨苄的吸收光谱,曲线3是头孢氨苄与FeCl3—K3[Fe(CN)6]反应产物(可溶性普鲁士蓝)的吸收光谱,曲线4是不含头孢氨苄的经过抽滤处理的牛奶样品的吸收光谱,曲线5是含头孢氨苄的经过抽滤处理的牛奶样品产物的吸收光谱。从图1中可以看出Fe(III)在420nm时有较大吸收,而在700nm处无明显吸收。反应生成物质的最大吸收波长为700nm,头孢氨苄在500~800nm范围内没有吸收,试剂空白在700nm处有比较小的吸收。为了消除其他试剂对吸光度的干扰,本实验以试剂空白为参比,测定700nm处生成物普鲁士蓝的吸光度而确定头孢氨苄的含量。
2.结果
2.1不同条件对吸光度的影响
2.1.1三氯化铁的量对吸光度的影响
固定其它条件不变,向七组比色管中均加入3.00mL、1.096g/L的头孢氨苄,1.00mL、1.5×10-2mol/L的K3[Fe(CN)6]。再分别向七组比色管中加入0.20mL、0.30mL、0.40mL、0.60mL、0.80mL、1.00mL、1.20mL的FeCl3,用蒸馏水定容至25mL。在20℃下反应40min,测得相应的吸光度分别为:0.028、0.058、0.091、0.12、0.129、0.130、0.125。由图2可知,吸光度随着FeCl3用量的增加先增大而后减小,在1.00mL处达到最大值。进而我们可以看出在3.00mL、1.096g/L的头孢氨苄溶液,1.00mL、1.5×10-2mol/L的K3[Fe(CN)6]和1.00mL、1.5×10-2mol/L的FeCl3反应时,此时吸光度达到最大,经计算反应比也接近1:2,说明实验原理推断的正确性。图2中头孢氨苄(1.096g/L):3.00mL;K3[Fe(CN)6](0.015mol/L):1.00mL;反应温度:20℃;反应时间:30min;总体积:25mL。
2.1.2铁氰化钾的量对吸光度的影响
固定其它条件不变,向九组比色管中均加入3.00mL、1.096g/L的头孢氨苄,1.00mL、1.5×10-2mol/L的FeCl3。再分别向九组比色管分别中加入0.10mL、0.15mL、0.20mL、0.30mL、0.40mL、0.60mL、0.80mL、1.00mL、1.20mL的K3[Fe(CN)6],用蒸馏水定容至25mL。在20℃下反应40min,测得相应的吸光度分别为:0.092、0.126、0.154、0.191、0.224、0.237、0.231、0.221、0.216。由图3可见,吸光度随着K3[Fe(CN)6]的用量的增加先增大后减小。
2.1.3温度对吸光度的影响
固定其它条件不变,向八组比色管中均加入3.00mL、1.096mol/L的头孢氨苄,1.00mL、1.5×10-2mol/L的FeCl3,1.00mL、1.5×10-2mol/L的K3[Fe(CN)6]。将八组比色管分别置于20℃、30℃、40℃、50℃、60℃、70℃、80℃、90℃、的水浴锅中40min。测得吸光度分别为0.084、0.160、0.268、0.349、0.588、0.719、0.868、1.021。由图4可知,吸光度随着温度的增大而增大。
2.1.4时间对吸光度的影响
固定其它条件不变,向九组比色管中均加入3.00mL、1.096g/L的头孢氨苄,1.00mL、1.5×10-2mol/L的FeCl3,1.00mL、1.5×10-2mol/L的K3[Fe(CN)6],用蒸馏水定容至25mL。在20℃下分别反应10min、20min、30min、40min、50min、60min、70min、80min、90min。测得吸光度分别为0.112、0.168、0.214、0.292、0.353、0.388、0.410、0.426、0.445,由图5分析可知,随着时间的推移吸光度是逐渐增大的。
2.2正交实验
根据以上实验结果,我们选择三氯化铁的量、铁氰化钾的量、反应时间、温度这四个因素作为研究对象进行正交实验。
如表3,构成了L16(4)4正交实验表;
如表4,测得实验数据并得出实验结果。
表3因素水平
表4正交实验数据
极差的大小顺序为Rd>Ra>Rb>Rc,最优方案为:A4 B2 C4 D3C。从表中可以看出影响因素最大的是温度,取加和最大的水平作为最佳条件。正交法得出的最优方案为:3.00mL、1.5×10-2mol/L的K3[Fe(CN)6],反应时间为40min、反应温度为50℃。在最优方案下,利用分光光度法完成了对头孢氨苄的测定。
2.3标准曲线
配制一系列头孢氨苄的标准溶液,其浓度分别为:8.77μg/mL、21.92μg/mL、35.08μg/mL、43.85μg/mL、52.62μg/mL、65.77μg/mL、78.93μg/mL、96.47μg/mL、109.62μg/mL、122.78μg/mL、135.56μg/mL、153.47μg/mL、166.63μg/mL、171.65μg/mL、188.96μg/mL、197.45μg/mL。按照方法2.2测量反应溶液的吸光度分别为0.078、0.166、0.345、0.374、0.438、0.534、0.633、0.726、0.854、0.924、1.044、1.184、1.299、1.411、1.621、1.798。以吸光度A与相应的头孢氨苄浓度c进行线性回归。头孢氨苄在80~160μg/mL范围内与吸光度呈现良好线性关系。线性回归方程为A=0.03281+0.00749c(μg/mL),线性相关系数R=0.9982。
2.4精密度检测
按照分析步骤平行测定12份试液,其吸光度分别为0.708、0.708、0.710、0.710、0.711、0.710、0.710、0.710、0.711、0.710、0.709、0.710,根据测得的吸光度求得其相对标准偏差为:δ=9.57×10-4。
2.5检出限的测定
按照分析步骤平行测定12份试剂空白试液,即:只在比色管中加入3.00mL、1.5×10-2mol/L的FeCl3,1.00mL、1.5×10-2mol/L的K3[Fe(CN)6],用蒸馏水定容至25mL,测得其吸光度分别为:0.643、0.643、0.642、0.642、0.642、0.643、0.643、0.642、0.642、0.642、0.642、0.641,求得标准偏差σ=5.95×10-4,由3σ/k(k为线性回归方程的斜率)计算检出限为0.2384μg/mL。2.6样品的制备与分析
2.6.1头孢氨苄样品的分析
分别移取2.28mL、2.74mL、3.65mL1.096g/L的头孢氨苄溶液于3支25mL比色管中,然后依次向每支比色管加入3.00mL FeCl3溶液、1.00mL K3[Fe(CN)6]溶液,用蒸馏水定容后在50℃恒温水浴中加热40min,然后对同一浓度的样品平行测定3次,进行加标回收实验(参比为不含药品的空白试剂),如表5。
表5样品及回收率的测定
FeCl3(0.015mol/L):3.00mL;K3[Fe(CN)6](0.015mol/L):1.00mL;
反应温度:50℃;反应时间:40min;总体积:25mL
2.6.2牛奶样品的制备及牛奶中头孢氨苄的测定
取4个小烧杯和4支比色管并编号。分别移取1.00mL新鲜纯牛奶至4个小烧杯中,再移取1.84mL、1.096g/L的头孢氨苄溶液至1、2、3号烧杯,移取1.00mL、pH=4.6的HAc-NaAc缓冲溶液至4个小烧杯,混合均匀后静置10min,烧杯中牛奶产生白色絮状沉淀。用循环水式多用真空泵对混合溶液进行抽滤,将抽滤后的清液倒入25mL比色管中,再用缓冲液冲洗抽滤瓶,将冲洗液也倒入比色管中,然后分别移取移取0.46mL、0.86mL、1.76mL 1.096g/L的头孢氨苄溶液于1、2、3号比色管中,再依次向每支比色管中加入3.00mLFeCl3、1.00mLK3[Fe(CN)6],用蒸馏水定容后在50℃恒温水浴中加热40min,以4号比色管为参比,对同一浓度的样品平行测定3次,进行加标回收实验,测定结果如表6。
表6牛奶中样品及回收率的测定
FeCl3(0.015mol/L):3.00mL;K3[Fe(CN)6](0.015mol/L):1.00mL;反应温度:50℃;
反应时间:40min;牛奶:1.00mL;pH=4.6的缓冲液:1.00mL;总体积:25mL
本申请采用分光光度实验对头孢氨苄进行分析,在铁氰化钾存在条件下,头孢氨苄可将三氯化铁中的Fe(III)还原为Fe(II),还原生成的Fe(II)与铁氰化钾反应生成可溶性的普鲁士蓝,其最大吸收波长为700nm。头孢氨苄在80~160μg/mL的浓度范围内与吸光度呈现良好的线性关系,线性回归方程为A=0.03281+0.00749c(μg/mL),线性相关系数R=0.9982,检出限为0.2384μg/mL。通过正交实验,确定最优方案为:3.00mL、1.5×10-2mol/L的FeCl3,1.00mL、1.5×10-2mol/L的K3[Fe(CN)6],反应时间为40min、反应温度为50℃。
实验结果表明此法可直接用于片剂头孢氨苄含量的测定,结果满意;同时,也可应用于对牛奶中头孢氨苄残留的检测,该方法的建立对实现牛奶质量的监测具有重要现实意义。
以上显示和描述了本发明的基本原理和主要特征和本发明的优点。本行业的技术人员应该了解,本发明不受上述实施例的限制,上述实施例和说明书中描述的只是说明本发明的原理,在不脱离本发明精神和范围的前提下,本发明还会有各种变化和改进,这些变化和改进都落入要求保护的本发明范围内。本发明要求保护范围由所附的权利要求书及其等效物界定。
- 还没有人留言评论。精彩留言会获得点赞!