一种基于具有拉曼和荧光双重信号的金‑上转换空间四面体结构的制备及应用的制作方法
本发明涉及一种基于具有拉曼和荧光双重信号的金-上转换空间四面体结构的制备及其应用,属于癌症标志物的检测技术领域。
背景技术:
癌症是一直困扰着医学界的一大难题,近年来,癌症的基础和临床研究得到广泛关注,但治疗方面始终面临许多难题。目前,以纳米材料为基础的癌症检测得到广泛关注,利用纳米材料的光学、结构等特性,能够实现癌症的早期检测和治疗,将其用于临床,是目前化学、生物、医学等专家的共同努力方向并且取得了巨大进步。
用DNA对纳米材料进行组装具有独特的优势。DNA 分子的这种结构能够特异性的用于生物分子的识别并且具有很高的特异性,因此可以精确控制纳米颗粒之间的距离以及纳米组装体的几何构型。适配体是一种能特异性识别癌症标志物的特殊DNA序列,可将用适配体组装的组装体用于癌症标志物的识别和检测。
金纳米颗粒是目前应用最为广泛的一种等离子体纳米材料,其最重要的光学特性是能够在可见光区内产生强烈的吸收峰,根本原因是发生了表面等离子体共振效应(Surface Plasmon Resonance,SPR)。另外,由于金纳米颗粒本身在细胞内不会产生危害,并且具有很好的荧光性、导电性和催化性质等,基于金纳米颗粒的组件已广泛应用于光学材料、生物传感器、小型化光学设备以及癌症早期诊断及药物传递等领域。
上转换纳米材料由于其独特的光学性能,即采用红外或近红外光(通常为980nm激光)激发,在可见光范围内发射,从而可有效避免生物体系自发荧光干扰,已成为生物分子分析检测以及细胞、活体成像等相关领域的研究热点。
技术实现要素:
本发明的目的是提供一种基于具有拉曼和荧光双重信号的金-上转换空间四面体结构的制备方法,并提供一种利用荧光、拉曼双重信号同时检测两种癌症标志物(前列腺特异抗原和凝血酶)的方法。
本发明的技术方案:本发明包括金纳米粒子的合成、金纳米粒子和上转换纳米粒子表面修饰适配体以及DNA核酸探针、金纳米粒子和上转换纳米粒子组装成空间四面体结构、修饰信标分子,将组装好的四面体结构与癌症标志物混合,实现金或上转换纳米粒子的脱落,通过观察拉曼和荧光信号的变化来确定癌症标志物的浓度。
(1)金纳米粒子的合成:
20nm粒径金纳米粒子的合成:采用柠檬酸钠还原合成法合成;在洁净的250mL的锥形瓶中加195mL超纯水,加5mL质量浓度0.4%的氯金酸溶液,搅拌并加热至沸腾,7-8min 后加4.5mL质量浓度1%的柠檬酸三钠溶液,至溶液从无色变为酒红色后,停止加热,继续搅拌,直至冷却至室温,即得到粒径为20nm的金纳米粒子。
(2)金-上转换空间四面体结构的组装
a、将步骤(1)制备所得的1mL的金纳米粒子溶液以8000rpm离心10min,除去上清,沉淀重悬于100μL1×TBE缓冲液中,得到金纳米粒子TBE溶液;
b、市售的上转换纳米粒子,从北京万德高科技发展有限公司购买,表面修饰了马来酰亚胺,能与巯基DNA偶联。取浓度为5×10-7mol/L上转换纳米粒子2μL,用1×TBE缓冲液稀释50倍得100μL 上转换纳米粒子TBE稀释溶液;
c、取两组步骤a的金纳米粒子TBE溶液各100μL,分别向其中加入10μM的凝血酶适配体(Apt 1)溶液及10μM DNA 1溶液各2μL(实验中使用的适配体Apt 1和普通DNA均为生工生物工程(上海)股份有限公司合成),混合均匀,得到Au 1及Au 2;取步骤b制备的上转换纳米粒子TBE稀释溶液两组,各100μL,分别向其中加入10μM的前列腺特异抗原适配体(Apt 2)溶液及10μM DNA 2溶液各2μL,并混合均匀,得到UCNP 1及UCNP 2;向Au 1、Au 2、UCNP 1、UCNP 2中各加入1μL 5mM的NaNO3溶液,混合均匀,37℃震荡12h,从而得到修饰了适配体及DNA的金及上转换纳米粒子;
d、将步骤c所得的Au 1及Au 2以8000rpm离心10min,UCNP 1及 UCNP 2以8000rpm离心15min,除去多余的未偶联的适配体及DNA,用1×TBE缓冲液重悬到原来的体积;将重悬后的Au 2、UCNP 2、2μL浓度为10μM DNA 3、2μL浓度为10μM DNA 4混合,再加入1μL浓度为5M的MgCl2溶液,混合均匀,在 90℃水浴中加热5min,自然冷却至室温,得到金-上转换二聚体;将其4000rpm离心10min,去掉上清,用1×TBE缓冲液重悬至原体积,除去未杂交的纳米粒子和多余DNA;
e、向步骤d得到的二聚体中加入Au 1和UCNP 1各100μL,加入4μL浓度为5M 的NaNO3溶液,震荡12h,得到金-上转换空间四面体结构,并用透射电镜表征其结构。
检测用适配体及DNA核酸探针的设计与合成,均为生工生物工程(上海)股份有限公司合成:
Apt 1 5’-SH-GGAATCTACG GTTGGTGTGG TTGGATCGTC CGA-3’;
Apt2:5’-SH-CGATGGCATA TTAAAGCTCG CCATCAAATA GCGTGGCCTG G-3’;
DNA 1:
5’-SH-GAGTCCGTCG GACGATGCGT AGATTCCTTT CGCGCACCTG AGACCTTCTA ATAGGGTTTG CGACAGTCGT TCAACTAGAA TGCCC-3’;
DNA 2:
5’-SH-CAATCTGCCA GGCCACTAAT GCCATCGTTT GGGCTGTTCC GAGTGTGGCT CGTCGGTTTG GGCATTCTAG TTGAACGACT GTCGC-3’;
DNA 3:
5’-AGATTGTTTC CCTATTAGAA GGTCTCAGGT GCGCGTTTCG GTAAGTAGAC GGGACCAGTT CGCC-3’;
DNA 4:
5’-GGACTCTTTC CGACGAGCCA CACTCGGAAC AGCCCTTTGG CGAACTGGTC CCGTCTACTT ACCG-3’。
(3)信标分子的修饰:将组装得到的金-上转换空间四面体结构与终浓度为10nM的4-氨基苯硫酚(4-ATP)混合,室温反应8h,得到具有拉曼和荧光双重信号的金-上转换空间四面体结构。
基于具有拉曼和荧光双重信号的金-上转换空间四面体结构的应用,用于癌症标志物前列腺特异抗原溶液及凝血酶溶液的检测,将组装好的具有拉曼和荧光双重信号的金-上转换空间四面体结构与癌症标志物混合,实现金或上转换纳米粒子的脱落,通过观察拉曼和荧光信号的变化来确定癌症标志物的浓度。
癌症标志物前列腺特异抗原溶液及凝血酶溶液的检测:
a、配置浓度为0-100 aM(10-15mol/L)前列腺特异抗原溶液,与金-上转换空间四面体结构以体积比为1︰100混合,室温下反应8h,使癌症标志物前列腺特异抗原与适配体结合,上转换纳米粒子脱落,测定组装体的荧光信号。
b、配置浓度为0-1000 fM(10-12mol/L)的凝血酶溶液,与金-上转换空间四面体结构以体积比为1︰100混合,室温下反应8h,使癌症标志物凝血酶与适配体结合,金纳米粒子脱落,测定修饰了4-ATP的组装体的拉曼信号。
本发明的有益效果:本发明提供了一种基于修饰了适配体的金-上转换空间四面体结构与癌症标志物结合后光学信号的改变,实现了对两种癌症标志物前列腺特异抗原及凝血酶的同时检测,此方法具有工作量少、操作简便、灵敏度高等优点。
附图说明
图1是本发明金-上转换空间四面体结构的电镜图。
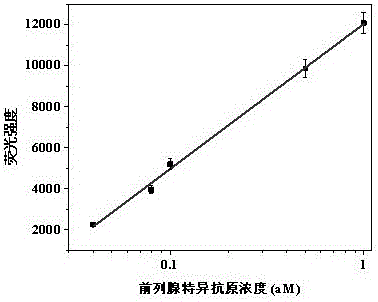
图2是前列腺特异抗原(PSA)检测的标准曲线。
图3是凝血酶(thrombin)检测的标准曲线。
具体实施方式
(1)金纳米粒子的合成:20nm的金纳米粒子采用柠檬酸钠还原合成法合成;在洁净的250mL的锥形瓶中加195mL超纯水,加5mL质量浓度0.4%的氯金酸溶液,搅拌并加热至沸腾,7-8min 后加4.5mL质量浓度1%的柠檬酸三钠溶液,至溶液从无色变为酒红色后,停止加热,继续搅拌,直至冷却至室温,即得到粒径为20nm的金纳米粒子。
(2)金-上转换空间四面体结构的组装
a、将步骤(1)制备所得的1mL的金纳米粒子溶液以8000rpm离心10min,除去上清,沉淀重悬于100μL 1×TBE缓冲液中,得到金纳米粒子溶液;
b、取从北京万德高科技发展有限公司购买的上转换纳米粒子,表面修饰了马来酰亚胺,能与巯基DNA偶联。取浓度为5×10-7mol/L上转换纳米粒子2μL用1×TBE缓冲液稀释50倍得100μL 上转换纳米粒子TBE稀释溶液;
c、取两组步骤a的金纳米粒子TBE溶液各100μL,分别向其中各加入10μM的凝血酶适配体(Apt 1)溶液及10μM DNA 1溶液各2μL,混合均匀,得到Au 1及Au 2;取步骤b制备的上转换纳米粒子TBE稀释溶液两组,各100μL,分别向其中加入10μM的前列腺特异抗原适配体(Apt 2)溶液及10μM DNA 2溶液各2μL,并混合均匀,得到UCNP 1及 UCNP 2;向Au 1、Au 2、UCNP 1、UCNP 2中各加入1μL 5mM的NaNO3溶液,混合均匀,37℃震荡12h,从而得到修饰了适配体及DNA的金及上转换纳米粒子;
d、将步骤c所得的Au 1及Au 2以8000rpm离心10min,UCNP 1及UCNP 2以8000rpm超滤15min,除去多余的未偶联的适配体及DNA,用1×TBE缓冲液重悬到原来的体积。将重悬后的Au 2、 UCNP 2、2μL10μM DNA 3、2μL10μM DNA 4混合,加入1μL 5M 的MgCl2溶液,混合均匀,在 90℃水浴中加热5min,自然冷却至室温,得到金-上转换二聚体。4000rpm离心10min,去掉上清,用1×TBE缓冲液除重悬至原体积,除去未杂交的纳米粒子和多余DNA。
e、向步骤d得到的二聚体中加入Au 1和UCNP 1各100μL,加入4μL 5M 的NaNO3溶液,震荡12h,得到金-上转换空间四面体结构,并用透射电镜表征其结构,具体结构如图1所示。
(3)检测用核酸探针的设计与合成
Apt 1: 5’-SH-GGAATCTACG GTTGGTGTGG TTGGATCGTC CGA-3’;
Apt2:
5’-SH-CGATGGCATATTAAAGCTCGCCATCAAATAGCGTGGCCTGG-3’;
DNA 1:
5’-SH-GAGTCCGTCG GACGATGCGT AGATTCCTTT CGCGCACCTG AGACCTTCTA ATAGGGTTTG CGACAGTCGT TCAACTAGAA TGCCC-3’;
DNA 2:
5’-SH-CAATCTGCCA GGCCACTAAT GCCATCGTTT GGGCTGTTCC GAGTGTGGCT CGTCGGTTTG GGCATTCTAG TTGAACGACT GTCGC-3’;
DNA 3:
5’-AGATTGTTTC CCTATTAGAA GGTCTCAGGT GCGCGTTTCG GTAAGTAGAC GGGACCAGTT CGCC-3’;
DNA 4:
5’-GGACTCTTTC CGACGAGCCA CACTCGGAAC AGCCCTTTGG CGAACTGGTC CCGTCTACTT ACCG-3’。
(4)信标分子的修饰:将组装得到的金-上转换空间四面体与终浓度为10nM的4-氨基苯硫酚(4-ATP)混合,室温反应8h。
(5)癌症标志物的检测:
a、配置浓度为0-100 aM前列腺特异抗原溶液,与金-上转换空间四面体以体积比为1:100混合,室温下反应8h,使癌症标志物与适配体结合,上转换纳米粒子脱落,测定组装体的荧光信号,具体如图2所示。
b、配置浓度为0-1000 fM的凝血酶溶液,与金-上转换空间四面体以体积比为1:100混合,室温下反应8h,使癌症标志物与适配体结合,金纳米粒子脱落,测定修饰了4-ATP的组装体的拉曼信号,具体如图3所示。
Apt 1:5’-SH-GGAATCTACG GTTGGTGTGG TTGGATCGTC CGA-3’
Apt 2:5’-SH-CGATGGCATA TTAAAGCTCG CCATCAAATA GCGTGGCCTG G-3’
DNA 1:5’-SH-GAGTCCGTCG GACGATGCGT AGATTCCTTT CGCGCACCTG AGACCTTCTA ATAGGGTTTG CGACAGTCGT TCAACTAGAA TGCCC-3’
DNA 2:5’-SH-CAATCTGCCA GGCCACTAAT GCCATCGTTT GGGCTGTTCC GAGTGTGGCT CGTCGGTTTG GGCATTCTAG TTGAACGACT GTCGC-3’
DNA 3:5’-AGATTGTTTC CCTATTAGAA GGTCTCAGGT GCGCGTTTCG GTAAGTAGAC GGGACCAGTT CGCC-3’
DNA 4:5’-GGACTCTTTC CGACGAGCCA CACTCGGAAC AGCCCTTTGG CGAACTGGTC CCGTCTACTT ACCG-3’
- 还没有人留言评论。精彩留言会获得点赞!