一种神经递质类代谢物全同位素内标质谱定量方法与流程
本发明涉及一种神经递质类代谢物质谱定量方法,进一步说是一种神经递质类代谢物全同位素内标质谱定量方法。
背景技术:
神经递质是脑内维持各种生理功能的一类重要的生物活性分子。它们的含量变化与许多神经紊乱如抑郁、帕金森病、精神分裂症等疾病密切相关。这类物质代谢主要涉及色氨酸通路、γ-氨基丁酸通路和儿茶酚胺通路等。定量研究这类物质的组成及其含量变化对于神经科学研究和临床诊断具有极其重要的意义。目前主要采用高效液相色谱-电化学检测方法对神经递质类物质检测,该方法仅能对少数几个浓度高的物质进行检测,且通量低和定性定量准确度差,因而限制了其临床应用和神经科学研究的深度。高效液相色谱-串联四极杆质谱联用技术因其特异性好、灵敏度高、定量准确和高通量等优点而逐渐被生命科学研究、药物研发和临床等应用,已成为定量检测的金标准。但是,神经递质类代谢物尤其是儿茶酚胺类代谢物因其高度亲水性和热不稳定性,在反相色谱柱上具有保留极差的缺点,在电喷雾离子化时常常发生源内降解,结果导致这些物质的色谱-质谱法检测难于检测或定量准确度非常差,且每次只能检测少数几个物质,与实际应用具有非常大的差距。
最近,韩国科学家采用hmds(hexamethyldisilazane)和mbhfba(n-methyl-bis-heptafluorobutyramide)这两种衍生试剂分别对不同活性基团进行选择性衍生,并采用gc-ms/ms(mrm模式)行检测,成功地对该类物质进行定量检测,具有特异性好和灵敏度高(定量限在ng/ml水平)等优点(hongj.y.,j.chromatogr.b2013,940:94-103)。但是繁琐的样本纯化步骤和衍生步骤,非常耗时。最近,科学家采用多种化学衍生法对该类物质的活性基团如氨基、羧基和酚羟基进行化学衍生,再行lc-ms/ms(mrm模式)法检测,有效地提高了待检测物的热稳定性、色谱保留和检测灵敏度。如中科院上海有机化学所采用dmmsp(4,6-dimethoxy-2-(methylsulfonyl)pyrimidine)对4个儿茶酚胺物质的酚羟基进行化学衍生,提高了热稳定性和检测灵敏度,但是存在衍生温度高达70℃且衍生反应结束后的衍生试剂清除复杂等缺点(高玉平等,中国化学学报,2010,28,1704-1708)。
grecos等采用sptpp(5-n-succinimidoxy-5-oxopentyl)triphenylphosphoniumbromide)对3个单胺类神经递质的活性基团氨基进行化学衍生和高选择性、高灵敏度和高通量分析(grecos.,analyticachimicaacta2013,771:65-72)。以上两个衍生方法都存在仅能对一种活性基团进行衍生且无商业化可用的稳定性同位素衍生试剂等缺点。最近,我们采用一种常见的紫外衍生反应的苯甲酰氯反应试剂——苯甲酰氯及同位素标记的苯甲酰氯,可实现同时对活性基团如氨基、亚氨基和酚羟基进行衍生反应,有效地提高了神经递质类代谢物的热稳定性、色谱保留、检测灵敏度和定量准确性,实现同时对多个神经地质类代谢物的高灵敏度质谱检测定量。
技术实现要素:
本发明的目的是提供一种神经递质类代谢物全同位素内标质谱定量方法,解决现有的对色氨酸通路、γ-氨基丁酸通路、儿茶酚胺通路等神经递质代谢相关的多个化合物检测定量存在灵敏度低和准确度不高的问题。
为了达到上述目的,本发明是通过以下技术方案实现的:
本发明提供一种神经递质类代谢物全同位素内标质谱定量方法,该方法采用神经递质类代谢物标准品与稳定同位素标记的苯甲酰氯的衍生产物作为定量内标参照物,对生物样本中神经递质类代谢物进行基于质谱技术平台的定性定量分析测试,包括以下具体步骤:
(1)神经递质类代谢物标准品的非标记苯甲酰氯衍生产物和稳定性同位素标记苯甲酰氯衍生产物的制备:取神经递质类代谢物混合标准品母液两份,干燥,分别向两份干燥物中加入四硼酸钠缓冲液,然后分别加入非标记的苯甲酰氯和稳定性同位素标记的苯甲酰氯,进行酰化衍生反应,分别得到神经递质类代谢物的非标记苯甲酰氯衍生产物和稳定性同位素标记苯甲酰氯衍生产物,其中,同位素标记苯甲酰氯衍生产物的溶液作为内标母液,对该内标母液进一步稀释,获得基准内标溶液,用于标准曲线和生物样本的制备。
(2)质谱定性定量方法的建立:采用流动注射法分别对神经递质类代谢物的非标记的苯甲酰氯衍生产物和稳定性同位素标记的苯甲酰氯衍生产物进行电喷雾离子化质谱检测参数优化,建立非标记苯甲酰氯衍生产物和稳定性同位素标记苯甲酰氯衍生产物的多反应监测(mrm)条件;并将串联四极杆质谱与液相色谱仪联用,采用反相液相色谱柱对神经递质类代谢物的非标记苯甲酰氯衍生产物和稳定性同位素标记苯甲酰氯衍生产物进行色谱分离,确定各物质的色谱保留时间,建立神经递质类代谢物的定性、定量检测条件。
(3)神经递质类代谢物定量标准曲线的制备:对步骤(1)获得的非标记苯甲酰氯衍生产物进行梯度稀释,并与步骤(1)获得的内标母液进行混合;采用步骤(2)中建立的质谱定性定量方法进行检测定量,以进样浓度为横坐标,以测得的各神经递质类代谢物的非标记苯甲酰氯衍生产物与基准内标溶液中与之对应的稳定性同位素标记苯甲酰氯衍生产物的峰面积或峰高的丰度比值为纵坐标,建立定量标准曲线。
(4)生物样本的制备、检测和定量:取生物样本,采用直接或经提取、干燥后再复溶后,加入四硼酸钠缓冲液和非标记的苯甲酰氯试剂,进行衍生反应,再加入基准内标溶液,涡旋震荡,上清液用于检测,检测方法为步骤(2)建立和优化的方法;分别计算各神经递质类代谢物的非标记苯甲酰氯衍生产物及基准内标溶液中与之对应的稳定性同位素标记苯甲酰氯衍生产物的峰面积或峰高的丰度比值,代入定量标准曲线,计算得到样本中神经递质类代谢物的含量。
本发明的进一步改进在于:步骤(1)中的神经递质类代谢物指天然或人工合成的色氨酸通路、γ-氨基丁酸通路、儿茶酚胺通路中所有代谢物或代谢中间物。
本发明的进一步改进在于:步骤(1)和(4)的加入四硼酸钠缓冲液,具体条件指四硼酸钠缓冲液的浓度为10-200mm,体积为生物样本体积或以毫克为单位的质量的0.5-20倍。
本发明的进一步改进在于:步骤(4)中的非标记的苯甲酰氯试剂具体指为体积百分比0.1%至10%苯甲酰氯的乙腈溶液。
本发明的进一步改进在于:步骤(1)和(2)中的稳定性同位素标记的苯甲酰氯是指碳13或氘原子标记的苯甲酰氯。
本发明的进一步改进在于:碳13标记或氘原子标记的苯甲酰氯是指含有2-6个碳13或1-5个氘原子的苯甲酰氯。
本发明的进一步改进在于:碳13或氘原子标记的苯甲酰氯具体为体积百分比0.1%至10%的乙腈溶液。
本发明的进一步改进在于:步骤(1)和(4)的衍生反应,具体条件指温度为10-50℃,时间为5秒-5分钟。
本发明的进一步改进在于:生物样本是指来自于人或动物的脑脊液、脊髓液、血浆、血清、脑组织匀浆、尿液、细胞、滤纸干血片中的任一种。
本发明的色氨酸通路、γ-氨基丁酸通路、儿茶酚胺通路化合物全同位素内标定量检测方法,是指对色氨酸通路、γ-氨基丁酸通路、儿茶酚胺通路化合物的串联质谱或者液相色谱-串联质谱联用分析中的内标采用色氨酸通路、γ-氨基丁酸通路、儿茶酚胺通路化合物标准品与稳定同位素标记的苯甲酰氯的衍生产物作为定量内标。
本发明的优点和有益效果在于:本发明涉及的是一种生物样本中与神经递质代谢相关的色氨酸通路、γ-氨基丁酸通路、儿茶酚胺通路化合物的质谱定量检测分析方法,进一步说是一种以稳定性同位素标记的苯甲酰氯试剂与这些化合物的化学衍生产物作为定量内标参照物质,以液相色谱质谱联用仪,尤其是超高效液相色谱-串联四极杆质谱仪的多反应监测(mrm)模式为检测手段,对生物样本中这些化合物的衍生产物同时进行定性定量分析的方法,该方法具有如下特点:(1)无需对样本进行复杂的前处理如干燥和固相微萃取等;(2)无需对衍生后的衍生试剂进行清除,可直接上机检测,(3)反应条件温和(无需加热)、快速;(4)衍生产物对光不敏感、常温下较稳定且不存在电喷雾离子源内降解现象;(5)高特异性、高灵敏度(定量限在亚pg/ml水平)和定量准确度高。该方法已在脑组织、血浆或血清、脑脊液、脊髓液和尿液等生物样本定量检测方面成功应用。本发明方法将有助于显著改善神经递质类代谢物的检测定量,具有可预期的临床应用前景,本发明针对当前科学研究和临床需要,采用稳定性同位素标记的苯甲酰氯和非标记的标准品的衍生产物为定量内标参照物,实现同时对色氨酸代谢通路、γ-氨基丁酸和儿茶酚胺代谢通路中的神经递质代谢相关物质进行同时定量分析。
本发明不需要所有色氨酸通路、γ-氨基丁酸通路、儿茶酚胺通路化合物的稳定性同位素标准品,仅需要普通(非同位素标记)的色氨酸通路、γ-氨基丁酸通路、儿茶酚胺通路化合物标准品以及稳定性同位素标记的苯甲酰氯试剂。色氨酸通路、γ-氨基丁酸通路、儿茶酚胺通路化合物标准品以及稳定性同位素标记的苯甲酰氯试剂在商业上可以获得,而色氨酸通路、γ-氨基丁酸通路、儿茶酚胺通路化合物的同位素标记标准品目前仅能提供少数,且价格过于昂贵。因此,本方法提供的是一种定性定量准确、高通量和花费成本低的色氨酸通路、γ-氨基丁酸通路、儿茶酚胺通路类物质的全同位素内标质谱定量检测分析方法。该方法可以用于多种生物样本如干血纸片、血浆或血清、尿液、脑脊液、精液、细胞、肌肉、肝脏、脂肪和肾脏组织等色氨酸通路、γ-氨基丁酸通路、儿茶酚胺通路化合物的质谱定量检测分析,既适合于临床疑似代谢病的筛选,也适于高端生命科学研究。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动性的前提下,还可以根据这些附图获得其他的附图。
图1为以五羟色氨酸为例,说明该方法的化学反应原理图(苯甲酰氯与带酚羟基或氨基酰化反应)。
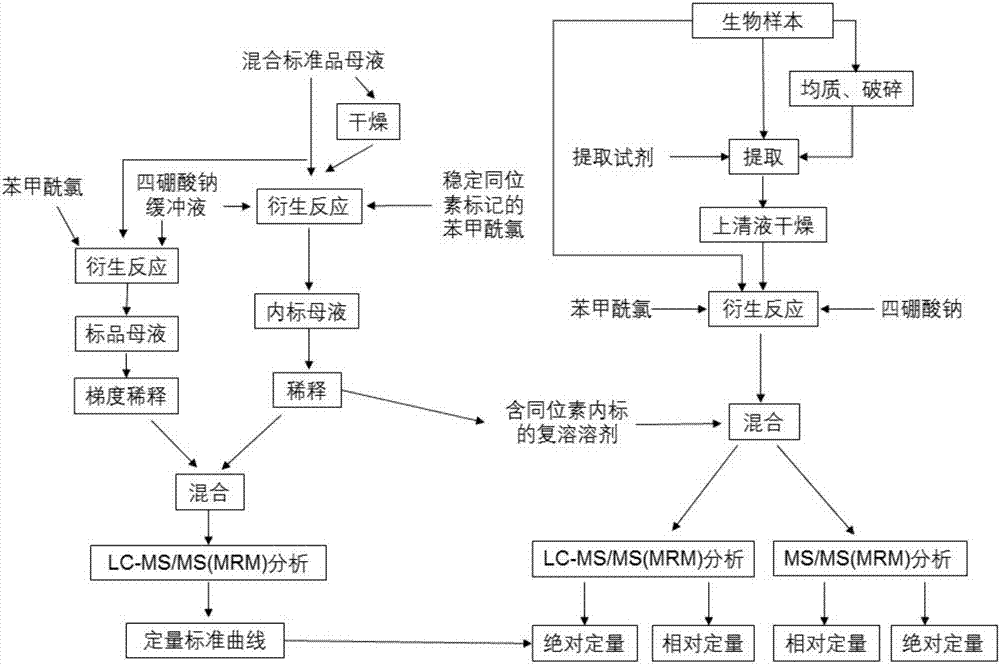
图2为生物样本中神经递质类化合物的全同位素质谱法定性定量分析流程示意图。
图3为色氨酸通路、γ-氨基丁酸通路、儿茶酚胺通路化合物的苯甲酰氯与d5-苯甲酰氯衍生物的uplc-ms/ms分析的提取离子色谱图。
图4为从小鼠脑组织可定性定量检测到22种神经递质类代谢物,代表性的提取离子色谱图。
图5为从人血浆中定性定量得到22种神经递质类代谢物,代表性的提取离子色谱图。
具体实施方式
下面结合附图和实施例,对本发明的具体实施方式作进一步描述。以下实施例仅用于更加清楚地说明本发明的技术方案,而不能以此来限制本发明的保护范围。
实施例1:
本实施例的目的是建立神经递质类化合物同位素试剂衍生法的uplc-ms/ms定量方法,如图1-3所示。
配制色氨酸通路、γ-氨基丁酸通路、儿茶酚胺通路化合物标准品的50%乙腈溶液(混合标准品母液),稀释,取100微升稀释液两份,氮气吹干,分别加入30微升(范围为20-50微升,以下范围取值用此方法表示)浓度为100mm(50-200mm)四硼酸钠缓冲液,接着分别加入30微升(20-50微升)的5%苯甲酰氯溶液(体积比)的稳定性同位素标记的衍生试剂和非标记衍生试剂,30℃反应25分钟,分别得到色氨酸通路、γ-氨基丁酸通路、儿茶酚胺通路化合物的同位素标记衍生产物和非标记的衍生产物;氮气吹干,分别加入700微升(200-1000微升)80%乙腈水溶液(体积比)复溶,分别得到色氨酸通路、γ-氨基丁酸通路、儿茶酚胺通路化合物与苯甲酰氯或d5-苯甲酰氯的酰化衍生产物。采用流动注射法和absciex5500串联四极杆质谱仪对以上获得的酰化衍生产物进行电喷雾离子化质谱检测参数如dp和ce值进行优化,建立mrm检测条件,其中每个同位素衍生标准品的母离子(precursor)为非同位素衍生标准品的分子量加5,将各个色氨酸通路、γ-氨基丁酸通路、儿茶酚胺通路化合物的同位素标记和非标记的衍生产物的mrm条件输入质谱方法中,接上高效液相色谱仪,在无色谱柱分离的情况下,直接将经自动进样器进样的衍生标准品引入质谱离子源进行离子化和mrm检测,从而建立流动注射法质谱mrm检测方法。
进一步地,采用waters超高效液相色谱仪(uplc)并在色谱和质谱间连接一根uplc色谱柱(watersacquityuplcbehc18色谱柱,1.7μm,2.1x100mm),对进样的色氨酸通路、γ-氨基丁酸通路、儿茶酚胺通路化合物的苯甲酰氯和d5-苯甲酰氯衍生物同时进行色谱分离和质谱mrm检测,建立色氨酸通路、γ-氨基丁酸通路、儿茶酚胺通路化合物的uplc-ms/ms检测方法;代表性的色氨酸通路、γ-氨基丁酸通路、儿茶酚胺通路化合物的苯甲酰氯与d5-苯甲酰氯衍生物的uplc-ms/ms分析的提取离子色谱图如附图3所示。
对色氨酸通路、γ-氨基丁酸通路、儿茶酚胺通路化合物的d5-苯甲酰氯衍生物母液进行梯度稀释1-1000倍,用以上建立的检测方法进行检测,得到积分面积或峰高,以各浓度的积分面积或峰高与内标之比作为纵坐标,以各浓度为横坐标,建立标准曲线。结果,所有色氨酸通路、γ-氨基丁酸通路、儿茶酚胺通路化合物标准曲线的线性范围均为1-1000倍,r2值均大于0.99。
实施例2:
本实施例的目的是采用建立的色氨酸通路、γ-氨基丁酸通路、儿茶酚胺通路化合物的uplc-/ms/ms定量方法对小鼠脑组织进行半定量的分析,为科学研究提供重要的研究数据。
取神经递质类代谢物混合标准品母液乙腈溶液,稀释,取50微升,氮气吹干,先加入四硼酸钠缓冲液(预冷)100微升(50-200微升),然后加入100微升(50-200微升)稳定性同位素标记的衍生试剂d5-苯甲酰氯,进行衍生反应,50℃加热处理30秒钟,得到神经递质类代谢物的同位素标记衍生产物,对神经递质类代谢物同位素标记的衍生产物进行稀释15倍,得到稳定同位素标记的内标母液。
取冷冻保存的脑组织匀浆样本40微升,加入四硼酸钠缓冲液(预冷)50微升(50-200微升),置-60℃保存过夜,取出低温(4℃)超声破碎脑组织7分钟,冷冻离心(4℃,16000g,15min),取60微升上清液,氮气吹干,向干燥残渣中加入苯甲酰氯的乙腈溶液20微升,50℃加热处理30秒钟,氮气吹干,加入50微升内标母液复溶,低温离心(4℃,16000g,15min),上清液用于检测;采用超高效液相色谱结合反相色谱柱分离(watersacquityuplchsst3色谱柱,1.7μm,2.1x100mm),进样量2微升,洗脱物进入串联四极杆质谱仪进行电喷雾离子化和mrm检测分析。通过比较样本中每个神经递质类代谢物的非标记苯甲酰氯酰化衍生物与其相应的d5-苯甲酰氯酰化衍生物的色谱保留时间和transition(母离子→子离子对)进行定性,通过计算它们的峰面积比进行相对定量。
结果,从小鼠脑组织可定性定量检测到22种神经递质类代谢物,代表性的提取离子色谱图如附图4所示。
实施例3
本实施例的目的是采用建立的色氨酸通路、γ-氨基丁酸通路、儿茶酚胺通路化合物的uplc-/ms/ms定量方法对人血浆样本进行定量分析。
取神经递质类代谢物混合标准品母液乙腈溶液60微升,先加入四硼酸钠缓冲液100微升(50-200微升),然后加入稳定性同位素标记的衍生试剂13c6-苯甲酰氯,进行酰化衍生反应,10℃加热处理30分钟,得到神经递质类代谢物的13c6-苯甲酰氯酰化衍生产物,对神经递质类代谢物同位素标记的衍生产物进行稀释15倍,得到稳定同位素标记的内标母液。
取冷冻保存人血浆样本,解冻,短时震荡混匀,取30微升解冻血浆,加入四硼酸钠缓冲液(预冷)70微升(50-200微升),置-20℃保持20分钟,取出,冷冻离心(4℃,16000g,15min),上清液用氮气吹干。向干燥残渣中加入苯甲酰氯的乙腈溶液25微升,10℃加热处理30分钟,氮气吹干,加入60微升内标溶液复溶,低温离心(4℃,16000g,15min),上清液用于检测。采用超高效液相色谱结合反相色谱柱分离(watersacquityuplcbehc18色谱柱,1.7μm,2.1x100mm),进样量3微升(2-5微升),洗脱物进入串联四极杆质谱仪进行电喷雾离子化和mrm检测分析。通过比较样本中每个神经递质类代谢物的非标记衍生物与其相应的13c6标记的苯甲酰氯酰化衍生物的色谱保留时间和transition(母离子→子离子对)进行定性,进一步计算每个神经递质类代谢物的非标记苯甲酰氯酰化衍生物与其相应的13c6标记的13c6-苯甲酰氯酰化衍生物的峰面积比,采用定量校正曲线进行相对定量,最终得到人血浆中的神经递质类代谢物及其浓度。
结果,采用该方法从人血浆中定性定量得到22种神经递质类代谢物,代表性的提取离子色谱图如附图5所示。
本发明是一种新的同时对生物样本中色氨酸通路、γ-氨基丁酸通路、儿茶酚胺通路神经递质类代谢物进行全同位素衍生内标的质谱定量方法,所述的方法是指:采用稳定性同位素标记的苯甲酰氯试剂与该类物质的标准品的化学衍生反应产物作为定量内标,以液相色谱-串联四极杆质谱为检测手段的神经递质类代谢化合物的全同位素衍生内标定量法。
本发明具有样本制备简单、定性定量准确、高通量和花费低等优点,具有可预期的临床应用前景。本发明提供的方法弥补了当前该类神经递质代谢化合物测试定性定量准确度低、成本高以及仅能同时对几个物质进行同时分析等低通量缺点。
本发明的目的是提供一种以色氨酸通路、γ-氨基丁酸通路、儿茶酚胺通路化合物标准品与稳定性同位素标记的苯甲酰氯的衍生反应产物作为定量内标,从而显著性提供流动注射-串联四极杆质谱或液相色谱-串联四极杆质谱定性定量分析生物样本中色氨酸通路、γ-氨基丁酸通路、儿茶酚胺通路中重要化合物的准确性。该分析方法具有定性定量准确、高通量和花费低等优点,将有助于改善科学研究和临床检测水平。
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!