一种液体即用型抗凝血酶Ⅲ活性测定试剂的制作方法
本发明属于生物学检测技术领域,具体涉及一种液体即用型抗凝血酶ⅲ活性测定试剂及相应的试剂盒。
背景技术:
凝血过程是一个多因子参与的调控的过程。在血管受损伤时,机体通过内外途径激活凝血过程,最终凝血酶被激活,凝血酶将纤维蛋白原分解变成纤维蛋白,产生凝血。抗凝血酶ⅲ是凝血过程中的一个调控因子。抗凝血酶ⅲ可和参与凝血过程的多个因子结合,并抑制这些凝血因子的活性,例如fxa,fixa,fxia,fiia。但是在没有肝素存在的条件下抗凝血酶ⅲ和fxa,fiia结合的速度很慢,在肝素存在的条件下,肝素和抗凝血酶ⅲ结合形成复合物,改变抗凝血酶ⅲ了的构象,大大提高抗凝血酶ⅲ和凝血因子的结合速度,这种结合速度可增加1000倍。凝血酶ⅲ主要由肝脏合成,是分子量约为60000da蛋白质。正常抗凝血酶ⅲ的血浆浓度为20~30mg/dl,活性为80%~130%。在血浆中承担着70%的抗凝血酶活性,抗凝血酶ⅲ在維持血液生理性凝血与抗凝血平衡中起着重要的作用。
血液中抗凝血酶ⅲ的含量或者活性降低,大大增加血栓形成的风险,容易导致静脉血栓或者肺栓塞症。引起血液中抗凝血酶ⅲ的含量或者活性降低的原因很多。抗凝血酶ⅲ的含量或者活性低既有遗传性的也有获得性的。先天性遗传引起的血液中抗凝血酶ⅲ缺乏又分为i型和ii型,i型抗凝血酶ⅲ缺乏的特征是抗凝血酶ⅲ合成的降低,血液中抗凝血酶ⅲ总量下降。ii型抗凝血酶ⅲ缺乏的特征是抗凝血酶ⅲ合成正常,血液中抗凝血酶ⅲ总量是正常的但由于部分抗凝血酶ⅲ功能丧失,表现出抗凝血酶ⅲ缺乏。获得性的抗凝血酶ⅲ含量或者活性低的原因有多种,包括肝病引起的抗凝血酶ⅲ合成减少,肾病引起的抗凝血酶ⅲ流失,使用肝素等药物引起的抗凝血酶ⅲ损失,以及弥散性血管内凝血引起的抗凝血酶ⅲ消耗。无论是遗传性的还是获得性的抗凝血酶ⅲ缺失症都给患者带来血栓的风险,给他们的健康和生命带来难以预测的威胁。抗凝血酶ⅲ活性的检测在先天性抗凝血酶ⅲ缺陷或异常的临床诊断具有非常重要的意义。
目前測定抗凝血酶ⅲ的方法主要有免疫学分析方法、凝固法和发色底物法。免疫学分析方法利用抗原抗体结合的原理通过单向放射免疫扩散法、免疫比浊法以及酶联免疫吸附法测定样本中at-ⅲ的浓度。这种方法比较特异和灵敏,但是操作繁琐、耗时,而且无法测定ii型抗凝血酶ⅲ缺乏。凝固法是通过血浆凝固时间来测定样本中at-ⅲ活性,由于受影响的因素较多,因此特异性,准确度较差。而且操作繁琐。底物发色法测定血浆中抗凝血酶ⅲ含量的方法由于灵敏度高、准确性好、检测时间短等特点,且能够适用于多种自动化分析仪器,目前,临床上已被广泛应用。底物发色法是在过量的凝血酶和肝素存在下,血浆中的抗凝血酶ⅲ与凝血酶形成1:1的复合物从而抑制凝血酶的活性,剰余的没有和抗凝血酶ⅲ形成复合物的凝血酶作用于凝血酶特异发色底物,将底物裂解产生4-硝基苯胺(4-nitroaniline,pna)显色基团,4-硝基苯胺量和405nm处吸光度的变化呈正相关,而产生的4-硝基苯胺的量是和中抗凝血酶ⅲ的活性成反比。因此,利用测量405nm处吸光度的变化,可计算出血浆中抗凝血酶ⅲ的活性水平。
在血浆中除了抗凝血酶ⅲ对凝血酶的活性具有抑制作用外,还有其它因子,例如肝素辅助因子ii,对凝血酶具有抑制作用。大约70%的凝血酶抑制活性是由抗凝血酶ⅲ引起。因此基于凝血酶的底物发色法不能准确地反映血浆中抗凝血酶ⅲ的真实水平。虽然通过离子强度,肝素浓度的优化,以及利用牛凝血酶取代人凝血酶可降低肝素辅助因子ii对抗凝血酶ⅲ检测的影响,但不能完全去除肝素辅助因子ii对检测的影响。肝素辅助因子ii对fxa没有抑制作用,用fxa替代凝血酶可克服了上述抗凝血酶ⅲ检测方法的缺点,更能准确的反映血浆中抗凝血酶ⅲ的真实水平(thrombosisandhemostasia,1991,69(3):231-235)。中国专利cn106153612a公开了一种基于fxa的抗凝血酶ⅲ的检测试剂,该试剂在4℃相对稳定,但是在25℃下只能放置5天,对储存和运输的要求很高,保管稍有不慎就会导致试剂失活,极大地影响检测结果。目前市场上基于fxa的抗凝血酶ⅲ的检测试剂多使用冻干粉制剂,然而冻干粉试剂需要冰冻干燥工序,生产起来比较复杂,而且在使用时需要复溶,由于冰冻干燥过程中,各瓶冰冻效果的差异,以及复溶过程中,加样量的不同,都会导致冻干粉制剂瓶间差,批间差很大。
技术实现要素:
本发明针对现有技术不足,通过对条件的优化,筛选不同的保护剂建立了稳定的液体即用型抗凝血酶ⅲ检测试剂。具有稳定性好,灵敏度高,特异性好,批间差小以及使用方便等诸多优点。
本发明具体技术方案如下:
一种液体即用型抗凝血酶ⅲ活性测定试剂,包括试剂1和试剂2,所述试剂1包括fxa、肝素、缓冲液和保护剂;所述试剂2包括fxa的发色底物和甘露醇,所述保护剂包括牛血清白蛋白、peg6000和甘露醇。
优选的,所述保护剂为质量体积百分比为0.1%-5%的牛血清白蛋白,0.1%-5%聚乙二醇6000和1%-10%甘露醇。更优选1%的牛血清白蛋白,1%聚乙二醇6000和5%甘露醇。
本发明所述缓冲液优选ph为6.5-9.0的三羟甲基氨基甲烷-盐酸缓冲液,三羟甲基氨基甲烷-咪唑缓冲液或者咪唑-盐酸缓冲液。优选缓冲液的选工作浓度为0.01-0.3mol/l。
本发明所述xa因子的发色底物选自bz-ile-glu-gly-arg-pna、suc-ile-glu(gamma-pip)-gly-arg-pna·hcl、n-α-z-d-arg-gly-arg-pna·2hcl、z-d-arg-gly-arg-pna·2hcl中的一种或几种。优选n-α-z-d-arg-gly-arg-pna·2hcl。优选工作浓度为0.6mmol/l-1.5mmol/l。
为了保证试剂1缓冲溶液中的离子强度,可以选择添加无机盐如氯化钾、氯化钙或氯化钠中的一种或几种,优选选工作浓度为0.01-0.25mol/l。
本发明所述fxa选自人、牛、猪fxa中的任意一种,优选牛fxa。优选工作浓度为0.1-5u/ml。
本发明所述试剂1和试剂2还可以含有防腐剂,如叠氮钠或者proclin300,优选工作浓度质量体积百分比为0.02-0.5%,更优选0.05%。
本发明所述液体即用型抗凝血酶ⅲ活性测定试剂可作为检测试剂用于制备检测抗凝血酶ⅲ活性检测试剂盒。
本发明所述液体即用型抗凝血酶ⅲ活性测定试剂可制备相应的检测试剂盒,包括盒体和装有上述试剂的试剂瓶,试剂瓶放置于所述盒体内。试剂盒分别包含试剂1和试剂2。该试剂盒检测待测样品中抗凝血酶ⅲ活性时,将待测样品与试剂1混合并孵育,再加入试剂2混合并孵育后,读取待测样品中发色底物的信号强度;最后通过计算信号强度并和已知浓度标准品的标准曲线比对得到血液中抗凝血酶活性。
本发明所述液体即用型抗凝血酶ⅲ活性测定试剂在使用时,采用发色底物法,将待测样品与上述抗凝血酶活性活性检测试剂混合并孵育后,检测发色底物的信号强度;而产生的吸光度信号是和样品中抗凝血酶ⅲ的活性成反比的。最后通过计算信号强度并和标准曲线比对获得待测样品中抗凝血酶ⅲ的活性。
本发明优点:
本发明所述的液体即用型抗凝血酶ⅲ活性测定试剂,试剂1和试剂2均为液体,开瓶即用,无需复溶,使用方便,具有良好的稳定性,能够在37℃具有相对长期的稳定性,在存储和运输不容易失去活性。
本发明所述的液体即用型抗凝血酶ⅲ活性测定试剂相较于冻干粉剂制备过程简便,成本相对较低,液态试剂克服冻干粉试剂复溶过程或冻干干燥过程带来的缺陷,可保证所有成份构成均一的悬浮溶液,灌装时不会使成份或浓度发生变化,不存在冻干粉制剂瓶间差,批间差的问题。具有很高的临床应用价值。
附图说明
图1为本发明实施例2的标准曲线。
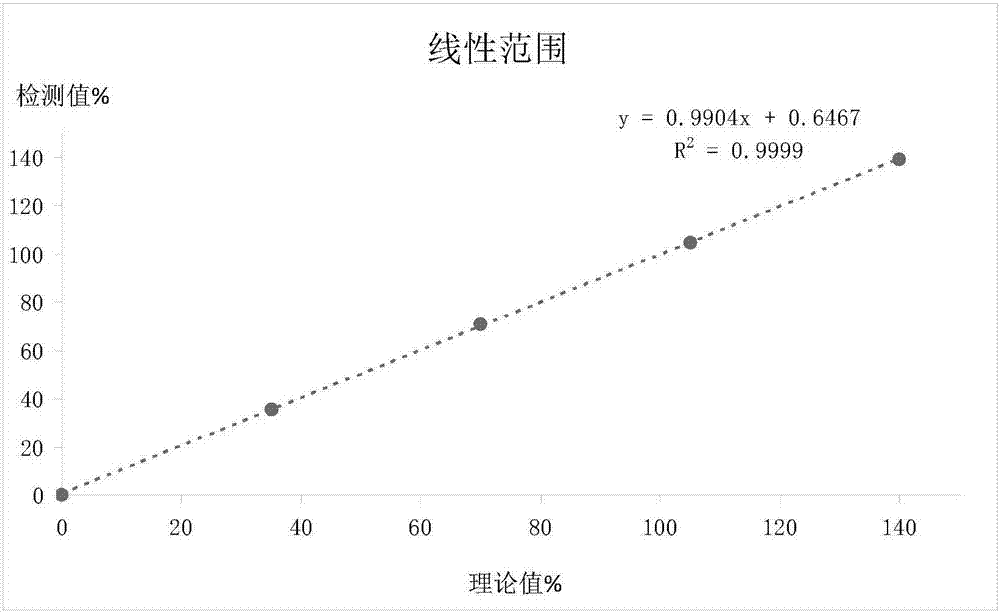
图2为本发明实施例3的线性回归曲线。
具体实施方式
在本发明中所使用的术语,除非另有说明,一般具有本领域普通技术人员通常理解的含义。
下面结合具体实施例并参照数据进一步详细描述本发明。应理解,该实施例只是为了举例说明本发明,而非以任何方式限制本发明的范围。
在以下实施例中,未详细描述的各种过程和方法是本领域中公知的常规方法。下述实例中所用的材料、试剂、装置、仪器、设备等,如无特殊说明,均可从商业途径获得。
下面结合具体实施例对本发明进一步说明。
实施例1试剂1和试剂2的制备
保护剂的配制:使用ph8.1的20mmol/l的三羟甲基氨基甲烷缓冲液,配制不同组分的保护剂,向保护剂中加入防腐剂,防腐剂为工作浓度为0.05%的叠氮钠。
保护剂1:2%bsa,10%蔗糖,2%peg6000,10%甘露醇。
保护剂2:2%bsa,10%蔗糖,2%peg6000。
保护剂3:2%bsa,2%peg6000,10%甘露醇。
保护剂4:10%蔗糖,2%peg6000,10%甘露醇。
试剂1的配制:称取tris2.428g、氯化钠1.02g、加入900ml纯净水,充分溶解,调ph至8.1,加入fxa(购自sigma公司),缓慢混匀,至浓度为0.4u/ml,用纯净水定容终体积至1000ml,分别加入等体积的上述不同保护剂的溶液,使得fxa的终浓度为0.2u/ml。试剂2的配制:将发色底物n-α-z-d-arg-gly-arg-pna·2hcl复溶,用醋酸调ph至6.5,加入甘露醇和叠氮钠,用水调至浓度为1.5mmol/l,甘露醇浓度为5%,叠氮钠浓度为0.05%。
保护剂筛选:将含不同保护剂的试剂1分别放置于4℃和37℃,每天取160μl试剂1样品,加入4μl的水,加入40μl的试剂2,利用希森美康血凝仪ca1500测定其od405,结果如表1所示。
表1
结果显示,含有保护剂1,2和4的试剂1在37℃放置1天后均不同程度上出现活性损失。保护剂3在4℃和37℃放置7天具有较好的稳定性,更能保护试剂1的活性。
实施例2标准曲线制作
按实例1的方法配制配制试剂1和试剂2。试剂1的保护剂选取保护剂3。取浓度为100%的抗凝血酶ⅲ标准品用0.9%的生理盐水稀悉成浓度为50%和0%的标准品溶液,取4μl标准液加人160μl试剂1孵育2分钟,加入40μl的试剂2用动力学法测定od405吸光度变化率,将od405吸光度变化率和对应的抗凝血酶ⅲ浓度采取对数线性方程做出标准曲线,如图1所示。
实施例3线形范围检测
分别配制抗凝血酶ⅲ活性浓度约为20%,60%,100%和140%的样本,用希森美康血凝仪ca1500重复检测四次,取平均值,如表2所示,做线性回归曲线,线性范围为0~140%,结果图2所示。
表2
实施例4批间差考察
连续配制3批样品,然后对内质控品进行同时测试,结果显示各批之间批间差很小,如表3所示。
表3
实施例5稳定性考察
以cn106153612a实施例1公开的方法配制的试剂作为对比试剂(其试剂1:ch3so2-d-leu-gly-arg-p-nitroanilide·acoh2mm,氯化钠0.2m,聚乙二醇-80001%,试剂3:肝素2iu/ml,氯化钠0.2m。试剂4:fxa0.5μm,氯化钠0.2m,聚乙二醇-80001%),以及本发明所述试剂1和试剂2分别放置于4℃和37℃,每隔7天取样,分别对质控品2(85%)进行测定。。测试结果如表4所示。
表4
试验结果显示,本发明所述液体即用型抗凝血酶ⅲ活性测定试剂相比现有技术的液体试剂,在4℃和37℃具有更高的稳定性。本发明试剂在37℃可稳定28天。说明稳定性很好。
- 还没有人留言评论。精彩留言会获得点赞!