一种稳态进动梯度多回波水脂分离成像方法与流程
本发明涉及核磁成像技术领域,尤其涉及一种稳态进动梯度多回波水脂分离成像方法。
背景技术:
化学位移成像是目前最有效的磁共振压脂成像技术之一,在四肢关节诊断上应用较多,但对于腹部等运动器官,这类压脂技术的临床应用常常由于运动伪影干扰而受到限制。扫描加速技术开发一直是临床mri学术研究和商业化应用的一个重要方向,这不仅有利于提高mri成像技术的临床检查效率也有利于克服运动伪影干扰。迄今为止,多种通用的扫描加速技术,例如,并行采集、半傅立叶采集和压缩感知采集,已在临床上获得应用,但仍不足以充分满足腹部和心肺快速成像和实时成像的需要,具有快速和超快速扫描特征的特殊成像方法(包括序列和算法)的开发一直是磁共振领域前沿研究热点之一,这类特殊成像方法与通用加速技术的结合有望提高磁共振扫描的时间分辨率达到秒级甚至毫秒级。其中,稳态进动成像方法是在保持高信噪比的同时实现快速扫描的一种十分有效的方法,尽管这种方法对序列设计要求和系统质量控制要求明显偏高。临床上已实现常规应用的稳态进动序列通常是在一个序列重复周期内每层仅激发并采集一个梯度回波,通过空间编码和图像重建得到一幅图像,主要用于腹部水成像和心脏电影。实际上,稳态进动序列可以在一个序列重复周期内通过序列重复时间(tr)和回波时间(te)参数控制以及相位循环或频移等方式进行选择性激发并采集不同的回波组份,人们可以利用这个技术特征将稳态进动成像方法与化学位移相位编码技术结合应用以便实现快速水脂分离成像。
在近几年主要有三个版本的稳态进动水脂分离成像方法在斯坦福大学等欧美实验室环境初步开发成功,其中一个版本是,基于水和脂肪的共振频率差值δf设置稳态进动序列的回波时间分别为te、te+1/δf/n和te+1/δf/n(n为任意正整数),进行三次独立的扫描得到三幅图像,然后通过最小二乘法拟合得到水像和脂肪像,扫描时间比常规稳态进动扫描要延长三倍;第二个版本是,每次扫描采用不同的te和tr参数值并在6次射频脉冲相位循环条件下逐个检测每个回波组份,其中第一个回波的实部和虚部的相位差需要精确控制为90度,这种扫描方式对脉冲翻转角、射频相位和偏共振效应很敏感,在实际临床环境下扫描时间较长,并且实现不同回波组份分离的te和tr的合理选择存在较大难度;第三个版本是,将两点dixon水脂分离技术与稳态进动技术相结合,基于双极性频率编码梯度在一个序列周期内同时检测两个回波,一个为同相水脂信号,另一个为反相水脂信号,然后基于传统的两点dixon图像重建方法进行水脂信号归属,但水脂交界处可能存在水脂信号归属误差,主要适用于高场胰胆管水成像。此外,上述方法基本上没有考虑涡流效应、剩磁效应和回波时间较长可能引起的相位缠绕问题,在各种型号的mri设备上不具有普遍适用性。
技术实现要素:
为了充分满足快速成像和精准诊断的需要,本发明提供了一种基于一次激发三点直接相位编码的稳态进动水脂分离成像方法和扫描校准技术。
本发明提供了一种稳态进动梯度多回波水脂分离成像方法,以磁共振成像系统上常规扫描用的稳态进动成像序列为基础,射频脉冲每间隔一个10ms量级或更小短周期tr就重复激发成像区域,脉冲翻转角在第一个序列重复周期内设置为+α/2并取消采样期,在后续序列重复周期内脉冲翻转角交替设置为+α和-α,同时通过选层梯度、相位编码梯度和频率编码梯度进行三维空间编码,每个方位的梯度积分面积之和为零,使得质子磁化矢量进动趋于稳态,在每个tr期间磁化矢量在三个或两个正负极性交替的频率编码梯度作用下形成三个或两个梯度回波,频率编码方向的梯度积分面积之和为零,并基于回波峰间隔时间和水脂化学位移差值对三个或两个回波进行直接相位编码。
优选的,直接相位编码方法的有效回波时间te设置为最小值或水脂同相位时间,序列重复时间设置为tr=2te+2δτ,δτ设置为1/δf/n,n优选为3或4,且tr不小于其最小值,te不小于其最小值,tr最小值和te最小值估算包括射频脉冲响应延迟、梯度脉冲响应延迟、接收机响应延迟和梯度方位矩阵运算时间以及序列指令执行时间的精确测定值。
优选的,信号调试方法采用下述方案进行回波信号优化:
(1)关闭相位编码梯度,在实时调试模式下运行成像序列,采集水模的质子
回波信号并显示幅值;
(2)先在采样窗第一个读梯度施加条件下调整序列周期tr和回波时间te
得到一个梯度回波并优化信号幅度和对称性;
(3)再在第一个至第二个乃至第三个读梯度施加条件下调整梯度幅度gr1
直到各回波组份分离开且回波峰等距。
优选的,其信号调试方法在扫描模式下采集k空间线,累加多次并保存为一维复矩阵,按采样数据点数dim1分离为两个复矩阵k1和k2或三个复矩阵k1,k2和k3,选取k1和k2*信噪比较高的数据点并计算各自的相位均值<φ1>和<φ2>及二者差值δφ。
优选的,数据采集处理方法是将人体扫描k空间数据沿选层方向进行一维离散逆傅立叶变换,得到每个层面的k空间矩阵,再沿频率编码方向按采样点数将k空间矩阵分离为两个复矩阵i0和i1或三个复矩阵i0,i1和i2并将i1进行时间反演和矩阵共轭后乘以e-iδφ进行初级相位校正以消除剩磁和涡流等效应引起的相位误差。
优选的,数据采集处理方法是在正交接收或多通道接收模式下,信号合成在图像域且在水脂分离之前按下述方式进行:
这里
优选的,在不对称回波相位编码情况下基于下式
对图像域复数矩阵采用最小二乘法拟合分析得到水像和脂肪像,这里上标r和i分别表示复数的实部和虚部;或者,在场强足够高(一般在1.5t至11.7t)而适用对称回波相位编码的情况下,在稳态多回波序列中基于水脂化学位移差(例如3.0t时420hz)设置te=2.4(ms),δτ=1/δf/2=1.2(ms),tr=2·te+2·δτ=7.2(ms),采用常规三点dixon数据处理方式获得水像和脂肪像。
优选的,最小二乘法拟合分析采用矩阵运算按照式(3)和式(4),即,
优选的,在中低场mri系统上采用不对称相位编码,即π/2和π,通过水模测试基于
有益效果:本发明的成像方法可在保持高信噪比条件下实现秒级时间分辨率,并改善水脂分离的精确性,尤其是有助于抑制腹部水脂分离成像的运动伪影,不仅适用于高场成像系统也适用于中低场成像系统。
附图说明
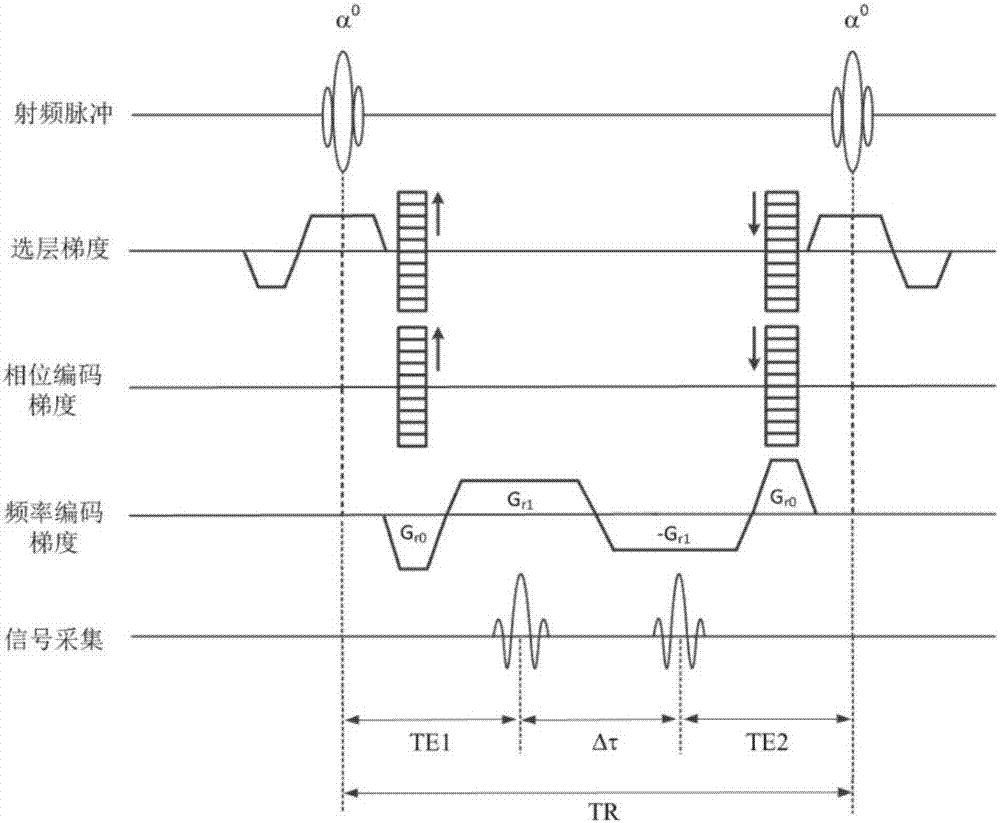
图1为基于单次激发三点相位编码的三维稳态进动水脂分离序列。其中,te是回波时间,δτ是相邻回波的峰值之间的时间间隔,gr0是预备读梯度,gr1是二维平面频率编码梯度。
图2为基于单次激发两点相位编码的三维稳态进动水脂分离序列。其中,te是回波时间,δτ是相邻回波的峰值之间的时间间隔,gr0是预备读梯度,gr1是二维平面频率编码梯度。
图3为基于单次激发三点相位编码的二维稳态进动水脂分离序列。其中,te是回波时间,δτ是相邻回波的峰值之间的时间间隔,gr0是预备读梯度,gr1是二维平面频率编码梯度。
图4为基于单次激发两点相位编码的二维稳态进动水脂分离序列。
其中,te是回波时间,δτ是相邻回波的峰值之间的时间间隔,gr0是预备读梯度,gr1是二维平面频率编码梯度。
图5为本发明成像序列调试方案
图6为本发明多通道信号合成参数标定方案。
具体实施方式
为使本发明解决的技术问题、采用的技术方案和达到的技术效果更加清楚,下面结合附图和实施例对本发明作进一步的详细说明。可以理解的是,此处所描述的具体实施例仅仅用于解释本发明,而非对本发明的限定。另外还需要说明的是,为了便于描述,附图中仅示出了与本发明相关的部分而非全部内容。
本发明的一种稳态进动梯度多回波水脂分离成像方法,是由多回波水脂分离序列、信号调试模块、数据采集处理模块和水脂分离模块构成。其中,成像序列以磁共振成像系统上常规扫描的真稳态进动成像序列为基础,在10ms量级或更短的序列重复周期内射频脉冲反复激发成像区的质子磁共振信号,脉冲翻转角在第一个序列重复周期内设置为+α/2并取消采样期,在后续序列重复周期内脉冲翻转角交替设置为+α和-α,同时通过选层梯度、相位编码梯度和频率编码梯度进行三维空间编码,每个方位的梯度积分面积之和为零,使得质子磁化矢量进动趋于稳态,其特征在于,采样期施加三个(或两个)极性交替的频率编码梯度,且频率编码方向的梯度总积分面积为零,使得质子磁化矢量进动达到完全稳态后产生三个(或两个)高信噪比的梯度回波信号,并基于相邻回波峰的时间间隔δτ和水脂化学位移差δf对梯度回波进行直接相位编码,在序列参数表中设置δτ为1/δf/n,n优先为3(或4),并设置序列重复时间tr=2·te+2·δτ(或tr=te1+te2+δτ),其中te、te1和te2为回波时间,取最小值或设置为1/δf;并且,为了充分抑制场不均匀性效应,在序列执行过程中精确测试射频系统和梯度系统的响应延迟时间、接收机采样延迟时间、梯度矩阵的运算时间和其它序列指令执行时间,然后在序列内精确设置最小回波时间temin和最小序列重复时间trmin,且te≧temin,tr≧trmin,序列重复执行直到磁化矢量进动达到稳态后开始采样,在每个采样期内磁化矢量在极性正负交替的多个(这里优先为三个或两个)频率编码梯度作用下形成多个梯度回波,回波时间依次为t1=te,t2=te+δτ,t3=te+2·δτ(或t1=te1,t2=te1+δτ),采用正交采集或多通道并行采集模式接收信号并数字化;尤其是,为了克服涡流场效应、麦克斯韦场效应和回波时间较长可能引起的相位缠绕问题,成像系统通过一个专用的信号调试模块在相位编码梯度关闭条件下调用上述成像序列对标准水模进行参考扫描,先在一个读梯度施加条件下调整tr和te(或te1、te2)进行单个梯度回波信号幅度和对称性优化,再在极性交替的三个(或两个)读梯度施加条件下调整gr0和gr1梯度幅度直到产生多个梯度回波组份,回波峰两两之间等距且δτ=1/δf/n,将参数调试结果保存到参数表,同时保存回波信号以计算双极性梯度作用下相邻梯度回波的相位差δφ=<φ1>-<φ2>并通过itoh算法进行相位解缠,接着,成像系统通过扫描模块调用上述成像序列和参数表进行油水混合物标样或人体扫描并存贮k空间数据,随后数据采集处理模块将k空间数据沿选层方向进行一维离散逆傅立叶变换,得到每个层面的k空间矩阵,按化学位移编码数(一般为3或2)将k空间矩阵在频率编码方向一分为三或一分为二,得到三组复矩阵i0、i1和i2(或两组复矩阵i0和i1),再将i1进行时间反演和矩阵共轭后乘以e-iδφ进行初级相位校正,最后,成像系统通过水脂分离模块进行二维离散逆傅立叶变换得到三幅图像s0、s1和s2(或两幅图像s0和s1),在单次激发三回波情况下水脂分离模块基于下式进行最小二乘法迭代拟合,消除场不均匀性导致的相位误差并得到水像和脂肪像。
这里,sj其任一像素对应的磁共振信号,sw和sf分别表示人体组织中水和脂肪的质子磁化矢量的初始值,上标r和i分别表示复数的实部和虚部,下标w和f分别表示水和脂肪,ν表示与磁场不均匀性有关的中心频率偏差,或者在单次激发双回波情况下水脂分离模块基于水模扫描的回波信号计算得到初始相位,再通过复数运算消除人体扫描的正交相位图s0和反相图s1的初始相位,所得正交相位图s'0的实部和虚部即为水像和脂肪像,所得反相图s1'的相位图(φi,j)dim1×dim2=2πδτ(νi,j)dim1×dim2进行相位展开后产生场图(νi,j)dim1×dim2,这里dim1和dim2分别为频率编码数和相位编码数,然后将s1'乘以e-i·φ得到消除了场不均匀效应的反相图。
上述成像序列的二维版也可按同样方式基于水脂化学位移差实现梯度回波直接相位编码,除序列参数表中设置梯度相位编码数设置为1以外,按类似方式进行信号调试、数据采集处理和水脂分离得到水像和脂肪像。
实施例1:在1.5tmri系统的序列库中安装图1或图3所示序列,其中射频脉冲采用最小相位slr波形,脉宽为1ms或更短,梯度上下沿时间为0.1ms或更短,并在序列参数表中设置频率编码数设置为dim1=160,相位编码数设置为dim2=256,选层方向相位编码数设置为dim3=32,化学位移相位编码数设置为dim4=3,视野设置为fov=220mm,接收机带宽设置为bw=125khz,δτ优选为1/δf/3=1.5ms,每组回波的回波时间依次为t1=4.1ms,t2=5.6ms,t3=7.1ms,相应的回波编码相位依次为-π/6,π/2和7π/6,并设置te=4.5ms,tr=12ms,δf≈220hz,。然后,在临床操作软件中安装并依次执行信号调试模块、扫描模块、数据采集处理模块和水脂分离模块,各模块的设计方式和工作流程说明如下:
信号调试模块按照图5所示的调试方案进行序列参数校准,该模块执行时要求使用标准水模,并关闭相位编码梯度在实时模式下采集和显示梯度回波信号。参数校准完毕,将标准水模的回波信号保存为复矩阵k作为参考信号供数据采集处理模块调用,并将优化的参数值保存到序列参数表。其中,油水混合物标样测试仅在首次运行本发明的成像序列时需要,用于在临床扫描前验证参数校准的精确度。
扫描模块基于上述优化的序列参数值运行图1或图3所示的成像序列,对人体检查部位进行一次扫描获得化学位移编码的k空间数据。
数据采集处理模块调用参考信号复矩阵k并按dim1=256和dim4=3分离为三个复矩阵k1,k2和k3,选取k1和k2*信噪比较大的数据点并计算各自的相位均值<φ1>和<φ2>,然后调用人体扫描数据并沿选层方向进行一维离散逆傅立叶变换,得到32个层面的k空间矩阵(480×256),再按dim1=256和dim4=3将每个层面的k空间矩阵沿频率编码方向一分为三,保存为三组大小为dim1×dim2(这里160×256)的复矩阵,即i0,i1和i2,并将i1进行矩阵共轭转置后乘以
最后,水脂分离模块调用初级相位校正后的三组复矩阵(i0,i1和i2)并进行二维离散逆傅立叶变换(2difft),得到三幅图像,即,s0=2difft{i0},s1=2difft{i1}和s2=2difft{i2},并对这三幅图像进行数据分析,有关算法设计说明如下:
对于任一层面j所对应的图像,其任一像素对应的磁共振信号sj可描述为
这里,sw和sf分别表示人体组织中水和脂肪的质子自旋密度的初始值,后者分别构成水像和脂肪像的复数矩阵,下标w和f分别表示水和脂肪,tn表示三幅图像(s0、s1和s2)对应的t1、t2和t3,ν表示场不均匀性或涡流效应引起的频率偏差。在多通道接收或正交接收模式下,采用并行采集重建方式(例如sense和grappa等)或直接信号合成方式,即
这里采用线性最小二乘法拟合求解上述线性方程组,具体步骤如下:
(1)设ν的初始值为ν0=0,按照下式进行水脂信号分析
上式中上标t表示复矩阵转置,
(2)使用下式计算δν
上式中
(3)计算ν=ν0+δν,将
(4)重复上述步骤直到δν<0.5hz;
(5)建立大小为(2k+1)(2k+1)的高斯模板
(6)对于其它层面的图像数据重复上述所有步骤得到水像和脂肪像。
上述不对称回波相位编码和数据处理方式不仅有利于减少稳态进动成像的重复时间tr,也有利于避免水和脂肪含量相当的个别像素出现异常的计算误差。显然,如果场强足够高(例如3.0t),对称回波相位编码所要求的δτ很短以至于稳态进动条件易于建立,在这样的情况下图一和图三所示的序列中设置te=2.4(ms),δτ=1/δf/2=1.2(ms),tr=2·te+2·δτ=7.2(ms),水脂分离模块可采用常规三点dixon数据处理方式获得水像和脂肪像。
实施例2:
在低场强(例如0.35t)情况下,信号调试模块和扫描模块调用图2或图4所示的成像序列,参数表中设置te=1/δf/4和δτ=1/δf/4,回波峰的化学位移编码相位分别为π/2和π,然后按照上述类似方式进行扫描和信号处理,得到正交相位图s0和反相图s1,最后水脂分离模块采用下述方式对这两幅图像进行数据处理:
首先,基于
s'0=sw+i·sf(7)
s1'=(sw-sf)·ei2πνδτ(8)
于是,水像和脂肪像分别计算为sw=re(s'0),sf=im(s'0),这里re和im分别表示复数的实部和虚部。最后,通过四象限反正切函数计算s1'的像素(i,j)的相角φi,j=2πνi,jδτ并基于区域增长法对(φi,j)进行相位解缠,再将s1'的像素(i,j)乘以e-φ(i,j),得到消除了场不均匀效应的反相图。
最后应说明的是:以上各实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述各实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围。
- 还没有人留言评论。精彩留言会获得点赞!