制备用于确定脂质干扰的脂血血浆或血清样本的制作方法
本发明涉及体外诊断领域,并且涉及制备脂血血浆或血清样本的方法以及使用该方法用于在定量地测定血浆或血清样本中分析物的量或活性中对脂质干扰进行确立。
背景技术:
血浆和血清样本中临床相关参数的测定可能受到甘油三酯浓度(脂血)升高的显著影响。会相对频繁地出现甘油三酯浓度升高的脂血样本,并且例如可以由高脂膳食、糖尿病、慢性肾衰竭、胰腺炎、红斑狼疮、多发性骨髓瘤或摄取药物或摄取口服避孕药引起。
甘油三酯浓度升高的干扰作用主要基于样本的浑浊(浊度),这种浑浊肉眼有时可见并导致光散射和吸收增加。这种现象最主要会干扰光度分析系统。另一个干扰作用是会损害待检测分析物的溶解度。
因此,现代自动分析仪越来越多地包括所谓的预先分析分析单元,在该预先分析分析单元中,在执行一种或多种特定分析物的实际试验之前,相对于任何干扰物质(诸如脂质、血红蛋白和胆红素)来分析样本材料。如果在样本中确立了一种或多种干扰物质的临界量,则例如可向针对样本获得的试验结果提供警告,这意指用户被告知在此可能测量到错误的结果。
由于引起显著干扰的、用于每个试验的甘油三酯浓度是不同的,并且甘油三酯浓度取决于所使用的分析仪、所使用的试剂等,因此必须针对每个试验执行干扰研究,以便确定在哪个甘油三酯浓度中的特定试验不再提供可靠的试验结果。
存在这样问题,即尚未有标准化的、执行干扰研究所需的脂血样本材料。迄今为止,脂肪乳剂(intralipid),一种大豆脂质乳剂,被经常添加到人血浆样本或血浆池中,以便模拟脂血干扰。然而,已发现添加脂肪乳剂的方法并不能普遍适用于脂质干扰的测定,因为在所有情况下由脂肪乳剂引起的干扰与在天然脂血样本中发生的干扰没有相关联(bornhorst,j.a等,天然和脂肪乳剂补充样本中脂质干扰的特定分析的差异,临床化学,2004年,第50卷(第11期):2197-2201)。因此,优选使用脂血供体样本用于干扰研究。
然而,因为必需要检验极大的供体组,所以只能通过非常大的气力才能获得足够量的天然脂血患者样本,特别是具有异常高的甘油三酯浓度(>500mg/dl)的那些样本。
技术实现要素:
因此,本发明的目的是找到一种提供脂血血浆或血清样本的更简单的方法。
根据本发明,该目的通过对含脂质的血浆或血清样本进行离心以便获得脂质浓缩相,并且然后将脂质浓缩相添加到血浆或血清样本中来实现。
这具有以下优点:可以不必须使用例如脂肪乳剂的人造物质来产生任何期望的甘油三酯浓度。
因此,本发明提供了制备脂血血浆或血清样本的方法。该方法包括以下步骤:
(a)对含脂质的血浆或血清样本进行离心,以便将含脂质的上清液与脂质贫化相分离;
(b)移除含脂质的上清液;以及
(c)将含脂质的上清液与血浆或血清样本混合。
同义地使用术语“甘油三酯”和“脂质”。
术语“脂血血浆或血清样本”理解为意指来自单个供体的血浆或血清样本或者来自多个供体的血浆或血清样本的混合物(池),其甘油三酯浓度高于参考范围,即,甘油三酯浓度为150mg/dl(1.71mmol/l)或更高。
术语“含脂质的血浆或血清样本”理解为意指来自单个供体的血浆或血清样本或者来自多个供体的血浆或血清样本的混合物(池),其甘油三酯浓度在参考范围内或高于参考范围,参考范围为≤150mg/dl(1.71mmol/l)。
本发明特别是基于人血浆和血清样本。然而,类似的方法原则上也可应用于动物血浆和血清样本。
在优选的实施例中,对含脂质的血浆或血清样本进行划分,并且在该方法的步骤(a)中对含脂质的血浆或血清样本的第一子份额进行离心,然后在步骤(b)中移除含脂质的上清液,然后在步骤(c)中将含脂质的上清液与相同的含脂质的血浆或血清样本的第二子份额混合。这具有以下优点:在具有例如确定的分析物浓度或活性的该特定样本中,只有脂质分数增加,而剩余的样本组成保持不变。此外,其优点在于,可以检验由该特定样本的脂质引起的干扰。因此,在对多种不同的脂血样本的研究中,也可包括所述样本相对于在干扰极限的最终测定中的干扰的可变性。
可替选地,在步骤(c)中可将移除的含脂质的上清液与离心的样本的脂质贫化相的子份额混合。
含脂质的上清液和血浆或血清样本的混合比显然取决于起始材料的甘油三酯浓度和期望的甘油三酯浓度。
步骤(a)中对含脂质的血浆或血清样本的离心优选在至少2000×g下进行至少10分钟。使用更长的离心时间和更高的离心力也是绝对合理的,诸如,例如在15000×g下进行10分钟或在82000×g下进行60分钟,或者在133000×g下进行60分钟。
含脂质的血浆或血清样本的离心使得浑浊的、含脂质的上清液与下方澄清的、脂质贫化相分离,该分离是肉眼可见的。例如通过使用移液针小心地穿透含脂质的上清液并小心地吸除脂质贫化相,可以实现移除含脂质的上清液,这意指在容器中仅保留含脂质的上清液。将血浆或血清样本添加到容器中并振荡之后,样本与含脂质的上清液混合。还可使用其它已知的均化方法,诸如,例如超声处理。
本发明还提供了在对用于定量地测定血浆或血清样本中分析物的量或活性的方法中的脂质干扰进行确立的方法中、使用根据本发明的方法制备的脂血血浆或血清样本的使用方法。
优选地,根据本发明制备的脂血血浆或血清样本用于在定量地测定血浆或血清样本中分析物的量或活性的方法中对脂质干扰进行确立的方法,其中确立脂质干扰的方法包括以下步骤:
(a)通过将至少一种分析物专用的检测试剂与具有分析物浓度或活性的非脂血血浆或血清样本混合来提供第一试验混合物,并测量第一试验结果;
(b)通过将相同的至少一种分析物专用的检测试剂与具有相同分析物浓度或活性的脂血血浆或血清样本混合来提供第二试验混合物,并测量第二试验结果;
(c)确立第一试验结果与第二试验结果之间的差异;以及
(d)当第一试验结果与第二试验结果之间的差异超过预定的容差极限时,例如当第一试验结果与第二试验结果之间的差异为5%或以上时,确立脂质干扰。
以这种方式,对于每个分析试验,可合理地确定从哪个甘油三酯浓度中的试验不再提供可靠的试验结果。
“分析物”应理解为意指在样本材料(在这种情况下为血浆或血清)中待检测的物质或样本材料的可测量属性,该属性受多种物质的影响。例如,分析物可以是肽、蛋白质、多糖或核酸,特别是具有特定生物学功能的蛋白质或蛋白质复合体,诸如,例如免疫球蛋白、细胞因子、受体、酶、激素、癌抗原、组织专用的抗原、血液凝固因子、来自微生物病原体的抗原等等。典型的受多种物质影响的血浆样本属性例如为凝血时间。凝血试验允许借助于测量体外纤维蛋白形成速率来测量单个或多个凝血因子的活性。
用于定量地测定血浆或血清样本中分析物的量或活性的方法可以是任何可想到的试验原理,诸如,例如颗粒增强免疫分析法、显色试验法或凝血试验法。
分析物专用的检测试剂含有一种或多种物质,其允许检测特定分析物或样本的另一个可测量的属性,例如一种或多种抗体或抗原、显色肽底物和/或酶活化剂。例如,可以设想将液体检测试剂与样本混合,该试剂含有溶解形式的分析物专用的物质。可替选地,可以设想,检测试剂由涂覆有一种或多种分析物专用的物质的固相组成。
取决于所使用的试验原理,可通过例如分光光度法、浊度测量法、比浊测量法、发光测量法、荧光测量法、辐射测量法等等进行试验结果的测量。
为了确立脂质干扰,即对试验方法的测量精度的显著损害,使用作为参考样本的非脂血血浆或血清样本(具有≤150mg/dl的甘油三酯浓度)以及使用至少一种根据本发明制备的血浆或血清样本(具有>150mg/dl的甘油三酯浓度)两者来执行相同的试验方法。如果两个样本具有相同的分析物浓度或活性,则第一试验结果与第二试验结果之间的差异可归因于脂血样本的甘油三酯浓度升高。优选地,参考样本是含脂质样本的脂质贫化相,其为了制备脂血样本而被离心。
当第一试验结果与第二试验结果之间的差异超过预定的容差极限时,例如当第一试验结果与第二试验结果之间的相对差异为5%或以上时,存在脂质干扰。也可以将最大绝对分析物差异限定为容差极限。
优选地,对于每种样本类型的脂质干扰研究,测量多个样本,优选10至20个样本,使得能够执行统计学评估。优选地,测量正常分析物浓度或活性的10至20个非脂血样本和正常分析物浓度或活性的相同数量的脂血样本。另外地或可替选地,可以并行地测量多个非脂血样本和相同数量的脂血样本,该脂血样本具有覆盖试验方法测量范围的分析物浓度或活性。此外,也可测量正常的、降低的或升高的分析物浓度或活性的不同脂血样本类型,这些样本类型具有高于参考范围的不同的甘油三酯浓度,即在150mg/dl与3000mg/dl之间的浓度。
优选地,使用已经由相同的含脂质的血浆或血清样本制备的、作为起始材料的、脂血血浆或血清样本以及非脂血血浆或血清样本来确立脂质干扰。这具有以下优点:在两个样本中,除了脂质分数之外,样本组成以及因此分析物浓度是相同的,脂质分数的影响是待检验的。
进一步优选地,使用包括以下步骤的方法来制备非脂血血浆或血清样本:
(a)对含脂质的血浆或血清样本进行离心,并且将脂质贫化相与含脂质的上清液分离。
这具有以下优点:可使用在旨在用于制备脂血样本的含脂质上清液的制备中作为副产物产生的脂质贫化相,使得能够以最小的耗费使用现有起始材料。
根据本发明制备的脂血血浆或血清样本也可用于对定量地测定血浆或血清样本中分析物的量或活性的方法中的脂质干扰进行确立的方法,其中确立脂质干扰的方法包括以下步骤:
(a)通过将至少一种分析物专用的检测试剂与非脂血血浆或血清样本的第一子份额混合来提供第一试验混合物,并测量第一试验结果;
(b)通过将相同的至少一种分析物专用的检测试剂与相同的非脂血血浆或血清样本的第二子份额的脂质贫化相混合来提供第二试验混合物,该非脂血血浆或血清样本先前已经在至少2000×g下离心至少10分钟,并测量第二试验结果;以及
(c)确立第一试验结果与第二试验结果之间的第一差异;以及
(d)通过将相同的至少一种分析物专用的检测试剂与脂血血浆或血清样本的第一子份额混合来提供第三试验混合物,并测量第三试验结果;
(e)通过将相同的至少一种分析物专用的检测试剂与相同脂血血浆或血清样本的第二子份额的脂质贫化相混合来提供第四试验混合物,该非脂血血浆或血清样本先前已经以至少2000×g下离心至少10分钟,并测量第四试验结果;以及
(f)确立第三试验结果与第四试验结果之间的第二差异;以及
(g)当第一差异与第二差异之间的偏差超过预定的容差极限时,例如当第一差异与第二差异之间的、例如分别表示为相对差异的偏差,超过5%或以上时,确立脂质干扰。
根据本发明制备的脂血血浆或血清样本也可用于在用于对定量测定血浆或血清样本中分析物的量或活性的方法中的脂质干扰进行确立的方法的一个实施方案中,其中确立脂质干扰的方法的该实施方案包括以下步骤:
(a)通过分别将至少一种分析物专用的检测试剂与非脂血血浆或血清样本的第一子份额分别混合来提供多个第一试验混合物,并测量多个第一试验结果;
(b)通过分别将相同的至少一种分析物特定的检测试剂与相同非脂血血浆或血清样本的第二子份额的脂质贫化相分别混合来提供多个第二试验混合物,其中非脂血血浆或血清样本先前已经在至少2000×g下离心至少10分钟,并测量多个第二试验结果;以及
(c)确立特定的第一试验结果与第二试验结果之间的第一差异,并计算所有的确立的第一差异的平均值;以及
(d)通过将相同的至少一种分析物专用的检测试剂与脂血血浆或血清样本的第一子份额混合来提供第三试验混合物,并测量第三试验结果;
(e)通过将相同的至少一种分析物专用的检测试剂与相同脂血血浆或血清样本的第二子份额的脂质贫化相混合来提供第四试验混合物,该脂血血浆或血清样本先前已经在至少2000×g下离心至少10分钟,并测量第四试验结果;以及
(f)确立第三试验结果与第四试验结果之间的第二差异;以及
(g)通过减去所有确立的第一差异的平均值来计算校正的第二差值;以及
(h)当校正的第二差异超过预定的容差极限时,例如当校正的差异超过先前确定的10%置信区间时,确立脂质干扰。
这具有以下优点:可识别用来制备样本的脂质贫化相的离心方法的任意作用,这些作用可改变分析物浓度。如果离心方法本身改变样本的分析物水平,在确定干扰时必须考虑到这种作用。例如,在凝血试验的情况下可以想到,由于离心使重要的囊泡结合因子沉淀,并且这单独导致凝血时间改变。由于该原因,离心方法不仅用于脂血样本,还用于非脂血样本。例如,如果在脂血样本的情况下以及在非脂质样本的情况下,分别确立了分析物水平在脂质贫化相中相对于未离心样本的10%的相对偏差,则这可归因于离心。那么就不存在甘油三酯干扰。如果离心方法在非脂血样本的分析物水平上产生+10%的偏差,并且在脂血样本中观察到+20%的偏差,则能够从中推断出10%的干扰是由甘油三酸酯引起的。
由于在单个非脂血和脂血样本中,干扰的程度和离心方法的潜在影响两者都可能变化很大,因此测量具有不同甘油三酯水平的和不同分析物水平的脂血样本以及具有不同分析物水平的非脂血样本是有益的。
附图说明
图1对用于测定aptt的方法中的脂质干扰进行测定;
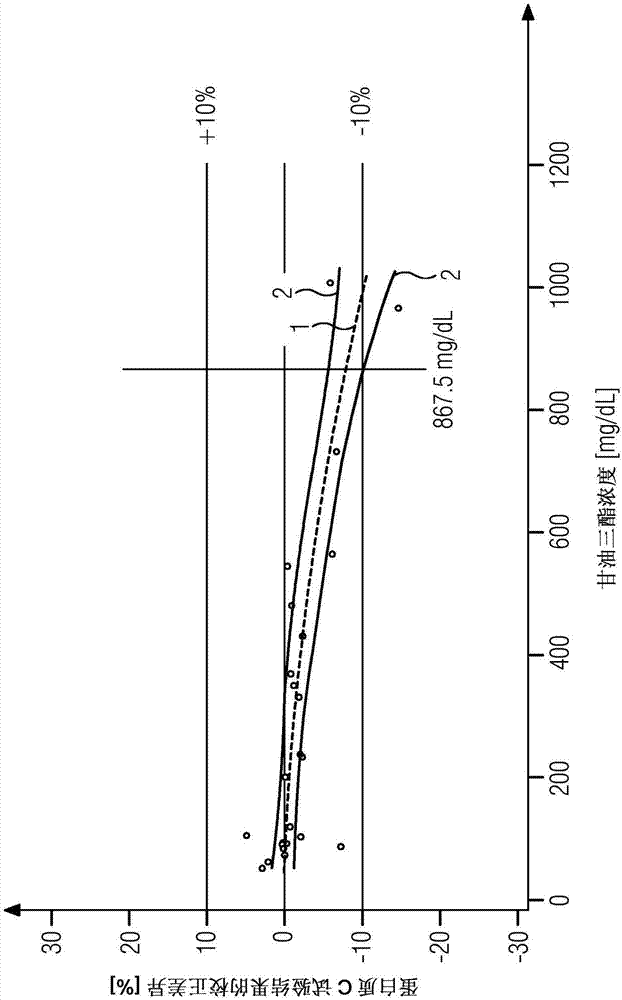
图2对用于测定蛋白质c的方法中的脂质干扰进行测定。
以下示例性实施例用来说明根据本发明的方法并且不应被理解为限制。
具体实施方式
实例1:对用于测定aptt的方法中的脂质干扰进行测定
1a)根据本发明制备用于在对使用dade肌动蛋白试剂的aptt进行测定的方法中测定脂质干扰的脂血血浆样本
使用来自7个供体的7个天然脂血柠檬酸盐血浆样本(甘油三酯水平>150mg/dl)。使用trig试验法并且使用dimensionvistasystem(美国,纽瓦克市,西门子医疗)来测定甘油三酯水平。将约18ml至20ml的所述样本在超速离心机(德国,哈瑙,赛默飞世尔的赛默飞科技sorvalwxultra,转子t-1250)中以对应于133000×g的33200rpm进行离心1小时。在移液管的帮助下,小心地移除最上层的富含脂质的上清液,同时避免与下层的脂质贫化相混合。取决于样本,将0.7ml至3.0ml所述富含脂质的上清液与来自同一供体的天然柠檬酸盐血浆样本的未离心子份额混合,并且在一些情况下与非脂血因子缺乏血浆(甘油三酯水平通常大约为100mg/dl)混合。由此制备的脂血样本的总体积约为12ml。再次测量由此制备的样本的甘油三酯水平,并且其水平为在234mg/dl至1007mg/dl之间。
表1包含根据本发明制备的脂血样本号l3-l9的和三个另外的天然脂血样本(样本号l1、l2和l10)的最终甘油三酯浓度,以及也包含来自供体的天然(未离心的、未处理的)血浆样本、含脂质的上清液、缺乏血浆和肝素溶液的量的混合比。进行与缺陷血浆或肝素溶液的混合以扩大aptt测量范围。
表2包含同样用于干扰研究的、非脂血样本号nl1-nl12的组成和最终甘油三酯浓度。
表1:脂质样本的组成
■表2:非脂血样本的组成
■
1b)在对使用dade肌动蛋白试剂的aptt进行测定的方法中测定脂质干扰
在活化部分凝血活酶时间(aptt)的情况下,将血浆样本与含有磷脂和表面活化剂(dade肌动蛋白试剂,德国,马尔堡,西门子医疗)的试剂混合。在培养时间之后,通过添加cacl2开始凝血。在此处描述的实例中,在sysmexcs-5100分析仪(西门子医疗,德国,马尔堡)上自动处理aptt。随着吸光度的增加,用光度法测量凝血反应。直到吸光度特定地增加为止的时间是以秒计的凝血时间,其表示aptt试验的结果。
从根据1a)制备的所有样本中,使用一个子份额用于aptt的测量(试验结果1)。将根据1a)制备的每个样本的第二子份额在133000×g下离心1小时,并且使用脂质贫化相作为aptt测量的样本(试验结果2)。如果离心没有影响,则离心等分试样的脂质贫化相应含有与未离心样本相同的分析物量。将每个样本的两个试验结果(凝血时间,以秒为单位)彼此进行比较,并计算以%为单位的相对差异100×(试验结果1-试验结果2)/试验结果2。
从非脂血样本的试验结果的相对差异中,计算平均值(在这种情况下为:0.6)。由于非脂血样本没有表现出由于脂血引起的干扰,因此该平均差异归因于该方法的非特定的影响因子(例如,离心)。为了校正该作用,通过从相对差中减去所述平均值来确定每个样本的校正差异。校正差异为由脂质引起的干扰的量度。
表3示出了每个样本的试验结果1和2、确定的相对差异和校正差异。差异值是舍入值。
■表3:aptt试验结果和偏差
■
将校正差异,即未离心样本的试验结果与离心样本的试验结果的偏差(减少了非脂血样本的差异的平均值),对未离心样本的甘油三酯浓度作图(图1,线1)。应用多项式拟合方法,并计算相关的置信区间(图1,线2)。置信区间极限与10%相对偏差的标准的交叉点确定了甘油三酯浓度,根据该甘油三酯浓度,预料到在测试的aptt试验方法(676.5mg/dl)中有脂质干扰。
实例2:对测定蛋白质c的方法中的脂质干扰进行测定
2a)根据本发明制备用于在测定使用berichrom蛋白质c试验的蛋白质c的方法中对脂质干扰进行测定的脂血血浆样本
使用来自12个供体的12个天然脂血柠檬酸盐血浆样本(甘油三酯水平>150mg/dl),并执行如1a)所描述的方法。再次测量由此制备的样本的甘油三酯水平,并且其水平为在199mg/dl至1007mg/dl之间。
表4包含根据本发明制备的脂血样本号l1-l12的和另外的天然脂血样本(样本号l13)的最终甘油三酯浓度,以及来自供体的天然(未离心的、未处理的)血浆样本、含脂质的上清液、缺乏血浆和肝素溶液的量的混合比。进行与缺乏血浆的混合以扩大蛋白质c测量范围。
表5包含同样用于干扰研究的、非脂血样本号nl1-nl12的组成和最终甘油三酯浓度。
表4:脂血样本的组成
■表5:脂血样本的组成
■
2b)对在使用berichrom蛋白质c试验测定蛋白质c的方法中的脂质干扰进行测定
在试验混合物中,将血浆样本与蛇毒活化剂一起培养,从而引起蛋白质c的活化。此外,添加被活化蛋白质c切割的显色肽底物。该反应实现了增加在405nm下测量的吸光度。基于校正曲线,吸光度的增加被转换为蛋白质c的结果(标准的%)。在这里描述的实例中,在sysmexcs-5100分析仪(西门子医疗,德国,马尔堡)上自动处理蛋白质c试验。
从在2a)情况下制备的所有样本中,使用一个子份额用于测量蛋白质c(试验结果1)。将在2a)下制备的每个样本的第二子份额在133000×g下离心1小时,并且使用脂质贫化相作为蛋白质c测量的样本(试验结果2)。如果离心没有影响,则离心等分试样的脂质贫化相应含有与未离心样本相同的分析物量。将每个样本的两个试验结果(标准的%)彼此进行比较,并以%为单位计算相对差异100×(试验结果1-试验结果2)/试验结果2。
从非脂血样本的试验结果的相对差异中,计算平均值(在这种情况下为:-2.4)。由于非脂血样本没有表现出由于脂血引起的干扰,因此该平均差异归因于该方法的非特定的影响因子(例如,由于离心)。对于该作用的校正,通过从相对差中减去所述平均值来确定每个样本的校正差异。校正差异为由脂质引起的干扰的量度。
表6示出了每个样本的试验结果1和2、确定的相对差异和校正差异。差异值是舍入值。
■表6:蛋白质c试验结果和偏差
■
将校正差异,即未离心样本的试验结果与离心样本的试验结果的偏差(减少了非脂血样本的差异的平均值),对未离心样本的甘油三酯浓度作图(图2,线1)。应用多项式拟合方法,并计算相关的置信区间(图2,线2)。置信区间极限与10%的相对偏差的标准的交叉点确定了甘油三酯浓度,根据该甘油三酯浓度,预料到在测试的蛋白质c试验方法(876.5mg/dl)中有脂质干扰。
- 还没有人留言评论。精彩留言会获得点赞!