一种均相发光法检测动物降钙素原的试剂盒的制作方法
本发明属于试剂盒技术领域,尤其是一种均相发光法检测动物降钙素原的试剂盒。
背景技术:
化学发光法是目前最先进的免疫检测方法学,按标记物不同分为直接化学发光法、酶促化学发光法和电化学发光法;按是否存在分离清洗步骤,分为异相化学发光法和均相化学发光法。目前,在人医体外诊断检测方面,国内外使用直接化学发光法和酶促化学发光法的检测产品较多,都属于异相化学发光法。国外厂家包括雅培、西门子、索林、贝克曼和希斯美康等,国内厂家包括新产业、安图、迈克、迈瑞、泽成、长光华医等。各厂家仪器平台大同小异,尤其是国内厂家,仪器结构复杂、故障率较高,质量参差不齐,影响了客户对产品的信任。同时,国内厂家在试剂品种上未进行大胆的创新,只是重复别人有的品种,使用的原料(抗原抗体)同一来源,导致同质化严重,市场竞争激烈。现阶段仅有西门子一家使用纯态氧介导的均相化学发光法(光激化学发光法)产品上市,检测需要特殊的loci模块。loci技术是一步式化学发光夹心免疫检测方法,试剂中含有两种合成珠试剂和一种生物素化学的单克隆抗体。第一种珠试剂(敏感珠)包被有链霉亲和素,并含有光敏感染料;第二种珠试剂(化学珠)包被另一种抗体,并含有化学发光染料;样本和化学珠及生物素化抗体进行孵育后形成夹心复合物;然后加入敏感珠,与生物素结合后形成聚集的免疫复合物;复合物在680nm光照射下其中的敏感珠会产生单线态氧,单线态氧弥散到化学珠后可引发化学发光反应,在612nm波长下测量反应所产生的化学发光信号。该方法需要激发光,对设备要求高,标记材料特殊,不易获取。
lumigen公司发明了一种均相化学发光法1,2,使用化学发光标记物标记抗原或抗体,同时辣根过氧化物酶(hrp)标记另一株抗原或抗体,一起去检测样本中的分析物,在纯液相条件下直接注入激发物质产生化学发光,达到定量检测目的。该方法不仅保证了化学发光法检测性能的优势,同时对检测设备要求降低,设备小型化、简易化。我们将该方法用于对动物(包括犬和猪)的降钙素原(pct)的检测。
降钙素原,一种14kd的蛋白质,为降钙素的前体。细菌感染时会表达上调,在人医中作为脓毒症的标志物,指导抗生素使用。文献报道3犬发生感染和炎症了,pctmrna表达上调。另有文献报道,lps诱导猪pct的表达4,而且免疫中和pct能够抑制猪的脓毒症发展进程5。
目前,针对人的降钙素原检测平台较多,包括免疫层析、化学发光等,但未出现均相化学发光用于人的pct检测。在兽医领域更是没有,还未出现pct这个检测项目。我们通过pct蛋白同源性分析,发现pct序列在一些物种间高度保守,包括猪、犬和猫等。我们通过制备多克隆抗体通过抗体夹心法均相化学发光法检测各物种的pct,发现在猪和犬细菌感染性疾病中的诊断价值较高,故开发此试剂盒。兽医现有诊断细菌感染性疾病的检测手段主要为血常规和crp,诊断特异性不高,抗生素使用比较混乱,迫切需要pct项目的出现。
技术实现要素:
本发明的目的是:克服现有技术中的不足,提供一种均相化学发光法检测动物降钙素原的试剂盒。
为解决上述技术问题,本发明采用的技术方案如下:
一种均相化学发光法检测动物降钙素原的试剂盒,
所述试剂盒中的测试管中的成分为10mmpbs缓冲液,ph=7.0,每测试份为170.ul体积,其中含有20ug/ml吖啶酯标记pct抗体和20ug/mlhrp标记pct抗体,另外还含有0.01%的proclin300;
所述试剂盒采用以下制备方法制得:
(1)pct抗原设计与制备,包括:pct抗原氨基酸序列和碱基序列设计,序列表达,质粒构建,质粒提取、蛋白表达、蛋白纯化与检测;
(2)pct抗体制备,包括:免疫采血,杂交瘤融合筛选;
(3)吖啶衍生物标记pct抗体;
(4)hrp标记pct抗体;
(5)夹心法检测。
优选的,所述pct抗原氨基酸序列如:seqidno.1,碱基序列如:seqidno.2。
优选的,所述质粒构建包括合成基因序列,包括包括5’端ecori,3’端xhoi酶切位点,n端添加kozak(gccgccacc)以及cd33信号肽序列(atgccgctgctgctactgctgcccctgctgtgggcaggggcgctagct),c端添加histag序列(catcatcaccatcaccat)以及终止密码(tgatag),并将此序列构建至pcdna4.0tomychisa载体,合成的基因序列如:seqidno.3。
优选的,用真核表达载体大量提取无内毒素质粒,将所提取的无内毒素质粒进行细胞转染,收集细胞上清及细胞裂解液,采用ni柱亲和层析,收集样品进行sds-pagewesternblot检验,浓度检测,将合格样品,透析至pbs,并将蛋白浓缩至>1.0mg/ml。
优选的,所述杂交瘤融合筛选包括以下步骤:
(1)融合前饲养层细胞制备,包括巨噬细胞和胸腺细胞,制备在无菌环境中进行;
(2)融合前骨髓瘤细胞制备;
(3)提取免疫成功的脾脏细胞;
(4)细胞融合;
(5)elisa检测;
(6)亚克隆筛选。
采用本发明的技术方案的有益效果是:
1、均相化学发光省去异相化学发光所需要的固液分离和清洗步骤,反应步骤简单,检测快速,设备简易化,实现化学发光poct检测;
2、检测结果精准,延续化学发光平台的优势,灵敏度高,线性范围宽,稳定性好;
3、增加兽医感染疾病检测指标,pct相对crp和血常规,诊断价值更高,可指导兽医抗生素使用。
附图说明
下面结合附图和实施例对本发明进一步说明。
图1为本发明的蛋白纯化结果图。
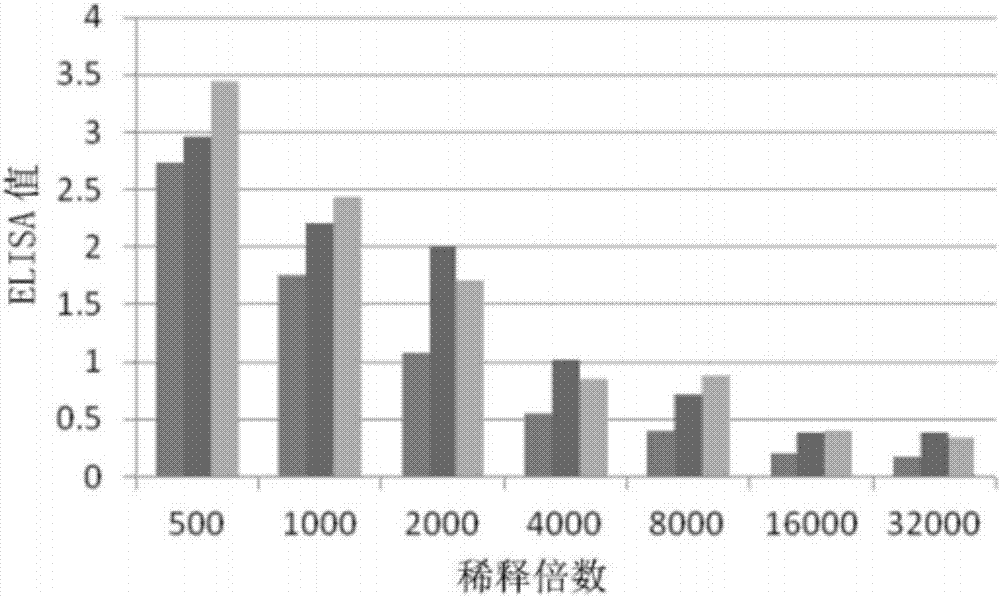
图2为本发明的elisa检测结果图。
图3为本发明的技术原理图。
图4为本发明的实施例一中降钙素原定量测试的示意图。
图5为本发明的实施例二中降钙素原定量测试的示意图。
具体实施方式
为使本发明的上述目的、特征和优点能够更加明显易懂,下面结合具体实施方式对本发明作进一步详细的说明。
首先,此处所称的“一个实施例”或“实施例”是指可包含于本发明至少一个实现方式中的特定特征、结构或特性。在本说明书中不同地方出现的“在一个实施例中”并非均指同一个实施例,也并不是单独的或选择性的与其他实施例互相排斥的实施例。
一、pct抗原设计与制备
1.pct抗原氨基酸序列(seqidno.1):
apfrsalesspadpatlsedearlllaalvqnyvqmkaseleqeqeregssldsprskrcgnlstcmlgtytqdfnkfhtfpqtaigvgapgkkrdmssdlerdhrphvsmpqnan
碱基序列(seqidno.2):
gctcctttccgcagcgctctcgaatctagccccgccgacccagctacactgtccgaggacgaggctagactgctgctggccgccctggtgcagaactatgtacagatgaaggcttctgagctggagcaggaacaagagcgggaggggtcgagcctcgactctcctagatcgaagcggtgcggaaacctgtctacctgtatgctcggaacatacacccaggacttcaacaagttccacacattccctcagacagctattggcgtgggcgctcccggcaagaagcgcgacatgtcttctgacttagaaagagaccaccggcctcacgtttccatgccacagaacgccaac
2.表达系统
采用293f真核系统表达。
hek293细胞表达的重组蛋白具有准确的转录后修饰功能,表达的糖基化药物蛋白在分子结构、理化特性和生物学功能方面接近于天然蛋白分子。293f现已可采用无血清悬浮培养,无血清悬浮培养是用已知人源或动物来源的蛋白或激素代替动物血清的一种细胞培养方式,它能减少后期纯化工作,提高产品质量。
3.质粒构建
合成基因序列:包括5’端ecori,3’端xhoi酶切位点,n端添加kozak(gccgccacc)以及cd33信号肽序列(atgccgctgctgctactgctgcccctgctgtgggcaggggcgctagct),c端添加histag序列(catcatcaccatcaccat)以及终止密码(tgatag)。并将此序列构建至pcdna4.0tomychisa载体。合成的基因序列如下(seqidno.3):
gaattcgccgccaccatgccgctgctgctactgctgcccctgctgtgggcaggggcgctagctgctcctttccgcagcgctctcgaatctagccccgccgacccagctacactgtccgaggacgaggctagactgctgctggccgccctggtgcagaactatgtacagatgaaggcttctgagctggagcaggaacaagagcgggaggggtcgagcctcgactctcctagatcgaagcggtgcggaaacctgtctacctgtatgctcggaacatacacccaggacttcaacaagttccacacattccctcagacagctattggcgtgggcgctcccggcaagaagcgcgacatgtcttctgacttagaaagagaccaccggcctcacgtttccatgccacagaacgccaaccatcatcaccatcaccattgatagctcgag
4.质粒提取、蛋白表达、蛋白纯化与检测
用真核表达载体大量提取无内毒素质粒(maxextract)。将所提取的无内毒素质粒进行细胞转染。收集细胞上清及细胞裂解液,采用ni柱亲和层析,收集样品进行sds-pagewesternblot检验,浓度检测,将合格样品(纯度>90%)透析至pbs(磷酸盐缓冲液),并将蛋白浓缩至>1.0mg/ml,蛋白纯化结果如图1所示。
二、pct抗体制备
1.免疫与采血
1)选取3只balb/c小鼠(雌性,6周龄以上)进行免疫。
2)第0周:免疫前,小鼠眼眶静脉采血50μl/只,37℃放置1h后,以5000rpm离心5min,制备阴性血清,-20℃保存。进行小鼠第一次免疫,抗原剂量为100μg/只,弗氏完全佐剂(sigma-f5881),分多点皮下注射。
3)第2周:小鼠第二次免疫,抗原剂量为50μg/只,不完全佐剂(sigma-f5506),注射方式与剂量同初次免疫。
4)第4周:小鼠第三次免疫,免疫剂量和免疫方法同第二次免疫。
5)第5周:小鼠眼眶静脉采血50μl/只,37℃放置1h后,以5000rpm离心5min,制备血清,进行elisa检测,检测结果如图2所示。剩余血清-20℃保存。取血清转阳后滴度不再变化的小鼠(第2只小鼠,1/4000稀释时,elisa值大于1)停止免疫,隔日加强免疫,抗原剂量50μg/只,3日后进行细胞融合。
2.杂交瘤融合筛选
2.1.融合前饲养层细胞制备(包括巨噬细胞和胸腺细胞,制备在无菌环境中进行)
1)采用脱颈法处死5周龄小鼠,浸入75%乙醇中。撕开小鼠腹部皮肤,用5ml注射器吸取20%imdmht5ml,灌洗小鼠腹腔(针头平刺,不可伤及内脏)。提住两腿上下摇晃小鼠,将含有巨噬细胞的培养液抽回,置于50ml离心管中,尽量将腹腔中的液体全部吸出。
2)处死两周龄小鼠,75%乙醇浸润。沿胸骨两侧呈倒三角形打开小鼠胸腔,取出胸腺,放入bd公司的一次性筛网中,用2ml注射器的内管研磨研磨,将细胞匀浆吸入20%imdmht中。
3)将含有腹腔巨噬细胞和胸腺细胞的混合培养液加入加样槽内,加入适量碳酸缓冲液,混匀,以1.0×104/孔的密度铺96孔板,100ul/孔,8块。铺好细胞的96孔细胞培养板放入37℃、5%co2的培养箱内,观察,如无污染,则放置培养箱内备用。
2.2.融合前骨髓瘤细胞制备
1)融合前5-7天,解冻骨髓瘤细胞,进行细胞维护扩大培养,调整细胞状态,使其达到对数生长期,细胞活率在95%以上。
2)将对数生长期的骨髓瘤细胞从培养箱中取出,倒掉细胞培养液,加入3-5mlimdm培养液到培养皿中,轻摇培养皿,倒掉培养液。加入3ml新鲜imdm培养液,用移液器将细胞从培养皿上吹下,收集细胞悬液于50ml离心管,1000rpm离心5min,弃去培养液,再加入20ml新鲜imdm培养液重悬细胞,1000rpm离心5min,弃上清。
3)用新鲜的imdm培养液10ml重悬细胞,放置在超净台内备用。
2.3.提取免疫成功的脾脏细胞
1)融合前,将小鼠摘眼球取血,37℃1h后,以1000rpm5min离心制备血清作为阳性对照,-20℃保存,处死的小鼠浸入75%乙醇中5-10min。
2)将小鼠置入一个无菌培养皿中,腹部向上,无菌操作剪开并撕开皮肤,使后腹肌肉层充分与皮肤剥离。换用新剪刀剪开腹腔膜,取出脾脏。
3)在培养皿中用10ml已预热的imdm培养液清洗脾脏2次,剔除脾脏表面黏连的脂肪和结缔组织,然后转入另一含10mlimdm培养液的无菌培养皿中。
4)用1ml注射器吸取培养液后选取不同的点注射到脾脏内部,使脾脏鼓起,利于细胞释放。用1ml注射器柄在培养皿中挤压脾,使细胞尽可能的分离出来。
5)将挤压混合脾细胞的培养液用一次性无菌巴氏吸管吸取后,通过细胞筛网至50ml离心管中,用新鲜的imdm培养液冲洗筛网后,1000rpm离心10min,弃上清。加入新鲜的imdm培养液重悬脾细胞,1000rpm离心10min,弃上清。将脾细胞轻轻敲散,加入imdm培养液重悬脾细胞,再将骨髓瘤细胞悬液加入至脾细胞悬液中,定容至30ml,混匀,1000rpm离心10min,弃上清,用移液器将残留的液体吸尽,待下一步融合用。
2.4.细胞融合
1)轻轻敲散细胞,用2ml移液管缓慢加入1ml37℃预热的浓度为50%的peg1500,轻柔吹吸细胞100s,使peg(聚乙二醇)与细胞充分接触。
2)迅速加入15ml37℃预热的imdm培养液,混匀,终止peg的反应,将细胞重悬,离心管置于37℃水浴10min。
3)1000rpm离心10min,弃上清。
4)取10mlimdmhat培养液重悬细胞,将细胞液转入加样槽中,加入80mlimdmhat培养液重悬细胞,将细胞悬液混合均匀,加入已铺饲养层的96孔板,铺板8块,100μl/孔,然后将细胞板置于37℃、5%co2培养箱内培养。
5)融合2-3天后观察是否污染,若无污染,用移液器小心悬空吸取96孔板内培养液丢弃,换取新鲜20%imdmht培养液进行培养,5-6天后观察克隆长势,进行elisa检测。
2.5.elisa检测
1)将pct抗原按适当浓度溶解于包被液中;
2)在对应的孔中加入100μl抗原,4℃过夜;
3)倒空液体并拍干残留液体,洗涤液冲洗5次;
4)每孔加200μl封闭液,37℃孵育1小时或者4℃过夜;
5)倒空液体并拍干残留液体,洗涤液冲洗3次;
6)每孔加100μl一抗,37℃孵育1小时;
7)倒空液体并拍干残留液体,洗涤液冲洗7次;
8)每孔加100μl二抗,37℃孵育1小时;
9)倒空液体并拍干残留液体,洗涤液冲洗7次;
10)拍干孔中残留液体,每孔加100μl显色液,37℃避光显色10min;
11)每孔加50μl2mh2so4终止显色,并立即读取450nmod值。挑选elisa阳性、细胞健康的克隆转至24孔板扩大培养(elisa阳性挑选标准:elisaod值大于1.0,或大于阴性1000倍稀释值的3倍)。
2.6.亚克隆筛选
1)挑选10-20个多克隆,细胞活率90%以上、细胞密度60%-80%;
2)每个克隆进行细胞计数。将细胞按照梯度稀释法稀释,克隆前准备好1块24孔培养板,每孔加入900μl的imdmht培养液,将克隆细胞在原孔中混合均匀,吸取100μl的细胞悬液至准备好的24孔板相应的克隆孔中,同时在克隆原液中取微量的细胞悬液至细胞计数板上进行细胞计数,记录好每个克隆的细胞密度;
3)根据稀释细胞的个数(3个细胞/孔)和克隆的板数,取一定量的细胞进行稀释,直至稀释到需要的细胞个数,加入到加样槽中,加入12ml的imdmht培养液,混合均匀。a和b排吸取200μl/孔,在加样槽中加入6mlimdmht培养液,混合均匀,取200μl/孔加入至c、d、e排。加样槽中加入6mlimdmht液,混合均匀,取200μl/孔加入至f、g、h排,并在克隆板上做好标记(克隆号、板号、日期、操作人、克隆次数)后放入二氧化碳培养箱内培养;
4)克隆后要适时观察克隆的长势,一般在7-14天送样检测elisa;
5)将挑选的克隆转入24孔板中培养,进行第二次亚克隆筛选,克隆的操作方法同第一次亚克隆筛选,克隆后适时做elisa、westernblot检测及亚型鉴定。
三、吖啶衍生物标记pct抗体
1)将多聚赖氨酸溶解于1ml150mmpbs缓冲液(ph7.4)中,终浓度10nmol/l,加入10μl溶解于dmso溶剂的10mmol/l吖啶酯,于25℃反应1h,用5ml7kd截留分子量的脱盐柱(thermofish公司)以150mmpbs(ph7.4)缓冲液作为换液缓冲液,过柱3遍,除去游离的吖啶酯及反应副产物,得到吖啶-多聚赖氨酸溶液。
2)向上述纯化过的吖啶-多聚赖氨酸溶液中加入edc(终浓度为5mmol/l)和nhs(终浓度为10mmol/l)。加入25℃反应30分钟后,加入终浓度为10mm的巯基乙醇,得到活化后的吖啶-多聚赖氨酸。
3)在加入1mg抗pct抗体,混匀,置于25℃反应1h,用5ml7kd截留分子量的脱盐柱(thermofish公司)以150mmpbs(ph7.4)缓冲液作为换液缓冲液,过柱3遍,除去游离的nhs及反应副产物,得到结合物吖啶酯-多聚赖氨酸-pct抗体溶液。
四、hrp标记pct抗体
1)将5mg过氧化物酶(hrp)溶于1.2ml10mmpbs缓冲液(ph=7.0)中,加入0.3ml新鲜配置的0.1m高碘酸钠溶液,37℃孵育20分钟。
2)在10mm醋酸钠缓冲液(ph=4.0)中透析,4℃过夜。
3)将pct抗体溶于20mm碳酸钠缓冲液(ph=9.5),浓度为10mg/ml,加入0.5mlpct抗体与hrp中,37℃孵育2小时。
4)加入100μl4mg/ml硼氢化钠,4℃下放置2小时。
5)在10mmpbs缓冲液(ph=7.0)中透析,4℃过夜。
五、夹心法检测
技术原理图如图3。
1.试剂盒的组装
本发明试剂盒中的测试管中主要成分为10mmpbs缓冲液(ph=7.0),每测试份为170.ul体积,其中含有20ug/ml吖啶酯标记pct抗体和20ug/mlhrp标记pct抗体,另外还含有0.01%的proclin300。
2.降钙素原的定量测试
1)标准曲线的制作:将pct标准品用小牛血清稀释,配成浓度一些列浓度为0ng/ml,5ng/ml,20ng/ml,50ng/ml,100ng/ml,300ng/ml的降钙素原标准品各150μl,取30μl加入本发明中的测试管,将测试管置于配套的小型设备中,放置15min。每个样本分别重复测定3次。配套仪器根据rlu和pct浓度间的比例关系,自动拟合计算出pct浓度,取三次测定平均值,绘制标准曲线。
2)取待检样本200μl,置于本发明中的测试管,每次取样30μl,重复测定3次,根据1)中绘制的标准曲线即可获得待检样品中降钙素原的浓度值。
3)结果表明:采用本发明所述方法通过进一步的试验,检测灵敏度为0.06ng/ml,检测范围为0.01ng/ml-200ng/ml,批间cv小于5%,批内cv小于1.5%,且未出现hook效应,无需对检测样本进行稀释处理。
案例1
常规方法
1.试剂盒的组装
本案例试剂盒中的测试管中主要成分为10mmpbs缓冲液(ph=7.0),每测试份为170.ul体积,其中含有20ug/ml吖啶酯标记pct抗体和20ug/mlhrp标记pct抗体,另外还含有0.01%的proclin300,如图4所示。
2.降钙素原的定量测试
1)标准曲线的制作:将pct标准品用小牛血清稀释,配成浓度一些列浓度为0ng/ml,5ng/ml,20ng/ml,50ng/ml,100ng/ml,300ng/ml的降钙素原标准品各150μl,取30μl加入本案例中的测试管,将测试管置于配套的小型设备中,放置15min。每个样本分别重复测定3次。配套仪器根据rlu和pct浓度间的比例关系,自动拟合计算出pct浓度,取三次测定平均值,绘制标准曲线。
2)取待检样本200μl,置于本案例中的测试管,每次取样30μl,重复测定3次,根据1)中绘制的标准曲线即可获得待检样品中降钙素原的浓度值。
3)结果表明:采用本案例所述方法通过进一步的试验,检测灵敏度为0.1ng/ml,检测范围为0.02ng/ml-200ng/ml,批间cv小于5%,批内cv小于1.5%,且未出现hook效应,无需对检测样本进行稀释处理。
案例2
采用生物素-亲和素放大系统,由于生物素和亲和素的亲和力更高,且一个亲和素分子可以结合4个生物素分子,使检测灵敏度比常规检测方法提高了4-5倍;如图5所示。
1.生物素标记pct抗体
称取hpdp-lc-生物素溶于dmf中,使浓度为2mg/ml。每毫升1mg/mlpct抗体溶液中加入100μl的hpdp-lc-生物素溶液,室温反应90min。以sephadexg25柱除去未反应的hpdp-lc-生物素溶液。
2.hrp标记亲和素
1)将5mg过氧化物酶(hrp)溶于1.2ml10mmpbs缓冲液(ph=7.0)中,加入0.3ml新鲜配置的0.1m高碘酸钠溶液,37℃孵育20分钟。
2)在10mm醋酸钠缓冲液(ph=4.0)中透析,4℃过夜。
3)将亲和素溶于20mm碳酸钠缓冲液(ph=9.5),浓度为10mg/ml,加入0.5mlpct抗体与hrp中,37℃孵育2小时。
4)加入100μl4mg/ml硼氢化钠,4℃下放置2小时。
5)在10mmpbs缓冲液(ph=7.0)中透析,4℃过夜。
3.试剂盒组装
本案例试剂盒中的测试管中主要成分为10mmpbs缓冲液(ph=7.0),每测试份为170.ul体积,其中含有20ug/ml吖啶酯标记pct抗体,20ug/ml生物素标记pct抗体以及100ug/mlsa-hrp,另外还含有0.01%的proclin300。
4.降钙素原的定量测试
1)标准曲线的制作:将pct标准品用小牛血清稀释,配成浓度一些列浓度为0ng/ml,5ng/ml,20ng/ml,50ng/ml,100ng/ml,300ng/ml的降钙素原标准品各150μl,取30μl加入本案例中的测试管,将测试管置于配套的小型设备中,放置15min。每个样本分别重复测定3次。配套仪器根据rlu和pct浓度间的比例关系,自动拟合计算出pct浓度,取三次测定平均值,绘制标准曲线。
2)取待检样本200μl,置于本案例中的测试管,每次取样30μl,重复测定3次,根据1)中绘制的标准曲线即可获得待检样品中降钙素原的浓度值。
3)结果表明:采用本案例所述方法通过进一步的试验,检测灵敏度为0.06ng/ml,检测范围为0.01ng/ml-200ng/ml,批间cv小于5%,批内cv小于1.5%,且未出现hook效应,无需对检测样本进行稀释处理。
以上述依据本发明的理想实施例为启示,通过上述的说明内容,相关工作人员完全可以在不偏离本项发明技术思想的范围内,进行多样的变更以及修改。本项发明的技术性范围并不局限于说明书上的内容,必须要根据权利要求范围来确定其技术性范围。
- 还没有人留言评论。精彩留言会获得点赞!