一种甲胎蛋白检测试剂盒及其检测方法与流程
本发明属于荧光免疫分析领域,具体涉及一种甲胎蛋白检测试剂盒及其检测方法。
背景技术:
中国抗癌协会最近的数据表明,在中国每天有近6000人死于癌症,癌症成为最常见的致死原因,在全球范围内癌症将成为未来几十年发病和死亡的主要原因之一。因此,癌症生物标志物的灵敏检测对早期临床诊断,疾病预防和生物医学研究越来越重要。电化学、荧光、微流控芯片、裸眼睛检测和表面等离子体共振传感等方法已经成功地用于癌症生物标志物的检测,并取得了重大进展。值得注意的是,荧光免疫分析由于其高灵敏度、高通量和效率已经得到越来越多关注。甲胎蛋白(afp)是肝癌患者血清中的一个重要标志物,正常成年人血清中afp含量通常低于20ng/ml,甚至低于5ng/ml,而肝癌患者血清中afp含量异常升高,通常大于400ng/ml。因此,afp的准确定量对肝癌疾病的诊断和预防具有重大意义。
在众多免疫分析方法中,酶联免疫吸附测试(elisa)是最常见的免疫分析方法之一,elisa是将抗原抗体特异性识别作用和酶的生物催化性质相结合,并以酶作为信号输出单元而实现抗原高灵敏检测的技术。基于贵金属纳米粒子的等离子体性质已经建立了一系列的比色elisa,而荧光elisa主要基于酶解产物对荧光物质的猝灭或增强作用实现检测,因此具有更高的灵敏度。传统的elisa主要采用碱性磷酸酶或辣根过氧化物酶作为信号输出酶,而其他的酶由于不容易制备酶-抗体偶联物,因而较少作为信号输出酶用于elisa。
酪氨酸酶是一种含铜的氧化酶,能够催化单酚衍生物羟基化而生成儿茶酚衍生物,或者进一步氧化儿茶酚衍生物生成邻苯二醌衍生物。现有技术中还没有将酪氨酸酶应用在检测甲胎蛋白方面的报道。
技术实现要素:
本发明的目的是为了提供一种甲胎蛋白检测试剂盒及其检测方法,该检测方法灵敏度高,具有普适性。
本发明首先提供一种甲胎蛋白检测试剂盒,包括:
afp捕获抗体、afp检测一抗、afp标准溶液、生物素标记的二抗、酪氨酸酶-链霉亲和素偶联物、包被缓冲液、洗涤液、样品稀释液、酪胺、间苯二酚和碳酸钠。
优选的是,所述的包被缓冲液是ph=8.0~9.6的10~100mm碳酸盐,洗涤缓冲液是ph=7.4的含有0.05~0.5%tween-20和10~100mm磷酸根/磷酸氢根/磷酸二氢根的混合溶液;样品稀释液是含牛血清蛋白的缓冲液。
本发明还提供一种检测方法,该方法包括:
步骤一:将酪氨酸酶和生物素3-磺基-n-羟基琥珀酰亚胺酯钠盐溶于磷酸缓冲溶液中,室温下孵育60min得到生物素标记的酪氨酸酶,用截留分子量30kda的amiconultra离心管离心纯化,重复3次,然后将链霉亲和素加入纯化后的生物素-酪氨酸酶偶联物,室温下孵育30-60min,得到酪氨酸酶-链霉亲和素偶联物;
步骤二:将afp捕获抗体用包被稀释液稀释200倍,取100μl加入96孔板后在4℃静置包被过夜或者室温包被2.5h,弃去孔内液体并用300μl洗涤缓冲液冲洗,在孔内加入200μl0.01mg/ml样品稀释液,37℃封闭1h后弃去孔内液体,再用300μl洗涤缓冲液冲洗,之后加入afp标准溶液并在37℃孵育1h,弃去孔内液体后用300μl洗涤缓冲液冲洗96孔板,加入100μl稀释后的afp检测一抗,37℃孵育1h后弃去孔内液体后并冲洗,加入100μl生物素标记的二抗,37℃孵育1h后弃去孔内液体后并冲洗,然后加入步骤一中得到的酪氨酸酶-链霉亲和素偶联物,37℃孵育45min后弃去孔内液体后并冲洗;
步骤三:在孔内加入15μl100~200mm磷酸缓冲溶液和200μl2.0~10.0mm酪胺溶液,37℃孵育90min后依次加入40μl10~50mm间苯二酚水溶液和15μl500mm碳酸钠溶液,并调整ph至9-14,室温震荡5min后进行荧光光谱测试。
优选的是,所述的步骤一中酪氨酸酶和生物素3-磺基-n-羟基琥珀酰亚胺酯钠盐的摩尔比为1:(20-200)。
优选的是,所述的酪氨酸酶和生物素3-磺基-n-羟基琥珀酰亚胺酯钠盐的摩尔比为1:50。
优选的是,所述步骤一离心转速为10000r/min,离心时间为10min。
优选的是,所述步骤一磷酸缓冲溶液是ph=6.5~8.0的含有10~100mm磷酸根/磷酸氢根/磷酸二氢根的溶液。
优选的是,所述步骤一链霉亲和素的浓度为500μg/ml。
优选的是,所述的步骤二中afp捕获抗体的浓度为10~50μg/ml,afp检测一抗的浓度为5~20μg/ml,生物素标记的二抗的浓度为0.5~1μg/ml,酪氨酸酶-链霉亲和素偶联物的浓度为5~50μg/ml。
优选的是,所述的酪氨酸酶-链霉亲和素偶联物的浓度为20μg/ml。
本发明的有益效果
本发明首先提供一种甲胎蛋白检测试剂盒,该试剂盒是基于酪氨酸酶引发的荧光反应检测肝癌标志物afp,其原理是基于抗原抗体相互作用,通过在96孔板上依次吸附捕获抗体、afp和一抗来形成类似夹心式的结构,后续依次加入生物素标记的二抗、酪氨酸酶-链霉亲和素偶联物,酪氨酸酶与二抗的偶联物特异性地与检测一抗结合,最后加入底物酪胺,在酪氨酸酶作用下生成多巴胺,与后续加入的间苯二酚在碱性条件下反应生成强荧光发射的基团,进而实现对afp的定量检测,最终afp浓度与酪氨酸酶浓度正相关,其中酪氨酸酶作为连接afp浓度和荧光信号的桥梁。酪氨酸酶-链霉亲和素的偶联是基于生物素-链霉亲和素之间的强亲和力实现,同时利用酪氨酸酶引发的荧光反应作为信号输出模式。将该试剂盒用于正常人和肝癌患者的血清检测,结果表明该试剂盒的检测结果与基于3,3’,5,5’-四甲基联苯胺(tmb)的标准elisa方法相符,证明该试剂盒可通过荧光激活而灵敏检测afp,并最终成功用于诊断肝癌疾病。同时,该方法具有普适性,只需根据不同的靶标抗原更换相应的捕获抗体和检测一抗,就可将其应用拓展到其他抗原的检测。
本发明还提供一种检测方法,该方法是以酪氨酸酶作为elisa信号输出酶来提供一种荧光的信号输出模式,酪氨酸酶具有的单酚氧化性将酪胺羟基化转变成多巴胺,然后加入间苯二酚溶液并调整ph至碱性,进而在室温下短时间内产生具有强荧光发射的有机分子azamonardine,最终通过荧光激活来检测肿瘤标志物。
附图说明
图1为本发明实施例2基于酪氨酸酶引发的荧光反应检测肝癌标志物afp的酶联免疫方法示意图。
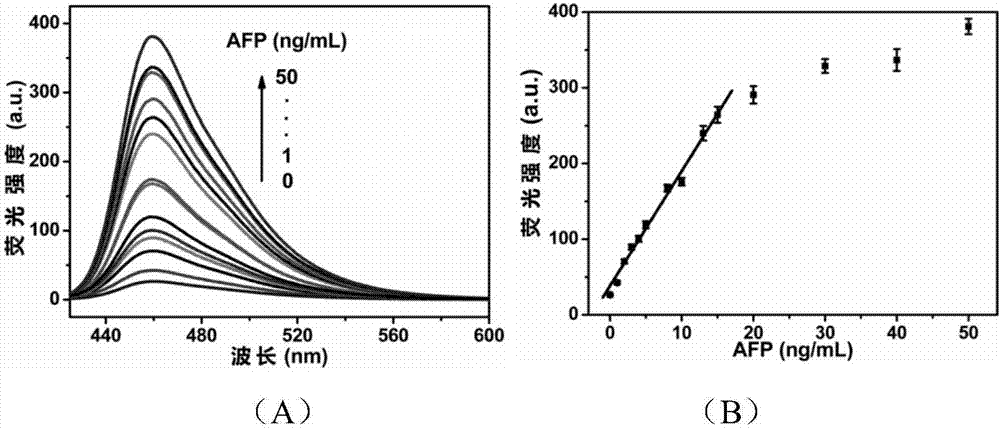
图2为本发明实施例2中的夹心式elisa的荧光强度和afp浓度的曲线关系图。
具体实施方式
下面的实施案例中将对本发明作进一步的阐述,但本发明不限于此。需要说明的是,实施例中涉及到的原料均为商购获得。
实施例1
酪氨酸酶-链霉亲和素偶联物的制备
将1mg酪氨酸酶和0.185mg生物素3-磺基-n-羟基琥珀酰亚胺酯钠盐(摩尔比=1:50)溶于500μl10mm磷酸缓冲溶液(ph=7.4)中,室温下孵育60min得到生物素标记的酪氨酸酶,用截留分子量30kda的amiconultra离心管纯化,离心转速10000r/min,离心时间10min,重复3次。然后将500μl链霉亲和素(500μg/ml)加入纯化后的生物素-酪氨酸酶偶联物,室温下孵育30min后,得到酪氨酸酶-链霉亲和素偶联物,放4℃冰箱待用。
实施例2
基于酪氨酸酶引发的荧光反应的夹心式elisa操作步骤:
首先,鼠单抗(抗afp)用包被稀释液稀释200倍,取100μl加入96孔板后在4℃静置包被过夜。弃去孔内液体并用300μl洗涤缓冲液冲洗,在孔内加入200μl牛血清蛋白(0.01mg/ml),37℃封闭1h后弃去孔内液体,再用300μl洗涤缓冲液冲洗,之后加入100μl不同浓度afp标准溶液(0,1,2,3,4,5,7,10,15,20,30,40,50ng/ml)并在37℃孵育1h,弃去孔内液体后用300μl洗涤缓冲液冲洗96孔板。加入100μl稀释后的兔多抗(抗afp,1:500),37℃孵育1h后弃去孔内液体后并冲洗。加入100μl生物素标记的二抗(1:2000),37℃孵育1h后弃去孔内液体后并冲洗,加入实施例1中得到的酪氨酸酶-链霉亲和素偶联物(50μg/ml),37℃孵育45min后弃去孔内液体后并冲洗。此荧光夹心式elisa模型的方法示意图如图1所示。
最后,加入15μl200mm磷酸缓冲溶液(ph=7.4)和200μl2.0mm酪胺溶液,37℃孵育90min后依次加入40μl10mm间苯二酚水溶液和15μl500mm碳酸钠溶液,室温震荡5min后进行荧光光谱测试。加入的间苯二酚和强碱性碳酸钠溶液都能抑制酪氨酸酶的活性,因而测试前不需要加入终止液。
图2为本发明实施例2中的夹心式elisa的荧光强度和afp浓度的曲线关系图,其中图(a)为夹心式elisa的荧光强度随afp浓度增加的变化曲线图(激发波长为415nm);图(b)为荧光发射强度随afp浓度的变化与线性响应关系(横坐标为afp浓度,纵坐标为460nm处的荧光发射强度)。图2说明,体系中加入不同浓度的afp(0~50ng/ml)所测得的荧光光谱和460nm处的荧光强度,荧光强度与afp浓度在0.2ng/ml~15ng/ml之间呈现较好的线性关系,拟合的线性方程为i=38.2+15.1cafp(ng/ml),r2=0.980,在afp浓度高于30ng/ml时,荧光强度几乎不再增大。该试剂盒能特异性检出0.2ng/ml的afp,能够满足测试血清中afp含量的需求。
实施例3
肝癌患者和正常人血清中afp含量检测:
肝癌患者和正常人的临床血清样本由吉林大学第二医院提供,血清的荧光夹心elisa方法与实施例2中的抗原测定方法基本相同,不同之处在于用实际血清样品代替其中的抗原标准溶液。检测前将所有血清样品稀释20~100倍后加入孔中。同时以传统的tmb-elisa方法作为对照,按照tmb-elisa-afp试剂盒中的操作步骤进行血清中afp含量的检测。
如表1所示,正常人和肝癌患者的血清中afp含量的检测结果表明,本试剂盒的检测结果和传统的tmb-elisa-afp试剂盒的检测结果相当,表明本发明的试剂盒能用于临床检测,检测结果可靠。
表1.肝癌患者和正常人血清中的afp检测结果(mean±sd;n=3).
还需要说明的是,本发明的具体实施例只是用来示例性说明,并不以任何方式限定本发明的保护范围,本领域的相关技术人员可以根据上述一些说明加以改进或变化,但所有这些改进和变化都应属于本发明权利要求的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!