一种多信号探针的用途的制作方法
本申请是申请日为:2017年4月19日、申请号为:201710256229.5、名称为:一种多信号探针及其制备方法和用途的发明专利的分案申请。
本发明属于环境检测领域,具体涉及一种多信号探针及其制备方法和用途,可用于环境中锌离子的测定。
背景技术:
zn2+是生物体内一种不可缺少的微量元素,广泛的存在于细胞和体液中,在生长发育、生殖、神经信号传递、基因录入、核酸识别、细胞生长调节、凋亡等生理过程中zn2+具有重要作用。zn2+的摄入量过多或不足都会使生物体的生长发育紊乱,引起多种疾病,如食欲下降、免疫力低下、糖尿病、前列腺癌等疾病都与锌离子失衡有关。因此如何有效的检测zn2+对于生物科学和环境科学等都具有重要的意义。
技术实现要素:
本发明是针对上述存在的问题提供一种用于检测锌离子的多信号探针及其制备方法和用途。
本发明的目的可以通过以下技术方案实现:、
一种多信号探针,该探针的结构式如下所示:
一种上述所述的多信号探针的制备方法,该方法的反应路线如下:
在一些具体的技术方案中:该方法包括以下步骤:
第一步:在酸性试剂和除水剂存在的条件下,化合物ⅰ与二氨基马来腈进行反应,制备得到化合物ⅲ;
第二步:在酸性试剂和除水剂存在的条件下,化合物ⅲ与二茂铁甲醛进行反应,制备得到化合物ⅳ。
在一些优选的技术方案中:第一步和第二中所述的酸性试剂为冰醋酸、盐酸、硫酸或者磷酸。
在一些优选的技术方案中:第一步和第二步中所述的除水剂为分子筛或者无水硫酸钠。
在一些优选的技术方案中:第一步中:第一步中:酸性试剂与化合物ⅰ的体积摩尔比比例为40~100l/mol,除水剂与化合物ⅰ的重量摩尔比为1000~4000g/mol。
在一些优选的技术方案中:第二步中:酸性试剂与化合物ⅲ的体积摩尔比为70~160l/mol,除水剂与化合物ⅰ的重量摩尔比为1200~6000g/mol。
本发明技术方案中:化合物ⅰ与二氨基马来腈的摩尔比为1:2~6。
本发明技术方案中:化合物ⅲ与二茂铁甲醛的摩尔比为1:2~6。
在一些优选的技术方案中:第一步和第二步的反应温度均为加热回流温度。
本发明技术方案中:所述的多信号探针作为检测锌离子的应用;优选所述的多信号探针在环境中作为检测锌离子的应用。
本发明的有益效果:
本发明所提供的多信号探针分子制备方法简单,易于工业化生产。且制备得到的多信号探针对锌离子的检出限低且选择性高。
附图说明
图1为多信号探针对zn2+的选择性识别的吸收光谱图。
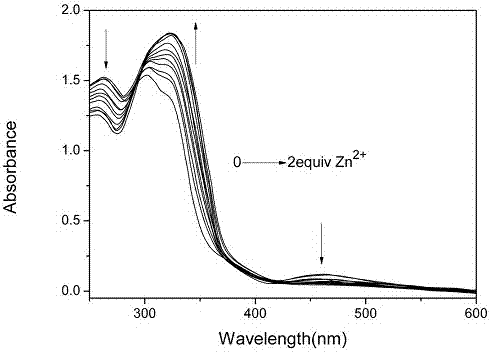
图2为zn2+对多信号探针的吸收光谱滴定图。
图3为多信号探针对zn2+的选择性识别dpv图。
图4为zn2+对多信号探针的dpv滴定图。
图5为zn2+对多信号探针的cv滴定图。
具体实施方式
下面结合实施例对本发明做进一步说明,但本发明的保护范围不限于此:
实施例1
在250ml的三颈烧瓶中依次加入无水乙醇(50ml)、2,6-吡啶二醛(0.135g,1mmol)、冰醋酸(0.1ml)和无水硫酸钠(1g),加热回流。在通入n2的条件下,用恒压漏斗缓慢滴加溶有二氨基马来腈(0.216g,2mmol)的50ml无水乙醇溶液,滴加完毕后继续反应,tlc监测反应进程,待反应结束后趁热过滤除去硫酸钠,将滤液旋转蒸干得白色固体,将粗产物用无水乙醇重结晶,得白色晶体产物0.29g,产率94.2%,纯度99.46%。
元素分析:(%)forc15h9n9:计算值:c57.14;h2.88;n39.98,实测值:c54.37;h2.78;n38.71。
ir(kbr),ν,cm-1:3327,3210,2234,1578,1460,1285,1147,981,741。
1hnmr(500mhz,cdcl3,tms):δ=5.17(s,4h,nh2),8.04(d,j=8.0,2h,py-h),8.19(t,j=7.4,1h,py-h),8.37(s,2h,n=ch)ppm.
在100ml的三颈烧瓶中依次加入无水乙醇(30ml)、化合物ⅲ(0.157g,0.5mmol)、冰醋酸(0.08ml)和无水硫酸钠(0.6g),加热回流。在通入n2的条件下,用恒压漏斗缓慢滴加溶有二茂铁甲醛(0.214g,1mmol)的50ml无水乙醇溶液,滴加完毕后继续反应,tlc监测反应进程,待反应结束后趁热过滤除去硫酸钠,将滤液旋转蒸干得深红色固体,将粗产物用无水乙醇重结晶,得红色晶体产物0.34g,产率92.6%,纯度99.38%。
元素分析:(%)forc37h25n9fe2:计算值:c62.83;h3.56;n17.82,实测值:c62.67;h3.69;n17.94。
ir(kbr),ν,cm-1:3334,3228,2239,1561,1517,1361,1307,997,791,732。
1hnmr(500mhz,cdcl3,tms):δ=4.32(s,10h,cp-h),4.57(t,j=7.6,4h,cp-h),4.69(t,j=7.6,4h,cp-h),8.05(d,j=8.0,2h,py-h),8.21(t,j=7.4,1h,py-h),8.39(s,2h,n=ch),8.44(s,2h,n=ch)ppm.
实施例2
在250ml的三颈烧瓶中依次加入无水乙醇(50ml)、2,6-吡啶二醛(0.135g,1mmol)、浓盐酸(0.08ml)和无水硫酸钠(1.5g),加热回流。在通入n2的条件下,用恒压漏斗缓慢滴加溶有二氨基马来腈(0.324g,3mmol)的50ml无水乙醇溶液,滴加完毕后继续反应,tlc监测反应进程,待反应结束后趁热过滤除去硫酸钠,将滤液旋转蒸干得白色固体,将粗产物用无水乙醇重结晶,得白色晶体产物0.30g,产率93.7%,纯度99.93%。
在100ml的三颈烧瓶中依次加入无水乙醇(30ml)、化合物ⅲ(0.157g,0.5mmol)、浓盐酸(0.08ml)和无水硫酸钠(1g),加热回流。在通入n2的条件下,用恒压漏斗缓慢滴加溶有二茂铁甲醛(0.321g,1.5mmol)的50ml无水乙醇溶液,滴加完毕后继续反应,tlc监测反应进程,待反应结束后趁热过滤除去硫酸钠,将滤液旋转蒸干得深红色固体,将粗产物用无水乙醇重结晶,得红色晶体产物0.33g,产率91.5%,纯度99.88%。
实施例3
在250ml的三颈烧瓶中依次加入无水乙醇(50ml)、2,6-吡啶二醛(0.135g,1mmol)、浓硫酸(0.05ml)和分子筛(2g),加热回流。在通入n2的条件下,用恒压漏斗缓慢滴加溶有二氨基马来腈(0.432g,4mmol)的50ml无水乙醇溶液,滴加完毕后继续反应,tlc监测反应进程,待反应结束后趁热过滤除去分子筛,将滤液旋转蒸干得白色固体,将粗产物用无水乙醇重结晶,得白色晶体产物0.29g,产率90.1%,纯度99.91%。
在100ml的三颈烧瓶中依次加入无水乙醇(30ml)、化合物ⅲ(0.157g,0.5mmol)、浓硫酸(0.04ml)和分子筛(1.5g),加热回流。在通入n2的条件下,用恒压漏斗缓慢滴加溶有二茂铁甲醛(0.428g,2mmol)的50ml无水乙醇溶液,滴加完毕后继续反应,tlc监测反应进程,待反应结束后趁热过滤除去分子筛,将滤液旋转蒸干得深红色固体,将粗产物用无水乙醇重结晶,得红色晶体产物0.31g,产率91.4%,纯度99.42%。
实施例4
在250ml的三颈烧瓶中依次加入无水乙醇(50ml)、2,6-吡啶二醛(0.135g,1mmol)、磷酸(0.04ml)和分子筛(4.0g),加热回流。在通入n2的条件下,用恒压漏斗缓慢滴加溶有二氨基马来腈(0.648g,6mmol)的50ml无水乙醇溶液,滴加完毕后继续反应,tlc监测反应进程,待反应结束后趁热过滤除去分子筛,将滤液旋转蒸干得白色固体,将粗产物用无水乙醇重结晶,得白色晶体产物0.29g,产率90.8%,纯度99.87%。
在100ml的三颈烧瓶中依次加入无水乙醇(30ml)、化合物ⅲ(0.157g,0.5mmol)、磷酸(0.035ml)和分子筛(3.0g),加热回流。在通入n2的条件下,用恒压漏斗缓慢滴加溶有二茂铁甲醛(0.642g,3mmol)的50ml无水乙醇溶液,滴加完毕后继续反应,tlc监测反应进程,待反应结束后趁热过滤除去分子筛,将滤液旋转蒸干得深红色固体,将粗产物用无水乙醇重结晶,得红色晶体产物0.33g,产率92.8%,纯度99.46%。
性质实验
下面吸收光谱实验和电化学使用中所用的多信号探针均采用实施例1制备得到的多信号探针。
1、吸收光谱实验
图1为多信号探针对zn2+的选择性识别的吸收光谱图。在10μmol/l的多信号探针的乙腈/水(4:1,v:v)的混合溶液中分别加入2倍量的金属离子(zn2+、na+、ag+、mg2+、ca2+、pb2+、co2+、cd2+、cu2+、ni2+、fe2+、al3+)。吸收光谱在shimadzuuv2450型紫外可见分光光度计上测得。
从图1中可以看出在溶液体系中加入zn2+后,溶液的吸收曲线发生明显变化,原来在265nm处吸收峰强度降低,302nm处的吸收峰强度增强并红移(24nm)至326nm处,460nm处吸收峰强度降低。而在加入其它金属离子后,溶液的吸收曲线没有明显的变化。这说明了该多信号探针在溶液中能选择性识别zn2+。
图2为zn2+对多信号探针的吸收光谱滴定图。在10μmol/l的多信号探针的乙腈/水(4:1,v:v)的混合溶液中,分别加入0、0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9、1.0、1.5和2.0倍量的zn2+。吸收光谱在shimadzuuv2450型紫外可见分光光度计上测得。
从图2中可以看出,在滴定的过程中,265nm处吸收峰强度逐渐降低,302nm处的吸收峰强度逐渐增强并红移(24nm)至326nm处,460nm处吸收峰强度逐渐降低。同时溶液的颜色由黄色逐渐变为紫色,说明该多信号探针可以用来实现裸眼检测zn2+。
2、电化学实验
图3是多信号探针对zn2+的选择性识别dpv图。在10ml浓度为0.1mmol/l多信号探针溶液中分别加入10μl浓度为0.1mol/l(1倍摩尔量的)的金属离子溶液(zn2+、na+、ag+、mg2+、ca2+、pb2+、co2+、cd2+、cu2+、ni2+、fe2+、al3+)。实验中所使用的溶液体系均为乙腈/水(4:1,v:v)的混合溶液,n-bu4npf6(0.1mol/l)作为支持电解质,三电极体系使用铂圆盘电极为工作电极,铂丝电极为辅助电极,ag/agcl电极为参比电极,测定温度为25℃,溶液在通氮气30分钟后进行测定。常规差分脉冲伏安法(dpv)在chi660c型电化学工作站上测定。
常规差分脉冲伏安法(dpv)响应显示了一个可逆的单电子氧化过程,半波电位(e1/2)为0.38v,归属于fc+/fc的氧化还原峰。在上述实验条件下加入一倍量的金属离子后,发现只有在加入zn2+后,0.38v处的峰消失,0.42v处出现一个新的峰。而在加入其他金属离子后则没有这一现象,这说明多信号探针对zn2+有着独特的电化学响应。
图4为zn2+对多信号探针的dpv滴定图。在10ml浓度为0.1mmol/l多信号探针溶液中依次加入0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9、1.0、1.5、2.0倍量的zn2+。实验中所使用的溶液体系均为乙腈/水(4:1,v:v)的混合溶液,n-bu4npf6(0.1mol/l)作为支持电解质,三电极体系使用铂圆盘电极为工作电极,铂丝电极为辅助电极,ag/agcl电极为参比电极,测定温度为25℃,溶液在通氮气30分钟后进行测定。常规差分脉冲伏安法(dpv)在chi660c型电化学工作站上测定。
由图4中可以看出,随着zn2+的加入,fc+/fc的氧化还原峰逐渐从0.38v移动到0.42v处,并逐渐降低。当zn2+加入量达到探针分子一倍量后,fc+/fc的氧化还原峰不再发生位移,且峰的强度基本不变。这说明多信号探针与zn2+是1:1配位的。
图5为zn2+对多信号探针的cv滴定图。在10ml浓度为0.1mmol/l多信号探针溶液中依次加入0、0.2、0.4、0.6、0.8、1.0、1.5、2.0倍量的zn2+。实验中所使用的溶液体系均为乙腈/水(4:1,v:v)的混合溶液,n-bu4npf6(0.1mol/l)作为支持电解质,三电极体系使用铂圆盘电极为工作电极,铂丝电极为辅助电极,ag/agcl电极为参比电极,扫描速度为100mv/s,测定温度为25℃,溶液在通氮气30分钟后进行测定。循环伏安法(cv)在chi660c型电化学工作站上测定。
从图5可以看出,随着zn2+的加入,循环伏安图中半波电位e1/2正移了55mv,并且在加入一倍量的zn2+后半波电位e1/2基本不再移动。这是由于zn2+和多信号探针形成了1:1的配合物,增加了二茂铁的拉电子能力,使得二茂铁更难被氧化。
- 还没有人留言评论。精彩留言会获得点赞!