一种用于糖尿病高灵敏度检测的液滴微流控芯片及检测方法与流程
本发明涉及一种用于糖尿病高灵敏度检测的液滴微流控芯片及检测方法,属于微流控技术领域,也属于医疗设备技术领域。
背景技术:
糖尿病是一组以高血糖为特征的代谢性疾病,发病率高,是目前危害人类健康的四大主要疾病之一。长期患糖尿病易引发糖尿病酮症、心血管疾病、神经病变、糖尿病足、糖尿病肾病等并发症,严重威胁人类健康。根据中华医学会糖尿病学分会2013年公布,估计我国有1.39亿糖尿病患者,其中60.7%的糖尿病患者未得到诊断。
多年来,糖尿病诊断都是以血浆葡萄糖水平为标准,包括空腹血糖和口服糖耐量试验2小时血糖值。然而,血糖检测方法易受饮食、运动、药物等因素的影响以及需要特定时间采血,这极大地限制了检测结果的准确性,同时给患者带了不便。2010年,美国糖尿病协会(ada)明确规定将糖化血红蛋白(hba1c)作为监测糖尿病血糖控制的“金标准”,其反应2-3个月内平均血糖控制水平,而且不受急性血糖波动的影响,稳定性好,精确度高,无需空腹或特定时间取血。
目前临床实验室中应用的hba1c检测方法主要有两大类:一类方法基于糖化血红蛋白与非糖化血红蛋白所带的电荷不同,如离子交换层析法、电泳法等方法;另一类方法基于血红蛋白上糖化基团的结构特点,如亲和层析法、离子捕获法和免疫法等。2002年,国际临床化学联合会(ifcc)公布了hba1c检测的国际标准法,即通过高压液相色谱法与质谱(hplc-ms)联合检测方法。然而,hplc-ms联合检测方法需要贵重的仪器以及复杂的操作,使得其在临床推广上存在困难。目前,离子交换hplc法被认为是分析检测hba1c的金标准,其测定的是血液中hba1c占总血红蛋白(hb)的百分含量。文献[1](m.v.antunes,2009,brazilianjournalofpharmaceuticalsciences,45(4),651-657.)提出了将阳离子交换hplc法和紫外-可见分光光度法联用作为检测hba1c的标准化方法。然而,该方法采用商用阳离子交换色谱柱结合柱外检测的方法,导致试剂消耗量较大和分析时间较长,而且色谱柱末端与检测器之间由于管路连接存在较大的死体积,使得被分离的样品组分容易发生扩散和重新混合,从而降低了检测灵敏度。
为了提高检测灵敏度,我们提出了将阳离子交换色谱柱和检测池集成到微流控芯片上,并且在色谱柱末端与检测池之间增加了液滴发生器,该方法不仅避免了管路连接产生的死体积,而且以液滴的方式进行检测避免了样品在色谱柱末端的扩散和重新混合,因此提高了检测灵敏度。此外,检测池的结构设计为z型,增加了光程,从而进一步提高了检测灵敏度。该液滴微流控芯片不仅适用于hba1c的高灵敏度检测,也普遍适用于在紫外-可见光波段具有吸收峰的多肽、核酸和蛋白质等生物大分子的检测。
技术实现要素:
为了克服现有技术存在的检测灵敏度较低、检测仪器体积大和操作步骤复杂等方面的不足,本发明提出了一种用于糖尿病高灵敏度检测的液滴微流控芯片,该微流控芯片体积小,成本低廉,操作简单,有利于现场实时检测。此外,本发明还提出了一种糖尿病高灵敏度检测方法,该方法不仅适用于hba1c样品的高灵敏度检测,而且适用于多肽、核酸和蛋白质等生物大分子的检测。
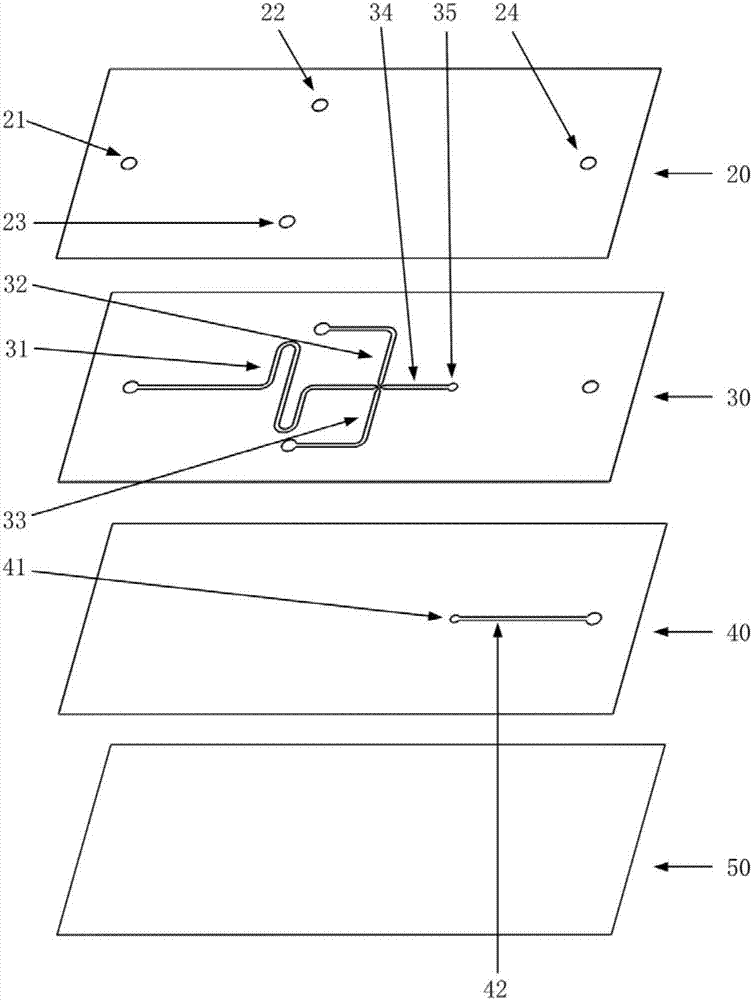
参阅图2,本发明提出的一种用于糖尿病高灵敏度检测的液滴微流控芯片,其特征在于:所述液滴微流控芯片依次由盖片层20、上流体通道层30、下流体通道层40和基底层50构成;其中水相入口21贯通盖片层20,与上流体通道层30上的水相引入通道31连通;所述水相引入通道31内部有色谱柱;贯穿于盖片层20的第一油相入口22和第二油相入口23,分别通过上流体通道层30上的第一油相引入通道32和第二油相引入通道33,与所述水相引入通道31和第一液滴通道34形成十字型通道;参阅图3,贯通上流体通道层30的第一小孔35和贯通下流体通道层40的第二小孔41位置相应,两者贯通后形成微型检测池;所述微型检测池连通上流体通道层30上的第一液滴通道34与贯穿下流体通道层40的第二液滴通道42;第二液滴通道42通过依次贯通下流体通道层40、上流体通道层30和盖片层20的流体出口24实现与外界流通。
所述的液滴微流控芯片为透明热塑性材料,例如:聚甲基丙烯酸甲酯(pmma)、聚碳酸酯(pc)、聚苯乙烯(ps)、环烯烃共聚物(coc)等材料中的一种或几种。
作为一种优选方式,上述的液滴微流控芯片,所述水相引入通道31的形状为弯曲蛇形,其内部填充满强阳离子交换聚合物整体柱,该强阳离子交换聚合物整体柱即为色谱柱,它的材料为丙烯酸酯共聚物,内部疏松多孔;该强阳离子交换聚合物整体柱通过光或热引发聚合反应生成,整体柱的机械强度、孔径大小、ph值耐受范围、交换容量等性能参数可以通过改变聚合物的种类和配比来调节。整体柱通道长度可以设置在1至25厘米范围内,通道深度可以设置为0.05至1毫米范围内,通道宽度可以设置为0.05至2毫米范围内。
参阅图4,作为一种优选方式,上述的液滴微流控芯片,所述第一油相引入通道32和第二油相引入通道33,与水相引入通道31和第一液滴通道34所形成的十字型通道,即为液滴发生器;所述十字型通道是带有弧形的收缩结构,有利于产生尺寸较小的液滴,其宽度满足关系2*w1≥w2≥0.5*w1,2*w1≥w3=w4≥0.5*w1且w>w2;其中,w1为水相引入通道31末端通道宽度,w2为第一液滴通道34入口通道宽度,w3为第一油相引入通道32末端通道宽度,w4为第二油相引入通道33末端通道宽度,w是第一液滴通道34的宽度;其工作原理是:使用外部泵或阀驱动系统分别将油相和水相溶液从各自入口注入,在十字通道交叉口处,由于水相受到油相的挤压,在剪切力、粘性力、表面张力和惯性力等力之间的相互作用产生油包水(w/o)液滴,并被油相带入第一液滴通道34。所述液滴发生器产生液滴的尺寸可以通过调节第一油相引入通道32和第二油相引入通道33与水相引入通道31中流体的流速比值来改变。
上述的液滴微流控芯片,所述水相引入通道31内部强阳离子交换聚合物整体柱的制备,在芯片其余部件都制备好之后进行,其制备方法包括以下步骤:
第一步,氧等离子体清洗。使用氧等离子体清洗机对液滴微流控芯片微通道内壁进行处理,时间为5~10分钟,空气流量为100~300sccm,功率为20~100w,反应腔室压力为10~20pa。
第二步,硅烷化处理。20wt%3-(异丁烯酰氧)丙基三甲氧基硅烷的乙醇溶液通过加入甲酸调节ph至4~6,并将其从水相入口21通入液滴微流控芯片的水相引入通道31中,流速为0.1~10μl/min,时间为0.5~3h,然后用乙醇清洗液滴微流控芯片微通道;接着向液滴微流控芯片中通入氮气10~20分钟至完全充满整个通道,最后将流体入口和出口密封待用。
第三步,光或热引发聚合反应。将单体、交联剂、致孔剂和引发剂混合溶解形成预聚物,其中单体、交联剂、致孔剂和引发剂的质量分数比例分别为20~30:15~20:50~70:1~5;所述致孔剂由致孔剂ⅰ和致孔剂ⅱ两种组分构成,致孔剂ⅰ和致孔剂ⅱ的质量分数比例为2~3:1;将预聚物通入液滴微流控芯片的水相引入通道31中,在紫外光或加热条件下使预聚物发生聚合反应生成聚合物整体柱。然后用清洗液(乙醇:去离子水=0.5~2:1,体积比)通过聚合物整体柱除去致孔剂和残留的单体,流速为0.5~2μl/min,时间为0.5~2h。
所述第三步中的单体为甲基丙烯酸缩水甘油酯(gma);交联剂为二甲基丙烯酸乙二醇酯(edma)、甲基丙烯酸甲酯(mma)、甲基丙烯酸丁酯(bma)中的一种;致孔剂ⅰ为十二烷醇、液态石蜡、二甲基硅油中的一种,致孔剂ⅱ为环己醇、1,4-丁二醇、异丙醇中的一种;引发剂为安息香二甲醚、苯偶酰双甲醚和偶氮二异丁腈中的一种。
第四步,整体柱修饰。将0.5~2mol/l亚硫酸钠溶液通过聚合物整体柱,流速为1~10μl/min,时间为5~20min。将所有流体入口和出口密封,并将液滴微流控芯片置于70~80摄氏度的烤箱中烘烤8~24h。最后,将5~20mmol/l硝酸溶液通过聚合物整体柱,流速为1~10μl/min,时间为0.5~2h;接着通入去离子水,流速为2~10μl/min,时间为20~30h。
以上方法的效果:提供一种表面疏松多孔,低背压且比表面积大,柱容量高和渗透性好的色谱分离柱,而且该色谱柱的柱参数如孔径大小,固定相颗粒大小都可以通过控制预聚物的种类、比例以及引发条件来控制,实现不同功能的分离效果。提供的强阳离子交换聚合物整体柱芯片主要功能部件由聚合物整体柱、液滴发生器和微型检测池构成,可以根据实际应用中的不同需求,改变聚合物整体柱的尺寸和孔结构、液滴发生器的宽度和微型检测池的有效长度。
参阅图1,本发明提出的一种基于上述液滴微流控芯片的糖尿病高灵敏度检测装置,包括高压液相色谱泵2,进样阀3,液滴微流控芯片6,氘灯和卤钨灯光源10,紫外-可见光光谱仪11和数据处理软件13;所述高压液相色谱泵2提供驱动压力将缓冲液1泵入到管路中;所述进样阀3将hba1c样品从样品入口4通入,并从样品废液出口5流出,完成定量进样;所述液滴微流控芯片6包括强阳离子交换聚合物整体柱7、液滴发生器8和微型检测池9;所述强阳离子交换聚合物整体柱7用以分离hba1c样品中的各组分;所述液滴发生器8用以包裹被分离的hba1c组分形成一系列不同浓度的油包水液滴;所述微型检测池9与紫外-可见光光谱仪11的光路对齐;所述氘灯和卤钨灯光源10提供紫外光和可见光;所述紫外-可见光光谱仪11用以接收紫外-可见光并通过光纤12将信号传输至数据处理软件13进行数据处理,最后完成进行吸光度检测。
本发明还提供了基于上述糖尿病高灵敏度检测装置的检测方法:参阅图2,包括以下步骤:
第一步,缓冲液带动hba1c样品完成各组分的分离:通过外部泵或阀提供驱动力对流体进行操控,将载有样品的缓冲液从水相入口21泵入水相引入通道31,由于样品中的不同组分与水相引入通道31中的聚合物整体柱作用力不同,样品在聚合物整体柱中的移动速度存在差异,被分离的组分依次流出聚合物整体柱;
第二步,被分离的hba1c样品组分被油相包裹,产生油包水液滴:油溶液分别由第一油相入口22和第二油相入口23,经第一油相引入通道32和第二油相引入通道33,与水相引入通道31末端被分离出来的组分水溶液在十字型通道处汇合,通过控制油溶液和水溶液的流速比,形成粒径可控的油包水液滴,进入第一液滴通道34,
第三步,油包水液滴流入微型检测池,在微型检测池中用紫外-可见分光光度计检测油包水液滴中的hba1c样品组分,对油包水液滴中包裹的各组分进行吸光度分析,得到基于液滴检测的离子色谱图,即被分离组分的色谱图;最后,经过吸光度检测的油包水液滴经由第二液滴通道42从流体出口24流出。
第四步,通过计算色谱图中hba1c的峰面积占总hb的峰面积得到hba1c浓度比值。
本发明的有益效果:参阅图2,载有样品的缓冲液从水相入口11进入弯曲蛇形的水相引入通道31,该弯曲蛇形结构能够在不增加液滴微流控芯片长度的条件下,增加水相引入通道31中聚合物整体柱的长度,有利于样品的高通量分离和分析。而且,该聚合物整体柱具有耐受ph值范围宽、压降小、多孔、交换容量高等优点,对驱动装置输出高压的要求大大降低,同时对流动相有更多的选择。此外,可以通过调整预聚物的比例来制备孔径和比表面积不同的聚合物整体柱,有利于提高分离效率和分离速度。当样品在聚合物整体柱中完成色谱分离后,分别从第一油相引入通道32和第二油相引入通道33注入的油溶液在剪切力、表面张力、粘性力和惯性力的作用下将色谱柱末端流出的样品组分以液滴的形式包裹起来,这样有利于保证被分离组分在进入微型检测池前不会发生分子扩散,避免了峰带展宽效应和被分离组分重新混合,提高了分离效果。此外,将微型检测池集成在液滴微流控芯片上有利于实时、在线监测被分离组分的吸光度,从而获得样品的实时浓度,而且该微型检测池贯通上流体通道层30和下流体通道层40,增加了检测池光程,同时实现了全透明的检测池,大大提高了检测灵敏度。
附图说明
图1是本发明所提供的一种糖尿病高灵敏度检测装置示意图。其中,1-缓冲液,2-高压液相色谱泵,3-进样阀,4-样品入口,5-样品废液出口,6-液滴微流控芯片,7-强阳离子交换聚合物整体柱,8-液滴发生器,9-微型检测池,10-氘灯和卤钨灯光源,11-紫外-可见光光谱仪,12-光纤,13-数据处理软件;
图2是本发明所提供的一种用于糖尿病高灵敏度检测的液滴微流控芯片的结构示意图。其中,20-盖片层,30-上流体通道层,40-下流体通道层,50-基底层,21-水相入口,22-第一油相入口,23-第二油相入口,24-流体出口,31-水相引入通道,32-第一油相引入通道,33-第二油相引入通道,34-第一液滴通道,35-第一小孔,41-第二小孔,42-第二液滴通道;
图3是本发明所提供的一种用于糖尿病高灵敏度检测的液滴微流控芯片的截面结构示意图;
图4是本发明所提供的一种用于糖尿病高灵敏度检测的液滴微流控芯片的液滴发生器的结构示意图;
图5是实施例一中的一种用于糖尿病高灵敏度检测的液滴微流控芯片的强阳离子交换聚合物整体柱截面的扫描电镜图;其中,图5(a)和5(b)分别是放大倍率为1k和7k时的扫描电镜图;
图6是实施例一中的一种糖尿病高灵敏度检测方法示意图。其中,60-样品,61-组分c,62-组分b,63-组分a,64-聚合物整体柱,65-液滴发生器,66-油包水液滴,67-检测位点,68-色谱图。
具体实施方式
实施例一
参阅图2,本实施例中的一种用于糖尿病高灵敏度检测的液滴微流控芯片,材料为pmma,其包括四层简单的平面结构:盖片层20,上流体通道层30,下流体通道层40,基底层50。盖片层20与基底层50厚度均为2mm,上流体通道层30和下流体通道层40厚度均为1mm,聚合物整体柱长约50mm,宽0.5mm,高0.5mm;液滴发生器十字通道高0.5mm,w1=w2=w3=w4=0.2mm,w=0.5mm;微型检测池直径1mm,高2mm;水相入口21,第一油相入口22,第二油相入口23和流体出口24直径均为1.6mm。
本实施例中的本实施例中的一种用于糖尿病高灵敏度检测的液滴微流控芯片中强阳离子交换聚合物整体柱的制备过程:采用光引发聚合反应制备强阳离子交换聚合物整体柱。第一步,使用氧等离子体清洗机对液滴微流控芯片微通道内壁进行处理,时间为10分钟,空气流量为200sccm,功率为40w,反应腔室压力为10~20pa;第二步,20wt%3-(异丁烯酰氧)丙基三甲氧基硅烷的乙醇溶液通过加入甲酸调节ph至5,然后将其通入液滴微流控芯片的聚合物整体柱微通道中,流速为0.25μl/min,时间为90分钟;接着用乙醇清洗液滴微流控芯片微通道,然后向液滴微流控芯片中通入氮气10分钟至完全充满整个通道,再将通道入口和出口密封待用;第三步,将单体、交联剂、致孔剂和引发剂混合溶解形成预聚物,该预聚物由25.5%甲基丙烯酸缩水甘油酯(gma),17.5%二甲基丙烯酸乙二醇酯(edma),40%十二烷醇,17%环己醇,1%安息香二甲醚组成,以上所有百分比均为质量比;将预聚物通入液滴微流控芯片的水相引入通道31中,在紫外光下使预聚物发生光聚合反应生成聚合物整体柱,紫外光波长为320~390nm,紫外曝光功率为50mw/cm2,曝光时间为30s~5min;然后用清洗液(乙醇:去离子水=1:1,体积比)通过聚合物整体柱除去致孔剂和残留的单体,流速为0.5μl/min,时间为1小时;第四步,将1mol/l亚硫酸钠溶液通过聚合物整体柱,流速为3μl/min,时间为10分钟;然后将所有入口和出口密封,并将液滴微流控芯片置于75摄氏度的烤箱中烘烤12小时;接着将10mmol/l硝酸溶液通过聚合物整体柱,流速为3μl/min,时间为1小时;最后通入去离子水,流速为3μl/min,时间为24小时。
参阅图5(a)和图5(b),本实施例中制备的一种强阳离子交换聚合物整体柱,其表面疏松多孔,比表面积大,柱容量高,孔径大小为1~2μm,颗粒大小为0.5~3μm,具有渗透性好、低背压的优点。
本实施例中的一种糖尿病高灵敏度检测方法:参阅图6,在外置泵或阀的驱动力下,缓冲液带动样品60流过液滴微流控芯片上的强阳离子交换聚合物整体柱64,根据样品60中组分a63、组分b62和组分c61在缓冲液中所带电荷差异,其在聚合物整体柱中的迁移速度不同。被分离的组分a63、组分b62和组分c61依次流出聚合物整体柱64;油溶液经第一油相引入通道32和第二油相引入通道33,与水相引入通道31末端被分离出来的组分水溶液在液滴发生器65的十字型通道处汇合,通过控制油溶液和水溶液的流速比,形成一系列含有不同浓度样品组分的油包水液滴66,在检测位点67对油包水液滴中包裹的组分进行吸光度分析,得到基于液滴检测的色谱图68。
实施例二
参阅图2,本实施例中的一种用于糖尿病高灵敏度检测的液滴微流控芯片,材料为coc,其盖片层20与基底层50厚度均为2mm,上流体通道层30和下流体通道层40厚度均为0.5mm,聚合物整体柱长约30mm,宽0.5mm,高0.3mm;液滴发生器十字通道高0.3mm,w1=w2=w3=w4=0.3mm,w=0.5mm;微型检测池直径0.6mm,高1mm;水相入口21,第一油相入口22,第二油相入口23和流体出口24直径均为1.0mm。
本实施例中的一种用于糖尿病高灵敏度检测的液滴微流控芯片中强阳离子交换聚合物整体柱的制备过程:采用热引发聚合反应制备强阳离子交换聚合物整体柱。第一步和第二步同实施例一;第三步,将单体、交联剂、致孔剂和引发剂混合溶解形成预聚物,该预聚物由25.5%甲基丙烯酸缩水甘油酯(gma),17.5%二甲基丙烯酸乙二醇酯(edma),40%十二烷醇,17%环己醇,1%偶氮二异丁氰组成,以上所有百分比均为质量比;将预聚物通入液滴微流控芯片的水相引入通道31中,然后将所有流体入口和出口密封后置于70摄氏度的烤箱中烘烤24小时使预聚物发生聚合反应;然后用清洗液(乙醇:去离子水=2:1,体积比)通过聚合物整体柱除去致孔剂和残留的单体,流速为0.5μl/min,时间为1小时;第四步同实施例一。
本实施例中的一种糖尿病高灵敏度检测方法同实施例一。
- 还没有人留言评论。精彩留言会获得点赞!