一种细胞多生物物理特性的检测装置及方法与流程
本发明涉及细胞特性检测领域,特别涉及一种细胞多生物物理特性的检测装置及方法。
背景技术:
目前,通常采用单细胞特性测量技术去了解细胞的状态以及机械特性。具体为通过一定的压力控制,采用微吸管将细胞的一部分吸入微吸管内来获取细胞的状态以及机械特性。但是这种微吸管技术在测量细胞的机械特性过程中,由于高精度的图像处理过程难以保证质量,且对压力即时性的控制要求比较高,所以获得的数据误差较大,在细胞鉴别和区分工作上并不能获得理想的结果。
另外,现有的微吸管技术只能够测量细胞的机械特性,而细胞的电学特性需要另外的设备进行测量。若想测量细胞的多种生物物理特性,需要多种设备,操作比较繁琐,效率低。因此,如何获得一种检测精度和检测效率均高且能够同时测量细胞的机械特性和电学特性的装置,是细胞特性测量领域急需解决的技术问题。
技术实现要素:
本发明的目的是提供了一种细胞多生物物理特性的检测装置及方法,不仅能够同时检测细胞的机械特性和电学特性,而且还提高细胞多特性的检测精度和检测效率。
为实现上述目的,本发明提供了如下方案:
一种细胞多生物物理特性的检测装置,所述检测装置包括:微吸管、银电极、培养皿、阻抗分析仪、图像获取模块、压力调节模块以及控制器;所述培养皿内放置被测细胞;所述微吸管的输入端与所述培养皿连接;所述银电极包括第一银电极和第二银电极;所述阻抗分析仪包括第一接口和第二接口;
所述第一银电极的一端从所述微吸管的输出端伸入到所述微吸管的内部,所述第一银电极的另一端与所述第一接口连接;所述第二银电极的一端放置在所述培养皿中,位于所述培养皿中的液面下,所述第二银电极的另一端与所述第二接口连接;当所述被测细胞完全被吸入到所述微吸管后,所述培养皿、所述微吸管、所述银电极以及所述阻抗分析仪形成回路;
所述压力调节模块与所述微吸管的输出端连接;所述培养皿设置在所述图像获取模块内;
所述控制器,与所述压力调节模块、所述图像获取模块、所述阻抗分析仪均连接,用于计算所述被测细胞的多生物物理特性,所述多生物物理特性包括机械特性和电学特性。
可选的,所述图像获取模块包括倒置的显微镜和ccd相机;所述培养皿放置在所述显微镜上;所述ccd相机与所述显微镜连接,所述控制器与所述ccd相机连接;所述显微镜用于记录所述被测细胞的放大图像;所述ccd相机用于获取所述被测细胞的放大图像。
可选的,所述压力调节模块包括驱动器、压力传感器以及直线推杆;所述直线推杆包括内套筒和外套筒,且所述内套筒的一端与所述外套筒的一端连接;所述内套筒的另一端与所述微吸管的输出端套接;所述外套筒的另一端与所述压力传感器、所述驱动器均连接;所述压力传感器通过所述直线推杆实时检测所述微吸管内部的压力;
所述控制器还与所述驱动器、所述压力传感器均连接,用于根据获取的所述微吸管内部的压力,输出压力调节命令,并将所述压力调节命令发送到所述驱动器,以驱动所述直线推杆的外套筒移动。
可选的,所述检测装置还包括机械臂;所述机械臂用于支撑所述微吸管;所述控制器还与所述机械臂连接,用于移动所述机械臂,使所述微吸管移动至所述被测细胞处。
可选的,所述检测装置还包括操作平台;所述操作平台穿过所述显微镜;所述培养皿放置在所述操作平台上。
可选的,所述检测装置还包括显示器;所述控制器还与所述显示器连接;所述显示器用于显示所述被测细胞的放大图像以及所述被测细胞的机械特性和电学特性。
可选的,所述微吸管末端管口处的半径为所述被测细胞半径的1/2。
本发明还提供了一种细胞多生物物理特性的检测方法,所述检测方法应用于所述的细胞多生物物理特性的检测装置;所述检测方法包括:
获取被测细胞的放大图像;
根据所述被测细胞的放大图像,判断微吸管是否移动至所述被测细胞处,得到第一判断结果;
若所述第一判断结果表示所述微吸管未移动至所述被测细胞处,则移动机械臂使所述微吸管移动至所述被测细胞处,并返回获取被测细胞的放大图像的步骤;
若所述第一判断结果表示所述微吸管移动至所述被测细胞处,则调节所述微吸管内部的压力,使所述被测细胞匀速进入所述微吸管内,并获取所述被测细胞进入所述微吸管过程的放大图像和所述微吸管内部的压力;
根据所述被测细胞进入所述微吸管过程的放大图像,判断所述被测细胞是否完全进入所述微吸管内,得到第二判断结果;
若所述第二判断结果表示所述被测细胞完全进入所述微吸管内,则获取所述被测细胞的阻抗曲线和所述被测细胞完全进入所述微吸管后的放大图像;
若所述第二判断结果表示所述被测细胞未完全进入所述微吸管内,则返回调节所述微吸管内部的压力,使所述被测细胞匀速进入所述微吸管内的步骤;
根据所述被测细胞进入所述微吸管过程的放大图像和所述微吸管内部的压力,计算所述被测细胞的机械特性;所述机械特性包括杨氏模量和粘性系数;
根据所述被测细胞的阻抗曲线和所述被测细胞完全进入所述微吸管后的放大图像,计算所述被测细胞的电学特性;所述电学特性包括细胞质电阻率和细胞膜比电容。
可选的,根据所述被测细胞进入所述微吸管过程的放大图像和所述微吸管内部的压力,计算所述被测细胞的机械特性,具体包括:
对所述被测细胞进入所述微吸管过程的放大图像进行阈值化处理和轮廓线提取,并采用实时跟踪算法,获取所述被测细胞的形态信息;
根据所述被测细胞的形态信息和所述微吸管内部的压力,采用力学模型,计算所述被测细胞的杨氏模量和粘性系数。
可选的,根据所述被测细胞的阻抗曲线和所述被测细胞完全进入所述微吸管后的放大图像,计算所述被测细胞的电学特性,具体包括:
对所述被测细胞完全进入所述微吸管后的放大图像进行阈值化处理和轮廓线提取,得到所述被测细胞完全进入所述微吸管后的外形信息;
根据所述外形信息和所述被测细胞的阻抗曲线,计算所述被测细胞的细胞质电阻率和细胞膜比电容。
根据本发明提供的具体实施例,本发明公开了以下技术效果:
本发明提供了一种细胞多生物物理特性的检测装置及方法,该装置包括微吸管、银电极、培养皿、阻抗分析仪、图像获取模块、压力调节模块以及控制器;所述培养皿内放置被测细胞;所述微吸管的输入端与所述培养皿连接;所述银电极包括第一银电极和第二银电极;所述阻抗分析仪包括第一接口和第二接口;所述控制器,与所述压力调节模块、所述图像获取模块、所述阻抗分析仪均连接;
所述压力调节模块与所述微吸管的输出端连接;所述培养皿设置在所述图像获取模块内;通过压力调节模块使被测细胞匀速缓慢的进入微吸管,并通过图像获取模块采集被测细胞进入微吸管过程的图像,然后根据压力调节模块输出的压力值和采集的图像,计算被测细胞的机械特性;
所述第一银电极的一端从所述微吸管的输出端伸入到所述微吸管的内部,所述第一银电极的另一端与所述第一接口连接;所述第二银电极的一端放置在所述培养皿的液面下,所述第二银电极的另一端与所述第二接口连接;当被测细胞完全进入微吸管后形成回路,然后通过被测细胞的阻抗曲线和被测细胞完全进入微吸管后的大图像,计算被测细胞的电学特性。
通过控制器与压力调节模块、图像获取模块均连接,实现压力的自动调节和图像的自动采集,解决由于压力无法调节,使被测细胞快速进入微吸管内,导致采集的图像较少,计算误差较大,被测细胞多特性检测精度较低的问题。
综上所述,本发明提供的细胞多生物物理特性检测装置或方法,能够同时检测细胞的机械特性和电学特性,提高了检测效率,同时还能够实现压力的自动调节和图像的自动采集,提高了测细胞多特性的检测精度。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动性的前提下,还可以根据这些附图获得其他的附图。
图1为本发明实施例细胞多生物物理特性检测装置的结构示意图;
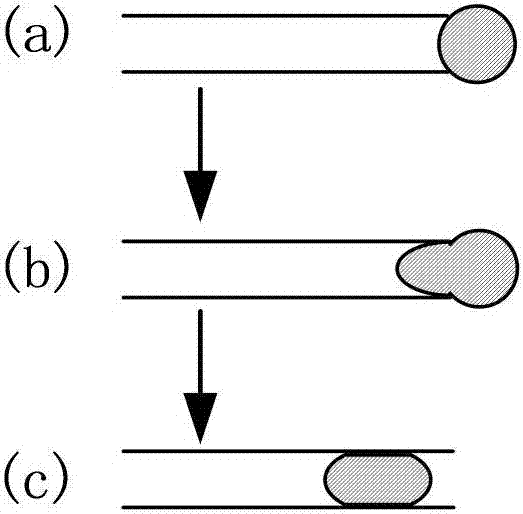
图2为本发明被测细胞进入微吸管的过程示意图;
图3为本发明实施例细胞多生物物理特性检测方法的流程示意图;
具体实施方式
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
本发明的目的是提供了一种细胞多生物物理特性的检测装置及方法,不仅能够同时检测细胞的机械特性和电学特性,而且还提高细胞多特性的检测精度和检测效率。
为使本发明的上述目的、特征和优点能够更加明显易懂,下面结合附图和具体实施方式对本发明作进一步详细的说明。
图1为本发明实施例细胞多生物物理特性检测装置的结构示意图。
如图1所示,本发明提供的细胞多生物物理特性检测装置包括:微吸管1、银电极2、培养皿3、阻抗分析仪4、图像获取模块5、压力调节模块6、控制器7、机械臂8、操作平台9以及显示器10。所述培养皿3内放置被测细胞;所述微吸管1的输入端与所述培养皿3连接;所述银电极2包括第一银电极201和第二银电极301;所述阻抗分析仪4包括第一接口和第二接口;所述培养皿3设置在所述图像获取模块5内,所述压力调节模块6与所述微吸管1的输出端连接。
所述控制器7,与所述阻抗分析仪4、所述图像获取模块5、所述压力调节模块6、所述机械臂8、所述显示器10均连接。
所述第一银电极201的一端从所述微吸管1的输出端伸入到所述微吸管1的内部,所述第一银电极201的另一端与所述第一接口连接;所述第二银电极202的一端放置在所述培养皿3的液面下,所述第二银电极202的另一端与所述第二接口连接;当所述被测细胞完全被吸入到所述微吸管1后,所述培养皿3、所述微吸管1、所述银电极2以及所述阻抗分析仪4形成回路。
所述图像获取模块5包括倒置的显微镜501和ccd相机502。
所述操作平台9穿过所述显微镜501;所述培养皿3放置在所述操作平台9上。所述显微镜501用于记录所述被测细胞的放大图像;所述ccd相机502,与所述显微镜501、所述控制器7均连接,用于将获取所述被测细胞的放大图像传输到所述控制器7内。
所述压力调节模块6包括驱动器601、压力传感器602以及直线推杆603。
所述直线推杆603包括内套筒和外套筒,且内套筒的一端与外套筒的一端连接;所述内套筒的另一端与所述微吸管1的输出端紧密套接;所述外套筒的另一端与所述压力传感器602、所述驱动器601均连接;所述压力传感器602通过所述直线推杆603实时检测所述微吸管1内部的压力。
所述控制器7内设pid算法;所述控制器7,与所述驱动器601、所述压力传感器602均连接,用于根据获取的所述微吸管1内部的压力,通过pid算法自动输出压力调节命令,并将所述压力调节命令发送到所述驱动器601,以驱动所述直线推杆603的外套筒移动。
所述机械臂8用于支撑所述微吸管1。微吸管1可以被机械臂8夹持并可沿各方向运动。优选的,所述机械臂8为三自由度机械手臂。
所述控制器7与所述机械臂8连接用于控制移动所述机械臂8使所述微吸管1移动至所述被测细胞处。
所述控制器7还与所述显示器10连接,用于将被测细胞的放大图像以及所述被测细胞的机械特性和电学特性传输到所述显示器10。所述显示器10用于显示所述被测细胞的放大图像以及所述被测细胞的机械特性和电学特性。
所述微吸管1末端管口处的半径为所述被测细胞半径的1/2。
优选的,所用微吸管1的内径为8~12um,被测细胞的半径为13-15um。压力调节模块6提供的压力为-1000pa~1000pa,精度为±5pa。
图2为本发明被测细胞进入微吸管的过程示意图,如图2所示,(a)为微吸管靠近被测细胞,未增加压力的状态。(b)为缓慢增加压力,被测细胞的一部分被缓缓吸入微吸管中,此时通过图像获取模块获得的图像,然后处理可以用于被测细胞的机械特性。(c)为被测细胞经过一定的压力后被完全吸入微吸管内,此时记录阻抗分析仪上的阻抗曲线,可以获得细胞的电学特性。
本发明所采用的细胞多生物物理特性的检测装置是:在现有测量细胞机械特性的微吸管吸附系统中,在微吸管1输入端引出第一银电极201,同时在培养皿3的液面下固结第二银电极202,第一银电极201和第二银电极202分别与阻抗分析仪4的正负极相连。当被测细胞被完全吸入微吸管时即可形成回路,可检测被测细胞的电学特性。
具体为:微吸管1与一个压力调节模块6中的直线推杆603密闭连接,通过控制器7和压力调节模块6可控制微吸管1尖端输出负压或正压,完成被测细胞吸入或吐出操作,同时实时获取微吸管1尖端的压力大小。被测细胞在压力的作用下,被匀速缓慢的吸入进入微吸管1时,被测细胞将产生压缩变形。此时通过控制器7和图像获取模块6测量获取被测细胞产生的形变量,监测被测细胞吸附动态变化过程,实时反馈被测细胞进入微吸管1的长度,被测细胞尺寸大小等几何信息。结合微吸管1尖端施加的压力的大小与被测细胞的形态信息,获得在不同时刻、不同压力下被测细胞的瞬态吸入长度和稳态吸入长度,可通过半空间模型获得被测细胞的吸入长度和施加压力之间的关系,通过力学模型计算出被测细胞的杨氏模量(弹性模量)、粘性系数等机械特性参数
在测得被测细胞机械特性参数后,需进一步加大吸入压力将被测细胞整体全部吸入微吸管1内,此时对被测细胞进行电学建模,可将其等效成一个细胞质电阻与细胞膜电容串联。利用阻抗分析仪4中提供的阻抗曲线,进行阻抗频谱非线性拟合,并基于控制器7和图像获取模块6得到被测细胞全部吸入微吸管后的被测细胞的外形信息,计算细胞质电阻率及细胞膜比电容等电学特性参数。
本发明实施例提供了一种基于微管吸附技术的细胞多生物物理特性的检测装置,在现有的微吸管技术上进行改进,使其在可以测量机械特性的同时,也测得细胞的电学特性,获得单个细胞更多的特性以获得更好的分析数据。另外,通过控制器与压力调节模块、图像获取模块连接,实现压力的自动调节和图像的自动采集,解决由于压力无法调节,使被测细胞快速进入微吸管内,导致采集的图像较少,计算误差较大,被测细胞多特性检测精度较低的问题。
为实现上述目的,本发明还提供了一种细胞多生物物理特性的检测方法。所述细胞多生物物理特性的检测方法应用于本发明提供的所述细胞多生物物理特性的检测装置。
图3为本发明实施例的细胞多生物物理特性检测方法的流程示意图,如图3所示,本发明提供的细胞多生物物理特性的检测方法包括:
步骤301:获取被测细胞的放大图像。
步骤302:根据所述被测细胞的放大图像,判断微吸管是否移动至所述被测细胞处,得到第一判断结果。
若所述第一判断结果表示所述微吸管未移动至所述被测细胞处,则执行步骤303;若所述第一判断结果表示所述微吸管移动至所述被测细胞处,则执行步骤304。
步骤303:移动机械臂使所述微吸管移动至所述被测细胞处,并返回步骤301。
步骤304:调节所述微吸管内部的压力,使所述被测细胞匀速进入所述微吸管内,并获取所述被测细胞进入所述微吸管过程的放大图像和所述微吸管内部的压力。
步骤305:根据所述被测细胞进入所述微吸管过程的放大图像,判断所述被测细胞是否完全进入所述微吸管内,得到第二判断结果;
若所述第二判断结果表示所述被测细胞完全进入所述微吸管内,则执行步骤306;若所述第二判断结果表示所述被测细胞未完全进入所述微吸管内,则返回步骤304。
步骤306:获取所述被测细胞的阻抗曲线和所述被测细胞完全进入所述微吸管后的放大图像。
步骤307:根据所述被测细胞进入所述微吸管过程的放大图像和所述微吸管内部的压力,计算所述被测细胞的机械特性;所述机械特性包括杨氏模量和粘性系数。
步骤308:根据所述被测细胞的阻抗曲线和所述被测细胞完全进入所述微吸管后的放大图像,计算所述被测细胞的电学特性;所述电学特性包括细胞质电阻率和细胞膜比电容。
在执行步骤301之前,还包括准备细胞培养皿,并在细胞培养皿内放置被测细胞,然后启动电源,使细胞多生物物理特性检测装置通电。
所述步骤307具体包括:
对所述被测细胞进入所述微吸管过程的放大图像进行阈值化处理和轮廓线提取,并采用实时跟踪算法,获取所述被测细胞的形态信息。
根据所述被测细胞的形态信息和所述微吸管内部的压力,采用力学模型,计算所述被测细胞的杨氏模量和粘性系数。
所述步骤308具体包括:
对所述被测细胞完全进入所述微吸管后的放大图像进行阈值化处理和轮廓线提取,得到所述被测细胞完全进入所述微吸管后的外形信息。
根据所述外形信息和所述被测细胞的阻抗曲线,计算所述被测细胞的细胞质电阻率和细胞膜比电容。
本发明实施例提供的细胞多生物物理特性检测方法,相较于现有的吸管系统,提出了一种引入电极丝测量细胞电学特性的方法,采用该方法能够测量更丰富的参数,使微吸管可以同时测量细胞的机械特性及电学特性,可以极大地提高微吸管测量技术的效率,使微吸管技术能够测量单个细胞更全面的特性。
本说明书中各个实施例采用递进的方式描述,每个实施例重点说明的都是与其他实施例的不同之处,各个实施例之间相同相似部分互相参见即可。对于实施例公开的系统而言,由于其与实施例公开的方法相对应,所以描述的比较简单,相关之处参见方法部分说明即可。
本文中应用了具体个例对本发明的原理及实施方式进行了阐述,以上实施例的说明只是用于帮助理解本发明的方法及其核心思想;同时,对于本领域的一般技术人员,依据本发明的思想,在具体实施方式及应用范围上均会有改变之处。综上所述,本说明书内容不应理解为对本发明的限制。
- 还没有人留言评论。精彩留言会获得点赞!