阿维菌素/埃普菌素/伊维菌素三合一检测试剂盒的制作方法
本发明涉及到一种阿维菌素类三合一检测试剂盒,具体涉及阿维菌素/埃普菌素/伊维菌素在动物性食品中残留的酶联免疫检测试剂盒。
背景技术:
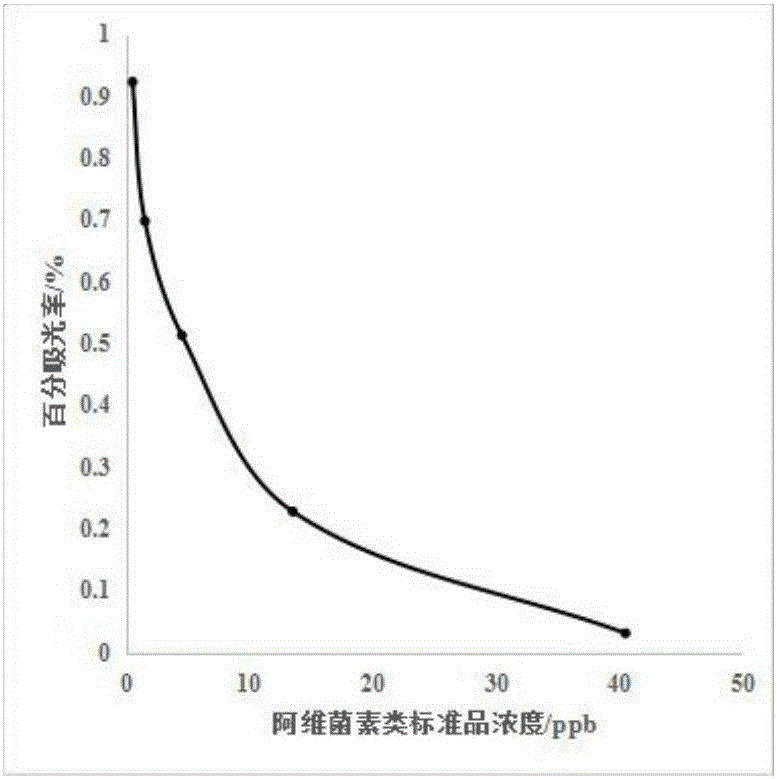
:阿维菌素/埃普菌素/伊维菌素是一类具有高效广谱的抗生素类药物,是一类优质的新型畜禽抗生素。可经链霉菌发酵获得,阿维菌素类抗生素由一组大环内酯组成。阿维菌素类对动植物寄生线虫及节肢动物具有较强驱杀性,由于杀虫能力强并且杀虫广谱,被大量用在农产品生产过程及水产养殖。该药物对神经及发育具有毒性,世界卫生组织已将其列入高毒化合物。阿维菌素类药物脂溶性极好、代谢慢,长期无监管非合理正确使用该类药物,导致药物大量残留在养殖动物体内,最终被人体吸收,从而对人类安全产生巨大影响。目前,各类有关阿维菌素类检测方法研究报道相对较多,但综合检测多种阿维菌素类残留试剂盒相对较少。技术实现要素:本发明拟提供一种专门针对阿维菌素/埃普菌素/伊维菌素残留检测的试剂盒,并提供一种准确、简便、满足大批量样本筛选的定性、定量检测和试剂盒制备方法。本发明所述的阿维菌素/埃普菌素/伊维菌素残留检测试剂盒,其主要包含以下试剂:包被阿维菌素类特异性抗体的酶标板、阿维菌素类药物标准溶液、酶标抗原、酶标抗原浓缩稀释液、底物液、终止液、浓缩洗涤液、浓缩复溶液所组成。所述阿维菌素类药物标准溶液6瓶,浓度分别为0ng/ml、0.5ng/ml、1.5ng/ml、4.5ng/ml、13.5ng/ml、40.5ng/ml。酶标抗原:是由阿维菌素药物与bsa偶联制成的人工抗原与碱性磷酸酶(ap)经戊二醛法或碘酸钠法偶联制备得到。酶标抗原浓缩稀释液:含0.5-1%的酪蛋白ph7-8,0.1-0.2mpbs缓冲液,所述百分比为质量体积百分比。底物液为碱性磷酸酶显色液,试剂a为10%二乙醇胺缓冲液,试剂b为5%对硝基苯磷酸二钠(pnpp)缓冲液,试剂c为0.01%氯化镁tris-bace缓冲液。所述终止液为0.1mol/l氢氧化钠。所述浓缩洗涤液为1%-1.5%tween-20和0.01%的叠氮钠的ph=7.20.2-0.5mol/lpb缓冲液,所述百分比为质量体积百分比。所述浓缩复溶液为ph=7.2含有5%-8%酪蛋白的0.1-0.2mol/lpb缓冲液,所述百分比为质量体积百分比。所述阿维菌素类特异性抗体是经阿维菌素半抗原-载体蛋白偶联为免疫原免疫获得,所述阿维菌素类特异性抗体可为阿维菌素类单克隆抗体或阿维菌素类多克隆抗体,其中优选阿维菌素类单克隆抗体。所述阿维菌素类特异性抗体的酶标板经包被缓冲液稀释阿维菌素类特异性抗体为0.1μg/ml,每孔加入100ul,37℃恒温孵育1h后4℃过夜,倒去孔中液体,用洗涤液洗涤1次,停留30s,拍干,每孔加入150μl封闭液,37℃孵育2-3h,倒去孔内液体,拍干后放置25℃恒温晾干,抽检合格后将酶标板真空包装,4℃保存。所述阿维菌素类特异性抗体的酶标板制备过程,使用包被缓冲液为ph=9.2-9.6浓度0.1-0.2mol/l碳酸盐缓冲液,封闭液为ph=7.0-7.4含1%-5%酪蛋白,浓度0.1-0.2mol/lpbs缓冲液,所述百分比为质量体积百分比。本发明所述酶标抗原浓缩稀释液、浓缩洗涤液、浓缩复溶液配置成工作液方法如下所述:酶标抗原工作液,用去离子水将酶标抗原浓缩稀释液按1:19体积比进行稀释,用于酶标抗原的稀释,酶标抗原工作液在4℃环境可保存一个月。洗涤工作液,用去离子水将浓缩洗涤液按1:19体积比进行稀释,用于酶标板的洗涤,洗涤工作液在4℃环境可保存一个月。复溶工作液,用去离子水将浓缩复溶液按1:19体积比进行稀释,用于样品的稀释,复溶工作液在4℃环境可保存一个月。本发明所述试剂盒基于抗原抗体免疫反应,其检测方法主要包括以下步骤:1)样品前处理,将样品中待测药物通过有机溶剂提取出来;2)将所有试剂与酶标板回温至20-25℃;3)加标准品/样本和酶标抗原工作液:加标准品/样本50ml到对应的微孔中,然后加入酶标抗原工作液50ml/孔,轻轻振荡混匀,用盖板膜盖板后置25℃避光环境中反应45min;4)洗板:小心揭开盖板膜,将孔内液体甩干,加入洗涤工作液250ml/孔,充分洗涤3-5次,泼掉板孔内洗涤液,用吸水纸拍干;5)显色:取a液250μl,加入到盛有10mlc液管内,再加入b液300μl充分混匀;每孔加入100μl,轻轻振荡混匀,用盖板膜盖板后置25℃避光环境中反应10min;6)检测:加入终止液50ml/孔,轻轻振荡混匀,设定酶标仪于405nm检测每孔od值。本发明的检测原理为:本发明采用抗原抗体反应的高度特异性与碱性磷酸酶催化的高度灵敏性结合起来,利用碱性磷酸酶催化底物显色检测产物浓度,在酶标板微孔条上包被阿维菌素类特异性抗体的酶标板,样品中残留的阿维菌素/埃普菌素/伊维菌素和酶标抗原竞争阿维菌素类特异性抗体,加入底物显色,样品吸光度值与所含残留物阿维菌素/埃普菌素/伊维菌素的含量呈负相关,与标准曲线比较,即可得出样品中阿维菌素/埃普菌素/伊维菌素的残留量。本发明阿维菌素/埃普菌素/伊维菌素三合一检测试剂盒具有灵敏度高、简捷方便、准确的特点,在对阿维菌素类残留检测具有重要作用。附图说明图1阿维菌素/埃普菌素/伊维菌素三合一检测试剂盒标准曲线。具体实施方式实施例1阿维菌素/埃普菌素/伊维菌素三合一检测试剂盒组分制备1、阿维菌素抗原制备及鉴定称取43.5mg阿维菌素半抗原溶解于2mldmf中,加入edc和nhs进行活化30min,加入到100-200mg载体蛋白bsa溶于5ml水溶液中,调溶液ph至7.6-8.0,4℃搅拌24h;用0.01mol/lpbs在4℃透析3d,每天更换3次透析袋,以除去未反应的小分子物质;分装,于-20℃保存备用。将bsa、阿维菌素抗原、阿维菌素半抗原-载体蛋白偶联物用ph7.4磷酸缓冲液配成0.5mg/ml的溶液,用紫外分光光度计在200-800nm波长进行扫描,得到载体蛋白、阿维菌素半抗原、阿维菌素半抗原-载体蛋白偶联物的吸收曲线。并出现不同的吸收曲线,表明阿维菌素半抗原与载体蛋白偶联成功。2、阿维菌素类单克隆抗体的制备动物免疫:将免疫原注入balb/c小鼠体内,剂量为50μg/只。细胞融合和克隆化:取免疫balb/c小鼠脾细胞与sp2/0骨髓瘤细胞融合,利用有限稀释法对阳性孔进行克隆化,得到稳定分泌单克隆抗体的杂交瘤细胞株。细胞冻存和复苏:将单克隆杂交瘤细胞株用冻存液制成1×108个/ml的细胞悬液,在液氮中长期保存。复苏时取出冻存管,立即放入42℃水浴中速融,离心去除冻存液后,移入培养瓶内培养。单克隆抗体的制备与纯化:balb/c小鼠腹腔注射灭菌石蜡油,7天后腹腔注射单克隆杂交瘤细胞株5×105个/只,采集腹水。3、酶标抗原的制备称取2mghrp溶解于0.5ml双蒸水中,加入0.5ml新配置的0.05mol/lnaio4溶液,4℃避光反应2h;加入180mmol/l的乙二醇0.5ml,4℃反应1h;加入阿维菌素药物抗原2mg,混匀后用0.05mol/lpbs透析过夜;透析液加入1/4体积新配置的0.5%nabh4溶液,4℃静置过夜,;加入等体积饱和硫酸铵,4℃静置2-4h,4℃,5000r/min离心30min,取沉淀;将沉淀溶解于ph=8.0的0.05mol/lpbs缓冲液,用0.01mol/lpbs4℃透析过夜;透析液4℃,10000r/min离心30min取上清,加入等体积甘油,分装-20℃保存。实施例2阿维菌素/埃普菌素/伊维菌素三合一检测试剂盒1、阿维菌素/埃普菌素/伊维菌素三合一检测试剂盒组成包被有阿维菌素类特异性抗体的酶标板;阿维菌素类药物标准溶液6瓶,浓度分别为0ng/ml、0.5ng/ml、1.5ng/ml、4.5ng/ml、13.5ng/ml、40.5ng/ml;酶标抗原由阿维菌素药物和bsa偶联制成的人工抗原与碱性磷酸酶(ap)经戊二醛法或碘酸钠法偶联制备得到;酶标抗原浓缩稀释液为0.5-1%的酪蛋白ph7-8,0.1-0.2mpbs缓冲液;底物显色液试剂a为10%二乙醇胺缓冲液,试剂b为5%对硝基苯磷酸二钠(pnpp)缓冲液,试剂c为0.01%氯化镁tris-bace缓冲液;终止液为0.1mol/l氢氧化钠;浓缩洗涤液为1%-1.5%tween-20和0.01%的叠氮钠的ph=7.20.2-0.5mol/lpb缓冲液;浓缩复溶液为ph=7.2含有5%-8%酪蛋白的0.1-0.2mol/lpb缓冲液。2、阿维菌素类特异性抗体的酶标板的制备用ph=9.2-9.6浓度0.1-0.2mol/l碳酸盐缓冲液稀释阿维菌素类特异性抗体为0.1μg/ml,每孔加入100ul,37℃恒温孵育1h后4℃过夜,倒去孔中液体,用洗涤液洗涤1次,停留30s,拍干,每孔加入150μlph=7.0-7.4含1%-5%酪蛋白,浓度0.1-0.2mol/lpbs缓冲液,37℃孵育2-3h,倒去孔内液体,拍干后放置25℃恒温晾干,抽检合格后将酶标板真空包装,4℃保存。实施例3阿维菌素/埃普菌素/伊维菌素三合一检测试剂盒的应用1、试剂配置1)酶标抗原工作液,用去离子水将酶标抗原浓缩稀释液按1:19体积比进行稀释,用于酶标抗原的稀释;2)洗涤工作液,用去离子水将浓缩洗涤液按1:19体积比进行稀释,用于酶标板的洗涤;3)复溶工作液,用去离子水将浓缩复溶液按1:19体积比进行稀释,用于样品的稀释;4)显色液:取a液250μl,加入到盛有10mlc液管内,再加入b液300μl充分混匀。2、样品前处理1)鸡肉、牛肉等家畜肉类:用均质器均质样本,称取5g样品,加入5ml甲醇,涡旋振荡10min,5000r/min离心10min;取上清,按1:9体积比经复溶工作液稀释;2)虾仁、鱼等水产:用均质器均质样本,称取5g样品,加入10ml乙腈、5ml正己烷,涡旋振荡10min,5000r/min离心10min;取上清,水浴氮气流下吹干,加入1ml复溶工作液稀释;3、检测步骤1)加标准品/样本和酶标抗原工作液:加标准品/样本50ml到对应的微孔中,然后加入酶标抗原工作液50ml/孔,轻轻振荡混匀,用盖板膜盖板后置25℃避光环境中反应45min;2)洗板:小心揭开盖板膜,将孔内液体甩干,加入洗涤工作液250ml/孔,充分洗涤3-5次,泼掉板孔内洗涤液,用吸水纸拍干;3)显色:取a液250μl,加入到盛有10mlc液管内,再加入b液300μl,充分混匀;轻轻混合即可,每孔加入100μl,轻轻振荡混匀,用盖板膜盖板后置25℃避光环境中反应10min;4)检测:加入终止液50ml/孔,轻轻振荡混匀,设定酶标仪于405nm检测每孔od值。4、结果分析百分吸光率的计算,标准品或样本的百分吸光率等于标准品或样本的吸光度值的平均值(双孔)除以第一个标准品(0标准)的吸光度值的平均值,再乘以100%,即百分吸光率(%)=×100%b—标准品或样本溶液的平均吸光度值,b0—0ppb标准溶液的平均吸光度值。以阿维菌素类标准品浓度(ppb)为横坐标,标准品百分吸光度率为纵坐标,绘制标准曲线,求出线性方程。将样本的百分吸光率代入标准曲线,从标准曲线读出样本对应浓度,乘以稀释倍数即为样本中阿维菌素类残留的浓度。实施例4试剂盒特异性验证特异性是指交叉反应率,抗体与抗原发生结合的能力强弱。通过测定阿维菌素类药物ic50值,选择不同阿维菌素药物类似结构的药物测定ic50值,计算交叉反应率来判断试剂盒检测的特异性。交叉反应率(%)=×100%计算结果如下表所示:表1阿维菌素类药物交叉反应率药物名称交叉反应率/%阿维菌素100埃维菌素130伊维菌素95当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1