尿液中氟代-β-丙氨酸的检测方法及检测试剂盒与流程
本发明属于尿液定量检测技术领域,具体涉及一种尿液中氟代-β-丙氨酸的检测方法及用于尿液中氟代-β-丙氨酸检测的检测试剂盒。
背景技术
据报道,2013年全国消化道恶性肿瘤新发患者约为105万,其中结直肠癌新发患者为35万,结直肠癌死亡患者为16万[陈万青,郑荣寿,张思维,等.2013年中国恶性肿瘤发病和死亡分析.中国肿瘤,2017,26(1):1-10.]。自1998以来,我国结直肠癌发病率和死亡率逐年上升,发病率位于恶性肿瘤发病率的第四位,死亡率位于恶性肿瘤死亡率的第五位,发病率和死亡率均居前列[lius,zhengr,zhangm,etal.incidenceandmortalityofcolorectalcancerinchina,2011.chinesejournalofcancerresearch,2015,27(1):22-28.]。高发的结直肠癌给患者家庭以及社会造成了严重的经济负担。目前,氟尿嘧啶类化合物仍为结直肠癌患者辅助化疗的首选,在其数十年的使用过程中,有效提高了患者的生存期。卡培他滨是5-氟尿嘧啶的前药,因其口服给药的便利性以及药效的部分靶向性,目前已成为结直肠癌患者临床化疗的一线用药。
氟代-β-丙氨酸(fbal)是卡培他滨的终产物,也是卡培他滨发生不良反应的一个关键产物[reignerb,bleschk,weidekamme.clinicalpharmacokineticsofcapecitabine.clinicalpharmacokinetics,2001,40(2):85-104.],氟代-β-丙氨酸的化学结构式如下:
卡培他滨经过6步代谢后,可生成终产物氟代-β-丙氨酸,并随尿液排出体外。有研究报道,同其它卡培他滨代谢物相比较,氟代-β-丙氨酸具有较长的消除半衰期(4h),在使用卡培他滨一段时间后,氟代-β-丙氨酸可在体内明显蓄积[abdizd,lavau-deness,prémauda,etal.pharmacokineticsandexposure–effectrelationshipsofcapecitabineinelderlypatientswithbreastorcolorectalcancer.cancerchemotherapyandpharmacology,2014,73(6):1285-1293.]。这种蓄积作用使得患者需要额外的时间来排泄氟代-β-丙氨酸。
研究报道,体内蓄积的氟代-β-丙氨酸与患者服用卡培他滨发生不良反应之间具有非常密切的相关性。动物研究显示,累积的氟代-β-丙氨酸可使beagle犬发生明显的神经毒性症状及神经生理改变[yamashitak,yadah,ariyoshit.neurotoxiceffectsofalpha-fluoro-beta-alanine(fβal)andfluoroaceticacid(fa)ondogs.journaloftoxicologicalsciences,2004,29(2):155-166.akibat,okedar,tajimat.metabolitesof5-fluorouracil,alpha-fluoro-beta-alanineandfluoroaceticacid,directlyinjuremyelinatedfibersintissueculture.actaneuropathologica,1996,92(1):8-13.],而在部分结直肠癌患者中,累积的氟代-β-丙氨酸可诱导可逆性的心前区疼痛并伴随右束支阻滞和高血氨症[nishikaway,funakoshit,horimatsut,etal.accumulationofalpha-fluoro-beta-alanineandfluoromonoacetateinapatientwith5-fluorouracil-associatedhyperammonemia.cancerchemotherapyandpharmacology,2017,79(3):629-633.muneokak,shiraiy,yokoyaman,etal.5-fluorouracilcardiotoxicityinducedbyalpha-fluoro-beta-alanine.internationaljournalofclinicaloncology,2005,10(6):441-443.]。
但是,目前氟代-β-丙氨酸的体内暴露量与其不良反应之间的关联尚未阐明,且不良反应发生的阈值尚未确定,主要原因在于血液中的氟代-β-丙氨酸难以被定量。目前,已有部分的研究报道了通过液相-串联质谱方法(liquidchromatography-tandemmassspectrometry,lc-ms/ms)定量生物样本中的氟代-β-丙氨酸[deenenmj,rosingh,hillebrandmj,etal.quantitativedeterminationofcapecitabineanditssixmetabolitesinhumanplasmausingliquidchromatographycoupledtoelectrospraytandemmassspectrometry.journalofchromatographyb,2013,s913-914(2):30-40.licea-perezh,wangs,bowenc.developmentofasensitiveandselectivelc-ms/msmethodforthedeterminationofα-fluoro-β-alanine,5-fluorouracilandcapecitabineinhumanplasma.journalofchromatographybanalyticaltechnologiesinthebiomedical&lifesciences,2009,877(11-12):1040-1046.chavanio,jensenbp,strotherrm,etal.development,validationandapplicationofanovelliquidchromatographytandemmassspectrometryassaymeasuringuracil,5,6-dihydrouracil,5-fluorouracil,5,6-dihydro-5-fluorouracil,α-fluoro-β-ureidopropionicacidandα-fluoro-β-alanineinhumanplasma.journalofpharmaceuticalandbiomedicalanalysis,2017,142:125-135.ndaws,denisf,marsanp,etal.biologicalmonitoringofoccupationalexposureto5-fluorouracil:urinaryα-fluoro-β-alanineassaybyhighperformanceliquidchromatographytandemmassspectrometryinhealthcarepersonnel.journalofchromatographybanalyticaltechnologiesinthebiomedical&lifesciences,2010,878(27):2630-2634.]。此类方法通常需要较长的分析时间,或需要衍生化等特殊的前处理方法用以提取生物基质中的氟代-β-丙氨酸,并且血样采集患者依从性差,不利于临床推广应用。代谢产物的尿液排泄量通常能够反映该代谢产物的体内暴露量,一个简单,无需衍生化的提取方法可能对氟代-β-丙氨酸体内暴露量的监测具有重要作用,但目前尚无此种方法的文献报道。
技术实现要素:
本发明是为解决上述问题而进行的,目的在于提供一种能够快速、直接对尿液中的氟代-β-丙氨酸进行检测的检测方法以及检测试剂盒。
本发明的第一方面,提供了一种尿液中氟代-β-丙氨酸的检测方法,采用超高效液相色谱-串联质谱进行检测,包括以下步骤:
a)对待检尿液样本进行预处理;
b)采用超高效液相色谱将预处理后待检尿液样本中的氟代-β-丙氨酸与尿液中的其它成分进行分离;
c)采用串联质谱检测氟代-β-丙氨酸的含量,以丙氨酸的同位素化合物为内标,采用校正曲线法计算尿液中氟代-β-丙氨酸的含量,
其中,步骤b)中的色谱条件为:色谱柱为xbridgehilic柱(3.5μm,2.1mm×100mm);流速为0.35ml/min,柱温为35℃,进样量为5μl;流动相a为10mmol/l乙酸铵水溶液,流动相b为乙腈,采用梯度洗脱方式进行分离;流动相洗脱参数如下:0min~3min,流动相a为17%~40%,流动相b为83%~60%,
步骤c)中的质谱条件为:在电喷雾电离、正离子解离模式下,采用多重反应监测的质谱扫描模式;毛细管电压为±4000v,喷雾器压力为50psi,碰撞气压力为0.2mpa;干燥气温度为325℃,干燥气流速为10l/min;鞘气温度为350℃,鞘气流速为12l/min;待测化合物氟代-β-丙氨酸的离子对为m/z108→62、f值为75v、ce值为13ev,内标化合物的离子对为m/z94→48、f值为34v、ce值为13ev。
步骤a)中对待检尿液样本进行预处理的方法如下:取尿液样本于1.5ml离心管中,加入提取液,涡旋1min后以14500×g的离心力室温下离心10min,转移上清液于进样小瓶中进行分析。优选尿液样本与提取液之间的体积比为1:9,如取10μl尿液样本于1.5ml离心管中,则需加入90μl提取液。
优选的,提取液为含1μg/ml内标的体积分数为50%乙腈水溶液,内标为丙氨酸-d4化合物。
此外,步骤c)中,校正曲线包含有s1~s9九个浓度点,校正曲线的建立方法如下:
取一定体积的对照品母液,加入9倍体积稀释液2,涡旋混匀后得工作液,再加入9倍工作液体积的稀释液1,涡旋1~2min混匀,得到校正曲线最高浓度点s9;取一定体积的s9,加入体积为s9三分之一的稀释液1,涡旋混匀,即得s8;分别取一定体积的s9,加入稀释液1分别稀释4倍和2倍,涡旋混匀,即得s6、s7;取一定体积的s6、s7,分别加入稀释液1稀释5倍,涡旋混匀,即得s4、s5;取一定体积的s4、s5,分别加入稀释液1稀释10倍,涡旋混匀,即得s2、s3;取一定体积的s3,加入稀释液1稀释5倍,涡旋混匀,即得s1,
取s1、s2、s3、s4、s5、s6、s7、s8、s9各10μl,按照步骤a)中所述的预处理方法对上述9个校正曲线浓度点样本进行预处理,再进样测定,以对照品浓度作为x轴,待测化合物与内标化合物的峰面积比值作为y轴,建立校正曲线。
在进行实际尿液样本检测时,将串联质谱测得的待测尿液样本中氟代-β-丙氨酸的峰面积与内标化合物的峰面积比值代入校正曲线中,通过计算即可得出该待测尿液样本中氟代-β-丙氨酸含量。
在建立校正曲线过程中,所用对照品母液为1mg/ml的氟代-β-丙氨酸甲醇溶液;所用稀释液1为空白尿液,稀释液2为双蒸水。
本发明的第二方面,提供了一种尿液中氟代-β-丙氨酸检测试剂盒,该检测试剂盒包括洗脱液、对照品母液、稀释液、提取液以及质控液。
其中,洗脱液包括洗脱液a和洗脱液b,分别作为超高效液相色谱的流动相a和流动相b,洗脱液a为500ml的10mmol/l乙酸铵水溶液,洗脱液b为500ml的乙腈,
对照品母液的制备方法为:取氟代-β-丙氨酸,精密称定质量,加入甲醇溶解,得1mg/ml的对照品母液,
稀释液包括稀释液1和稀释液2,稀释液1为10ml空白尿液,稀释液2为10ml双蒸水,
提取液的制备方法为:取丙氨酸-d4,精密称定质量,加入甲醇溶解,得1mg/ml的内标溶液,而后加入50%乙腈逐级稀释,得1μg/ml的提取液,
质控液为含有氟代-β-丙氨酸的空白尿液,包括7500ng/ml的高浓度质控液、2500ng/ml的中浓度质控液、50ng/ml的低浓度质控液。
优选的,质控液的制备方法如下:
取对照品母液,加入双蒸水定容,制备浓度为100μg/ml的对照品溶液,精密吸取对照品溶液,加入9倍体积的稀释液1,涡旋混匀,得中间液a,
精密吸取中间液a,加入体积为中间液a体积三分之一的稀释液1,涡旋混匀,即得浓度为7500ng/ml的高浓度质控液,
精密吸取中间液a,加入3倍体积的稀释液1,涡旋混匀,即得浓度为2500ng/ml的中浓度质控液,
精密吸取中间液a,加入19倍体积的稀释液1,涡旋混匀,即得浓度为50ng/ml的低浓度质控液。
本发明的有益保障及效果如下:
本发明提供的尿液中氟代-β-丙氨酸的检测方法只需要尿液预处理、高效液相色谱分离氟代-β-丙氨酸、采用校正曲线法和质谱测量三个步骤,就能实现尿液中氟代-β-丙氨酸的含量检测,并且预处理过程只需简单的提取和离心,色谱分离和质谱检测过程在3min内即可完成,回收率和基质效应满足中国药典要求,因此,本发明的检测方法灵敏度高、特异性强、检测准确,为快速、直接检测尿液中的氟代-β-丙氨酸提供了一种准确可靠的方法,具有一定的临床应用价值。
附图说明
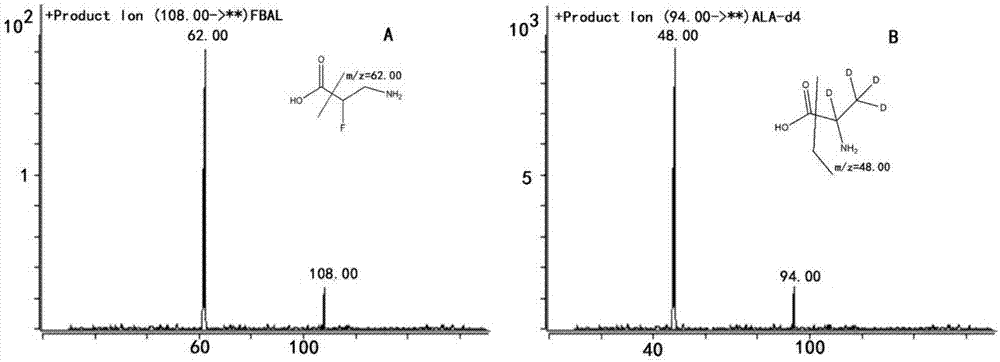
图1为氟代-β-丙氨酸及内标丙氨酸-d4的多重反应监测图,其中,a为氟代-β-丙氨酸多重反应监测图,b为丙氨酸-d4的多重反应监测图。
图2为氟代-β-丙氨酸及内标丙氨酸-d4的专属性色谱图,其中,a为空白尿液样品,b为内标添加尿液样品,c为标准添加尿液样品,d为实测尿液样品。
图3为氟代-β-丙氨酸及内标丙氨酸-d4的残留效应图,其中,a是氟代-β-丙氨酸的最高浓度点色谱图,b为丙氨酸-d4的最高浓度点色谱图,c氟代-β-丙氨酸最高浓度点之后的空白点色谱图,d为丙氨酸-d4最高浓度点之后的空白点色谱图。
图4为本发明实施例中各组大鼠尿液氟代-β-丙氨酸平均累积排泄量。
具体实施方式
为了更加清楚的说明本发明,下面结合实施例来对本发明进行进一步的说明。本领域技术人员应当理解,下面所具体描述的内容是说明性的而非限制性的,不应以此限制本发明的保护范围。
下列实施例中未注明具体条件的实验方法,通常按照常规条件,或按照制造厂商所建议的条件。本发明实施例所用试剂除另有注明,均可以从销售公司获得。
1.实验材料
实验用尿液样本来源于为验证异甘草酸镁注射液对卡培他滨所致大鼠肝损伤的保护作用,所给予卡培他滨及异甘草酸镁注射液后的大鼠尿液。
(1)仪器:agilent1290series超高效液相色谱仪,agilent6460a三重四级杆串联质谱仪(agilent公司);可调移液器(eppendorf公司,0.5~10μl、10~100μl、100~1000μl);电子天平(sartorius公司,cpa255d型,十万分之一);涡旋混合仪(labnet公司,vx-200型);离心机(eppendorf公司,minispinplus型)。
(2)试剂耗材:乙腈(merck公司,分析纯);乙酸铵(天地公司,分析纯);双蒸馏水(屈臣氏公司)。
(3)待测化合物对照品:氟代-β-丙氨酸(大连美仑公司,批号j0530a)。
(4)内标对照品:丙氨酸-d4(torontoresearchchemicals公司,批号a481502)。
(5)药品:卡培他滨片(希罗达),规格0.5g/片(上海罗氏制药公司,批号sh2435)。异甘草酸镁注射液,规格10ml:50mg/支(正大天晴药业集团公司,批号160918113)。谷胱甘肽,规格0.1g/片,(重庆药友制药公司,批号17040900)。
2.检测方法及检测试剂盒
本实施例中的尿液中氟代-β-丙氨酸的检测方法,采用超高效液相色谱-串联质谱进行检测,包括以下步骤:a)对待检尿液样本进行预处理;b)采用超高效液相色谱将预处理后待检尿液样本中的氟代-β-丙氨酸与尿液中的其它成分进行分离;c)采用串联质谱检测氟代-β-丙氨酸的含量,以丙氨酸的同位素化合物为内标,采用校正曲线法计算尿液中氟代-β-丙氨酸的含量。
(1)尿液样本预处理方法
取10μl待测尿液样本,置于1.5ml离心管中,加入90μl提取液(含1μg/ml内标的50%乙腈水溶液),涡旋1min后以14500×g的离心力室温下离心10min,转移80μl上清液于进样小瓶中进行分析。
(2)超高效液相色谱条件
色谱柱:waters公司xbridgehilic柱(3.5μm,2.1mm×100mm);流速为0.35ml/min,柱温为35℃,进样体积为5μl。洗脱液:流动相a为10mmol/l乙酸铵水溶液,流动相b为乙腈,采用梯度洗脱方式进行分离。流动相洗脱参数如下:0min~3min,流动相a为17%~40%,流动相b为83%~60%。
(3)质谱条件
电喷雾电离、正离子解离模式下,采用多重反应监测的质谱扫描模式检测氟代-β-丙氨酸、丙氨酸-d4。毛细管电压为±4000v,喷雾器压力为50psi,碰撞气压力为0.2mpa;干燥气温度为325℃,干燥气流速为10l/min;鞘气温度为350℃,鞘气流速为12l/min。待测化合物氟代-β-丙氨酸的离子对为m/z108→62、f值为75v、ce值为13ev,内标化合物丙氨酸-d4的离子对为m/z94→48、f值为34v、ce值为13ev。
(4)校正曲线的建立
校正曲线包含有9个浓度点,分别为s1、s2、s3、s4、s5、s6、s7、s8、s9。校正曲线的建立方法为:取4μl对照品母液,加入36μl稀释液2,涡旋混匀。再加入360μl稀释液1,涡旋1min混匀,即得校正曲线最高浓度点s9。取90μl的s9,加入30μl稀释液1,涡旋混匀,即得s8;取25μl、50μl的s9,分别加入稀释液1稀释至100μl,涡旋混匀,即得s6、s7;取20μl的s6、s7,分别加入80μl稀释液1,涡旋混匀,即得s4、s5;取10μl的s4、s5,分别加入90μl稀释液1,涡旋混匀,即得s2、s3;取20μl的s3,加入80μl稀释液1,涡旋混匀,即得s1。
取s1、s2、s3、s4、s5、s6、s7、s8、s9各10μl,按照上述预处理方法对上述9个校正曲线浓度点样本进行预处理,再进样测定,以对照品浓度作为x轴,待测化合物与内标化合物的峰面积比值作为y轴,建立校正曲线。
在进行实际尿液样本检测时,将串联质谱测得的待测尿液样本中氟代-β-丙氨酸的峰面积与内标化合物的峰面积比值代入校正曲线中,通过计算即可得出该待测尿液样本中氟代-β-丙氨酸含量。
(5)氟代-β-丙氨酸试剂盒的组成
氟代-β-丙氨酸试剂盒包括洗脱液、对照品母液、稀释液、提取液、质控液,具体见表1。
表1氟代-β-丙氨酸试剂盒
洗脱液的配制:洗脱液a为500ml10mmol/l的乙酸铵水溶液(称取乙酸铵0.385g,溶于500ml双蒸水中即得);洗脱液b为500ml的乙腈。
对照品母液的配制:取氟代-β-丙氨酸约1mg,精密称定质量,加入适量甲醇溶解,得1mg/ml的对照品母液。
稀释液的配制:稀释液有2种,稀释液1为空白尿液10ml,稀释液2为双蒸水10ml。
提取液的配制:取丙氨酸-d4约1mg,精密称定质量,加入适量甲醇溶解,得1mg/ml的内标溶液;精密吸取上述内标溶液10μl,加入50%乙腈溶液定容至1ml,再取该溶液100μl,加入50%乙腈溶液定容至1ml,得1μg/ml的提取液。
质控液的配制:取上述对照品母液100μl,加入双蒸水定容至1ml,即得100μg/ml的对照品溶液。精密吸取上述对照品溶液40μl,加入360μl稀释液1,涡旋混匀,得中间液a;精密吸取90μl上述中间液a,加入30μl稀释液1,涡旋混匀,即得浓度为7500ng/ml的高浓度质控液;精密吸取25μl上述中间液a,加入75μl稀释液1,涡旋混匀,即得浓度为2500ng/ml的中浓度质控液。精密吸取上述对照品溶液20μl,加入180μl稀释液1,涡旋混匀,得中间液b;精密吸取20μl上述中间液b,加入380μl稀释液1,涡旋混匀,即得浓度为50ng/ml的低浓度质控液。
3.方法的建立及优化
(1)提取剂组分的优化
(2)洗脱液组分的优化
(3)重要液相、质谱参数条件的优化
(5)方法的建立
对待测化合物氟代-β-丙氨酸和内标化合物丙氨酸-d4的质谱条件进行优化,使用全扫模式确定离子源极性,然后对f值、ce值进行优化,选择最佳离子对(q1/q3)。然后针对响应,优化包括干燥气、鞘气、喷雾器压力等离子源条件。
获得的最佳离子源条件如下:电喷雾电离、正离子解离模式下,采用多重反应监测的质谱扫描模式;毛细管电压为±4000v,喷雾器压力为50psi,碰撞气压力为0.2mpa;干燥气温度为325℃,干燥气流速为10l/min;鞘气温度为350℃,鞘气流速为12l/min。待测化合物氟代-β-丙氨酸的离子对为m/z108→62、f值为75v、ce值为13ev,内标化合物丙氨酸-d4的离子对为m/z94→48、f值为34v、ce值为13ev。
氟代-β-丙氨酸及丙氨酸-d4的多重反应监测图见图1。图中,a为氟代-β-丙氨酸多重反应监测图,b为丙氨酸-d4的多重反应监测图。
4.方法学验证
(1)专属性
在待测化合物和内标化合物相应的保留时间上杂质的响应不超过化合物最低定量下限响应的20%和内标响应的5%即为合格。氟代-β-丙氨酸及丙氨酸-d4的专属性色谱图见图2。图中,a为空白尿液样品,b为内标添加尿液样品,c为标准添加尿液样品,d为大鼠实测尿液样品。结果表明本方法的专属性符合中国药典规定。
(2)校正曲线
线性回归采用9个线性点的内标校正的峰面积同响应浓度的比值获得,权重系数使用1/x2,最低定量限浓度即为线性的最低点,对于每一个浓度点,回算偏移在±15%之内视为合格,最低定量限浓度在±20%之内视为合格。结果如下:y=1.57x+0.0012,r=0.998,lloq=20ng/ml,线性范围20~10000ng/ml,权重系数1/x2。所有浓度点回算偏移在±15%之内,符合药典要求。
(3)基质效应和提取回收率
基质效应和提取回收率采用高浓度和低浓度(高7500ng/ml,低50ng/ml)的6个不同来源基质进行评价。基质效应为提取后添加样本的化合物响应同浓度一致的水标的化合响应的比值,提取回收率为浓度一致的前添加样本化合物响应同后添加样本化合物浓度响应的比值。结果如下表所示,表明本预处理方法在既定线性范围内提取回收率和基质效应稳定,符合药典要求。见表2。
表2基质效应和提取回收率结果
(4)稳定性
稳定性包括长期稳定性(3月)、短期稳定性(进样器24h)及冻融三次的稳定性。采用高、低两个浓度进行评价并且每次评价均建立校正曲线计算浓度。相对于理论浓度,偏移在±15%之内视为合格。结果如上表所示,结果显示氟代-β-丙氨酸在尿液中3个月,预处理后24h,三次冻融后可保持稳定。
(5)日内日间精密度和准确度
日内日间精密度准确性分别在四个浓度水平评价(最低定量下限浓度、低浓度、中浓度、高浓度),每个浓度水平分别测定5次。随同线性评价三次,至少在两天完成,对于精密度,低浓度、中浓度、高浓度的相对标准偏差(relativestandarddeviation,rsd)不超过15%,最低定量下限浓度的相对标准偏差不超过20%视为合格。对于准确度,低浓度、中浓度、高浓度的相对误差(relativeerror,re)在±15%之内,最低定量下限浓度的相对误差在±20%之内即视为合格。结果如下表所示,表明本方法的日内日间精密度和准确度符合药典要求。见表3。
表3氟代-β-丙氨酸日内日间精密度及准确度结果
(6)残留效应
残留效应的评价采用先进样最高浓度点样本,后进空白样本的形式,重复循环三次,干扰杂质的响应小于最低定量下限待测化合物响应的20%和内标响应的5%即为合格。氟代-β-丙氨酸及丙氨酸-d4的残留效应色谱见图3。图中,a是氟代-β-丙氨酸的最高浓度点色谱图,b为丙氨酸-d4的最高浓度点色谱图,c氟代-β-丙氨酸最高浓度点之后的空白点色谱图,d为丙氨酸-d4最高浓度点之后的空白点色谱图。结果表明本方法中最高浓度的残留符合药典要求。
5.异甘草酸镁注射液对大鼠尿液氟代-β-丙氨酸平均累积排泄量
(1)动物实验设计及采样方法
sd雄性大鼠25只,随机分为5组,每组5只。禁食不禁水8h后,各组大鼠灌胃给予200mg/kg卡培他滨混悬液(1%羧甲基纤维素钠溶液配置)。第1组不给予肝保护剂,第2至第4组静脉给予10、25、40mg/kg异甘草酸镁注射液,第5组灌胃给予1.25g/kg阳性对照药物谷胱甘肽混悬液(1%羧甲基纤维素钠溶液配置)。给药后,大鼠放置于代谢笼内单独饲养,自由进食及饮水。收集每只大鼠0~3h、3~6h、6~12h、12~24h时间段的尿液。测量尿液体积后,置于-80℃冰箱内冷冻保存。共计收集到100例大鼠尿液样本。
(2)尿液样本检测
按照样本前处理方法进行处理提取待测化合物,随后进样分析,并建立随行的校正曲线,将尿液样本检测所的化合物的峰面积同内标峰面积的比值代入校正曲线,计算得出100例样本中氟代-β-丙氨酸的含量,统计每组大鼠24h平均累积排泄量。各组大鼠尿液氟代-β-丙氨酸平均累积排泄量见图4。表明本方法准确测定了大鼠尿液中氟代-β-丙氨酸的排泄量,具有实际可行性及临床应用价值。
以上显示和描述了本发明的基本原理、主要特征和本发明的优点。本行业的技术人员应该了解,本发明不受上述实施例的限制,上述实施例和说明书中描述的只是说明本发明的原理,在不脱离本发明精神和范围的前提下本发明还会有各种变化和改进,这些变化和改进都落入要求保护的本发明范围内。本发明要求保护范围由所附的权利要求书及其等同物界定。
- 还没有人留言评论。精彩留言会获得点赞!