嵌合抗原受体亲和力检测方法与流程
本发明属于细胞治疗领域,具体涉及bcmacar亲和力检测方法。
背景技术:
嵌合抗原受体(chimericantigenreceptor-tcell,car-t)t细胞是指经基因修饰后,能以mhc非限制性方式识别特定目的抗原,并且持续活化扩增的t细胞。2012年国际细胞治疗协会年会中指出生物免疫细胞治疗已经成为手术、放疗、化疗外的第四种治疗肿瘤的手段,并将成为未来肿瘤治疗必选手段。car-t细胞回输治疗是当前肿瘤治疗中最明确有效的免疫治疗形式。大量研究表明,car-t细胞可以有效的识别肿瘤抗原,引起特异性的抗肿瘤免疫应答,显著改善患者的生存状况。
嵌合抗原受体(car)是car-t的核心部件,赋予t细胞hla非依赖的方式识别肿瘤抗原的能力,这使得经过car改造的t细胞相较于天然t细胞表面受体tcr能够识别更广泛的目标。car的基础设计中包括一个肿瘤相关抗原(tumor-associatedantigen,taa)结合区(通常来源于单克隆抗体抗原结合区域的scfv段),一个胞外铰链区,一个跨膜区和一个胞内信号区。目标抗原的选择对于car的特异性、有效性以及基因改造t细胞自身的安全性来讲都是关键的决定因素。
car-t通过与肿瘤抗原的特异性结合来激活活化信号,从而对肿瘤细胞产生靶向杀伤功能。这种特异性的结合依赖于car结构中与抗原特异结合的抗体单链可变区(scfv)。抗人bcmat细胞注射液采用鼠抗人的bcmascfv,其中轻链可变区和重链可变区序列来源于c11d5.3克隆号的bcma抗体。因此,此单克隆号抗体与抗原结合亲和力的强弱是影响bcmacar-t细胞抗肿瘤活性的重要因素。
多发性骨髓瘤(mm)是骨髓恶性浆细胞克隆增殖,以克隆性浆细胞大量增生为特征的恶性肿瘤,导致骨髓造血受抑和溶骨性疾病。尽管应用传统化疗和造血干细胞移植以及靶向性药物治疗骨髓瘤,mm仍然不能完全治愈。
mm起源于骨髓中的浆细胞,而浆细胞是b淋巴细胞发育到最终功能阶段的细胞,因此通常将mm归到b淋巴细胞瘤的范畴。但mm的异常浆细胞几乎不表达cd19,而且大部分b细胞标志蛋白表达量极微,甚至不表达,因此针对mm的car-t治疗需要寻找新靶点。
mm的免疫治疗的一种候选抗原是b细胞成熟抗原(bcellmaturationantigen,bcma)。bcmarna在mm细胞中普遍检测到,多发性骨髓瘤患者的浆细胞表面可检测到bcma蛋白。bcma是肿瘤坏死因子受体(tnfr)超家族的成员,可结合b细胞激活因子(baff)和增殖诱导配体(april)。据报道,在正常细胞中,bcma主要由浆细胞和一部分成熟b细胞表达,而在大部分b细胞以及其它器官上都不表达。因此,抗人bcmat细胞注射液采用针对此bcma抗原特异的car结构,用来靶向识别和消灭表达bcma的细胞,拟用于bcma阳性的复发/难治性多发性骨髓瘤。
抗体亲和力是确定抗体性质的重要参数之一,它表示抗体结合位点和和抗原表位之间的结合牢固程度,常用解离平衡常数kd表示,指达到平衡后,结合半数抗原分子时所需抗体的浓度。抗体与抗原结合的亲和力可为选用不同用途的单抗提供依据,高亲和力的抗体对于定量检测、诊断及疾病的靶向治疗是有用的,它可以提高阳性检出率或提高治疗性抗体的药效;而亲和力相当的抗体用于亲和纯化,亲和力过低不易吸附,过高又不易洗脱。因此,要根据应用的目的选择不同亲和力的抗体,就需要先对抗体亲和力进行检测。
bcmacar的car结构用到了c11d5.3scfv,那么c11d5.3scfv对靶抗原亲和力高,bcmacar就会对靶抗原有较高的亲和力。本发明建立了bcmacar对靶抗原亲和力的检测方法。实验方法基于流式细胞仪进行相关项目检测。
技术实现要素:
本发明的目的在于提供一种检测bcmacar亲和力的方法,具有安全、灵敏度高、重复性好、检测结果稳定可靠等优点。
本发明解决其技术问题所采用的技术方案是:
(1)bcmaigg与bcma阳性细胞系结合亲和力
用本公司制备表达并纯化的anti-humanbcmaigg(克隆号:c11d5.3),设置起始浓度为100ug/ml,然后按1:3梯度稀释7个点,分别与3×105的人源bcma阳性细胞系mm.1s和h929共孵育,再用流式抗体pe-antihumanigg-fc来检测与靶细胞结合的bcmaigg,通过流式检测其荧光强度并判断结合亲和力。
(2)bcmaigg与bcma结合亲和力elisa检测
试验首先采用2μg/ml的humanbcma蛋白包被elisa板,1h后洗去游离蛋白,然后用本公司自制纯化的anti-humanbcmaigg2ug/ml1:3稀释8个浓度梯度,37℃孵育1h,洗去多余抗体,再依次用二抗biotingoatantimousef(ab)2和三抗streptavidin-hrp分别37℃孵育1h,最后显色,于酶标仪上读取od450/620数值。
附图说明
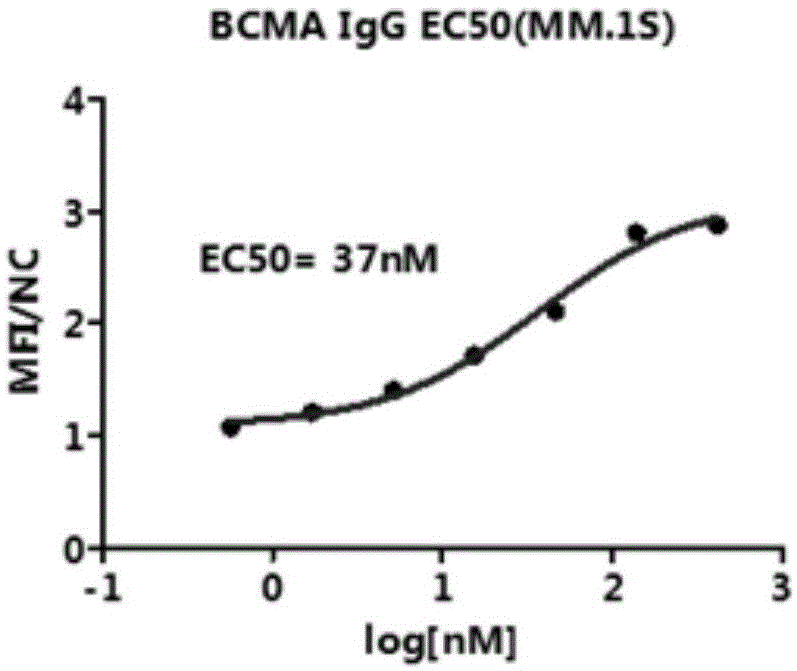
图1mm.1s与bcmaigg结合ec50结果
图2h929与bcmaigg结合ec50结果
图3elisa检测bcmaigg结合ec50结果
具体实施方式
本发明通过参考以下实验实施例进一步详细地进行描述。这些实施例仅出于说明性的目的提供,并不意欲为限制性的,除非另有规定。因此,本发明决不应被解释为限于以下实施例,而是应被解释为包括由于本文提供的教导变得显而易见的任何和全部的变化。实施例中所用的方法和试剂,除非另有说明,否则为本领域常规的方法和试剂。
实施例1:bcmaigg与bcma阳性细胞系结合亲和力
具体步骤为:用本公司制备表达并纯化的anti-humanbcmaigg(克隆号:c11d5.3),设置起始浓度为100ug/ml,然后按1:3梯度稀释7个点,分别与3×105的人源bcma阳性细胞系mm.1s和h929共孵育(具体分组参见表1),再用流式抗体pe-antihumanigg-fc来检测与靶细胞结合的bcmaigg,通过流式检测其荧光强度并判断结合亲和力。
表1bcmaigg与bcma阳性细胞系结合亲和力试验分组
实施例结果见图1、图2。其中,mm.1s结合bcmaigg亲和力ec50为37nm,h929达到57nm。
实施例2:bcmaigg与bcma结合亲和力elisa检测
具体步骤为:试验首先采用2μg/ml的humanbcma蛋白包被elisa板,1h后洗去游离蛋白,然后用本公司自制纯化的anti-humanbcmaigg2ug/ml1:3稀释8个浓度梯度,37℃孵育1h,洗去多余抗体,再依次用二抗biotingoatantimousef(ab)2和三抗streptavidin-hrp分别37℃孵育1h,最后显色,于酶标仪上读取od450/620数值。
本实施例结果见图1、图2。采用过量的humanbcma-fc蛋白包板,然后用起始浓度为2ug/ml,1:3梯度稀释8个浓度的anti-humanbcmaigg孵育,用elisa方式检测其结合亲和力,其ec50值为1.2nm。
- 还没有人留言评论。精彩留言会获得点赞!