一种透明质酸中邻苯二甲酸酯塑化剂残留的检测方法与流程
本发明涉及塑化剂的检测领域,具体涉及一种检测透明质酸中的邻苯二甲酸酯塑化剂残留的方法。
背景技术:
透明质酸(hyaluronicacid,简称ha)又名玻璃酸,是由(1-3)-2-乙酰氨基-2-脱氧-d-葡萄糖(1-4)-d-d-葡萄醛酸双糖重复单位所组成的高分子量的直链粘多糖。1934年由meyer等人从牛玻璃球眼中首次提取获得。
透明质酸以其独特的分子结构和理化性质在机体内显示出多种重要的生理功能,如润滑关节,调节血管壁的通透性,调节蛋白质,水电解质扩散及运转,促进创伤愈合等。尤为重要的是,透明质酸具有特殊的保水作用,是目前发现的自然界中保湿性最好的物质,被称为理想的天然保湿因子,由于ha具有良好的保湿性、粘弹性、渗透性和延展性,同时无任何免疫原性和毒性,被广泛应用于化妆品、食品、医药和临床治疗等行业领域。
透明质酸作为天然的保湿因子,早已被广泛应用到化妆品、医药等领域。近几年来,随着人们健康消费观念的形成,如何吃出健康与美丽成为人们关注的焦点,透明质酸在食品中的应用也越来越广泛,比如作为关节营养的膳食补充产品,以及作为补充水分、改善皮肤弹性的日常美容保健食品:透明质酸饮料、口服液、美容胶囊、酸奶、果冻、口香糖、绿茶等。若不能准确检测出透明质酸生产过程中带入的塑化剂含量,导致透明质酸塑化剂含量超标、纯度降低,长期使用塑化剂超标的透明质酸化妆品,或长期食用塑化剂超标的透明质酸产品,都会对健康造成很大的危害。
在应用透明质酸时为了良好地表现其特性以及对人体的安全性,需要保证其纯度和质量。由于透明质酸的生产原料以及生产过程中接触的容器、管线例如塑料软管等,不可避免会含有杂质。为了保证透明质酸中的杂质、特别是塑化剂的含量在规定范围以下,需要有效地检测塑化剂的方法。
塑化剂(plasticizer)是一种增加材料的柔软性或是材料液化的添加剂。其中最常见的塑化剂是邻苯二甲酸酯类物质(phthalateesters,paes),是邻苯二甲酸的酯化衍生物。邻苯二甲酸酯塑化剂是具些许芳香气味或无气味的无色液体,中等黏度、高稳定性、低挥发性、成本低廉、低水溶解度,但易溶于多数有机溶剂中。邻苯二甲酸酯类在日常及工业上被广泛使用,以邻苯二甲酸二(2-乙基己基)酯(dehp)为最大宗,占塑化剂产量的四分之三,其次是邻苯二甲酸二丁酯(dbp)。邻苯二甲酸酯类塑化剂被归类为疑似环境荷尔蒙,其生物毒性主要属雌激素与抗雄激素活性,会造成内分泌失调,阻害生物体生殖机能,包括生殖率降低、流产、天生缺陷、异常的精子数、睾丸损害,还会引发恶性肿瘤、造成畸形儿。
目前,有关paes的检测方法主要有高效液相色谱法(hplc)、气相色谱法(gc)、液质联用法(hplc-ms)和气质联用法(gc-ms)。例如在专利文献1中公开了一种食用油中邻苯二甲酸酯类塑化剂的检测方法,其中使用的是气相色谱-质谱联用检测。另外,在国家标准gb/t21911-2008“食品中邻苯二甲酸酯的测定”中,也公开了一种检测塑化剂残留的gc-ms法,其中,在试样处理中,对于不含油脂试样,是将5.0ml液体试样,加入正己烷2.0ml萃取后,取上层清液进行gc-ms分析,另外对于固体或半固体试样而言,是将5.00g试样加约50ml水进行检测。对于含油脂试样,是将油脂试样0.50g,用体积比为乙酸乙酯:环己烷10.0ml溶解处理后进行gc-ms分析。
现有技术文献
专利文献
专利文献1:cn104698109a
技术实现要素:
如果按照国家标准gb/t21911-2008中规定的不含油脂的固体样品配制方法,即称样量为5.0g,溶于50ml水,由于透明质酸属于大分子粘多糖类物质,将其直接溶解配置检测样品时将得到凝胶状物质,无法进行过滤和萃取。若调整称样量以得到粘度适当的溶液,则方法的检测限无法满足要求(由0.05mg/kg降至0.5mg/kg或更低)。因此,上述邻苯二甲酸酯类塑化剂的检测方法并不能有效地用于透明质酸中的塑化剂的检测。
为了解决上述技术问题,本发明人根据透明质酸和邻苯二甲酸塑化剂的溶解特性,开发了一种适合检测透明质酸中塑化剂的方法。
本发明专利采用的技术方案是:
1.一种透明质酸中邻苯二甲酸酯塑化剂残留的检测方法,其包括:
制样步骤,其中制样步骤包括:
(1)利用无水乙醇和塑化剂的标准品,经过过滤,制备塑化剂的标准品溶液,
(2)利用无水乙醇提取透明质酸中的塑化剂,进行过滤,制作供试品溶液,
(3)无水乙醇经过滤作为空白溶液;和
检测步骤,其中检测步骤包括:
使用高效液相色谱检测所得到的供试品溶液、标准品溶液和空白溶液,使用外标法确定塑化剂的残留量。
2.根据项1所述的方法,其中,所述邻苯二甲酸酯塑化剂为邻苯二甲酸二丁酯(dbp)。
3.根据项1或2所述的方法,其中,所述制样步骤中提取方法为对每10g样品用50~100ml的无水乙醇提取,即无水乙醇的体积/样品重量=5~10/1的比例来利用无水乙醇提取样品。
4.根据项1~3中任一项所述的方法,其中,所述检测步骤中,使用外标法对塑化剂的残留量进行检测。
5.根据项1~4中任一项所述的方法,其中,所述检测步骤中,采用的色谱柱为十八烷基硅烷键合硅胶色谱柱。
6.根据项5所述的方法,其中,所述硅胶液相色谱柱为teckmatec18或capcellc18。
7.根据项1~6中任一项所述的方法,其中,所述检测步骤中,采用的流动相为体积比为90:10~80:20的甲醇:水的溶液,优选为90:10(甲醇/水)。
8.根据项1~7中任一项所述的方法,其中,所述检测步骤中,采用的色谱条件为:流速0.5~1.0ml/min,优选为0.8ml/min,柱温30~60℃,优选为35℃,检测波长220~235nm,优选为228nm,进样量20~100微升,优选为20微升。
9、根据项1~8中任一项所述的方法,邻苯二甲酸二丁酯(dbp)的检测限小于等于0.06mg/kg。
发明的效果
本发明的透明质酸中塑化剂的检测方法简便易行,能够用于检测透明质酸中的邻苯二甲酸酯塑化剂、特别是邻苯二甲酸二丁酯(dbp)的残留。
本发明的检测方法采用无水乙醇直接提取透明质酸中的塑化剂,避免了透明质酸的溶解造成溶液粘度过高,又可将透明质酸中的塑化剂充分提取,经浓缩后直接经hplc检测,不需使用质谱,降低了检测成本,且该方法检测结果与国标一致,准确度较高,检测限也可达到0.06mg/kg。
附图说明
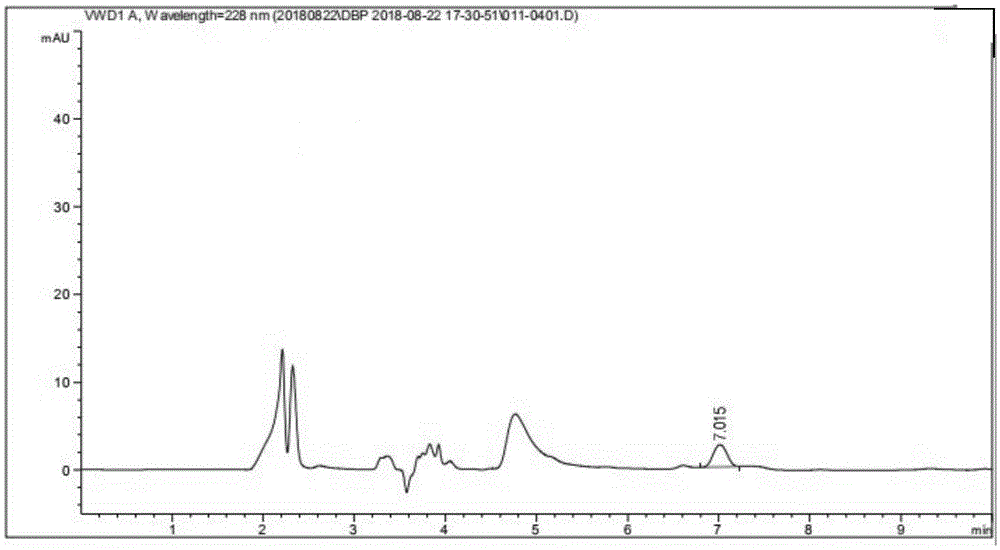
图1为实施例1中的供试品的色谱图。
图2为实施例1中的空白色谱图。
图3为实施例1中的对照品(dbp)色谱图。
具体实施方式
以下将对本发明做以详细说明。
根据本发明的一个方面,提供一种透明质酸中邻苯二甲酸酯塑化剂的检测方法,其包括:制样步骤,(1)利用无水乙醇和塑化剂的标准品,经过过滤,制备塑化剂的标准品溶液,(2)利用无水乙醇提取透明质酸中的塑化剂,进行过滤、浓缩,制作供试品溶液,(3)无水乙醇经过滤作为空白溶液;和检测步骤,使用高效液相色谱(highperformanceliquidchromatography\hplc)检测所得到的供试品溶液、标准品溶液和空白溶液,使用外标法确定塑化剂的残留量。
本发明人发现如果用国家标准gb/t21911-2008规定的塑化剂残留(气相色谱-质谱联用)测定方法来检测透明质酸中的塑化剂含量,会出现将称样量溶解将得到凝胶状物质,无法进行过滤及萃取。若调整称样量以得到粘度适当的溶液,则方法的检测限无法满足要求。而通过本发明的透明质酸中塑化剂的检测方法,由于采用无水乙醇直接提取固体粉末中的塑化剂,避免了透明质酸的溶解造成溶液粘度过高,又可将透明质酸中的塑化剂充分提取,经浓缩后直接经hplc检测,不需使用质谱,降低了检测成本。
在本发明的一个实施方式中,上述塑化剂为邻苯二甲酸二丁酯塑化剂(dbp)。在本发明的一个实施方式中,上述制样步骤中提取方法为对每10g样品用50~100ml的无水乙醇提取,即无水乙醇的体积/样品重量=5~10/1的比例来利用无水乙醇提取样品,例如如果针对100g的样品,可以采用500~1000ml的无水乙醇来提取,具体可以用乙醇浸泡并超声。其中,“无水乙醇”是指乙醇(酒精)含有为99.5%以上的乙醇。超声的时间例如为10min-1h,优选为15min-30min,特别优选为20min左右。通过使用无水乙醇而不是其他有机溶剂来提取透明质酸中的塑化剂,能够将透明质酸样品中的塑化剂更充分地提取出来,使得检测更加准确。而且避免对透明质酸本身的影响。
在本发明中,“检测限”是指可以检测到的极限浓度,即能够检测到的最低浓度,即在本发明中,如果说检测限为0.06mg/kg,即可以检测到低至0.06mg/kg的邻苯二甲酸二丁酯(dbp),即在体系中即使仅存在0.06mg/kg的邻苯二甲酸二丁酯(dbp)也可以检测到。
在本发明的一个实施方式中,在上述检测步骤中,使用外标法对塑化剂的残留量进行检测。“外标法”与内标法相对,是指添加一定量的标准品(对照品)于空白检材中制成对照样品,与未知检材平行地进行样品处理并检测,根据对照样品响应值与其中所添加标准品(对照品)浓度的函数关系推算未知检材中被测组分浓度的定量方法。本发明中采用的外标法没有限定,例如可以采用外标一点法。
其中,外标一点法是用一种浓度的对照品溶液与待测样品溶液i组分进行对比,将对照品与待测品多次在相同条件下进样,测得峰面积的平均值。可以通过下式(一)来计算待测样品溶液i的含量:
wi=ai(wi)s/(ai)s式(一)
式中,wi、ai分别是样品溶液进样体积中所含i组分的重量及色谱检测时获得的峰面积,(wi)s、(ai)s分别是对照品溶液中所含i组分的重量及色谱检测时获得的峰面积。
在本发明的一个实施方式中,在上述检测步骤中,采用的色谱柱为十八烷基硅烷键合硅胶色谱柱。hplc的固定相有以下几种:(1)硅胶表面键合或涂渍各种聚合物;(2)其他氧化物表面涂渍聚合物;(3)无孔单分散填料;(4)有机高聚填料;(5)灌注色谱填料;和(6)手性固定相填料。流动相是影响液相色谱的关键因素,高效液相色谱法中的流动相主要用水性溶剂、有机溶剂或它们的混合液。本发明的高效液相色谱法中采用的色谱柱只要能够检测邻苯二甲酸二丁酯(dbp)塑化剂的色谱柱即可,没有限制,例如,可以为teckmatec18或capcellc18色谱柱。
在本发明的一个实施方式中,在上述检测步骤中,采用的流动相为体积比为90:10~80:20的甲醇:水的溶液。本发明的高效液相色谱法中采用流动相还可以采用体积比为90:10的乙腈:水的溶液。
在本发明的一个实施方式中,在上述检测步骤中,采用的色谱条件为:流速0.5~1.0ml/min,优选为0.8ml/min,柱温30~60℃,优选为35℃,检测波长220~235nm,优选为228nm,进样量20~100微升,优选为20微升。通过在该色谱条件下,检测透明质酸中的邻苯二甲酸二丁酯(dbp)塑化剂,能够更加准确,其检测限小于等于0.06mg/kg,优选不高于0.05mg/kg。
利用本发明的方法检测透明质酸中残留的邻苯二甲酸酯塑化剂,与现有技术中的方法相比,能够将检测限大大降低,由此可以有效地实现对于透明质酸中可能残留的塑化剂成分进行严格地监控,从而杜绝透明质酸中塑化剂的残留,提高作为产物的透明质酸的质量。
实施例
以下利用实施例对本发明做以详细说明。然而应当理解,可以以各种形式实现本发明而不应被这里阐述的实施例所限制。相反,提供这些实施例是为了能够更透彻地理解本发明,并且能够将本发明的范围完整的传达给本领域的技术人员。在本发明中列举的数值范围均包括该数值范围的两个端点的数据,也包括该数值范围中具体的每一个数值,并且该数值可以与端点任意组合组成新的小范围。
仪器试剂
安捷伦1260液相色谱仪分析天平:梅特勒托利多al104
甲醇(色谱纯)、超纯水、无水乙醇(色谱纯)
dbp对照品(中检所)
实施例1
色谱条件
色谱柱:teckmatec18,4.6*250mm
流动相:甲醇:水=90:10
流速:0.8ml/min
柱温:35℃
检测波长:228nm
进样量:20微升
方法
对照品溶液:精密称取dbp对照品10mg至100ml容量瓶中,无水乙醇稀释至刻度,混匀,将上述溶液稀释100ml,过滤得到对照品溶液。
供试品溶液:称含有0.3mg/kgdbp的透明质酸取供试品10g至50ml容量瓶中,加无水乙醇适量浸泡,超声20min,定容,有机滤膜过滤,取滤液20ml置于培养皿中,氮气吹干并用无水乙醇定容到2ml容量瓶中,得到供试品溶液。
空白溶液:无水乙醇经有机膜过滤作为空白溶液。
取空白溶液、对照品溶液、供试品溶液进样,外标法计算供试品中dbp含量。
表1实施例1的检测结果
实施例2
将实施例1中的供试品溶液改变为0.05mg/kg,其他条件与实施例1相同,测定供试品溶液中透明质酸钠中dbp的含量。
表2实施例2的检测结果
实施例3
将实施例1中的供试品溶液改变为0.1mg/kg,其他条件与实施例1相同,测定供试品溶液中透明质酸钠中dbp的含量。
表3实施例3的检测结果
实施例4
将实施例1中的色谱的色谱柱改变为capcellc18,色谱条件与实施例1相同,测定供试品溶液中透明质酸钠中dbp的含量。
表4实施例4的检测结果
实施例5
将实施例1中的色谱的流动相改变为体积比为90:10的乙腈:水的溶液,其他条件与实施例1相同,测定供试品溶液中透明质酸钠中dbp的含量。
表5实施例5的检测结果
实施例6
将实施例1中的色谱的流速改变为1.0ml/min,将进样量改为50μl,其他条件与实施例1相同,测定供试品溶液中透明质酸钠中dbp的含量。
表6实施例6的检测结果
实施例7
将实施例1中的色谱的流速改变为0.5ml/min,将柱温改成30℃,其他条件与实施例1相同,测定供试品溶液中透明质酸钠中dbp的含量。
表7实施例7的检测结果
实施例8
将实施例1中的色谱的流动相改为体积比为80:20的甲醇:水的溶液,其他条件与实施例1相同,测定供试品溶液中透明质酸钠中dbp的含量。
表8实施例8的检测结果
实施例9
将实施例1中的色谱的柱温改变为60℃,其他条件与实施例1相同,测定供试品溶液中透明质酸钠中dbp的含量。
表9实施例9的检测结果
实施例10
将实施例1中的色谱的检测波长改变为235nm,将进样量改为100μl,其他条件与实施例1相同,测定供试品溶液中透明质酸钠中dbp的含量。
表10实施例10的检测结果
比较例1
将实施例1中的无水乙醇替换成丙酮,其他条件与实施例1相同,尝试测定供试品溶液中透明质酸钠中dbp的含量。
表11比较例1的检测结果
比较例2
将实施例1中的无水乙醇替换成95%浓度的乙醇,其他条件与实施例1相同,测定供试品溶液中透明质酸钠中dbp的含量。
表12比较例2的检测结果
比较例3
将实施例1中的无水乙醇替换成甲醇,其他条件与实施例1相同,测定供试品溶液中透明质酸钠中dbp的含量。
表13比较例3的检测结果
比较例4
将实施例1中的流动相替换成70:30的甲醇
表14比较例4的检测结果
在此条件下dbp不能出峰,因此未能取得检测结果。
比较例5
将实施例1中的柱温改变成65℃,其他条件与实施例1相同,测定供试品溶液中透明质酸钠中dbp的含量。
表15比较例5的检测结果
比较例6
将实施例1中的流速改变成1.5ml/min,其他条件与实施例1相同,测定供试品溶液中透明质酸钠中dbp的含量。
表16比较例6的检测结果
比较例7
使用eclipseplusc18色谱柱,其余与实施例1的相同,测定供试品溶液中透明质酸钠中dbp的含量。
表17比较例7的检测结果
尽管对本发明的实施方案和具体实施例进行了描述,但本发明并不局限于上述的具体实施方案和应用领域,上述的具体实施方案仅仅是示意性的、指导性的,而不是限制性的。本领域的普通技术人员在本说明书的启示下和在不脱离本发明权利要求所保护的范围的情况下,还可以做出很多种的形式,这些均属于本发明保护之列。
- 还没有人留言评论。精彩留言会获得点赞!