一种快速定量检测BNP的微流控荧光免疫芯片的制作方法
本发明涉及医疗诊断设备,特别是一种快速定量检测bnp的微流控荧光免疫芯片。
背景技术:
脑利尿钠肽(brainnatriureticpeptide,bnp),又称b型利钠肽,具有32个氨基酸,分子量为4千道尔顿(4kda)的氨基酸序列。当心室容积扩张和压力负荷增加时,心室肌细胞合成并分泌由108个氨基酸分子形成的bnp的前体,即前体bnp(pro-bnp),其后被水解成,形成无活性的带有氮末端的76个氨基酸(nt-probnp),和有活性的32-氨基酸,即bnp。
bnp主要参与尿钠肽系统功能,包括调节血压和体液平衡(bonow,r.o.,circulation93:1946-1950,1996)。相关试验已经证实,人类的血清/血浆/全血中,可以检测到nt-pro-bnp,bnp,和bnp前体以及它们的一些混合片段(tateyamaetah,biochem.biophys.res.commun.185:760-7,1992;huntetah,biochem.biophys.res.commun.214:1175-83,1995)。含有108个氨基酸的pro-bnp序列如下。其中pro-bnp和bnp的第一位置的2个残基可以通过水解或蛋白水解去掉,从bnp的前体(pro-bnp)生成bnp3-108分子,从nt-pro-bnp生成bnp3-76分子,从bnp生成bnp79-108分子。
心肌细胞分泌的pro-bnp,含有108个氨基酸的序列如下,下画线部分为有活性的bnp(bnp77-108)序列:
hplgspgsasdletsglqeqrnhlqgklselqveqtsleplqesprptgv50wksrevategirghrkmvlytlraprspkmvqgsgcfgrkmdrissssgl100gckvlrrh108
pro-bnp(bnp1-108)是由更大的前体pre-pro-bnp形成,该前体的序列如下(“前体”的特殊序列为粗体字母表示):
免疫检测和诊断相关疾病,可以通过构建并产生这些序列的特异性抗体,从而特异性结合上述不同bnp序列的多肽,继而确认并定量检测bnp的浓度。测定bnp的临床意义主要有:急性呼吸困难的鉴别诊断,心源性猝死预测,心力衰竭病人的危险分层及监测心力衰竭的治疗,同时,可以提示心力衰竭的预后。在2001年修订的欧洲心脏病学会(esc)心衰诊疗指南中,已经把脑钠肽作为心衰诊断的工具。2005年欧洲和美国心衰诊疗指南,都进一步肯定了脑钠肽在心衰诊断中的作用,可以作为一个更好的预示心衰状况的指标。我国2007年《慢性心力衰竭诊断治疗指南》和2010年《急性性心力衰竭诊断治疗指南》也推荐将bnp用于心衰的诊断和预后判断。
目前市场上测定血清/血浆/全血中的bnp方法,多用酶联免疫吸附法、放射免疫分析法、电化学发光法、免疫比浊法、荧光免疫法及胶体金免疫层析法等。专利cn101819208a公开了一种测定血清中脑钠肽的试剂盒,该试剂盒采用了纳米微球免疫比浊法,通过加入纳米微球标记抗体等不同试剂,形成不溶性的抗原-抗体的复合物,产生浊度,从而实现了脑钠肽的高灵敏检测。专利cn204188626u公开了一种b型利钠肽免疫层析半定量检测试纸,该方法通过参比线的设置以及对划线抗体含量的精确控制,采用胶体金作为标记物,实现对bnp浓度的半定量检测。专利cn104569429a公开了一种快速定量检测脑钠肽的荧光免疫方法,该方法采用均相荧光免疫检测法,实现对抗原bnp的定量检测。cn105021829a公开了一种定量检测b型钠尿肽的elisa试剂盒,该方法将纳米免疫磁珠分离技术与免疫荧光检测技术相结合,免疫磁珠和双抗体夹心荧光免疫法,对bnp进行了定量检测。但酶联免疫检测法操作复杂,检测耗时长;放射免疫分析法,核素污染;电化学发光法对专业技术要求高,虽具有准确、灵敏度高、特异性强等优点,但其所用仪器价格昂贵,不能快速提供检查结果。胶体金免疫层析法具有操作简便、检测快速,标本用量少,价格便宜的优势,但是当待测物质含量较低,通过肉眼来判断容易出现误判,灵敏度较低,同时,只能实现半定量的检测。荧光免疫层析法大多数采用荧光素或量子点等物质作为发光源,虽然有较高的线性范围,但受背景信号的干扰,本底值较高,不能够保证低端灵敏度,同时,重复性较低。
微流控技术(microfluidics)是把生物、化学、医学分析过程的样品制备、反应、分离、检测等基本操作单元集成到一块微米尺度的芯片上,自动完成分析全过程。由于它在生物、化学、医学等领域的巨大潜力,已经发展成为一个生物、化学、医学、流体、电子、材料、机械等学科交叉的崭新研究领域。微流控芯片,是微流控技术(microfluidics)实现的主要平台,有着体积轻巧、使用样品及试剂量少,且反应速度快、可大量平行处理及可即用即弃等优点。随着芯片微加工技术的快速发展,微流控技术得到了广泛的应用。美国专利us005458852a介绍了一种微流控芯片,该芯片包括检测装置、检测系统和流量控制单元等设备组件,涵盖目标配体结合区域,实现了液体流动控制与时间控制、反应孵化、分离清洗和检测等步骤,实现了传统中免疫层析试纸条的所有功能。美国专利us20110243795al公开了一种没有外部电源控制的微流控芯片,该芯片通过不同微结构区域,预处理环节、反应通道、清洗环节,来控制样品与缓冲液的加样时间差,保证了待测样品的重复性和稳定性。中国专利us771989b2阐述了一种基于特定控制阀控制液体流动的微流控芯片,该芯片采用免疫荧光检测法,通过不同功能区实现抗体包被、荧光抗体固定、抗原的检测与分析,应用于血清/血浆/尿液等样品中生物标志物的检测。中国专利cn105259162a公开了一种定量检测全血中脑钠肽的磁微粒化学发光微流控芯片,实现对全血样品中bnp的定量检测,但由于结构上的问题,其使用并不尽人意。
针对现有bnp检测设备的不足和缺陷,开发快速、准确、稳定性高、灵敏度高的bnp定量检测设备,具有巨大发展潜力和应用前景。微流控芯片技术能够实现样品制备、反应、分离、检测等基本操作单元集成于一块微米尺度的芯片,同时,微通道形成的网络,能够贯穿整个系统,具有便携、低能耗、易于制作等优点,易于满足生命科学对生物样品进行低剂量、更高效、高灵敏、快速分离分析的需求,有望为即时诊断和家庭医疗等领域提供新的快速诊断设备。
技术实现要素:
针对上述情况,为克服现有技术之缺陷,本发明之目的就是提供一种快速定量检测bnp的微流控荧光免疫芯片,可有效解决灵敏度低、重复性差、易受外界环境干扰,以及现有配套仪器昂贵、检测时间长的问题。
本发明解决的技术方案是,一种快速定量检测bnp的微流控荧光免疫芯片,包括底板、顶板、样品加样区、微栅反应腔、识别反应区、废液室和血细胞过滤区,所述的底板为空心凹槽长方形,顶板置于底板凹槽的正上方,构成底板和顶板的密封结构,顶板的上平面有样品加样口和负压接口,底板的凹槽内经回形管装有串接在一起的样品加样区、血细胞过滤区、微栅反应腔、时间阀、识别反应区和废液池,血细胞过滤区上装有血细胞滤膜,样品加样口正对底板样品凹槽内的样品加样区,回形管的负压端接负压接口,微栅反应腔预封装有bnp检测抗体和质控抗体,构成样品与荧光标记的bnp单克隆抗体混合反应区;识别反应区预封装bnp捕获抗体和质控抗体;样品加样区中的样品靠自虹吸作用移动或采用负压接口连接控制泵进行移动;
所述的bnp抗体的制备方法包括以下步骤:
(1)、荧光微球的活化、洗涤,将荧光微球表面修饰基团活化,取直径为200nm荧光微球,加入缓冲液离心,弃上清,沉淀用洗涤缓冲液重复洗涤3次;将末次沉淀重悬于所述洗涤缓冲液中,使荧光微球的质量体积比终浓度为1%,所述洗涤缓冲液选自pbs缓冲液和mes缓冲液中的一种:
(2)、bnp抗体偶联荧光微球,取1ml活化洗涤后的200nm胶乳溶液,加入抗bnp抗体,使抗bnp抗体终浓度为1mg/ml;混匀后,置4度,摇床以220rpm转速包被8h;用pbs缓冲液洗涤未与荧光微球结合的抗bnp抗体,重复3次;封闭:将洗涤后的抗bnp抗体的荧光微球溶于包含所述保护剂的缓冲液中,使所述荧光微球的质量体积比终浓度为0.1-0.14%;
(3)、抗bnp抗体和荧光微球结合后封闭,将所述荧光微球与所述抗bnp抗体混合物,加入bsa0.3%,室温下反应2h,离心,除去其中少量的沉淀物;清洗,将形成的荧光微球-抗bnp抗体复合物溶液离心,弃上清,加入磷酸盐缓冲液重复清洗3次;将末次沉淀溶于含所述保护剂和防腐剂的缓冲液中,使荧光微球质量体积比终浓度为0.04%-0.14%。
本发明结构简单,新颖独特,易生产制备,使用方便,准确率高,节能环保,经济和社会效益显著。
附图说明
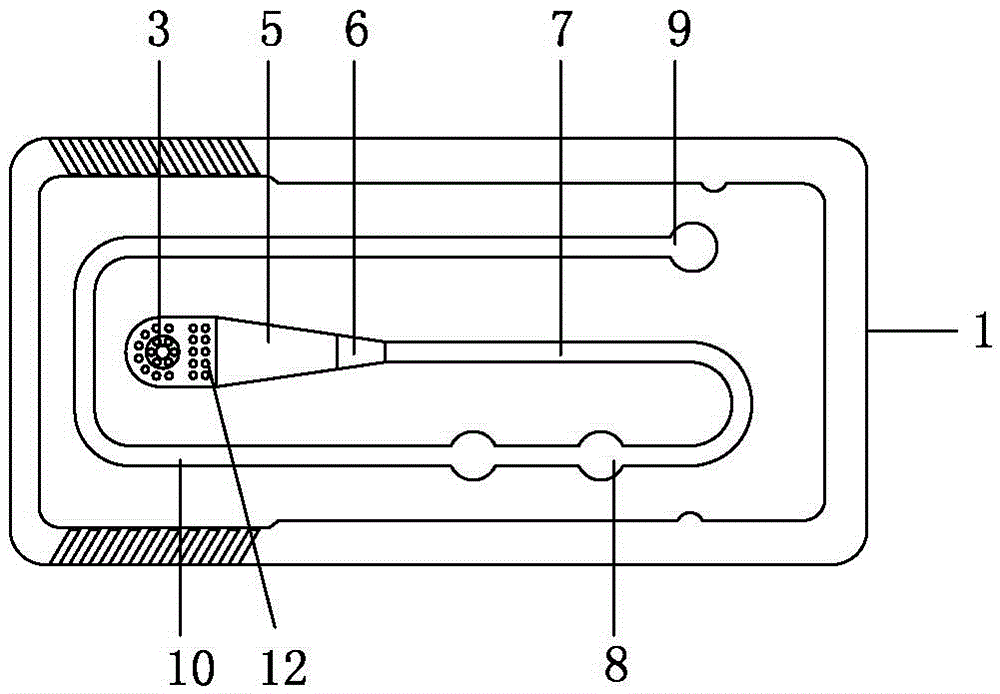
图1为本发明的结构主视图。
图2为本发明的底板部分结构主视图。
图3为本发明bnp微流控免疫芯片检测原理图。
图4为本发明bnp检测标准曲线图。
具体实施方式
以下结合附图和具体情况对本发明的具体实施方式作详细说明。
由图1、图2所示,本发明一种快速定量检测bnp的微流控荧光免疫芯片,包括底板、顶板、样品加样区、微栅反应腔、识别反应区、废液室和血细胞过滤区,所述的底板1为空心凹槽长方形,顶板2置于底板凹槽的正上方,构成底板和顶板的密封结构,顶板的上平面有样品加样口11和负压接口9,底板的凹槽内经回形管10装有串接在一起的样品加样区3、血细胞过滤区12、微栅反应腔5、时间阀6、识别反应区7和废液池8,血细胞过滤区12上装有血细胞滤膜4,样品加样口11正对底板样品凹槽内的样品加样区3,回形管10的负压端接负压接口9,微栅反应腔5预封装有bnp检测抗体和质控抗体,构成样品与荧光标记的bnp单克隆抗体混合反应区;识别反应区7预封装bnp捕获抗体和质控抗体;样品加样区3中的样品靠自虹吸作用移动或采用负压接口连接控制泵进行移动;
所述的bnp抗体的制备方法包括以下步骤:
(1)、荧光微球的活化、洗涤,将荧光微球表面修饰基团活化,取直径为200nm荧光微球,加入缓冲液离心,弃上清,沉淀用洗涤缓冲液重复洗涤3次;将末次沉淀重悬于所述洗涤缓冲液中,使荧光微球的质量体积比终浓度为1%,所述洗涤缓冲液选自pbs缓冲液和mes缓冲液中的一种:
(2)、bnp抗体偶联荧光微球,取1ml活化洗涤后的200nm胶乳溶液,加入抗bnp抗体,使抗bnp抗体终浓度为1mg/ml;混匀后,置4度,摇床以220rpm转速包被8h;用pbs缓冲液洗涤未与荧光微球结合的抗bnp抗体,重复3次;封闭:将洗涤后的抗bnp抗体的荧光微球溶于包含所述保护剂的缓冲液中,使所述荧光微球的质量体积比终浓度为0.1-0.14%;
(3)、抗bnp抗体和荧光微球结合后封闭,将所述荧光微球与所述抗bnp抗体混合物,加入bsa0.3%,室温下反应2h,离心,除去其中少量的沉淀物;清洗,将形成的荧光微球-抗bnp抗体复合物溶液离心,弃上清,加入磷酸盐缓冲液重复清洗3次;将末次沉淀溶于含所述保护剂和防腐剂的缓冲液中,使荧光微球质量体积比终浓度为0.04%-0.14%。
为了保证使用效果和使用方便,所述的顶板上开有排气孔;所述的样品加样区上开有圆形或方形的加样孔11(图中未标示);
所述底板为长方形的凹槽状,具有不同功能微结构,底板和顶板采用胶粘、机械固定、超声封合密封固定在一起;
所述微栅反应腔,包括有等间距排列的微结构,所述微结构为梯形、三角形、半圆形的一种;
所述时间阀包括阻滞栏结构形成的导流槽,每个阻滞栏呈下宽上窄的梯形、阶梯形或三角形;
所述识别反应区,包括有等间距排列的微结构,所述微结构为梯形、三角形、半圆形等;
所述识别反应区包括至少一个以上的检测位点。
本发明所述的微流控芯片,主要应用于血浆、全血、血清、尿液、脊髓液、羊膜水的检测等。
本发明所述的微流控芯片的底板和顶板均为pdms、ps、pc、pmma等高分子材料制成的长方形,但不局限于上述材料,优选为ps、pc、pmma,更优选为ps。
本发明在生产时,加工主要采用机械加工法、注塑法、模具法、光刻加工法等,优选为注塑法、模具法、光刻加工法,更优选为光刻加工法。
所述配对抗体,只要实现配对识别即可,可以是市售产品或用常规制备方法制得的抗体,可以是单克隆抗体,也可以是多克隆抗体,优选为单克隆抗体。
本发明所述抗体,为单克隆抗体时,为市售产品,或参照文献或国家公布制备方法,利用细胞融合技术或基因重组技术等制备的单克隆抗体,优选为细胞融合技术提取的单克隆抗体。
本发明所述抗体,是多克隆抗体时,为市售产品,或参照文献或国家公布制备方法,通过兔、大鼠、小鼠、绵羊、山羊、马等产生的多克隆抗体,优选为鼠源多克隆抗体。
所述配对抗体,厂家为genetexinc.、abcam、海肽生物,优选为abcam、海肽生物,优选为海肽生物。
所述荧光标记抗体为荧光微球标记抗体,所述荧光微球粒径为20-2000nm,优选为100-1000nm,更优选为100-500nm。
所述荧光微球,荧光微球的载体为天然或合成的有机高分子材料,负载的荧光物质有机物,其激发波长为600-800nm,发射波长为600-800nm,优选的,激发波长为650-700nm,发射波长为750-800nm。
所述负载的荧光物质有机物,为不同荧光染料的组合,激发分子为cyanine5.5系列荧光染料,发射分子为cyanine7系列荧光染料。其激发波长为670nm,发射波长为780nm,分子结构是:
所述荧光标记抗体,是通过抗体与荧光微球化学反应交联而制成,在所述抗体-荧光微球制备中,所述抗抗体与荧光微球的质量比为1:10-1:100,优选为1:10-50,更优选为1:10。
所述荧光微球,通过表面修饰基团与抗bnp抗体化学反应交联,表面修饰基团有多种,羧基,氨基,醛基,羰基,优选为羧基。
所述滤血膜为玻纤或无纺布材料,优选为玻纤材料。
所述滤血膜厂家为奥斯龙、沃夫曼,优选为沃夫曼。
所述bnp抗体溶液,终浓度为10-50ug/ml,优选为30-40ug/ml,更优选为30ug/ml。
所述bnp抗体溶液,缓冲液为pbs,cb,tris-hcl,优选为pbs。
所述保护剂包括牛血清白蛋白和明胶,质量体积比浓度为1-10%,优选为2%-5%,更优选为3%。
所述荧光标记的缓冲液选自硼酸盐缓冲液、mes缓冲液、碳酸盐缓冲液、tris-hcl缓冲液、磷酸盐缓冲液和甘氨酸缓冲液中的一种或多种,优选为硼酸盐缓冲液、mes缓冲液,更优选为硼酸盐缓冲液。
所述荧光标记的缓冲液,缓冲液的浓度为10-100mm,优选为10-50mm,更优选为10mm。
所述荧光标记的缓冲液,缓冲液的ph为7.0-7.5,优选为7.2-7.4,更优选为7.2。
所述反应活性剂选自吐温20,吐温100,优选为吐温20。
所述反应活性剂质量体积比为0.01-0.5%,优选为0.02-0.4%,优选为0.2%。
所述试剂防腐剂选自叠氮钠、硫柳汞和proclin300中的一种或多种,优选为proclin300。
所述试剂防腐剂,所述防腐剂的质量体积比为0.1%-2%,优选为1%-1.5%,更优选为1%。
进一步,bnp抗体的制备方法包括以下步骤:
(1)、荧光微球的活化、洗涤,将荧光微球表面修饰基团活化,取直径为200nm荧光微球,加入缓冲液离心,弃上清,沉淀用洗涤缓冲液重复洗涤3次;将末次沉淀重悬于所述洗涤缓冲液中,使荧光微球的质量体积比终浓度为1%,所述洗涤缓冲液选自pbs缓冲液和mes缓冲液中的一种:
(2)、bnp抗体偶联荧光微球,取1ml活化洗涤后的200nm胶乳溶液,加入抗bnp抗体,使抗bnp抗体终浓度为1mg/ml;混匀后,置4度,摇床以220rpm转速包被8h;用pbs缓冲液洗涤未与荧光微球结合的抗bnp抗体,重复3次;封闭:将洗涤后的抗bnp抗体的荧光微球溶于包含所述保护剂的缓冲液中,使所述荧光微球的质量体积比终浓度为0.1-0.14%;
(3)、抗bnp抗体和荧光微球结合后封闭,将所述荧光微球与所述抗bnp抗体混合物,加入bsa0.3%,室温下反应2h,离心,除去其中少量的沉淀物;清洗,将形成的荧光微球-抗bnp抗体复合物溶液离心,弃上清,加入磷酸盐缓冲液重复清洗3次;将末次沉淀溶于含所述保护剂和防腐剂的缓冲液中,使所述荧光微球质量体积比终浓度为0.04%-0.14%。
为了使本领域的技术人员更好地理解本发明的技术方案,下面结合具体实施例对本发明作进一步的详细说明。
荧光抗体的制备
(1)荧光微球的洗涤:取直径为200nm荧光微球,加入pb缓冲液离心,弃上清,沉淀用洗涤缓冲液重复洗涤3次;将末次沉淀重悬于所述洗涤缓冲液中,使荧光微球的质量体积比终浓度为1%;
(2)荧光微球的活化:配置活化剂edc、nhs溶液,浓度分别为1mg/ml、1mg/ml。取洗涤后的微球200ul,分别加入edc、nhs溶液50ul,震荡,反应30min;
(3)荧光抗体溶液的制备:用10mmol/l的溶液稀释bnp单克隆抗体至5ug/ml,取抗bnp抗体溶液,加入上述活化溶液,保证最后抗体浓度为25ug/ml,4度,反应3h;
(4)荧光抗体的封闭和保护:取含有3%bsa和1%pc300溶液,加入上述反应液,震荡反应30min;反应结束后,9000rpm离心力下,弃上清,取沉淀物置于pbs缓冲液,4度保存待用。
质控抗体标记的荧光微球的制备过程同bnp制备微球的过程相同。
bnp免疫荧光微流控芯片的制备
(1)包被抗体溶液的制备:用10mmol/l的pb溶液稀释bnp单克隆抗体至5ug/ml;
(2)质控抗体溶液的制备:用10mmol/l的pb溶液稀释bnp质控抗体至5ug/ml;
(3)点样:采用biodot仪器,将包被抗体和质控抗体分别喷于微流控底板的识别反应区和质控线位置,37度,3h;
(4)荧光微球固定:将荧光微球标记过得抗体固定于微栅反应腔,37度,3h;
(5)组合封装:将固定了抗体和荧光抗体的微流控底板与顶板组装,并采用超声焊接方法组合,与干燥剂一并封装与铝箔袋,置于干燥柜中保存,待用。
标准曲线的绘制:
用小牛血清稀释bnp标准品,浓度为:0、0.5、2.0、10.0、25.0、50.0、100.0ng/ml。
分别取50μl标准品滴加到微流控芯片加样孔,反应15分钟后,通过bnp微流控芯片读数仪读取系统检测信号,每个标准品的浓度检测三次,标准曲线如图3所示。
bnp样本检测:
选取40例国外荧光检测法检测bnp的临床样本(样本浓度覆盖标准品的检测范围),采用本发明的bnp微流控芯片及配套仪器进行检测。以荧光检测法检测的bnp浓度为横坐标,以本发明检测bnp浓度为纵坐标,绘制样本相关性曲线,如图4。其中,bnp的相关性系数r均大于0.97,完全符合临床试验的要求。
本发明与现有技术相比,具有以下突出的优点:
1)本发明采用免疫荧光法,具有灵敏度高、基质影响小的优点。
2)本发明采用的微流控芯片,将样本混合、反应、分离和检测功能集成于一个芯片上,并把反应所需的所有试剂组分集成到芯片,操作一体化,简单快速。
3)基于微流控检测芯片技术,通过精细稳定地控制免疫反应过程,达到有效地控制微反应的变异系数。
4)本发明操作简便,检测时,只需加入样本,把芯片放入小型便携配套仪器中即可。
5)本发明配套仪器是小型便携仪器,仪器只与芯片发生物理接触,芯片内液体不与仪器接触,不会污染仪器而产生交叉干扰。
- 还没有人留言评论。精彩留言会获得点赞!