一种基于二硫苏糖醇和金纳米复合膜的L-半胱氨酸传感器的制作方法
本实用新型属于化学/生物传感技术领域,具体涉及一种基于二硫苏糖醇和金纳米复合膜的L-半胱氨酸传感器,即一种选择性膜电位型传感器,适用于生命科学、临床医学等方面的检测。
背景技术:
L-半胱氨酸(L-cysteine,L-Cys)是一种脂肪族末端含有巯基(-SH)的极性α-氨基酸(如下图结构式),是生物体生命活动的一种条件氨基酸,对许多必需的生物化学物质如辅酶A、肝素、生物素、类脂酸和谷胱甘肽的代谢起着关键作用。同时,L-Cys作为含硫氨基酸在生物细胞代谢和稳态系统中也发挥着重要作用。而蛋白质基序中所存在的L-Cys,在早期进化中用于支持细胞中酶催化、转录调节、蛋白质折叠和代谢、翻译后修饰以及三维结构等。L-Cys不仅在细胞活动过程起着重要作用,也是生物体许多疾病的重要标志物,且生理水平的L-Cys浓度偏差(30-200μM)与高半胱氨酸血症、类风湿性关节炎、尿毒症、阿尔茨海默氏病等慢性疾病以及不良妊娠等有关,因此发展L-Cys的测定方法变得至关重要,近年来并逐渐引起了众多学者尤其是化学、生物学、医学工作者的兴趣。
目前,检测L-Cys的常用分析方法有高效液相色谱法、流动注射分析法、高效毛细管电泳法、气相色谱-质谱联用法、液相色谱-质谱联用法、拉曼光谱法、荧光分析法等。然而,这些分析方法往往需要昂贵的精密仪器、复杂的样品制备流程,且需要熟练的技术人员,不方便实时、在线使用,因而限制了其应用。L-半胱氨酸分子含有氨基、巯基等电化学活性基团(如下图结构式),因而具备应用电分析化学方法进行测定的必要条件。
电化学方法因具有快速、价廉、灵敏度高、易小型化等优点,在传感器的研发中引起了很多关注。目前,国内外电化学方法中主要应用电流型电化学传感器实现对L-Cys的测定,尽管电流型传感器电化学响应不断提高,仍然存在较繁琐的操作流程、不容易微型化和难以实现实时检测的缺点。
与电流型电化学传感分析方法相比,电位型电化学传感器具有易于微型化、在线监测、成本低等特点,且适用于生物体内和现场分析,对测定无机离子和有机小分子有很好的应用前景。2001年Saeed Shahrokhian等描述了一种基于铅酞菁(PbPc)作为离子载体的选择性电极,即将PbPc结合到聚氯乙烯膜中构建了一种L-Cys电位型传感器,其线性范围为1×10-6~5×10-2mol·L-1,检测下限为1×10-6mol·L-1。但目前用于高选择性、高灵敏性检测L-Cys的电位型传感分析方法仍然很少,且极具挑战性。本实用新型通过自组装方法,研制了一种简易的基于二硫苏糖醇/金纳米(DTT/AuNP)复合膜的延长栅金电极(GGE),利用场效应晶体管原位信号放大作用对L-半胱氨酸实现灵敏检测,具有超常规的、灵敏的两倍能斯特响应关系,线性范围达到1.0×10-8—1.0×10-4mol/L,响应灵敏度为119.4 mV·pc-1(25℃),检出限达到nM浓度;其制备过程简单便捷,响应时间快,在生命科学、临床医学和农畜产品安全检测等方面具有重要的应用前景。
技术实现要素:
本实用新型旨在克服现有技术的不足,提供一种基于二硫苏糖醇和金纳米复合膜的L- 半胱氨酸传感器。
为了达到上述目的,本实用新型提供的技术方案为:
所述基于二硫苏糖醇和金纳米复合膜的L-半胱氨酸传感器包括场效应晶体管,所述场效应晶体管上设有栅极延长的金电极,即,栅极金电极,所述栅极延长的金电极中,所述栅极部分延长0.1—500mm的距离,金电极的金膜层(10)表面组装有二硫苏糖醇/金纳米复合膜(12)。
其中,所述场效应晶体管包括Si基底层(1)和设于Si基底层(1)上的多晶硅栅极 (7);所述Si基底层(1)上植入p阱(2)和N型衬底(3),所述p阱(2)处设有源电极(4)和漏电极(5),被植入p阱(2)和N型衬底(3)并构建有源电极(4)和漏电极(5)的Si基底层(1)上设有二氧化硅层(6);所述多晶硅栅极(7)的基底层上依次镀上铝铜合金层(8)、铬钯合金层(9)和金膜层(10);在多晶硅栅极(7)的基底层和二氧化硅层(6)上还设有氮化硅层(11)。所述铝铜合金层(8)的厚度为20—600nm,铬钯合金层(9)的厚度为20—600nm,金膜层(10)的厚度为20—1000nm。
所述传感器对L-半胱氨酸(13)具有良好的两倍能斯特响应关系,线性范围为 1.0×10-8—1.0×10-4,响应灵敏度为119.4mV·pc-1,检出限达到nM浓度。
基于上述传感器的L-半胱氨酸的检测方法包括如下步骤:
(1)在场效应晶体管的Si基底层(1)上植入p阱(2)和N型衬底(3),采用热蒸发和磁控溅射技术在p阱(2)处构建源电极(4)和漏电极(5),然后在被植入p阱 (2)和N型衬底(3)并构建有源电极(4)和漏电极(5)的Si基底层(1)上构建二氧化硅层(6),再采用热蒸发和磁控溅射技术在多晶硅栅极(7)的基底层上依次镀上铝铜合金层(8)、铬钯合金层(9)和金膜层(10),最后在多晶硅栅极(7)的基底层和二氧化硅层(6)上构建氮化硅层(11);将栅极部分延长0.1—500mm的距离,制得具有栅极金电极的延长栅场效应晶体管;
(2)制备二硫苏糖醇的乙醇溶液,并将清洗后的延长栅场效应晶体管的栅极金电极在避光、干燥的环境下浸泡于其中,于25℃条件下静置,接着取出洗净后再滴加所制备的金纳米溶胶溶液,静置,然后洗净浸泡后的栅极金电极,制得二硫苏糖醇/金纳米复合膜(12) 修饰的二硫苏糖醇/金纳米复合膜栅极金电极;
(3)将参比电极、二硫苏糖醇/金纳米复合膜栅极金电极与延长栅场效应晶体管的电极接口相连形成双高阻差分放大电路,将参比电极、二硫苏糖醇/金纳米复合膜栅极金电极插入PBS缓冲溶液中,将延长栅场效应晶体管的电源接口分别与稳压电源的正负极相连,将延长栅场效应晶体管的信号输出接口与万用电表的测试端口相连,由此构成一个完整的传感检测回路;利用场效应晶体管的原位信号放大作用,可灵敏检测体系的电位变化;作为工作电极的二硫苏糖醇/金纳米复合膜栅极金电极在PBS缓冲溶液的电位会随着时间的增加而逐渐趋向于稳定,待电位稳定后加入含有不同浓度L-半胱氨酸(13)的待测样品,进而获得相应的电位响应数据,完成待测样品中L-半胱氨酸(13)的检测。
优选地,步骤(1)中,用热蒸发和磁控溅射技术在多晶硅栅极(7)的基底层上依次镀上铝铜合金层(8)、铬钯合金层(9)和金膜层(10)时,镀膜真空度≤5.0×10-6torr,且采用Si3N4进行钝化;铝铜合金层(8)包括如下重量份的组分:Al 40—68、Cu 30—60、Ni 2—12、Fe 1—8、Ti 1—6、Nb 0.01—0.50;铬钯合金层(9)包括如下重量份的组分:Cr 40—80、Pd 10—40、Ni 2—12、Fe 1—8、Ti 1—6、Nb 0.01—0.50;铝铜合金层(8)的厚度为20—600nm,铬钯合金层(9)的厚度为20—600nm,金膜层(10)的厚度为20—1000nm。
优选地,步骤(2)中的所述二硫苏糖醇乙醇溶液的浓度为1.0—50.0mmol/L;所述金纳米溶胶溶液的浓度为0.1—50.0mmol/L。步骤(2)中栅极金电极浸泡于二硫苏糖醇的乙醇溶液中的时间为1—72h;滴加金纳米溶胶溶液静置的时间为1—72h。
优选地,步骤(3)中的参比电极为饱和甘汞电极或内置饱和KCl溶液的Ag/AgCl电极,工作电极为二硫苏糖醇/金纳米复合膜栅极金电极。步骤(3)中的PBS缓冲溶液为 pH3.0—11.0、浓度为0.1mol/L的磷酸盐缓冲溶液,pH值优选为6.0。
下面对本实用新型作进一步说明:
本实用新型将场效应晶体管(FET)的栅极金电极(GGE)延长一定距离,如延伸 0.1—500mm,通过浸渍法,将二硫苏糖醇(DTT)和金纳米(AuNP)先后自组装固定修饰在金电极表面,制备了一种简易的基于二硫苏糖醇/金纳米(DTT/AuNP)复合膜的延长栅极金电极(GGE),考察了L-半胱氨酸(L-Cys)在此电极上的电化学行为,建立了一种电化学传感检测L-半胱氨酸的新方法。在优化的实验条件下,该传感器对L-半胱氨酸具有超常规的、灵敏的两倍能斯特响应关系,线性范围为1.0×10-8—1.0×10-4mol/L,响应灵敏度为119.4mV·pc-1(25℃),检出限达到nM浓度。且其制备过程简单便捷,响应时间快,具有良好的选择性,使用该电极对猪血清样品中的L-Cys含量进行检测,测得其回收率为 93.4%—108.1%,说明该电极可用于实际样品中L-半胱氨酸的检测,在生命科学、临床医学等方面具有着重要的应用前景。
附图说明
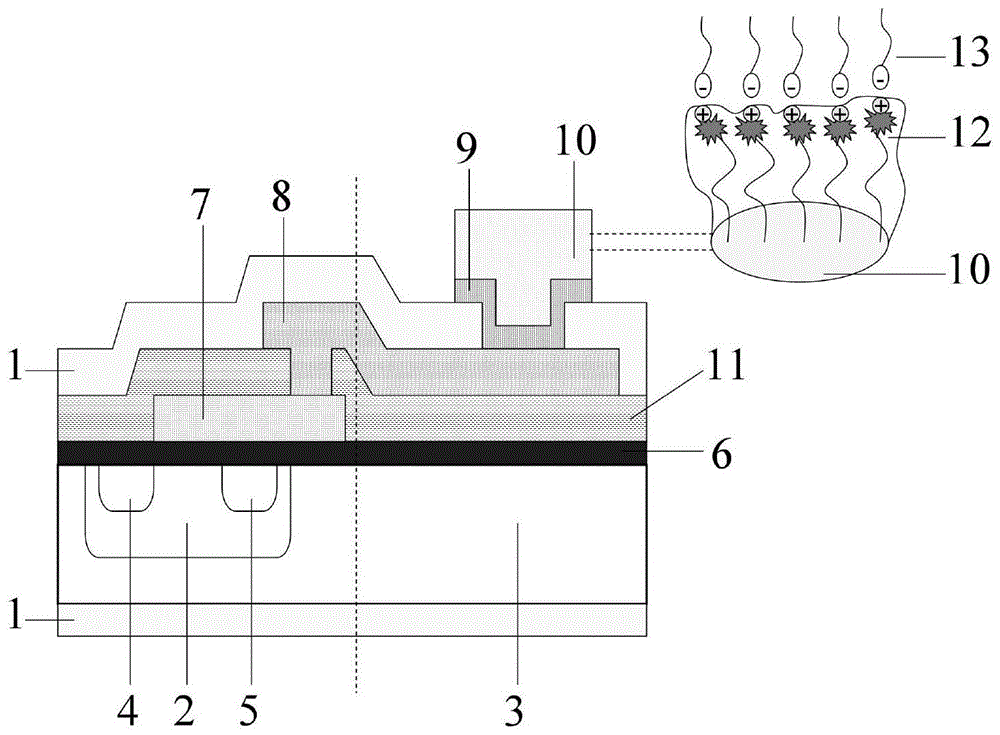
图1为延长栅极场效应晶体管及传感器的设计示意图;图中:1、Si基底层,2、源电极, 3、漏电极,4、p阱,5、N型衬底,6、二氧化硅层,7、多晶硅栅极,8、铝铜合金层,9、铬钯合金层,10、金膜层,11、氮化硅层,12、二硫苏糖醇/金纳米复合膜,13、L-半胱氨酸;
图2:图2A和图2B分别为金纳米的TEM表征图和金纳米溶胶的吸收光谱图;
图3为DTT/AuNP复合膜的组装及结合L-半胱氨酸分子的识别响应原理示意图;
图4:图4A和图4B分别为不同电极在铁氰化钾/亚铁氰化钾溶液(含有2.0mmol/L K3[Fe(CN)6],2.0mmol/L K4[Fe(CN)6],0.2mol/L Na2SO4)中的交流阻抗图和循环伏安图;图4A和图4B中:a、GGE,b、GGE/DTT,c、GGE/DTT/AuNP,d、GGE/DTT/AuNP/L-Cys;图5为GGE/DTT/AuNP电极在pH=6.0的PBS缓冲溶液中,结合不同浓度L-半胱氨酸后得到的电位响应曲线图。
具体实施方式
一、实验过程
1、延长栅极场效应晶体管的设计及栅极金电极的制备
图1是延长栅极场效应晶体管及传感器的设计示意图,即结合金属-氧化物-半导体场效应晶体管(MOSFET)的基本结构,在场效应晶体管的Si基底层1上植入p阱2和N型衬底3,采用热蒸发和磁控溅射技术在p阱2处构建源电极4和漏电极5,然后在被植入p 阱2和N型衬底3并构建有源电极4和漏电极5的Si基底层1上构建二氧化硅层6,再采用热蒸发和磁控溅射技术在多晶硅栅极7的基底层上依次镀上铝铜合金层8、铬钯合金层9和金膜层10,最后在多晶硅栅极7的基底层和二氧化硅层6上构建氮化硅层11;铝铜合金层8包括如下重量份的组分:Al 40—68、Cu 30—60、Ni 2—12、Fe 1—8、Ti 1—6、Nb 0.01—0.50;铬钯合金层9包括如下重量份的组分:Cr 40—80、Pd 10—40、Ni 2—12、Fe 1—8、Ti 1—6、Nb 0.01—0.50;铝铜合金层8的厚度为20—600nm,铬钯合金层9的厚度为20—600nm,金膜层10的厚度为20—1000nm;镀膜时,控制镀膜真空度≤5.0×10-6torr,将栅极部分的金电极延长250mm的距离,并且利用SiO2和Si3N4钝化场效应晶体管晶片,目的是防止晶片除Au外的部分与溶液接触,从而形成延长栅极场效应晶体管(EGFET)。对EGFET的延长栅极金电极(GGE)膜表面进行不同的物理/化学修饰处理,形成敏感膜以实现对待测目标物的灵敏检测。采用自组装方法,将二硫苏糖醇 (DTT)和金纳米(AuNP)先后自组装固定修饰在栅极金电极的表面,制得二硫苏糖醇/ 金纳米复合膜12修饰的二硫苏糖醇/金纳米复合膜栅极金电极(GGE/DTT/AuNP)。
2、金纳米溶胶的制备
称取0.1g氯金酸溶解于100mL二次蒸馏水中,加入0.0481g聚乙烯吡咯烷酮(PVP),加热煮沸,在剧烈的搅拌下(密闭系统,用磁子进行搅拌),快速加入25mL新配制的1%的柠檬酸钠水溶液,继续剧烈搅拌,沸腾5min,颜色从淡黄色变成无色,并逐渐转变成为紫色,再变成酒红色,继续加热搅拌15min,停止加热,继续搅拌冷却至室温,将制备好的金溶胶(约2.4mmol/L)转至棕色试剂瓶,于4℃冰箱中密封保存。
3、修饰金电极的制备
机械处理:首先将栅极金电极浸入具有强氧化性的Piranha溶液中,浸泡0.1—15.0 min,如2.0min;然后是打磨与抛光,在抛光布上倒入适量α-Al2O3(1.0μm、0.05μm、 0.3μm)与纯净水,从粗至细进行逐步抛光,每次抛光后应清洗表面污物;最后依次在超纯水、无水乙醇、超纯水中,分别超声清洗5min。
浸渍法修饰金电极:用移液枪分别取2mL二硫苏糖醇(5.0mmol/L)、2mL无水乙醇于事先干燥好的烧杯中,再将电极浸泡于该混合溶液中,用封装膜将烧杯口密闭封好,于避光、干燥的环境中浸泡修饰48h。接着,取出洗净电极后继续将其浸泡于2mL上述制备的金纳米溶胶溶液(约2.4mmol/L)、2mL无水乙醇的混合溶液里,修饰48h后,取出,冲净,备用。
4、修饰栅极金电极电化学性能的测试
先按上述方法制备不同电极,如裸栅极金电极(GGE)、DTT修饰栅极金电极 (GGE/DTT)、DTT与AuNP复合膜修饰栅极金电极(GGE/DTT/AuNP)、结合L-半胱氨酸后的DTT与AuNP复合膜修饰栅极金电极(GGE/DTT/AuNP/L-Cys),然后以铁氰化钾/亚铁氰化钾溶液(含有2.0mmol/L K3[Fe(CN)6],2.0mmol/L K4[Fe(CN)6],0.2mol/L Na2SO4)为介质,在电化学工作站中分别将不同电极作为工作电极,通过循环伏安法(扫速为0.05V/s)和交流阻抗分析等方法,对不同电极的电化学性能进行检测。
5、实验最佳响应条件的优化
(1)pH的优化:配制梯度pH的PBS溶液(3.00~11.00)。在不同pH下,以20mL PBS溶液(0.1mol/L)作为介质,依次加入不同浓度的L-半胱氨酸溶液(1.0×10-8、 1.0×10-7、1.0×10-6、5.0×10-6、1.0×10-5、5.0×10-5、1.0×10-4mol/L),以DTT/AuNP复合膜修饰金电极为工作电极,Ag/AgCl为参比电极,对溶液电位进行测定,作出pH和电位变化的关系曲线,找到实验最佳响应的pH。
(2)修饰时间的优化:以4h、8h、12h、24h、36h、48h、60h、72h、96h为修饰时间梯度,考查DTT、AuNP各自的修饰时间。
二、实验结果与分析
1、金纳米的表征分析
图2A和图2B分别为金纳米的TEM表征图及其溶胶溶液的吸收光谱图。从图2A中可以粗略估算所制备的金溶胶颗粒大小均一,分散性较好,通过对照片中的金纳米粒子的粒径进行统计分析,得出其粒径为10.42±0.49nm。从图2B可知金纳米粒子的吸收峰在 500~600之间,其最大吸收波长λmax是519.5nm。根据纳米粒子的粒径计算的经验公式:λmax=515.895+0.3421d,其中λmax为最大吸收波长,d为金纳米颗粒的平均粒径,则得金纳米粒子的粒径为10.54nm,表明两个方法的结果比较一致。
2、电极响应机理分析
二硫苏糖醇(DTT)是一种两端含有巯基的分子(其结构式如下图所示),一端巯基中的硫可以与Au形成Au-S键而自组装在金电极表面上,另一端巯基中的硫可以与金纳米颗粒的Au形成Au-S键而形成DTT/AuNP复合膜,从而组装形成GGE/DTT/AuNP电极。
在酸性条件下,DTT中含有巯基的一端倾向于带负电,AuNP倾向于带正电;同时,在酸性条件下,L-半胱氨酸带负电,含有巯基的一端,由于硫可以与AuNP形成稳定、牢固的Au-S键,则L-Cys的巯基与金纳米之间发生吸附结合;而且,DTT/AuNP复合膜的Au端可以结合两个L-Cys,使得L-Cys呈现-1/2的离子价态,其识别响应原理示意图如图3所示。
3、电极的电化学表征分析
为了验证二硫苏糖醇/金纳米复合膜载体与L-胱氨酸的相互作用,本实用新型采用交流阻抗和循环伏安方法考察了上述不同修饰膜电极的电化学行为,图4A和图4B分别为不同电极(a、GGE,b、GGE/DTT,c、GGE/DTT/AuNP,d、GGE/DTT/AuNP/L-Cys)在铁氰化钾/亚铁氰化钾溶液(含有2.0mmol/L K3[Fe(CN)6],2.0mmol/L K4[Fe(CN)6],0.2mol/L Na2SO4)中的交流阻抗图和循环伏安图。
如图4A的交流阻抗所示:a代表已进行完预处理的裸金电极,阻抗值很小,可以说明通过预处理后的裸金电极传递电子能力很强;b代表DTT修饰金电极,高频部分出现半圆,阻抗值明显非常大,说明DTT通过一端的巯基在金表面上形成了不导电的单分子自组装膜层,从而阻碍了[Fe(CN)6]3-/4-在电极表面进行电子传导;c是DTT/AuNP复合膜修饰电极后,阻抗明显减小,表征了修饰AuNP的成功,自组装膜层导电性增强;d是在结合 L-半胱氨酸后,电极的阻抗值再次减小,这是因为DTT/AuNP复合膜和L-半胱氨酸发生反应后,L-半胱氨酸由于表现出负离子特性,电子的传导性增强,从而增大电化学传导电流,使得界面阻抗减小。电极的循环伏安行为也能印证其阻抗的变化趋势(图4B),故该方法对L-半胱氨酸的识别检测是可行的。
4、实验最佳响应条件优化
4.1 pH的优化
实验考查了不同pH条件(pH3.00~11.00)下DTT/AuNP复合膜修饰GGE电极的电位随被测物L-半胱氨酸浓度变化的关系,在3.00≤pH≤6.00时,电极斜率随着pH的增大而增大;在6.00≤pH≤11.00时,电位变化基本上随着pH的增大而减小,所以优选pH=6.0为最佳实验条件。
4.2修饰时间的优化
实验探讨了GGE/DTT/AuNP电极在DTT修饰时间分别为4h、8h、12h、24h、36h、 48h、60h、72h、96h时,在pH=6.0的条件下,电极电位随L-半胱氨酸加入浓度的变化关系,并依次求出其响应斜率,找出响应斜率与修饰时间的关系,发现该电极在修饰时间为48h时具有较好的线性关系,误差较小,且电极斜率达到超常规的、稳定的两倍能斯特响应关系,因此本实验优选48h作为实验的最佳修饰时间。此外,实验也同样考查了金纳米的结合时间,发现电极在修饰48h时具有最佳的响应线性与灵敏度。
5、电极的电位响应性能
实验考查了GGE/DTT/AuNP电极在pH=6.0的PBS缓冲溶液中,结合不同浓度L-半胱氨酸后得到的电位响应关系。
随着L-半胱氨酸浓度的增大,电位值逐渐减小,说明该修饰电极表面键合的L-半胱氨酸增加,且该电极在pH=6.0的PBS缓冲溶液中对L-半胱氨酸离子在1.0×10-8—1.0×10-4 mol/L的浓度范围有良好的线性响应关系,通过最小二乘法拟合可得到线性方程为ΔE=-119.4logC-939.6,检测下限可以达到nmol/L。
6、干扰性的影响
实验考察了共存干扰组分对GGE/DTT/AuNP电极测定L-半胱氨酸的影响。在20mL pH=6.00的PBS缓冲溶液(0.1mol/L)中,加入1.0×10-5mol/L的L-半胱氨酸,再分别加入浓度为L-半胱氨酸浓度50倍的不同种类氨基酸,如L-组氨酸(L-His)、L-苯丙氨酸 (L-Phe)、L-甘氨酸(L-Ghy)、L-酪氨酸(L-Tyr)、L-脯氨酸(L-Pro)、L-异亮氨酸 (L-Ile)、L-谷氨酸(L-Glu)、L-天门冬氨酸(L-Asp)、L-色氨酸(L-Trp)等。结果发现,在已有L-半胱氨酸的溶液中加入其他几种氨基酸,响应电位未出现明显变化,即共存组分对GGE/DTT/AuNP电极测定L-半胱氨酸没有影响。
采用分别溶液法,进一步考察了GGE/DTT/AuNP电极对不同氨基酸,如L-组氨酸 (L-His)、L-苯丙氨酸(L-Phe)、L-甘氨酸(L-Ghy)、L-酪氨酸(L-Tyr)、L-脯氨酸 (L-Pro)、L-异亮氨酸(L-Ile)、L-谷氨酸(L-Glu)、L-天门冬氨酸(L-Asp)、L-色氨酸(L-Trp)的响应灵敏性比较,各氨基酸的浓度均为L-半胱氨酸浓度的50倍。结果表明,该电极对L-半胱氨酸的响应最大,其它氨基酸几乎响应很小,可以说明该电极对L-半胱氨酸的测定有很好的选择性。
7、电极的响应时间、稳定性和重现性
电极的响应时间、稳定性和重现性等参数是体现电极性能好坏的重要指标,因此也是发展复合膜载体选择性电极性能必不可少的考查指标。实验考查了GGE/DTT/AuNP电极对L-半胱氨酸在1.0×10-7mol/L—1.0×10-4mol/L浓度范围内的响应情况,响应时间以达到电位响应最大值的95%来计算,可以发现该电极的响应时间为36s。可以看出,在整个浓度范围内电极达到平衡的反应时间很短,表明该电极对L-半胱氨酸有很快的响应速度。
随后,将GGE/DTT/AuNP电极对浓度为1.0×10-6mol·L-1的L-半胱氨酸样品连续监测 30min,电位漂移≤±0.9mV,电位数据的相对标准偏差为1.77%(n=5),表明该电位传感器具有好的稳定性。将该电极对L-半胱氨酸样品连续测试30d,其响应斜率下降不大,说明该电位传感器可以使用至少一个月,具有较长的使用寿命。
还考察了GGE/DTT/AuNP电极结合不同浓度L-半胱氨酸样品的电位响应得重复性,即使用该电极在1.0×10-6mol/L和1.0×10-5mol/L的L-半胱氨酸样品中来回测定它们的电位值,各测3次,其相对标准偏差均小于5%,表明该电极对L-半胱氨酸的检测有很好的重现性。
8、电极的回收率
在最佳实验条件下,考察了GGE/DTT/AuNP电极对实际样品中如猪血清样品中L-半胱氨酸含量的检测应用。取猪血清样品六份,分别编号为K1、K2、K3、K4、K5和K6。取其上清液,采用pH=6.0的PBS缓冲液将样品稀释10倍,加入已知浓度的L-半胱氨酸。通过标准加入法,对电位值进行测定,与工作曲线做对比,测得猪血清样品的回收率在 93.4%—108.1%之间,说明该自组装电化学传感器具有较好的准确性、实用性,可以用于实际样品中L-半胱氨酸含量的测定分析,在生命科学、生物医学和农畜产品安全检测等领域中具有重要的应用价值。
总之,本实用新型提供了一种自组装DTT/AuNP复合膜修饰的栅极金电极,借助场效应晶体管原位放大电位信号,对L-半胱氨酸进行了灵敏检测,从而形成一种新型的生物传感器,对L-半胱氨酸显示出优异的分子识别作用,将之应用于猪血清样品中L-Cys的检测,显示出良好的稳定性、重现性、选择性和灵敏性,在生命科学、生物医学和农畜产品安全检测等领域具有很好的应用前景。
- 还没有人留言评论。精彩留言会获得点赞!