用于鉴别病毒性感染与细菌性感染的方法和设备与流程
本发明涉及用于鉴别病毒性感染与细菌性感染的即时检测(pointofcare,poc)分析领域。更具体地,本发明涉及一种快速区分病毒性感染和/或细菌性感染的免疫分析法。
背景技术:
发烧是导致儿童到全科诊所和儿科诊所的急诊中心就诊的常见原因。最常见的是,发烧与呼吸道感染或肠胃炎有关。儿童发烧的高发率和预防性施用不必要的抗生素,是对指示病毒性和/或细菌性感染的生物标记物进行快速筛选检测的开发的原因。
在大约60%的病例中,严重的社区获得性肺炎是由细菌性感染引起的,大约10%的患者需要进入重症监护病房(icu)。其余40%与呼吸道病毒有关。大多数呼吸道感染涉及咽炎,其中40%由病毒引起,而25-50%由a族β溶血性链球菌引起。后者会导致急性细支气管炎和肺炎。
所有抗菌药物中约有80%会在初级治疗中被开出处方,其中多达80%的处方用于呼吸道适应症。迄今为止,呼吸道感染是初级治疗中最常见的咳嗽原因。医生经常开广谱抗生素的处方来治疗咳嗽,包括急性支气管炎,而且其中许多处方对患者的益处微乎其微,并且可能引起副作用和可能增强抗生素耐药性。促使医生施用抗生素的因素包括缺乏适当的细菌性感染诊断标记物、对患者缺乏随访的担忧以及时间压力。
快速区分病毒性感染与细菌性感染仍然具有挑战性。最近,已经鉴别了许多新的诊断标记物。这些标记物中的数种表现出区分病毒性与细菌性感染的巨大前景。这类蛋白包括mx-gtp酶和c反应蛋白(crp)。
mx同源蛋白是高分子量gtp酶超家族的成员。因此,这些gtp酶由i型α/β或ii型干扰素(ifn)上调。mxgtp酶仅在ifnα/β而不在ifnγ处理的细胞中过度表达。i型干扰素在先天免疫反应中起重要作用,并具有免疫调节、抗增殖和抗病毒的功能。
发明人自己的研究表明,mx-同源人体蛋白具有以下优点:1)在人体中的mx-同源人体蛋白主要在细胞内表达。可以通过细胞内染色在大多数细胞室中看到它们[16]。2)mx-同源蛋白通过剂量依赖的方式进行诱导[6]。3)mx-同源人体蛋白由i型干扰素特异性诱导,而并非由ifn-γ、il-i、tnf-α或细菌性感染引起的其他任何细胞因子诱导[8,12]。4)与外周血系统中的i型干扰素相比,mx-同源人体蛋白具需要更长的检测时间[6]。因此,这些蛋白质是鉴别病毒性疾病的标记物[7,14,15]。此外,这些蛋白可用作标记物,以鉴别接受i型干扰素治疗的患者的ifn治疗是否成功[5,9,10,11]。在早期研究中,发明人通过sds-page后的westernblotting检测到了这些蛋白质。12但是该过程需要两天以上。因此,发明人建立了elisa,以在两天内检测这些蛋白质[13]。
基于这些事实和假设,即在细菌性感染患者体内i型干扰素保持在正常水平内,外周血中的mx-同源蛋白表达是对病毒性感染灵敏且特异的标记物。同样地,据报道,大多数病毒性感染引起的急性期反应浓度很小、c反应蛋白(crp)浓度小、降钙素原(pct)水平低和杀菌/通透性增强蛋白(bpi)浓度小。因此,这些蛋白质将用于区分病毒源性疾病与细菌性病因疾病。由于crp的血浆浓度在刺激后迅速增加,并以很短的半衰期迅速降低,因此crp在诊断和监测感染和炎性疾病中可成为非常有用的工具。在斯堪的纳维亚,一般情况下,即时检测crp测试是对呼吸道感染患者进行例行评估的一部分,其应用具有成本效益。一般情况下,已发现crp在诊断细菌性疾病以及部分区分细菌性与病毒性感染中具有重要价值。通常发现crp的诊断价值优于红细胞沉降率(esr),优于或等于白细胞计数(wbc)。即时检测的缺点是检测时间长。这些测试需要至少30分钟到2个小时。
在临床上,区分某些全身性病毒性感染与细菌性感染可能具有挑战性。通常在严重感染(例如肺炎)的情况下,或者当缺少诊断的结果导致严重并发症(例如链球菌性喉炎)时进行细菌培养。通常很难得到培养物。不幸的是,由于接收结果的显著时间延迟,病毒培养无法按常规进行。新的病毒筛选pcr组合(panel)是有用的,但价格昂贵,而且无法即时检测提供信息,因为结果只能在24小时后才能得到。因此,仍然需要一种简单,易于使用的诊断测试,其能够在短时间内区分病毒性和细菌性感染!
wo2010/033963公开了一种侧流免疫分析法,用于检测和区分病毒性感染与细菌性感染。细菌性标记物是crp,病毒性标记物是mx-a-蛋白。该分析法在欧洲以商标名
技术实现要素:
本发明的目的是提供一种改进的、更准确和特异的诊断分析法,用于在短时间内可靠地鉴别患者的细菌性感染与病毒性感染。通过本发明的主题来解决该目的。
根据本发明,提供了一种即时检测(poc)免疫分析设备,其包括:
a.加样区,和
b.检测区,该检测区具有对mx-b蛋白(mx-b)有结合亲和力的第一检测试剂,和对c反应蛋白(crp/pct)有结合亲和力的第二检测试剂,并且
其中,该设备配置为检测受试者样品中的mx-b和crp/pct,以鉴别细菌性感染与病毒性感染。
根据本发明另一实施例,提供了一种即时检测(poc)免疫分析设备,其包括:
a.加样区,和
b.检测区,该检测区具有对mx-b蛋白(mx-b)有结合亲和力的第一检测试剂,对c反应蛋白(crp)有结合亲和力的第二检测试剂,对降钙素原(pct)有结合亲和力的第三检测试剂和/或对杀菌/通透性增强蛋白bpi有结合亲和力的第四检测试剂,并且
其中,该设备配置为检测受试者样品中的mx-b和crp/pct,以鉴别细菌性感染与病毒性感染。
本发明的一个实施例涉及如本文所述的设备,还包括对bpi有结合亲和力的第三检测试剂。
本发明的一个实施例涉及如本文所述的设备,其中所述检测试剂选自合成分子、核苷酸、核酸、适体、肽、蛋白质、酶和抗体。
本发明的一个实施例涉及如本文所述的设备,其中所述检测试剂用可检测的标记物进行标记。
本发明的另一实施例涉及如本文所述的设备,其中可检测的标记物选自酶标签、荧光标签、放射性标签、颗粒标签、有色乳胶颗粒、有色塑料颗粒、有色荧光颗粒和荧光颗粒。
本发明的另一实施例涉及如本文所述的设备,还包括测试窗口,其配置为允许观察测试结果。
本发明的另一实施例涉及如本文所述的设备,其中所述检测试剂化学缀合至所述可检测的标记物,以形成永久的、不可逆的试剂标记物复合物。
本发明的另一实施例涉及如本文所述的设备,其中与检测试剂缀合的可检测的标记物配置为,当样品对mx-b和/或crp和/或pct和/或bpi呈阳性时对用户可见。
本发明的另一实施例涉及如本文所述的设备,其中所述设备配置为/或是人类血液样品中的pct和/或bpi。
本发明的一个实施例涉及一种用于鉴别受试者中的细菌性感染与病毒性感染的方法,其包括以下步骤:
a.提供源自所述受试者的样品,
b.提供本文所述的测试系统,
c.将样品加到测试系统中,
d.观察可检测的试剂标记物复合物的存在或缺乏,以确定样品是否含有mx-b和/或crp和/或pct和/或bpi,以及
e.确定患者的感染状态。
本发明的一个实施例涉及如本文所述的方法,其中
a.存在mx-b且缺乏crp/pct/bpi和/或其检测值低,指示为病毒性感染,
b.缺乏mx-b且存在crp/pct/bpi,指示为细菌性感染;以及
c.存在mx-b且存在crp/pct/bpi,指示为混合感染。
本发明的另一实施例涉及如本文所述的方法,进一步地观察可检测的试剂标记物复合物的存在或缺乏,以确定样品是否含有crp/pct/bpi。
本发明的一个实施例涉及如本文所述的方法,其中
a.存在mx-b且缺乏crp/pct和bpi,指示为病毒性感染,
b.缺乏mx-b且存在crp/pct和bpi,指示为细菌性感染;以及
c.存在mx-b且存在crp/pct和bpi,指示为混合感染。
本发明的另一实施例涉及如本文所述的方法,其中所述样品为血液样品。
本发明的另一实施例涉及如本文所述的方法,其中mx-b、crp/pct和/或bpi的存在是肉眼可见的。
附图说明
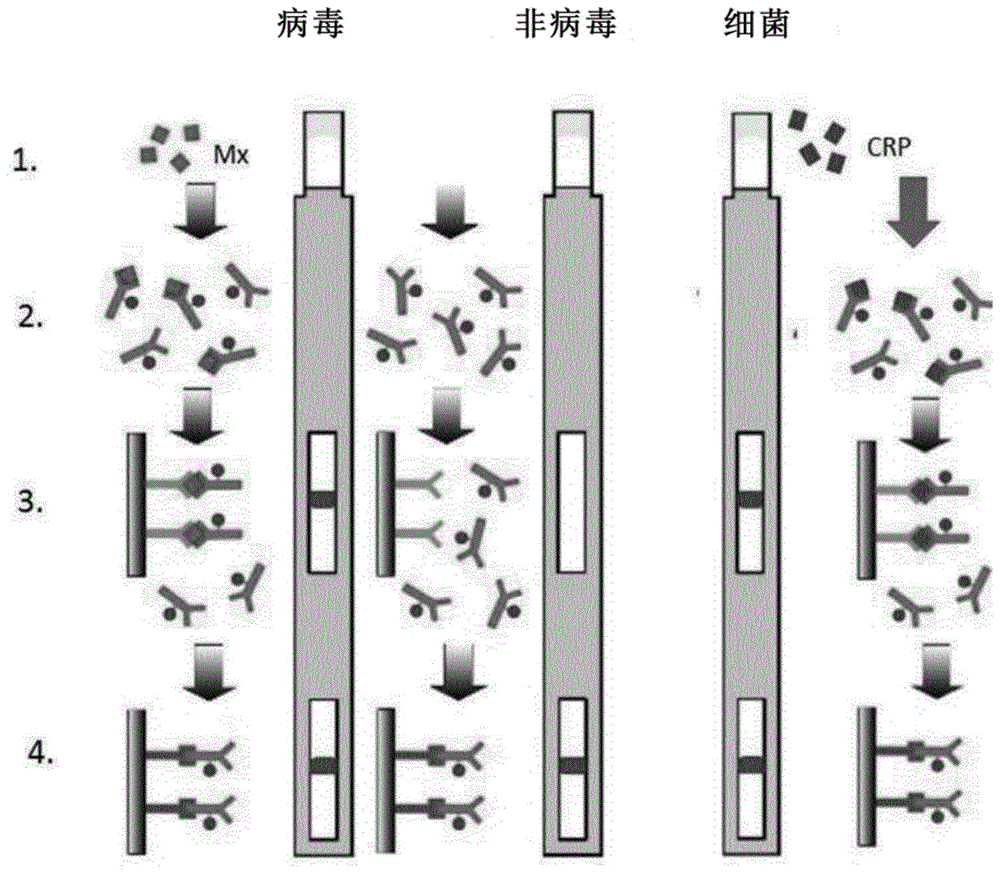
图1a描述了一个示例性测试步骤,其由三个涂有标记的抗体的测试条组成。
图1b描述了病毒性感染、细菌性感染、混合感染或可疑感染的不同测试图片。
图2示出了不同病毒和细菌病原体的结果。
具体实施方式
本发明提供了一种能够在短时间内,区分病毒性和细菌性感染的即时检测分析法。具体地,提供了一种包括针对病毒性和细菌性感染的测试标记物的即时检测诊断设备,其有效地帮助医生快速区分病毒性感染与细菌性感染。即时检测分析法具有以下优点:
1)该分析法可通过限制误诊从而限制抗生素的滥用和误用,显著降低医疗保健成本。
2)该分析法的有效性和可靠性在于降低对抗生素的耐药性,因为只有当出现细菌性感染时才会使用抗生素。
3)该分析法将增强医生诊所和药剂师的诊断组合。
因此,本发明有助于恰当使用抗生素。这意味着只有当需要时才使用抗生素,并且如果需要使用时,可以正确地使用抗生素。
抗生素不能抵抗感冒、流感、大多数喉咙痛和支气管炎等由病毒引起的感染。甚至很多鼻窦和耳朵感染无需抗生素也能好转。相反,缓解症状可能是治疗这些感染的最佳选择。服用抗生素治疗病毒性感染,例如感冒、流感、大多数喉咙痛和支气管炎:
-将不能治愈感染;
-将不能防止其他人致病;
-将不能帮助你或你的孩子感觉更好;
-将可能导致不必要和有害的副作用;以及
-可能导致抗生素耐药性,即细菌能够抵抗抗生素的作用并继续造成损害。
不正确地开抗生素处方的治疗效果令人怀疑,并使患者面临抗生素治疗的潜在并发症。从即时检测获得的快速结果从而使得诊断更正确,并协助医生作出开出正确的处方的决定。
对于即时检测分析法,不同的设备都可能适用,例如侧流免疫分析设备或光学传感器系统,其是在wo2016/116181中所述的设计用于与移动计算机设备交互的设备。
因此,根据本发明的一个实施例,使用样品分析设备,例如测试条,来确定感染是细菌性还是病毒性。测试条包括加样区和检测区。在本方法中,采集样品,并将其转移到测试条。检测区包括至少一种细菌标记物特异试剂和至少一种病毒标记物特异试剂。
在一个实施例中,病毒性感染的标记物是mx-b,细菌性感染的标记物是c反应蛋白(crp)。高mx-b蛋白水平与全身性病毒性感染密切相关。干扰素诱导粘液病毒(myxovirus,mx)蛋白在对抗多种病毒性感染方面发挥着重要作用。mx-同源蛋白可抑制rna和dna病毒。
最近发现mx-b蛋白是一种能将病毒成分运输到细胞外的重要蛋白[2]。例如,hiv蛋白会通过mx-b蛋白,而不是mx-a蛋白进行运输和排除[1]。因此,该即时检测分析法使用mx-b蛋白,因为它与mx-a蛋白只有63%的同源性,因此是mxgtp酶家族中的功能性mx蛋白[3]。结果表明,mx-b通过降低整合的病毒dna水平而强有力地抑制病毒性感染。此外,mx-b蛋白位于细胞核和细胞质内。相反地,mx-a蛋白只存在于细胞质中[4]。基于新的发现,mx-b被发明人选定为可靠的病毒性感染标记物。
c反应蛋白(crp),肝脏响应感染反应产生的急性期蛋白,是细菌性感染的可靠的生物标记物。健康个体的crp水平低于0.5mg/l,而crp水平在感染状况下升高。
降钙素原(pct)是一种含有116种氨基酸的多肽激素。这种蛋白质主要由甲状腺的c细胞产生。正常情况下,血液中的pct水平非常有限。相反地,在细菌性感染过程中,该蛋白会表达,并且浓度在0.5ng/ml到2ng/ml之间。这种蛋白的优点是在感染6小时后就能被检测到,而crp最早可被检测到的时间点则在12-16小时。
根据本发明的一个实施例,本发明涉及用于鉴别患者样品中mx-b和/或crp/pct/bpi的快速筛选测试。样品可以是,例如外周血样品、鼻咽抽取物、泪液、脊髓液和中耳抽取物。
杀菌/通透性增强蛋白(bpi)是一种多能蛋白,位于中性粒细胞和组织中,可能通过其抗生素和内毒素中和及处置功能,在宿主抵抗革兰氏阴性菌及其内毒素方面发挥关键作用。为了提高测试的可靠性和准确性,bpi被认为是改良即时检测的附加生物标记物。在细菌性感染过程中,这种蛋白质会表达,并且浓度在1μg/ml到20μg/ml之间。
因此,本发明的另一实施例涉及用于识别患者样品中mx-b、bpi和/或crp/pct的即时检测。
根据本发明的一个实施例,检测区包括至少一种对病毒标记物mx-b有结合亲和力的试剂和至少一种对细菌标记物crp/pct有结合亲和力的试剂,并且可选地包括至少一种对bpi有结合亲和力的试剂,使得当样品中存在的标记物与相应的试剂接触时,形成标记复合物。检测区包括与第一标记复合物结合的细菌标记物结合配偶体,和与第二标记复合物结合的病毒标记物结合配偶体。然后分析样品是否存在病毒标记物和/或细菌标记物。
检测区可通过固定与相应标记物特异结合的各种受体分子来实现功能化。受体分子可选自天然来源,例如抗体、抗体片段等。受体分子可以是合成产生的分子,例如适体。检测区包括至少一个传感器区域,在该传感器区域上设置有作为用于感测相应标记物的受体、抗体或其他特异性传授受体,例如与待检测的相应标记物特异结合的适体。因此,实现了传感器区域表面有效、易于应用的功能。
抗体或其他特异性传授受体,例如适体,对检测特定分析物具有高度选择性;因此,它们特别适合用于识别特定的疾病标记物。关于可能的受体,设置在传感器表面的抗体或其他特异性传授受体,例如适体,例如与待检测分析物结合,并在该过程中引起性质的改变。在一些实施例中,适体的优点在于它们更稳定,因此具有永久功能。
由于适体与抗体有着相似的应用,许多利用抗体的检测方法可以发展成为基于适体的方法。例如,大多数针对小分子的免疫分析法为竞争性分析,依赖于用溶液中的分析物替代表面结合抗体。
本发明的设备的一个实施例包括加样区。
本发明的另一实施例有关设备进一步包括试剂区。所述试剂区包括至少一种针对病毒细菌标记物的试剂,使得当样品中存在的病毒标记物接触所述试剂时,形成标记的病毒试剂复合物。此外,试剂区包括至少一种针对细菌标记物的试剂,使得当样品中存在的细菌标记物接触所述试剂时,形成标记的细菌试剂复合物。在本发明的一个实施例中,试剂区包括一种针对细菌标记物crp/pct的试剂和一种针对细菌标记物bpi的试剂,使得当样品中存在的所述细菌标记物接触所述试剂时,形成标记的复合物。
设备上的检测区包括与标记的病毒试剂复合物结合的病毒标记物结合配偶体,和与标记的细菌试剂复合物结合的细菌标记物结合配偶体。该设备可以是色谱测试条。
在一个优选实施例中,通过肉眼可见的测试线指示病毒标记物或细菌标记物的存在。由第一测试线指示病毒标记物的存在,而由第二和/或第三测试线指示细菌标记物的存在。在一些实施例中,第一测试线在阳性时显示第一颜色,第二测试线在阳性时显示与第一颜色不同的第二颜色,和/或第三测试线在阳性时显示与第一和第二颜色不同的第三颜色。在实施例中,第一、第二和第三测试线都位于样品分析设备上的同一空间,最好当第一、第二和/或第三测试线在阳性时能形成不同颜色。
在一个实施例中,两个或三个测试线在设备上,彼此空间地分隔开。在这样的实施例中,当测试线在阳性时,颜色可以相同。
在本发明的一个实施例中,将待分析样品加到载体上。载体可以由一种单一色谱材料,或者优选的由相同或不同材料制成的几种毛细管活性材料制成,并被固定在载体背衬上。这些材料彼此紧密接触,从而形成一条传输路径,其由毛细管力驱动的液体沿该路径从加样区经过试剂区,流向一个或多个检测区。
优选地,通过将载体的加样区浸入样品中,直接将样品加到载体上。或者,可以通过使用干燥或湿润的擦拭器件采集样品,将样品从可以转移的地方加到载体,可选地在润湿后,加到载体的加样区。通常擦拭器件是无菌的,在采集步骤之前可以是干燥的或用液体预处理。根据本发明适用于擦拭器件的材料可包括合成材料、织物或纤维网。
根据检测方法的类型,试剂区中存在不同的试剂,其位于加样区和检测区之间。在夹心免疫分析法中,优选为在试剂区内具有针对待检测病毒和细菌标记物的标记的、非固定化试剂。因此,当样品中存在的病毒或细菌标记物与试剂区中存在的相应标记的病毒或细菌试剂接触时,标记物与相应标记的试剂之间形成标记的复合物。标记的复合物反过来能够在检测区与固定化病毒或细菌标记物结合配偶体形成进一步的复合物。在竞争性免疫分析法中,试剂区优选含有标记的非固定化标记物类似物,该标记物类似物与检测区中针对固定化标记物结合配偶体的标记物竞争。试剂区和检测区中的标记物结合配偶体优选为单克隆抗体、多克隆抗体或重组抗体或者能够特异结合到相应标记物上的抗体片段。
在检测区中可以实现标记物的检测。固定化分子在检测区通过免疫反应或其他反应来结合标记的复合物或标记物类似物,从而在处理时在检测区中形成可见的检测线。优选地,该标记是光学可检测的标记。在检测区形成复合物将标记固定化,使测试线变为肉眼可见,指示阳性的测试结果。合适的是直接标记,例如特别是由肉眼最好识别的金色标记。此外,电子读出设备(例如,基于光度计、声学计、阻抗滴定计、电位计和/或安培计)可用于获得更精确的结果和分析物的半定量。其他合适的标记可以是乳胶、荧光团或磷光团。
在一个实施例中,通过向初始结合材料添加少量荧光染料或荧光乳胶珠结合物,增强视觉读取侧流免疫分析法测试的灵敏度。当可见光谱测试线可见时,观察并记录测试结果。
在本发明的一个实施例中,试剂配置为使得对应于存在病毒标记物的可见测试线与对应于存在细菌标记物的测试线分离。因此,可以简单地通过检测区中测试线的显影位置来容易地确定样品是否含有细菌或病毒标记物(或两者兼有)。在另一优选实施例中,可选择试剂以显影成不同颜色的测试线。也就是说,病毒标记物的存在将导致与细菌标记物存在时显影的颜色线不同。例如,对应于识别病毒标记物的试剂的标记可能是红色的,而对应于识别细菌标记物的试剂的标记可能是绿色的。可以附着在非固定化试剂上的不同着色标记是众所周知的。一些示例包括但不限于胶体金、胶体硒、胶体碳、乳胶珠、顺磁珠、荧光和化学发光及其混合物。
图1示出了一个色谱测试条,其测试线对应于病毒标记物的存在,第二条分离的测试线检测第一细菌标记物的存在,第三条分离的测试线检测第二细菌标记物的存在。将样品加到测试条的加样区。如图1所示,样品随后经过包含至少一个标记的病毒结合配偶体和至少一个标记的细菌结合配偶体的试剂区。标记的病毒结合配偶体能够特异结合到目标病毒标记物上以形成缀合物,该缀合物反过来能够特异结合到检测区中另一特异试剂或结合配偶体上。标记的细菌结合配偶体能够特异结合到目标细菌标记物上以形成结合物,该结合物反过来能够特异结合到检测区中另一特异试剂或结合配偶体上。
测试条还包括检测区,检测区包含至少一个用于检测病毒标记物的第一部分,例如,含有固定化特异结合配偶体的测试线,该固定化特异结合配偶体与由病毒标记物及其标记的结合配偶体形成的病毒试剂复合物互补。因此,在测试线上,检测区结合配偶体从试剂区捕获标记的病毒结合配偶体及其结合的病毒标记物。在测试线上,该病毒标记物与其标记的结合配偶体的位置给出了指示。在测试线上,通过标记的结合配偶体累积所导致的测试线指示的定性和/或定量读取结果来确定病毒标记物的存在。
检测区还包括至少一个用于检测细菌标记物的至少一个部分,例如,含有固定化特异结合配偶体的测试线,该固定化特异结合配偶体与由细菌标记物及其标记的结合配偶体形成的细菌试剂复合物互补。因此,在测试线上,检测区结合配偶体从试剂区捕获标记的细菌结合配偶体及其结合的细菌标记物。在测试线上,该细菌标记物与其标记的结合配偶体的位置给出了指示。在测试线上,通过标记的结合配偶体累积所导致的测试线指示的定性和/或定量读取结果来确定细菌标记物的存在。
在本发明的一个实施例中,检测区可包含另一测试线以检测第二细菌标记物。
用于区分病毒性和细菌性感染的即时检测的一个示例如图1所示。如上所述,mx-b是病毒性感染的诊断标记物,而crp和bpi是细菌性感染的诊断标记物。mx-b蛋白结果阳性,而crp/pct和bpi蛋白结果阴性指示病毒性感染。crp/pct和bpi结果阳性而mx-b蛋白结果阴性指示细菌性感染。mx-b、crp/pct和bpi的弱阳性结果指示同时感染了细菌和病毒(共感染)。mx-b、crp/pct和bpi的阴性结果指示没有细菌性和病毒性感染。虽然在本实施例中讨论了特定的颜色线,但以其他颜色或在测试条上不同位置的相同颜色指示病毒或细菌标记物,也属于在本发明的精神范围内。
当利用不同颜色线的显影时,这些线可以或可以不分隔开。在后一种情况下,选择标记使得当两种标记物都存在时,看到的颜色不同于当单种标记物存在时看到的颜色。例如,病毒标记物的存在可以用红色线指示;细菌标记物的存在可以用蓝色线指示;两者都存在可以用紫色线指示(红色和蓝色结合)。
在另一实施例中,测试条还可以包括指示测试条功能的对照区。如果存在,对照区可以设计成向用户传递设备已经工作的信号。例如,对照区可以包含试剂(例如抗体),该试剂可结合来自试剂区的标记的试剂。作为进一步选择,对照区可包含固定化的病毒和细菌标记物,这些标记物将与来自试剂区的多余的标记的试剂反应。对照区可以位于检测区的上游或下游。阳性对照指示告知用户样品已通过测试设备渗透到所需的距离。
在约10%的发热相关的细菌性感染中也可检测到mx同源蛋白。为了增强测试的可靠性,mx-b蛋白的截止值设定在0.01-0.05u/10000白细胞的范围内,优选地为0.025u/10000白细胞。对于crp,截止值设定在5-100mg/l的范围内,或在25-75mg/l的范围内,或40mg/l。对于pct,截止值设定在0.5ng/ml至>2ng/ml的范围内。对于bpi,截止值设定在1μg/ml至>10μg/ml的范围内。
实施例
下文实施例旨在帮助对本发明的理解而提出,但并不旨在,也不应理解为以任何方式限制本发明的范围。这些实施例不包括对常规方法的详细描述。这些方法为本领域普通技术人员所熟知。
实施例1——分析说明
使用侧流设备进行即时检测分析。每次分析所需的适当试剂已经包含在试剂瓶中。
步骤a:基于粘附力,将血滴(约0.005ml-0.010ml)从试剂瓶转移到设备中。
步骤b:首先,用约0.001ml的裂解缓冲液裂解血滴中的细胞,该裂解缓冲液由(20%的np-40,100mm的trishcl,ph7.2,0.05的叠氮化钠)组成。
步骤c:将裂解的血液导至两个测试条上方,然后进行孵育。
步骤d:抗mx-b的抗体溶液1与血液中可能存在的mx-b蛋白缀合。这种抗体已经与被标记物结合。
步骤d:将结合的mx-b蛋白导至第二载体溶液,其中具有抗mx-b的第二抗体。只有已经与第一标记的抗体结合的mx-b蛋白才能与第二抗体结合。
步骤e:漂洗载体溶液后,第一标记的且结合的抗体在测试条上以显色反应的形式呈现。
步骤f:按步骤a至步骤e进行crp/pct/bpi检测,但第二测试条上使用的是抗crp/pct的抗体和抗bpi的抗体。
实施例2——测试步骤
在两辆不同的救护车上,对不明原因的患者进行全血的mx-a蛋白、mx-b蛋白、crp/pct和bpi测试。所有患者根据赫尔辛基协议签署了一份同意声明,表明他们的数据仅供研究之用。113/5000。随后,在调查过程中继续回顾既往病历,并确定感染来源。由此,区分出了120例病毒性感染和50例细菌性感染。该调查结果如图2所示。借助于mx-b蛋白,检测到92%的病毒性感染。相反地,使用mx-a蛋白仅检测到77%的相同病毒性疾病。借助于检测crp/pct/bpi蛋白,细菌性疾病的检测谱提高到90%。如果只检测crp和pct蛋白,仅检测到80%的细菌性疾病。因此,将用于病毒性疾病的标记物mx-b蛋白和用于细菌性疾病的crp/pct/bpi结合起来,能够使检测灵敏度或特异性提高至90%以上。
实施例3——结果
病毒性感染结果的说明:为了证明显色反应正常,左侧的两个测试条都是对照。中间上方的测试条显色,下方的测试条保持无色。右侧的两个测试条保持无色。
细菌性感染结果的说明:
中间的两个测试条都保持无色,右侧上方的一个也保持无色,但右侧下方的测试条显色。
混合感染结果的说明:中间上方的测试条显色,而下方的测试条也显色。
参考文献:
[1]haller,o.,dynaminsareforevermx-binhibitshiv-1.cellhostmicrobe.2013oct16;14(4):371-3.
[2]weiw.,etal.,accumulationofmx-b/mx2-resistanthiv-1capsidvariantsduringexpansionofthehiv-1epidemicinhumanpopulations.ebiomedicine.2016jun;8:230–236.
[3]melen,k,.etal.,humanmx-bprotein,aninterferon-alphainduciblegtpase,containsanucleartargetingsignalandislocalizedintheheterochromatin-regionbeneaththenuclearenvelope.jbiolchem.1996sep20;271(38):23478-86.
[4]gao,s.,etal.,structuralbasisofoligomerizationinthestalkregionofdynamin-likemx-a.nature.2010may27;465(7297):502-6.
[5]wussow,p.v.,etal.,humoralresponsetorecombinantifn-α2binpatientsreceivingrecombinantifn-αtherapy.jinterferonres.1989sep;9suppl1:s25-31.
[6]jakschies,d.,etal.,emergenceanddecayofthehumanmxhomologinmononuclearcellsfromcancerpatientsduringandafterifn-αtherapy.jbiolresponsemod.1990jun;9(3):305-12.
[7]wussow,p.v.,etal.,theinterferon-inducedmx-homologousproteininpatientswithsymptomatichiv-1-infection.aids.1990feb;4(2):119-24.
[8]wussow,p.v.,etal.,thehumanmx-homologousproteinisspecificallyinducedbytype-i-ifns.eur.j.immunology.1990sep;20(9),20152019.
[9]jakschiesd.,etal.,correlationoftheantiproliferativeeffectandthemxhomologousproteininductionbyifnsinpatientswithmalignantmelanoma.jinvestdermatol.1990dec;95(6suppl):238s-241s.
[10]wussow,p.v.,etal.,effectivenaturalinterferon-alphatherapyinrecombinantinterferon-alpha-resistantpatientswithhairycellleukemia.blood.1991jul1;78(1):38-43.
[11]wussow,p.v.,etal.,treatmentofantirifn-α-2antibodypositivecml-patientswithnaturalifn-α.brjhaematol.1991jun;78(2):210-6.
[12]jakschies,d.,etal.,thehumanifninducedmx-homologousproteinsidentifiedby2dsds-pageisspecificallyinducedbytype-i-interferons.(1991).proc.int.meetingon2-d-electrophoresislondon,16.18.7.1991:163.
[13]towbin,h.,etal.,awholebloodimmunoassayfortheinterferon-induciblehumanmx-protein.jinterferonres.1992apr;12(2):67-74.
[14]jakschies,d.,etal.,strongtransientexpressionoftheinterferon-inducedmx-a-proteininhepatitisa,butnotinacutehepatitisbandc.hepatology.1994apr;19(4):857-65.
[15]rump,j.a.,etal.,commonvariableimmunodeficiency(cvid)andmx-a-proteinexpressioninbloodleucocytes.clinexpimmunol.1995jul;101(1):89-93.
[16]al-masri,a.,etal.,intracellularstainingofmxproteinsincellsfromperipheralblood,bonemarrowandskin.molpathol.1997feb;50(1):9-14.
[17]selfw.h.,etal.,diagnosticaccuracyoffebridx:arapidtesttodetectimmuneresponsestoviralandbacterialupperrespiratoryinfections.jclinmed.2017oct7;6(10).
- 还没有人留言评论。精彩留言会获得点赞!