用于选择患者的方法和试剂盒与流程
本发明涉及一种检测技术。更具体地说,本发明涉及一种用于选择可以对具有至少一个(经取代的苯基)-丙烯醛部分的化合物起反应的患者的方法。
背景技术:
靶向疗法是如今研究疾病治疗的主流方法。根据美国国立卫生研究院,靶向疗法是精准医学的根基。其是靶向帮助癌细胞生长、分裂和蔓延的癌细胞改变的癌症治疗的类型。当研究人员学习更多关于驱动癌症的细胞改变时,其更加能够设计靶向这些改变或阻断其效果的有前景的疗法。
众所周知,化学疗法通常造成严重的副作用。此外,化学疗法的成本可能非常昂贵。然而,化学疗法的效果不是令人满意的。如2004年临床肿瘤学杂志(journalofclinicaloncology)(细胞毒性化学疗法对成人恶性肿瘤5年存活率的贡献率(thecontributionofcytotoxicchemotherapyto5-yearsurvivalinadultmalignancies).临床肿瘤学(clinoncol)(皇家放射学会(rcollradiol)).2004年12月;16(8):549-560)中所公开,估计治愈性和辅助性细胞毒性化学疗法对成人5年存活率的总贡献率在澳大利亚是2.3%并且在美国是2.1%。因此,用于选择可以对特异性药物起反应的患者的筛选方法视为与治疗自身一样重要。
技术实现要素:
本发明提供一种用于选择可以对用于增加化学疗法的有效百分比并且优化医疗费用的药物起反应的患者的方法。
本发明提供一种用于选择可以对根据式i、iia、iib、iic、iii、iv、v、vi、vii或viii的化合物起反应的患者的方法,其包含使化合物与来源于患者的样品接触并且确定化合物是否减少选自ar、c-myc、aurora-a、突变p53、cdk4或her2的蛋白质的量或化合物是否增加样品中的活性氧类的量,其中蛋白质的减少或活性氧类的增加指示患者可以对化合物起反应;
其中在式i中:
r31和r41各自独立地选自由以下组成的群组:烷氧基、羟基和氢;并且
x1选自由以下组成的群组:羟基、烷氧基、乙基丙酸根、乙基甲基碳酸根和羰基烷基;
其中在式iia和式iib中:
r32、r42、r32'和r42'独立地选自由以下组成的群组:-h、-oh和-och3;
l2是c0-c8亚烷基;或当z2不存在时l2是不饱和亚烯基或炔基;
z2选自由以下组成的群组:-h、-oh、芳环、环烷基、-cor12、-co2r12、-conr12r22、-nr12r22、-c(x2)3,其中r12和r22独立地选自由以下组成的群组:-h、-ch3和-c2h5;并且
x2是选自由-f、-cl和-br组成的群组的卤素原子;
其中在式iic中:
r72、r82、r72'和r82'独立地选自由以下组成的群组:-h、-oh和-och3;并且
r52和r62独立地选自由以下组成的群组:-h、-ch3、-c2h5、经取代的芳基和经取代的苄基;
其中在式iii中:
r33、r43、r33'、r43'、r33”和r43”各自独立地选自由以下组成的群组:烷氧基、羟基和氢;
其中在式iv中:
r34、r44、r34'、r44'、r34”、r44”、r34”'和r44”'各自独立地选自由以下组成的群组:烷氧基、羟基和氢;
其中在式v中:
各“n5”独立地是1、2或3;
r35、r45、r35'和r45'独立地选自由以下组成的群组:-h、-oh和-och3;
l5-z5不存在;或
l5-z5存在,并且当z5不存在时l5选自由以下组成的群组:c0-c8亚烷基、不饱和亚烯基和炔基;
z5选自由以下组成的群组:-h、-oh、芳环、环烷基、-cor15、-co2r15、-conr15r25、-nr15r25、-c(x5)3;
r15和r25独立地选自由以下组成的群组:-h、-ch3和-c2h5;并且
x5是选自由-f、-cl和-br组成的群组的卤素原子;
其中在式vi和式vii中:
r16、r17、r26和r27是单或二取代的基团并且独立地选自由以下组成的群组:甲氧基、羟基、烷基磺酰基;
当z6和z7不存在时l6和l7各自选自由以下组成的群组:羰基、亚烷基、亚烯基和炔基;
z6和z7各自选自由以下组成的群组:-h、-oh、经取代的苯乙烯基、芳环、环烷基、-cor36、-conr36r46和-c(x6)3,其中r36和r46各自选自由以下组成的群组:-h、-ch3或-cn6h2n6+1、杂环和杂芳基部分;或r36和r46共同形成杂环;或
z6和z7各自是coor6;其中r6选自由以下组成的群组:-h、-ch3和-cn7h2n7+1;或
当y7不是h时z6和z7各自是环烷基;
n6和n7独立地是2到4的整数;
x6选自由以下组成的群组:-f、-cl和-br;
当l是亚烷基时y6和y7各自是h并且z6和z7是-conr37r47,r37和r47各自选自由以下组成的群组:-h、杂环、杂芳基和环烷基;或
y6和y7各自选自由以下组成的群组:c1-c3烷基、-f、cl和br;并且
r18和r28是单或二取代的基团并且独立地选自由以下组成的群组:甲氧基、羟基和烷基磺酰基;
r38选自由以下组成的群组:
r48选自由以下组成的群组:ch3、h、f和cl;并且
n8是1或2。
本发明还提供包含根据式i、iia、iib、iic、iii、iv、v、vi、vii或viii的化合物和用于检测选自ar、c-myc、aurora-a、突变p53、cdk4或her2的蛋白质的量的检测分子或用于检测活性氧类的量的检测分子的试剂盒。
本发明还提供一种用于识别可以治疗雄激素受体相关医学病况的候选化合物的方法,其包含使候选化合物与来源于罹患雄激素受体相关医学病况的患者的样品接触并且确定候选化合物是否减少选自ar、c-myc、aurora-a、突变p53、cdk4或her2的蛋白质的量或确定化合物是否增加样品中的活性氧类的量,其中蛋白质的减少或活性氧类的增加指示候选化合物可以治疗雄激素受体相关医学病况。
本发明还提供包含来源于罹患雄激素受体相关医学病况的患者的样品和用于检测选自ar、c-myc、aurora-a、突变p53、cdk4或her2的蛋白质的量的检测分子或用于检测活性氧类的量的检测分子的试剂盒。
本发明还提供通过如上所提到的方法识别的候选化合物。
在以下部分中详细描述本发明。本发明的其它特征、目标和优点可以发现于具体实施方式和权利要求书中。
附图说明
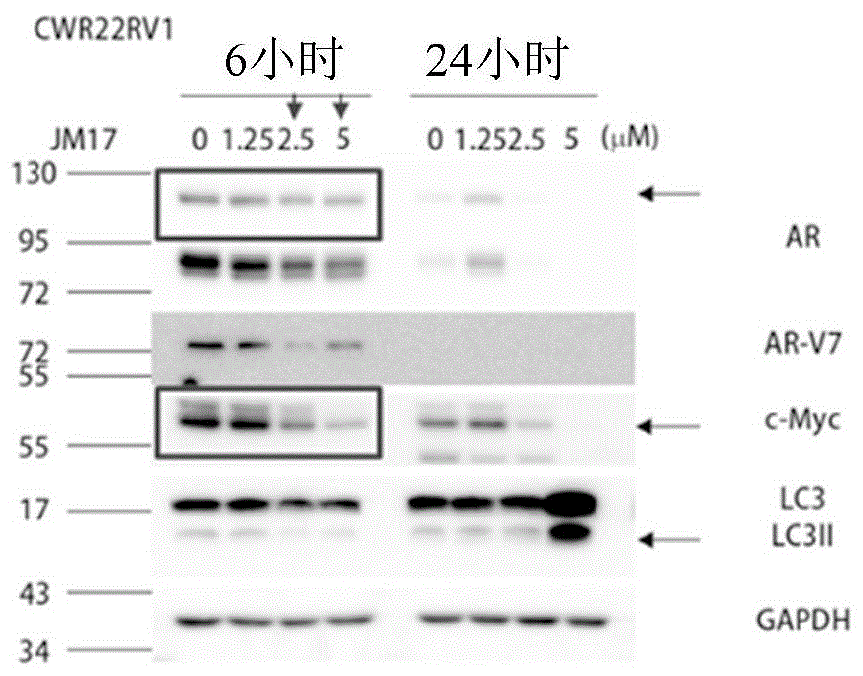
图1.jm17显示cwr22rv1即前列腺癌细胞系中的ar和c-myc蛋白质的减少。通过蛋白质印迹法用一系列剂量的jm17持续6小时(左)和24小时(右)分析ar、ar-v7、c-myc和lc3的蛋白质表达。
图2.jm17增强ar蛋白质降解。在存在或不存在5μmjm17的情况下用环己酰亚胺(chx)处理cwr22rv1细胞并且在指定时间点收获以用于蛋白质印迹法。归一化到gapdh的ar条带强度的定量显示在右侧。
图3.jm17增强c-myc蛋白质降解。在存在或不存在5μmjm17的情况下用环己酰亚胺(chx)处理cwr22rv1细胞并且在指定时间点收获以用于蛋白质印迹法。归一化到gapdh的c-myc条带强度的定量显示在右侧。
图4.jm17增强auroraa蛋白质降解。在存在或不存在5μmjm17的情况下用环己酰亚胺(chx)处理cwr22rv1细胞并且在指定时间点收获以用于auroraa的蛋白质印迹法。
图5.jm17触发前列腺癌细胞中的ros介导的蛋白质降解。用dmso对照物或jm17以1.25、2.5和5μm的剂量处理cwr22rv1细胞。在添加jm17之后10、30或60分钟时检测ros水平(图5a)。经由蛋白质印迹法检测ar、ar-v7、c-myc和p62的表达水平(图5b)。
图6.jm17遏制与her2、ar、c-myc、突变体p53和cdk4上的蛋白质表达减少配合的bt-474细胞生长。jm17显著地减少bt-474的细胞生长以用于48小时治疗(图6a)。jm17减少在1μm剂量下的her2、ar、c-myc、突变体p53和cdk4的蛋白质表达(图6b)。与对照组相比,**,p<0.01。
图7.jm17增强cdk4蛋白质降解。在存在或不存在2.5μmjm17的情况下用环己酰亚胺(chx)处理mda-mb-231细胞并且在指定时间点收获以用于cdk4蛋白质的蛋白质印迹法。
图8.jm17显示bt-474即乳腺癌细胞系中的her2、ar、c-myc、p53和cdk4蛋白质的减少。通过蛋白质印迹法用一系列剂量的jm17分析指定蛋白质的表达。
图9.jm17抑制乳腺异种移植模型中的肿瘤生长。在小鼠上皮下接种bt-474肿瘤细胞。通过以5、25或40mg/kg每日腹膜内注入给出jm17。通过卡尺每周测量肿瘤体积(左)。在jm17注入之后每周监测体重变化(右)。
图10.jm17降低异种移植中的her2、ar、c-myc、p53表达。在如图6中所描述的滑鼠处死之后,通过免疫印迹法用指定抗体测量肿瘤的蛋白质表达。
图11.jm17显著地降低小鼠异种移植模型中的mda-mb-231肿瘤的生长速率。上图显示在用媒剂(作为对照)、5mg/kg或20mg/kgjm17一周3次治疗28天之后皮下肿瘤的平均尺寸。jm17在20mg/kg剂量下显著地减小肿瘤尺寸。在媒剂、5mg/kg或20mg/kgjm17治疗之后第28天分离肿瘤以用于蛋白质提取(下图)。
具体实施方式
用一或多种生物标记物的癌症药物敏感性筛选是选择癌症患者以用于有效癌症治疗的有用工具。
本发明提供一种用于选择可以对具有至少一个(经取代的苯基)-丙烯醛部分的根据式i、iia、iib、iic、iii、iv、v、vi、vii或viii的化合物起反应的患者的方法,其包含使化合物与来源于患者的样品接触并且确定化合物是否减少选自ar、c-myc、aurora-a、突变p53、cdk4或her2的蛋白质的量或化合物是否增加样品中的活性氧类的量,其中蛋白质的减少或活性氧类的增加指示患者可以对化合物起反应。
如本文所使用的术语“(经取代的苯基)-丙烯醛部分”是指包括具有附接于其上的丙烯醛部分(当m等于1时)和烷氧基或羟基部分或烷基或经取代的烷基部分的苯基的组合物。取代可以相对于如本文所使用的丙烯醛部分间位或对位或邻位定位并且是指通式
如本文所使用的术语“烷基”是指仅由碳和氢原子组成、不含有不饱和基团、具有一到十个碳原子并且通过单键附接到分子的其余部分的直链或分支链烃链基,例如甲基、乙基、正丙基、1-甲基乙基(异丙基)、正丁基、正戊基、1,1-二甲基乙基(叔丁基)等等。
如本文所使用的术语“烯基”是指仅由碳和氢原子组成、含有至少一个双键、具有两到十个碳原子并且通过单键或双键附接到分子的其余部分的直链或分支链烃链基,例如乙烯基、丙-1-烯基、戊-1-烯基、戊-1,4-二烯基等等。
如本文所使用的术语“亚烯基”是指含有碳碳双键并且由式cph2p-2表示的直链或分支链烃链,其中氢可以替换为额外的碳碳双键一种单价取代基,例如亚乙烯基、亚丙-1-烯基等等。
如本文所使用的术语“烷氧基”是指具有式-or的基团,其中r是烷基、卤烷基或环烷基。“任选取代的烷氧基”是指具有式-or'的基团,其中r'是如本文所描述的任选取代的烷基。
如本文所使用的术语“炔基”是指仅由碳和氢原子组成、含有至少一个三键、具有两到十个碳原子并且通过单键或三键附接到分子的其余部分的直链或分支链烃链基,例如乙炔基、丙-1-炔基、丁-1-炔基、戊-1-炔基、戊-3-炔基等等。
如本文所使用的术语“芳基”是指具有其中环中之至少一个为芳环的碳环系统的基团。芳基可以是完全芳族的或可以含有与非芳环组合的芳环。“联芳基系统”是包括至少两种芳基的化合物。
如本文所使用的术语“环烷基”是指仅由碳和氢原子组成、具有三到十个碳原子并且为饱和的并通过单键附接到分子的其余部分的稳定的单价单环或双环烃基,例如环丙基、环丁基、环戊基、环己基等等。
如本文所使用的术语“二酮桥”或“酮-烯醇桥”是指包括分别紧密接近酮定位的两个酮或一个烯醇的直链或分支链烃链。“二酮桥”或“酮-烯醇桥”定位于至少两种芳基部分之间。
如本文所使用的术语“羟烷基”是指具有一到十个碳原子的直链或分支链羟基取代的烃链基,例如-ch2oh、-(ch2)2oh等等。
以下显示式i化合物:
其中在式i中:
r31和r41各自独立地选自由以下组成的群组:烷氧基、羟基和氢;并且
x1选自由以下组成的群组:羟基、烷氧基、乙基丙酸根、乙基甲基碳酸根和羰基烷基。
在一些实施例中,化合物具有选自由以下组成的群组的式:单体1、3、5、6和7。
以下提供这些单体:
单体:
在各种实施例中,还提供上文所提及的具有生物活性的单体的衍生物。衍生物可以具有在一或多个位置处的取代以增加一或多种特征,如活性、溶解度等等。这类衍生物可以调变化合物的偶极矩(dipolemoment)并且可以产生或强或弱的疏水性或亲水性组合物。
以下显示式iia和式iib化合物:
其中在式iia和式iib中:
r32、r42、r32'和r42'独立地选自由以下组成的群组:-h、-oh和-och3;
l2是c0-c8亚烷基;或当z2不存在时l2是不饱和亚烯基或炔基;
z2选自由以下组成的群组:-h、-oh、芳环、环烷基、-cor12、-co2r12、-conr12r22、-nr12r22、-c(x2)3,其中r12和r22独立地选自由以下组成的群组:-h、-ch3和-c2h5;并且
x2是选自由-f、-cl和-br组成的群组的卤素原子;并且
此外其中式iia和iib是作为二酮的普遍现象的平衡互变异构体。
在一些实施例中,化合物选自由以下组成的群组:ii-1、ii-2、ii-3、ii-4和ii-5。式是:
以下显示式iic化合物:
其中在式iic中:
r72、r82、r72'和r82'独立地选自由以下组成的群组:-h、-oh和-och3;并且
r52和r62独立地选自由以下组成的群组:-h、-ch3、-c2h5、经取代的芳基和经取代的苄基。
以下显示式iii化合物:
其中在式iii中:
r33、r43、r33'、r43'、r33”和r43”各自独立地选自由以下组成的群组:烷氧基、羟基和氢。
在一些实施例中,化合物包括式iii-1或iii-2,其是:
以下显示式iv化合物:
其中在式iv中:
r34、r44、r34'、r44'、r34”、r44”、r34”'和r44”'各自独立地选自由以下组成的群组:烷氧基、羟基和氢。
在一些实施例中,化合物包括式iv-1:
以下显示式v化合物:
其中在式v中:
各“n5”独立地是1、2或3;
r35、r45、r35'和r45'独立地选自由以下组成的群组:-h、-oh和-och3;
l5-z5不存在;或
l5-z5存在,并且当z5不存在时l5选自由以下组成的群组:c0-c8亚烷基、不饱和亚烯基和炔基;
z5选自由以下组成的群组:-h、-oh、芳环、环烷基、-cor15、-co2r15、-conr15r25、-nr15r25、-c(x5)3;
r15和r25独立地选自由以下组成的群组:-h、-ch3和-c2h5;并且
x5是选自由-f、-cl和-br组成的群组的卤素原子。
在一些实施例中,根据式v-1或v-2提供化合物:
以下显示式vi和式vii化合物:
其中在式vi和式vii中:
r16、r17、r26和r27是单或二取代的基团并且独立地选自由以下组成的群组:甲氧基、羟基、烷基磺酰基;
当z6和z7不存在时l6和l7各自选自由以下组成的群组:羰基、亚烷基、亚烯基和炔基;
z6和z7各自选自由以下组成的群组:-h、-oh、经取代的苯乙烯基、芳环、环烷基、-cor36、-conr36r46和-c(x6)3,其中r36和r46各自选自由以下组成的群组:-h、-ch3或-cn6h2n6+1、杂环和杂芳基部分;或r36和r46共同形成杂环;或
z6和z7各自是coor6;其中r6选自由以下组成的群组:-h、-ch3和-cn7h2n7+1;或
当y7不是h时z6和z7各自是环烷基;
n6和n7独立地是2到4的整数;
x6选自由以下组成的群组:-f、-cl和-br;
当l是亚烷基时y6和y7各自是h并且z6和z7是-conr37r47,r37和r47各自选自由以下组成的群组:-h、杂环、杂芳基和环烷基;或
y6和y7各自选自由以下组成的群组:c1-c3烷基、-f、cl和br。
以下显示式viii化合物:
r18和r28是单或二取代的基团并且独立地选自由以下组成的群组:甲氧基、羟基和烷基磺酰基;
r38选自由以下组成的群组:
r48选自由以下组成的群组:ch3、h、f和cl;并且
n8是1或2。
在本发明的一个优选实施例中,包括4,4-二取代1,7-双-(3,4-二甲氧基苯基)-庚-1,6-二烯-3,5-二酮和6,6-二取代1,11-双(经取代的苯基)-十一-1,3,8,10-四烯-5,7-二酮骨架的化合物如表1中所示。
表1:
在本发明的一个更优选实施例中,化合物是式viii,并且r18是3'4'-och3;r28是3'4'-och3;r38是
在本发明的一个实施例中,患者患有雄激素受体相关医学病况。
如本文所使用的术语“雄激素”是指如睾酮和二氢睾酮(dht)的雄激素激素。dht是通过5-α-还原酶进行的睾酮的转化产物。雄激素通过结合到雄激素受体、其进而结合到雄激素/ar-受控基因(dna)并活化或调变基因而刺激或控制脊椎动物中的男性特征和其它生理功能的发展和维护。
如本文所使用的术语“雄激素受体”或“ar”是指特异性结合雄激素(包括睾酮和dht)的细胞内受体。ar包括雄激素受体的所有哺乳动物同工型、剪接变异体(splicevariant)和多态性。
在本发明的一个实施例中,雄激素受体相关医学病况选自炎症、痤疮、秃发、多毛症、创伤、脊髓延髓肌肉萎缩(sbma,肯尼迪氏病(kennedy'sdisease))、不合需要的免疫反应、免疫病症或癌症。
癌症优选选自前列腺癌、肝癌、膀胱癌、子宫颈癌、肺癌和乳腺癌、皮肤癌、小细胞肺癌、睾丸癌、淋巴瘤、白血病、食道癌、胃癌、结肠癌、子宫内膜癌、卵巢癌、中枢神经系统癌症等等。
根据本发明,在所选的可以对化合物起反应的患者中,化合物可以诱导抗肿瘤细胞的细胞毒性或可以抑制肿瘤细胞生长。在一些实施例中,在所选的可以对化合物起反应的患者中,化合物的活性抑制癌细胞生长或增殖,任选地经刺激剂如dht刺激。
在其它实施例中,在所选的可以对化合物起反应的患者中,化合物、其衍生物、药物组合物等等用于预防、治疗或改善来自神经和神经肌肉病症如肯尼迪病的症状。脊髓延髓肌肉萎缩(sbma)或肯尼迪氏病是每40,000名男性中影响1人的性别特异性运动神经元病(由加津野等人2004年综述)。sbma患者具有含有延伸的多谷氨酰胺段的突变雄激素受体。延伸的多谷氨酰胺雄激素受体形成干扰细胞功能并且是造成与sbma相关联的近侧肌肉萎缩的因素的聚集物。在所选的可以对化合物起反应的患者中,化合物可以包括通过将突变体ar的量减少到可以更易于通过细胞的天然管家机构进行监管的水平来缓解由聚集物形成所导致的压力。在所选的可以对化合物起反应的患者中,化合物可以包括选择性地降解雄激素受体并且因此可以用作用于sbma的疗法。在所选的可以对化合物起反应的患者中,可以增强雄激素受体降解的化合物可以遏制受体的稳态水平,因此使患者中的聚集物形成的强度减弱。
在所选的可以对化合物起反应的患者中,化合物可以预防、治疗或改善来自雄激素相关毛发病症的症状。举例来说,雄性型秃发或“男性型脱发”是由毛囊和相邻细胞中的雄激素受体上的雄激素活性所导致的毛发损失。作为另一个实例,多毛症是其中女性毛发生长通常最少或不存在的位置中的厚、深色毛发的过度生长。这类终端体毛的男性型生长通常发生在雄激素刺激的位置中,如面部、胸部和乳晕。
在所选的可以对化合物起反应的患者中,化合物可以治疗炎症(例如类风湿性关节炎)、痤疮、秃发,并且可以加速创伤愈合。痤疮是由皮脂腺的雄激素诱导的ar活化所导致并且可以因此通过投予能够防止或减少ar活化的化合物来治疗。相信本发明的化合物诱导雄激素受体的降解并且因此提供抗这类医学病况的有效治疗。已知雄激素性秃发和其它毛发生长病症是由通过内源雄激素进行的毛囊中的雄激素受体(ar)活化所导致。也相信特定炎症病况和创伤愈合与对雄激素起反应的雄激素受体相关联。
在所选的可以对化合物起反应的患者中,化合物可以用于治疗内分泌病症。雄激素过量是女性中最常见内分泌病症中的一种(由布伦和阿达什2003年所综述)。这种病理生理学状况可以在患有各种内分泌病症的女性中看到,所述内分泌病症包括多囊卵巢综合症(pcos)、垂体腺瘤诱导的高催乳素血症、库欣氏综合征(cushing'ssyndrome)、先天性肾上腺增生、非经典肾上腺增生、卵巢或肾上腺肿瘤以及医原性雄激素过量。在这些病症当中,发生在5-10%育龄女性中的pcos是雄激素过多症的最通常识别的病因。最近,已经在绝经后女性中观察到循环雄激素与循环雌激素的比率中的相对增加(称为雄激素效力)(李等人,2004年)。雄激素效力是雌二醇和雌酮合成中的减少大于绝经后的雄激素合成的减少的结果并且其临床意义正在积极研究中。已经证明,更经常见到展现雄激素效力的女性患有中心型肥胖(佩雷尔曼等人,1995年)。腹壁中的脂肪沉积是代谢上活跃的并且与周围组织中的胰岛素抗性相关联(伊凡氏等人,1983年)。除上述内分泌紊乱以外,也可以在显示脂质营养不良综合症的人类免疫缺陷病毒(hiv)-感染的女性中检测到雄激素过多性症状(哈迪根等人,2000年)。已经表明,雄激素过多症可以参与在后一组患者中观察到的脂质失常。
本发明的方法包含使化合物与来源于患者的样品接触。样品的实例包括不限于活组织检查、血液、组织、尿液、细胞、排泄物或组织流体分泌物。样品优选来源于癌症的活组织检查。
所述方法包含使化合物与来源于患者的样品接触并且确定化合物是否减少选自ar、c-myc、aurora-a、突变p53、cdk4或her2的蛋白质的量或化合物是否增加样品中的活性氧类的量,其中蛋白质的减少或活性氧类的增加指示患者可以对化合物起反应。所述方法优选包含确定化合物是否增强蛋白质的降解。
用于确定蛋白质或活性氧类的量的方式包括但不限于蛋白质印迹法、免疫沉淀法或分光镜程序。方式优选基于抗体-抗原亲和力。
如实例中所示,jm17经由体外ros介导的途径增强前列腺癌细胞中的ar、c-myc和aurora-a蛋白质降解(图1到5)。不止ar、c-myc和aurora-a,也通过体外bt-474细胞(三阳性乳腺癌细胞系)中的jm17治疗降解cdk4、突变体p53和her2(图6)。为解决jm17是否缩短cdk4蛋白质的半衰期,施加环己酰亚胺以阻断蛋白质合成。结果显示jm17显著地缩短mda-mb-231细胞(三阴性乳腺癌细胞系)中的cdk4蛋白质的半衰期(图7)。
根据乳腺癌异种移植模型,jm17减少mda-mb-231细胞的肿瘤生长(三阴性乳腺癌细胞系)以及减少异种移植中的ar和c-myc的蛋白质表达(图11)。
本发明还提供包含式i、iia、iib、iic、iii、iv、v、vi、vii或viii化合物和用于检测选自ar、c-myc、aurora-a、突变p53、cdk4或her2的蛋白质的量的检测分子或用于检测活性氧类的量的检测分子的试剂盒。
检测分子优选是对ar、c-myc、aurora-a、突变p53、cdk4或her2或活性氧类具有特异性的抗体。
本发明还提供一种用于识别可以治疗雄激素受体相关医学病况的候选化合物的方法,其包含使候选化合物与来源于罹患雄激素受体相关医学病况的患者的样品接触并且确定候选化合物是否减少选自ar、c-myc、aurora-a、突变p53、cdk4或her2的蛋白质的量或确定化合物是否增加样品中的活性氧类的量,其中蛋白质的减少或活性氧类的增加指示候选化合物可以治疗雄激素受体相关医学病况如癌症。雄激素受体优选是所指定的蛋白质。
本发明还提供包含来源于罹患雄激素受体相关医学病况的患者的样品和用于检测选自ar、c-myc、aurora-a、突变p53、cdk4或her2的蛋白质的量的检测分子或用于检测活性氧类的量的检测分子的试剂盒。
本发明还提供通过如上所提到的方法识别的候选化合物。
提供以下实例来帮助所属领域的技术人员实践本发明。
实例
jm17增强ar和c-myc蛋白质降解.
根据nci-60细胞系筛选,测定ic50是约~5μm。我们也已经研究在分别以5和2.5μm治疗6小时的所选前列腺癌细胞系中jm17对ar和c-myc蛋白质水平的效果(图1)。
为解决在jm17治疗之后的ar和c-myc蛋白质的降低是否是因为蛋白质降解,我们在cwr22rv1(前列腺癌细胞)中使用阻断蛋白质合成的环己酰亚胺进行“转换”实验。与dmso媒剂对照物相比,jm17将ar蛋白质的半衰期从12小时显著地缩短到6小时(图2)并且将c-myc蛋白质的半衰期从~45分钟显著地缩短到~8分钟(图3)。除了ar和c-myc之外,我们还证实jm17增强auroraa蛋白质降解(图4)。
jm17触发前列腺癌细胞中的ros介导的蛋白质降解.
用dmso对照物或jm17以1.25、2.5和5μm的剂量处理cwr22rv1细胞即前列腺癌细胞系。随后,在添加jm17之后10、30或60分钟时检测ros水平。结果显示于图5中。与dmso对照物相比,jm17在60分钟内诱导ros(图5a)。在存在或不存在nac(ros清除剂,5mm)的情况下用jm17(5μm)共处理之后,经由蛋白质印迹法检测ar、ar-v7、c-myc和p62的表达水平。通过nac阻断jm17介导的蛋白质降解(图5b)。
jm17遏制与her2、ar、c-myc、突变体p53和cdk4上的蛋白质表达减少配合的bt-474细胞生长.
如图6中所示,jm17显著地减少bt-474即三阳性乳腺癌细胞系的细胞生长以用于48小时处理(图6a)。jm17减少在1μm剂量下的her2、ar、c-myc、突变体p53和cdk4的蛋白质表达(图6b)。
jm17增强cdk4蛋白质降解.
在存在或不存在2.5μmjm17的情况下用环己酰亚胺(chx)处理mda-mb-231细胞并且在指定时间点收获以用于cdk4蛋白质的蛋白质印迹法。计算归一化到gapdh的cdk4条带强度的定量。如图7中所示,jm17在12小时处理下显著地增强cdk4蛋白质降解。
jm17遏制乳腺癌异种移植模型中的肿瘤生长
为将jm17的应用扩展到其它癌症类型,将jm17诱导的蛋白质降解表征为乳腺癌细胞系即bt-474,其是具有ar表达的三阳性乳腺癌细胞系。除了ar和c-myc之外,免疫印迹法结果显示jm17也减少her2、p53和cdk4蛋白质表达(图8)。
为进一步探究jm17作为抗癌剂,我们估计皮下乳腺癌异种移植模型中的jm17的抗肿瘤功效。与携带bt-474肿瘤的滑鼠的媒剂对照物相比,低(5mg/kg)和高(40mg/kg)剂量的jm17处理组在第3周减小肿瘤体积(图9,左)。同时,jm17组显示体重增加,这意味着5mg/kg和40mg/kgjm17都不具有任何毒性严重问题(图9,右)。
在滑鼠处死之后,通过免疫印迹法用指定抗体测量肿瘤的蛋白质表达(图10)。
jm17对小鼠异种移植模型中的mda-mb-231肿瘤的生长速率的效果也显示于图11中。上图显示在用媒剂(作为对照物)即5mg/kg或20mg/kgjm17一周3次治疗28天之后皮下肿瘤的平均尺寸。jm17显著地减小在20mg/kg剂量下的肿瘤尺寸。在媒剂5mg/kg或20mg/kgjm17治疗之后第28天隔离肿瘤以用于蛋白质提取(下图)。jm17减少肿瘤样品中的ar和c-myc表达。
尽管已经结合上文所阐述的具体实施例来描述本发明,但对于其的许多替代方案和其修改和改变将对所属领域的技术人员显而易见。所有这类替代方案、修改和改变都视为落入本发明的范围内。
- 还没有人留言评论。精彩留言会获得点赞!